Галогены в периодической таблице расположены слева от благородных газов. Эти пять токсических неметаллических элементов входят в 7 группу периодической таблицы. К ним относятся фтор, хлор, бром, йод и астат. Хотя астат радиоактивен и имеет только короткоживущие изотопы, он ведет себя, как йод, и его часто причисляют к галогенам. Поскольку галогенные элементы имеют семь валентных электронов, им необходим лишь один дополнительный электрон для образования полного октета. Эта характеристика делает их более активными, чем другие группы неметаллов.
Галогены образуют двухатомные молекулы (вида Х2, где Х обозначает атом галогена) – устойчивую форму существования галогенов в виде свободных элементов. Связи этих двухатомных молекул являются неполярными, ковалентными и одинарными. Химические свойства галогенов позволяют им легко вступать в соединение с большинством элементов, поэтому они никогда не встречаются в несвязанном виде в природе. Фтор – наиболее активный галоген, а астат – наименее.
Все галогены образуют соли I группы с похожими свойствами. В этих соединениях галогены присутствуют в виде галоидных анионов с зарядом -1 (например, Cl-, Br-). Окончание -ид указывает на наличие галогенид-анионов; например Cl- называется «хлорид».
Кроме того, химические свойства галогенов позволяют им действовать в качестве окислителей – окислять металлы. Большинство химических реакций, в которых участвуют галогены – окислительно-восстановительные в водном растворе. Галогены образуют одинарные связи с углеродом или азотом в органических соединениях, где степень их окисления (СО) равна -1. Когда атом галогена замещён ковалентно-связанным атомом водорода в органическом соединении, префикс гало- может быть использован в общем смысле, или префиксы фтор-, хлор-, бром- , йод- – для конкретных галогенов. Галогенные элементы могут иметь перекрёстную связь с образованием двухатомных молекул с полярными ковалентными одинарными связями.
Хлор (Cl2) стал первым галогеном, открытым в 1774 г., затем были открыты йод (I2), бром (Br2), фтор (F2) и астат (At, обнаружен последним, в 1940 г.). Название «галоген» происходит от греческих корней hal- («соль») и -gen («образовывать»). Вместе эти слова означают «солеобразующий», подчёркивая тот факт, что галогены, вступая в реакцию с металлами, образуют соли. Галит – это название каменной соли, природного минерала, состоящего из хлорида натрия (NaCl). И, наконец, галогены используются в быту – фторид содержится в зубной пасте, хлор обеззараживает питьевую воду, а йод содействует выработке гормонов щитовидной железы.

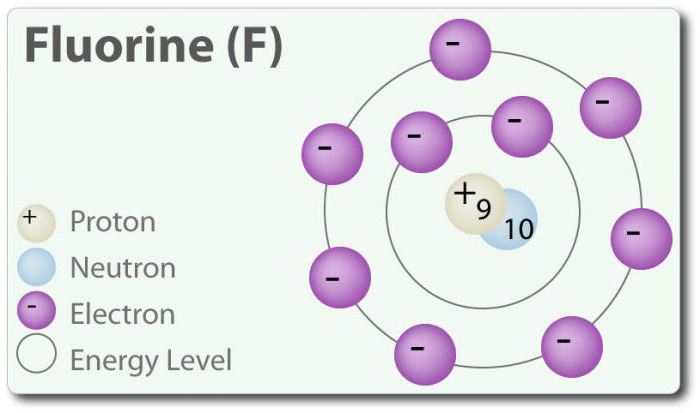
Фтор – элемент с атомным номером 9, обозначается символом F. Элементарный фтор впервые был обнаружен в 1886 г. путем выделения его из плавиковой кислоты. В свободном состоянии фтор существует в виде двухатомной молекулы (F2) и является наиболее распространенным галогеном в земной коре. Фтор – наиболее электроотрицательный элемент в периодической таблице. При комнатной температуре является бледно-жёлтым газом. Фтор также имеет относительно небольшой атомный радиус. Его СО – -1, за исключением элементарного двухатомного состояния, в котором его степень окисления равна нулю. Фтор чрезвычайно химически активен и непосредственно взаимодействует со всеми элементами, кроме гелия (He), неона (Ne) и аргона (Ar). В растворе h3O, плавиковой кислоты (HF) является слабой кислотой. Хотя фтор сильно электроотрицателен, его электроотрицательность не определяет кислотность; HF является слабой кислотой в связи с тем, что ион фтора основной (рН> 7). Кроме того, фтор производит очень мощные окислители. Например, фтор может вступать в реакцию с инертным газом ксеноном и образует сильный окислитель дифторид ксенона (XeF2). У фтора множество применений.
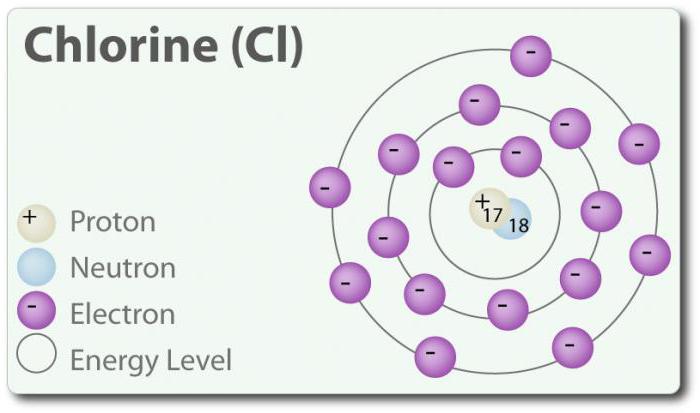
Хлор – элемент с атомным номером 17 и химическим символом Cl. Обнаружен в 1774 г. путём выделения его из соляной кислоты. В своём элементарном состоянии он образует двухатомную молекулу Cl2. Хлор имеет несколько СО: -1, +1, 3, 5 и 7. При комнатной температуре он является светло-зеленым газом. Так как связь, которая образуется между двумя атомами хлора, является слабой, молекула Cl2 обладает очень высокой способностью вступать в соединения. Хлор реагирует с металлами с образованием солей, которые называются хлориды. Ионы хлора являются наиболее распространенными ионами, они содержатся в морской воде. Хлор также имеет два изотопа: 35Cl и 37Cl. Хлорид натрия является наиболее распространенным соединением из всех хлоридов.
Бром – химический элемент с атомным номером 35 и символом Br. Впервые был обнаружен в 1826 г. В элементарной форме бром является двухатомной молекулой Br2. При комнатной температуре представляет собой красновато-коричневую жидкость. Его СО – -1, + 1, 3, 4 и 5. Бром более активен, чем йод, но менее активен, чем хлор. Кроме того, бром имеет два изотопа: 79Вг и 81Вг. Бром встречается в виде солей бромида, растворённых в морской воде. За последние годы производство бромида в мире значительно увеличилось благодаря его доступности и продолжительному времени жизни. Как и другие галогены, бром является окислителем и очень токсичен.
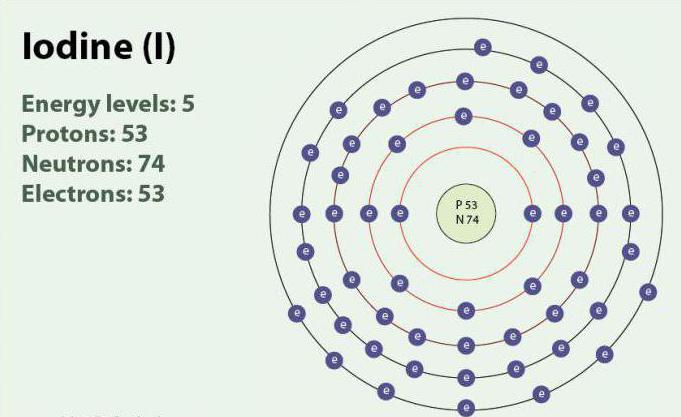
Йод – химический элемент с атомным номером 53 и символом I. Йод имеет степени окисления: -1, +1, +5 и +7. Существует в виде двухатомной молекулы, I2. При комнатной температуре является твёрдым веществом фиолетового цвета. Йод имеет один стабильный изотоп - 127I. Впервые обнаружен в 1811 г. с помощью морских водорослей и серной кислоты. В настоящее время ионы йода, могут быть выделены в морской воде. Несмотря на то что йод не очень хорошо растворим в воде, его растворимость может возрасти при использовании отдельных йодидов. Йод играет важную роль в организме, участвуя в выработке гормонов щитовидной железы.
Астат – радиоактивный элемент с атомным номером 85 и символом At. Его возможные степени окисления: -1, +1, 3, 5 и 7. Единственный галоген, не являющийся двухатомной молекулой. В нормальных условиях является металлическим твёрдым веществом чёрного цвета. Астат является очень редким элементом, поэтому о нём известно немного. Кроме того, астат имеет очень короткий период полураспада, не дольше нескольких часов. Получен в 1940 г. в результате синтеза. Полагают, что астат похож на йод. Отличается металлическими свойствами.
В таблице ниже показано строение атомов галогенов, структура внешнего слоя электронов.
Галоген | Конфигурация электронов |
Фтор | 1s2 2s2 2p5 |
Хлор | 3s2 3p5 |
Бром | 3d10 4s2 4p5 |
Иод | 4d10 5s2 5p5 |
Астат | 4f14 5d10 6s2 6p5 |
Подобное строение внешнего слоя электронов обусловливает то, что физические и химические свойства галогенов похожи. Вместе с тем при сопоставлении этих элементов наблюдаются и различия.
Физические свойства простых веществ галогенов изменяются с повышением порядкового номера элемента. Для лучшего усвоения и большей наглядности мы предлагаем вам несколько таблиц.
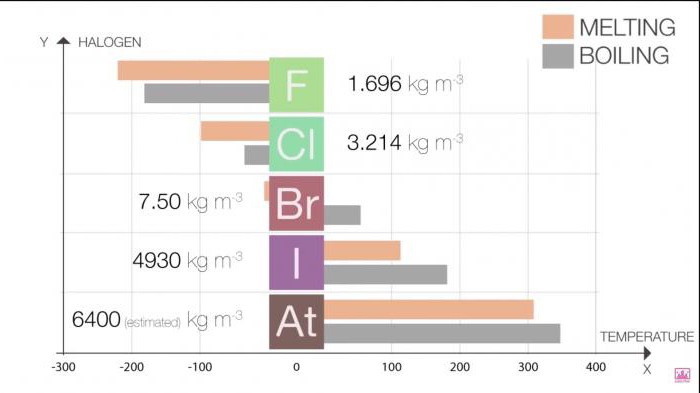
Точки плавления и кипения в группе возрастают по мере роста размера молекулы (F <Cl <Br <I <At). Это увеличение означает увеличение силы Ван-дер-Ваальса.
Таблица 1. Галогены. Физические свойства: точки плавления и кипения
Галоген | Т плавления (˚C) | Т кипения (˚C) |
Фтор | -220 | -188 |
Хлор | -101 | -35 |
Бром | -7.2 | 58.8 |
Иод | 114 | 184 |
Астат | 302 | 337 |
Размер ядра увеличивается (F < Cl < Br < I < At), так как увеличивается число протонов и нейтронов. Кроме того, с каждым периодом добавляется всё больше уровней энергии. Это приводит к большей орбитали, и, следовательно, к увеличению радиуса атома.
Таблица 2. Галогены. Физические свойства: атомные радиусы
Галоген | Ковалентный радиус (пм) | Ионный (X-) радиус (пм) |
Фтор | 71 | 133 |
Хлор | 99 | 181 |
Бром | 114 | 196 |
Иод | 133 | 220 |
Астат | 150 |
Если внешние валентные электроны не находятся вблизи ядра, то для их удаления от него не потребуется много энергии. Таким образом, энергия, необходимая для выталкивания внешнего электрона не столь высока в нижней части группы элементов, так как здесь больше энергетических уровней. Кроме того, высокая энергия ионизации заставляет элемент проявлять неметаллические качества. Йод и дисплей астат проявляют металлические свойства, потому что энергия ионизации снижается (At < I < Br < Cl < F).
Таблица 3. Галогены. Физические свойства: энергия ионизации
Галоген | Энергия ионизации (кДж/моль) |
фтор | 1681 |
хлор | 1251 |
бром | 1140 |
йод | 1008 |
астат | 890±40 |
Число валентных электронов в атоме возрастает с увеличением уровней энергии при прогрессивно более низких уровнях. Электроны прогрессивно дальше от ядра; Таким образом, ядро и электроны не как притягиваются друг к другу. Увеличение экранирования наблюдается. Поэтому Электроотрицательность уменьшается с ростом периода (At < I < Br < Cl < F).
Таблица 4. Галогены. Физические свойства: электроотрицательность
Галоген | Электроотрицательность |
фтор | 4.0 |
хлор | 3.0 |
бром | 2.8 |
иод | 2.5 |
астат | 2.2 |
Так как размер атома увеличивается с увеличением периода, сродство к электрону, как правило, уменьшается (В < I < Br < F < Cl). Исключение – фтор, сродство которого меньше, чем у хлора. Это можно объяснить меньшим размером фтора по сравнению с хлором.
Таблица 5. Сродство галогенов к электрону
Галоген | Сродство к электрону (кДж/моль) |
фтор | -328.0 |
хлор | -349.0 |
бром | -324.6 |
иод | -295.2 |
астат | -270.1 |
Реакционная способность галогенов падает с ростом периода (At <I <Br <Cl <F). Это связано с увеличением радиуса атома с возрастанием уровней энергии электронов. Это снижает притяжение валентных электронов других атомов, снижая реакционную способность. Это уменьшение также происходит из-за падения электроотрицательности с увеличением периода, что также снижает притяжение электронов. Кроме того, с увеличением размера атома снижается и окислительная способность.
Галогенид образуется, когда галоген реагирует с другим, менее электроотрицательным элементом с образованием бинарного соединения. Водород реагирует с галогенами, образуя галогениды вида НХ:
Галогениды водорода легко растворяются в воде с образованием галогенводородной (плавиковой, соляной, бромистоводородной, иодистоводородной) кислоты. Свойства этих кислот приведены ниже.
Кислоты образуются следующей реакцией: HX (aq) + h3O (l) → Х- (aq) + h4O+ (aq).
Все галоидоводороды образуют сильные кислоты, за исключением HF.
Кислотность галогеноводородных кислот увеличивается: HF <HCl <HBr <HI.
Плавиковая кислота способна гравировать стекло и некоторые неорганические фториды длительное время.
Может показаться нелогичным, что HF является самой слабой галогенводородной кислотой, так как фтор обладает самой высокой электроотрицательностью. Тем не менее связь Н-F очень сильна, в результате чего кислота очень слабая. Сильная связь определяется короткой длиной связи и большой энергией диссоциации. Из всех галогенидов водорода HF имеет самую короткую длину связи и самую большую энергию диссоциации связи.
Галогенные оксокислоты представляют собой кислоты с атомами водорода, кислорода и галогена. Их кислотность может быть определена с помощью анализа структуры. Галогенные оксокислоты приведены ниже:
В каждой из этих кислот протон связан с атомом кислорода, поэтому сравнение длин связей протонов здесь бесполезно. Доминирующую роль здесь играет электроотрицательность. Активность кислотны возрастает с увеличением числа атомов кислорода, связанный с центральным атомом.
Основные физические свойства галогенов кратко можно выразить в следующей таблице.
Состояние вещества (при комнатной температуре) | Галоген | Внешний вид |
твёрдое | йод | фиолетовый |
астат | чёрный | |
жидкое | бром | красно-коричневый |
газообразное | фтор | бледно-жёлто-коричневый |
хлор | бледно-зелёный |
Цвет галогенов является результатом поглощения видимого света молекулами, что вызывает возбуждение электронов. Фтор поглощает фиолетовый свет, и, следовательно, выглядит светло-жёлтым. Йод, наоборот, поглощает жёлтый свет и выглядит фиолетовым (жёлтый и фиолетовый – дополняющие цвета). Цвет галогенов становится темнее с ростом периода.
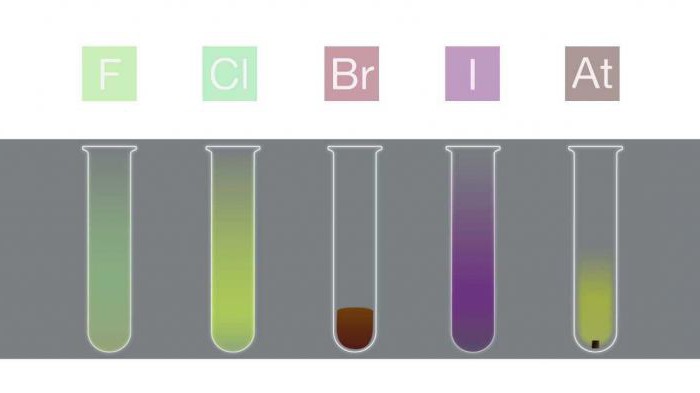
В закрытых ёмкостях жидкий бром и твёрдый йод находятся в равновесии со своими парами, которые можно наблюдать в виде цветного газа.
Хотя цвет астата неизвестен, предполагается, что он должен быть темнее йода (т. е. черным) в соответствии с наблюдаемой закономерностью.
Теперь, если вас попросят: «Охарактеризуйте физические свойства галогенов», вам будет что сказать.
Степень окисления часто используется вместо понятия "валентность галогенов". Как правило, степень окисления равна -1. Но если галоген связан с кислородом или другим галогеном, он может принимать другие состояния: СО кислорода -2 имеет приоритет. В случае двух различных атомов галогена, соединенных вместе, более электроотрицательный атом превалирует и принимает СО -1.
Например, в хлориде йода (ICl) хлор имеет СО -1, и йод +1. Хлор является более электроотрицательным, чем йод, поэтому его СО равна -1.
В бромной кислоте (HBrO4) кислород обладает СО -8 (-2 х 4 атома = -8). Водород имеет общую степень окисления +1. Сложение этих значений даёт СО -7. Так как конечное СО соединения должно быть нулевым, то СО брома равна +7.
Третьим исключением из правила является степень окисления галогена в элементарной форме (X2), где его СО равна нулю.
Галоген | СО в соединениях |
фтор | -1 |
хлор | -1, +1, +3, +5, +7 |
бром | -1, +1, +3, +4, +5 |
йод | -1, +1, +5, +7 |
астат | -1, +1, +3, +5, +7 |
Электроотрицательность увеличивается с ростом периода. Поэтому фтор имеет самую высокую электроотрицательность из всех элементов, что подтверждается его положением в периодической таблице. Его электронная конфигурация 1s2 2s2 2p5. Если фтор получает еще один электрон, крайние р-орбитали полностью заполнены и составляют полный октет. Поскольку фтор имеет высокую электроотрицательность, он может легко отобрать электрон у соседнего атома. Фтор в этом случае изоэлектронен инертному газу (с восемью валентными электронами), все его внешние орбитали заполнены. В таком состоянии фтор гораздо более стабилен.
В природе галогены находятся в состоянии анионов, поэтому свободные галогены получают методом окисления путём электролиза или с помощью окислителей. Например, хлор вырабатывается гидролизом раствора поваренной соли. Применение галогенов и их соединений многообразно.

fb.ru
Тема: Основные металлы и неметаллы
Урок: Водород и галогены
Неметаллы – это элементы, образующие простые вещества, которые не обладают типичными металлическими свойствами.
Неметаллы – это элементы с высокой электроотрицательностью (кроме инертных газов), которые располагаются в верхней правой части периодической системы, выше диагонали Ве – Аt. См. Рис. 1.
Водород
Водород – это первый элемент в Периодической системе Д.И. Менделеева. Заряд его атомного ядра – +1, строение электронной оболочки выражается формулой 1s1. Многие особенности свойств водорода связаны с тем, что в его атоме между электроном внешнего энергетического уровня и ядром нет других электронов.
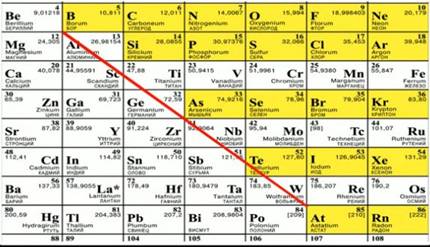
Рис. 1.
В соответствии со строением электронной оболочки, атом водорода, отдавая один электрон, проявляет степень окисления +1 (образуются ионы Н+). Это позволяет говорить о сходстве водорода со щелочными металлами. Поэтому водород может быть отнесен к главной подгруппе I группы, которую составляют щелочные металлы.
До завершения внешнего электронного слоя атому водорода не хватает одного электрона, что характерно также для элементов главной подгруппы VII группы – галогенов. Это обусловливает возможность помещения водорода в VII группу Периодической системы Д.И. Менделеева.
Водород может проявлять степень окисления +1, 0, -1. Степень окисления -1 проявляется в гидридах. Это бинарные соединения водорода с менее электроотрицательными атомами.
Например, это гидрид натрия NaH, гидрид кальция Cah3, силан Sih5, герман Geh5. Но намного чаще водород проявляет степень окисления +1.
Методы получения водорода
Промышленные методы получения
1. Паровая конверсия метана. Метан входит в состав природного газа. Образуемая смесь водорода и углекислого газа легко разделима.
Ch5↑ +2h3O 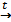 CO2↑ + 4 h3↑
CO2↑ + 4 h3↑
2. Газификация угля. В данном процессе уголь нагревается от 7000С до 10000С. При этом образуется уголь с большим содержанием углерода и газообразный водород.
3. Электролиз водных растворов солей.
Лабораторные методы получения водорода
1. Zn + 2HCl = ZnCl2 + h3 ↑
Все более актуальная задача – это хранение водорода.
Водород можно получать из воды. При его горении выделяется большое количество теплоты, и это один из перспективных источников энергии. Это очень хорошее топливо для автомобилей.
Один из способов хранения водорода – это переведение его в жидкое состояние. Но, чтобы держать его в жидком состоянии, нужны очень высокие давления. А чтобы сдерживать большое давление, нужны толстостенные сосуды, которые очень тяжелые. Поэтому этот метод не очень хорош.
Второй вариант хранения этого газа – это сорбция водорода на платиновых металлах. Этот способ невыгоден, так как платиновые металлы – дорогие.
Третий вариант – это образование комплексных гидридов – соединений, способных обратимо связывать и выделять водород.
Природные изотопы водорода
Водород встречается в виде трёх изотопов, которые имеют индивидуальные названия:
1H — протий (Н), 2Н — дейтерий (D), 3Н — тритий (T – радиоактивный). Протий и дейтерий являются стабильными изотопами с массовыми числами 1 и 2. Содержание их в природе соответственно составляет 99,9% и 0,01%. Это соотношение может незначительно меняться в зависимости от источника и способа получения водорода. Изотоп водорода 3Н (тритий) нестабилен. Его период полураспада составляет 12,32 лет.
Тритий содержится в природе в очень малых количествах. Природный водород состоит из молекул h3 и HD (дейтероводород) в соотношении 3200:1. Содержание чистого дейтерийного водорода D2 ещё меньше. Отношение концентраций HD и D2 примерно 6400:1.
Галогены (от греч. ἁλός — соль и γένος — рождение, происхождение) – химические элементы VII-й группы главной подгруппы Периодической таблицы химических элементов Д.И. Менделеева. К галогенам относятся фтор F, хлор Cl, бром Br, йод I, астат At, а также (формально) искусственный элемент унунсептий Uus.
Все галогены — энергичные окислители, поэтому встречаются в природе только в виде соединений.
С увеличением порядкового номера химическая активность галогенов уменьшается, химическая активность галогенид-ионов F−, Cl−, Br−, I−, At− уменьшается. Электронная конфигурация валентного слоя данных элементов – …ns2np5. Для получения электронной конфигурации благородного газа им не хватает одного электрона, который они получают от других элементов
ns2np5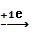 ns2np6.
ns2np6.
и существуют в форме аниона Hal-
Все галогены, кроме фтора, могут образовывать соединения, в которых они обладают положительными степенями окисления. Например, кислородсодержащие кислоты хлора. См. табл. 1.

Табл. 1.
Галогены в природе
Галогены в свободном виде в природе не встречаются из-за своей химической активности. Они входят в состав многих минералов. См. табл. 2.
|
|
|
|
|
|
Минералы фтора |
Минералы хлора. |
||
Табл. 2.
Галогены – простые вещества

Рис. 2.
Молекулы галогенов состоят из двух атомов, с ковалентной неполярной связью между ними. Галогенам не присуща аллотропия. Кристаллическая решетка простых веществ галогенов – молекулярная. Фтор – это зеленовато-желтый газ. Хлор – тоже газ желтого цвета. Бром – красно-бурая жидкость. Йод – черно-фиолетовые кристаллы с характерным металлическим блеском. Рис. 2, 3, 4. Температура кипения и плавления галогенов увеличивается по группе сверху вниз. Все эти вещества обладают резким, характерным запахом. Все они вредны для организма.


Рис. 3-4.
Химические свойства галогенов
1. Реагируют с металлами
2Al + 3Cl2 = 2AlCl3(кр) + 1405 кДж,
2Fe + ЗCl2 = 2FeCl3(кр) + 804 кДж,
Активность галогенов уменьшается с увеличением атомного радиуса. Это можно наблюдать при взаимодействии их с железом.
2. Взаимодействуют с неметаллами (кроме N2, O2, благородных газов). Свободный хлор очень реакционноспособен, хотя его активность и меньше, чем у фтора. Он непосредственно реагирует со всеми простыми веществами, за исключением кислорода, азота и благородных газов.
Н2 + Cl2 = 2HCl(г)+185 кДж.
Галогеноводороды – это типичные кислоты-неокислители. Но так как в их состав входят атомы галогенов в низших степенях окисления, то эти кислоты способны окисляться.
3. Взаимодействие с фосфором
2P + 5F2 → 2PF5
2P + 3Cl2 → 2PCl3
2P + 5Cl2 → 2PCl5
2P + 3Br2 → 2PBr3
2P + 5Br2 → 2PBr5
По мере повышения температуры глубина окисления возрастает.
4. Взаимодействие с графитом
С + 2F2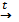 CF4 реагирует только с F2. Остальные галогены не реагируют с простыми веществами, образованными углеродом.
CF4 реагирует только с F2. Остальные галогены не реагируют с простыми веществами, образованными углеродом.
5. Со сложными веществами
5.1. С водой
3F2 + ЗН2О = OF2↑ + 4HF + Н2О2.
2F2 + 2Н2О = 4HF + O2
Cl2 + Н2О ↔HCl + HClO (Хлорная вода)
Br2 + Н2О ↔ HBr + HBrO (Бромная вода)
I2 + Н2О ↔HI + HIO
5.2. Реагируют со щелочами
Cl2 + 2NaOH = NaCl + NaClO + Н2О (на холоде),
3Cl2 + 6КОН = 5KCl + KClO3 + 3Н2О (при нагревании).
6. Галогены способны вытеснять друг друга из солей галогенидов и галогеноводородов. Более активный галоген вытесняет менее активный. Химическая активность галогенов последовательно уменьшается от фтора к астату. Каждый галоген в ряду F–At может вытеснять последующий из его соединений с водородом или металлами, то есть каждый галоген в виде простого вещества способен окислять галогенид-ион любого из последующих галогенов. Астат ещё менее реакционноспособен, чем йод.
2NaI + Cl2 = 2NaCl + I2
Качественная реакция на галогениды
Качественная реакция – это реакция, которая позволяет доказать присутствие в пробе того или иного вещества или иона.
При растворении растворимых галогенидов с раствором нитрата серебра выпадают осадки – нерастворимые галогениды серебра. Рис. 5.
NaCl + AgNO3 = NaNO3 + AgCl↓ (белый осадок)
NaBr + AgNO3 = NaNO3 + AgBr↓ (желтоватый осадок)
NaI + AgNO3 = NaNO3 + AgI↓ (желтый осадок)

Рис. 5
Галогениды можно определить также по окраске пламени. Если взять пробу и внести её в пламя горелки, то галогениды меди окрашивают пламя в зеленый или сине-зеленый цвет.
Йод – крахмальная проба. Она заключается в образовании комплексов между молекулой йода и одной из форм крахмала. Эти комплексы окрашены в интенсивный синий цвет. Рис. 6.

Рис. 6.
Это опыт можно проделать дома, капнув йодом на крахмалсодержащие продукты.
Получение хлора
Получение хлора в лаборатории
В лаборатории хлор получают из перманганата калия и концентрированной соляной кислоты. В колбу Вюрца помещают кристаллы перманганата калия. Закрывают колбу пробкой с капельной воронкой. В воронку наливается соляная кислота. Соляная кислота приливается из капельной воронки. Сразу же начинается энергичное выделение хлора. Через газоотводную трубку хлор постепенно заполняет цилиндр, вытесняя из него воздух. Рис. 7.

Рис. 7.
2KMnO4 + 16HCI = 2KCI + 2MnCI2 + 5CI2 + 8h3O
Многие соединения галогенов находят применение в нашей жизни. Хлорная известь используется как дезинфицирующее и отбеливающее средство. Бертолетова соль используется при получении спичек. Йод применяется для очистки некоторых металлов и как средство для дезинфекции ран.
Подведение итога урока
На данном уроке была рассмотрена тема «Водород. Галогены». Вы познакомились с важной группой химических веществ – неметаллами. Подробно рассмотрели водород и познакомились со способами его получения. Узнали вещества галогеновой группы. Вы узнали, где расположены эти вещества в периодической таблице, какими особенностями они обладают, их молекулярное строение и химические свойства: с какими веществами и как они взаимодействуют.
Список литературы
1. Рудзитис Г.Е. Химия. Основы общей химии. 11 класс: учебник для общеобразовательных учреждений: базовый уровень / Г.Е. Рудзитис, Ф.Г. Фельдман. – 14-е изд. – М.: Просвещение, 2012.
2. Попель П.П. Химия: 8 кл.: учебник для общеобразовательных учебных заведений / П.П. Попель, Л.С.Кривля. – К.: ИЦ «Академия», 2008. – 240 с.: ил.
3. Габриелян О.С. Химия. 11 класс. Базовый уровень. 2-е изд., стер. – М.: Дрофа, 2007. – 220 с.
Дополнительные рекомендованные ссылки на ресурсы сети Интернет
1. Internerurok.ru (Источник).
2. Hemi.nsu.ru (Источник).
3. Chemport.ru (Источник).
4. Химик.ру (Источник).
Домашнее задание
1. №№1, 3, 4 (с. 179) Габриелян О.С. Химия. 11 класс. Базовый уровень. 2-е изд., стер. – М.: Дрофа, 2007. – 220 с.
2. Какими кристаллическим строением и свойствами будут обладать летучие водородные соединения неметаллов?
3. Сравните ряд электроотрицательности неметаллов с электрохимическим рядом напряжений металлов.
interneturok.ru
Все галогены проявляют высокую окислительную активность, которая уменьшается при переходе от фтора к йоду. Фтор — самый активный из галогенов, реагирует со всеми металлами без исключения, многие из них в атмосфере фтора самовоспламеняются, выделяя большое количество теплоты, например:
2Аl + 3F2 = 2АlF3 + 2989 кДж,
2Fе + 3F2 = 2FеF3 + 1974 кДж.
Без нагревания фтор реагирует и со многими неметаллами (h3, S, С, Si, Р) — все реакции при этом сильно экзотермические, например:
Н2 + F2 = 2НF + 547 кДж,
Si + 2F2 = SiF4(г) + 1615 кДж.
При нагревании фтор окисляет все другие галогены по схеме
Hal2 + F2 = 2НаlF
где Наl = Сl, Вr, I, причем в соединениях НаlF степени окисления хлора, брома и иода равны +1.
Наконец, при облучении фтор реагирует даже с инертными (благородными) газами:
Хе + F2 = ХеF2 + 152 кДж.
Взаимодействие фтора со сложными веществами также протекает очень энергично. Так, он окисляет воду, при этом реакция носит взрывной характер:
3F2 + ЗН2О = F2О↑ + 4НF + Н2О2.
Свободный хлор также очень реакционноспособен, хотя его активность и меньше, чем у фтора. Он непосредственно реагирует со всеми простыми веществами, за исключением кислорода, азота и благородных газов. Для сравнения приведем уравнения реакций хлора с теми же простыми веществами, что и для фтора:
2Аl + ЗСl2 = 2АlСl3(кр) + 1405 кДж,
2Fе + ЗСl2 = 2FeСl3(кр) + 804 кДж,
Si + 2Сl2 = SiCl4(Ж) + 662 кДж,
Н2 + Сl2 = 2НСl(г)+185кДж.
Особый интерес представляет реакция с водородом. Так, при комнатной температуре, без освещения хлор практически не реагирует с водородом, тогда как при нагревании или при освещении (например, на прямом солнечном свету) эта реакция протекает со взрывом по приведенному ниже цепному механизму:
Cl2 + hν → 2Сl,
Сl + Н2 → НСl + Н,
Н + Cl2 → НСl + Сl,
Сl + Н2 → НCl + Н и т.д.
Возбуждение этой реакции происходит под действием фотонов (hv), которые вызывают диссоциацию молекул Сl2 на атомы — при этом возникает цепь последовательных реакций, в каждой из которых появляется частица, инициирующая начало последующей стадии.
Реакция между Н2 и Сl2 послужила одним из первых объектов исследования цепных фотохимических реакций. Наибольший вклад в развитие представлений о цепных реакциях внес русский ученый, лауреат Нобелевской премии (1956 г) Н.Н. Семенов.
Хлор вступает в реакцию со многими сложными веществами, например замещения и присоединения с углеводородами:
СН3-СН3 + Сl2 → СН3-СН2Сl + НСl,
СН2=СН2 + Сl2 → СН2Cl — СН2Сl.
Хлор способен при нагревании вытеснять бром или иод из их соединений с водородом или металлами:
Сl2 + 2НВr = 2НСl + Вr2,
Сl2 + 2НI = 2НСl + I2,
Сl2 + 2КВr = 2КСl + Вr2,
а также обратимо реагирует с водой:
Сl2 + Н2О = НСl + НСlO — 25 кДж.
Хлор, растворяясь в воде и частично реагируя с ней, как это показано выше, образует равновесную смесь веществ, называемую хлорной водой.
Заметим также, что хлор в левой части последнего уравнения имеет степень окисления 0. В результате реакции у одних атомов хлора степень окисления стала -1 (в НСl), у других +1 (в хлорноватистой кислоте НОСl). Такая реакция — пример реакции самоокисления-самовосстановления, или диспропорционирования.
Хлор может таким же образом реагировать (диспропорционировать) с щелочами:
Сl2 + 2NаОН = NаСl + NаСlO + Н2О (на холоде),
ЗСl2 + 6КОН = 2КСl + КClO3 + ЗН2О (при нагревании).
Химическая активность брома меньше, чем у фтора и хлора, но все же достаточно велика в связи с тем, что бром обычно используют в жидком состоянии и поэтому его исходные концентрации при прочих равных условиях больше, чем у хлора.
Для примера приведем реакции взаимодействия брома с кремнием и водородом:
Si +2Вr2 = SiBr4(ж) + 433 кДж,
Н2 + Вr2 = 2НВr(г) + 73 кДж.
Являясь более «мягким» реагентом, бром находит широкое применение в органической химии.
Отметим, что бром, так же, как и хлор, растворяется в воде, и, частично реагируя с ней, образует так называемую «бромную воду», тогда как йод практически в воде не растворим и не способен ее окислять даже при нагревании; по этой причине не существует «йодной воды».
Йод существенно отличается по химической активности от остальных галогенов. Он не реагирует с большинством неметаллов, а с металлами медленно реагирует только при нагревании. Взаимодействие же иода с водородом происходит только при сильном нагревании, реакция является эндотермической и сильно обратимой:
Н2 + I2 = 2НI — 53 кДж.
Таким образом, химическая активность галогенов последовательно уменьшается от фтора к йоду. Каждый галоген в ряду F — I может вытеснять последующий из его соединений с водородом или металлами, т.е. каждый галоген в виде простого вещества способен окислять галогенид-ион любого из последующих галогенов
<img border=«0» width=«449» height=«26» src=«ref-2_1985566674-2002.coolpic» alt="\mbox{Cl}{_2(g)} + \mbox{2X}{^-(aq)} ~ \stackrel{air}{\rightarrow} ~ \mbox{2Cl}{^-(aq)} + \mbox{X}{_2(g)} ~ \mbox{(X = Br or I)}" v:shapes=«Рисунок_x0020_3»> продолжение --PAGE_BREAK--
www.ronl.ru
Летучим характеристическим водородным соединением азота является аммиак,самое важное водородное соединение азота. По своей химической природе он представляет собой нитрид водорода h4N. В химическом строении аммиакаsp3-гибридные орбитали атома азота образуют три σ-связи с тремя атомами водорода, которые занимают три вершины чуть искаженного тетраэдра.Четвертая вершина тетраэдра занята неподеленной электронной парой азота, что обеспечивает химическую ненасыщенность и реакционноспособность молекул аммиака, а также большую величину электрического момента диполя.При н.у. бесцветный газ с резким запахом.
Получение:пром:N2+3h3=2Nh4,лаб:Nh5Cl+NaOH=Nh4+NaCl+h3O/РеакцииNh4+HOH⇄Nh5OH\ 4Nh4+ 3O2 → 2N2↑ + 6h3O\Nh4+HCl⇄Nh5Cl\Nh4+h4PO4 → (Nh5)3PO4 Аммиак взаимодействует с солями некоторых металлов с образованием комплексных соединений – аммиакатов:CuSO4+ 4Nh4→ [Cu(Nh4)4]SO4 сульфат тетрааммин меди (II),AgCl+ 2Nh4→ [Ag(Nh4)2]Clхлорид диаммин серебра (I).Аммиак восстанавливает некоторые металлы из их оксидов:2Nh4+ 3CuO→N2↑ +3Cu+3h3OОн токсичен: раздражает слизистые оболочки, а острое отравление вызывает поражение глаз и воспаление легких. Вследствие полярности молекул и достаточно высокой диэлектрической проницаемости жидкий аммиак является хорошим растворителем. В жидком аммиаке хорошо растворяются щелочные и щелочно-земельные металлы, сера, фосфор, йод, многие соли и кислоты. По растворимости в воде аммиак превосходит любой другой газ. Этот раствор называется аммиачной водой, или нашатырным спиртом. Прекрасная растворимость аммиака в воде обусловлена возникновением межмолекулярных водородных связей.
Галогеноводороды — бесцветные газы, с резким запахом, легко растворимы в воде.. Фтороводород смешивается с водой в любых соотношениях. Высокая растворимость этих соединений в воде позволяет получать концентрированные растворы.
При растворении в воде галогеноводороды диссоциируют по типу кислот. HF относится к слабо диссоциированным соединениям, что объясняется особой прочностью связи. Остальные же растворы галогеноводородов относятся к числу сильных кислот. HF — фтороводородная (плавиковая) кислота НСl— хлороводородная (соляная) кислота HBr — бромоводородная кислота HI — иодоводородная кислота
Сила кислот в ряду HF — НСl — HBr — HI возрастает, что объясняется уменьшением в том же направлении энергии связи и увеличением межъядерного расстояния. HI — самая сильная кислота из ряда галогеноводородных кислот.
Поляризуемость растет вследствие того, что вода поляризует больше ту связь, чья длина больше. Соли галогеноводородных кислот носят соответственно следующие названия: фториды, хлориды, бромиды, иодиды.
Химические свойства галогеноводородных кислот
В сухом виде галогеноводороды не действуют на большинство металлов.
1. Водные растворы галогеноводородов обладают свойствами бескислородных кислот. Энергично взаимодействуют со многими металлами, их оксидами и гидроксидами; на металлы, стоящие в электрохимическом ряду напряжений металлов после водорода, не действуют. Взаимодействуют с некоторыми солями и газами.
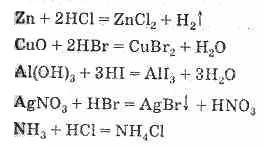
Фтороводородная кислота разрушает стекло и силикаты:
SiO2+4HF=SiF4+2Н2O
Поэтому она не может храниться в стеклянной посуде.
2. В окислительно-восстановительных реакциях галогеноводородные кислоты ведут себя как восстановители, причем восстановительная активность в ряду Сl-, Br-, I- повышается.
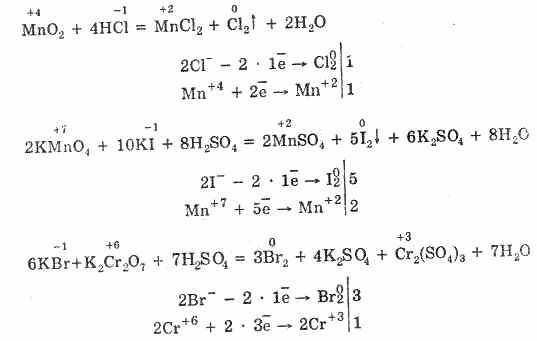
Получение
Фтороводород получают действием концентрированной серной кислоты на плавиковый шпат:
CaF2+h3SO4=CaSO4+2HF
Хлороводород получают непосредственным взаимодействием водорода с хлором:
Н2+Сl2=2НСl
Это синтетический способ получения.
Сульфатный способ основан на реакции концентрированной серной кислоты с NaCl.
При небольшом нагревании реакция протекает с образованием НСl и NaHSO4.
NaCl+h3SO4=NaHSO4+HCl
При более высокой температуре протекает вторая стадия реакции:
NaCl+NaHSO4=Na2SO4+HCl
Но аналогичным способом нельзя получить HBr и HI, т.к. их соединения с металлами при взаимодействии с концентрировавной серной кислотой окисляются, т.к. I- и Br- являются сильными восстановителями.
2NaBr-1+2h3S+6O4(к)=Br02+S+4O2+Na2SO4+2Н2O
Бромоводород и иодоводород получают гидролизом PBr3 и PI3: PBr3+3Н2O=3HBr+Н3PO3 PI3+3Н2О=3HI+Н3РO3
studfiles.net
Здесь читатель найдет сведения о галогенах, химических элементах периодической таблицы Д. И. Менделеева. Содержание статьи позволит вам ознакомиться с их химическими и физическими свойствами, нахождением в природе, способах применения и др.
Галогены – это все элементы химической таблицы Д. И. Менделеева, находящиеся в семнадцатой группе. По более строму способу классификации это все элементы седьмой группы, главной подгруппы.
Галогены – это элементы, способные вступать в реакции практически со всеми веществами простого типа за исключением некоторого количества неметаллов. Все они являются энергетическими окислителями, потому в условиях природы, как правило, находятся в смешанной форме с другими веществами. Показатель химической активности галогенов уменьшается с возрастанием их порядковой нумерации.
Галогенами считаются следующие элементы: фтор, хлор, бром, йод, астат и искусственно созданный теннесин.
Как говорилось ранее, все галогены – это окислители с ярко выраженными свойствами, к тому же все они являются неметаллами. Внешний энергетический уровень имеет семь электронов. Взаимодействие с металлами приводит к образованию ионной связи и солей. Почти все галогены, за исключением фтора, могут проявлять себя в качестве восстановителя, достигая высшей окислительной степени +7, однако для этого необходимо, чтобы они взаимодействовали с элементами, имеющими большую степень электроотрицательности.

В 1841 г. шведский ученый-химик Й. Берцелиус предложил ввести термин галогенов, относя к ним известные в то время F, Br, I. Однако до введения этого термина по отношению ко всей группе таких элементов, в 1811 г., немецкий ученый И. Швейггер этим же словом назывался хлор, сам термин переводился с греческого языка как «солерод».
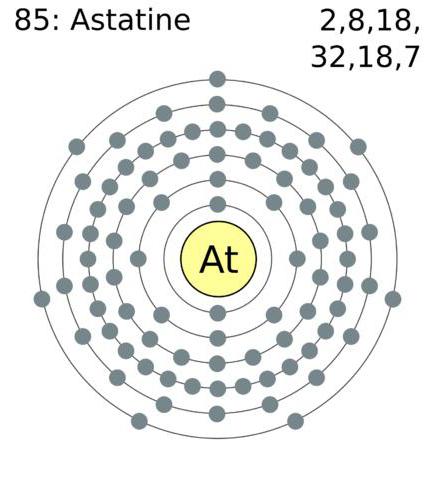
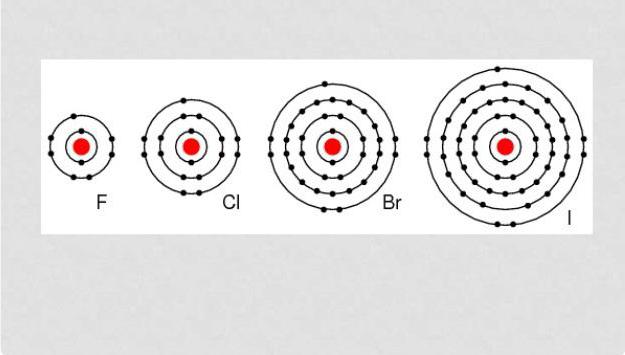
Конфигурация электронов внешней атомной оболочки галогенов имеет следующий вид: астат – 6s26p5, йод – 5s25p5, бром 4s24p5, хлор – 3s23p5, фтор 2s22p5.
Галогены – это элементы, имеющие на электронной оболочке внешнего типа семь электронов, что позволяет им «без особых усилий» присоединять электрон, которого недостаточно для завершения оболочки. Обычно степень окисления проявляется в виде -1. Cl, Br, I и At вступая в реакцию с элементами, имеющими более высокую степень, начинают проявлять положительную окислительную степень: +1, +3, +5, +7. Фтор имеет постоянную окислительную степень -1.
Ввиду своей высокой степени реакционной способности галогены обычно находятся в виде соединений. Уровень распространения в коре земли убывает в соответствии с увеличением атомного радиуса от F к I. Астат в коре земли измеряется вовсе в граммах, а теннессин создается искусственно.
Галогены встречаются в природе чаще всего в соединениях галогенидов, а йод также может принимать форму йодата калия или натрия. В связи со своей растворимостью в воде присутствуют в океанических водах и рассолах природного происхождения. F – малорастворимый представитель галогенов и чаще всего обнаруживается в породах осадочного типа, а его главный источник – это фторид кальция.
Галогены между собой могут сильно отличаться, и они имеют следующие физические свойства:

Галогены – это элементы с очень высокой окислительной активностью, которая ослабевает в направлении от F к At. Фтор, будучи самым активным представителем галогенов, реагировать может со всеми видами металлов, не исключая ни один известный. Большинство представителей металлов, попадая в атмосферу фтора, подвергаются самовоспламенению, при этом выделяя теплоту в огромных количествах.
Без подвергания фтора нагреванию он может реагировать с большим количеством неметаллов, например h3, C, P, S, Si. Тип реакций в таком случае является экзотермическим и может сопровождаться взрывом. Нагреваясь, F принуждает окисляться остальные галогены, а подвергаясь облучению, этот элемент способен и вовсе реагировать с тяжелыми газами инертной природы.
Вступая во взаимодействие с веществами сложного типа, фтор вызывает высоко энергетические реакции, например, окисляя воду, он может вызывать взрыв.

Реакционноспособным может быть и хлор, особенно в свободном состоянии. Уровень активности его меньше, чем у фтора, но он способен реагировать почти со всеми простыми веществам, но азот, кислород и благородные газы в реакцию не вступают с ним. Взаимодействуя с водородом, при нагревании или хорошем освещении хлор создает бурнопротекающую реакцию, сопровождаемую взрывом.
В реакциях присоединения и замещения Cl может реагировать с большим количеством веществ сложного типа. Способен вытеснять Br и I в результате нагревания из соединений, созданных ими с металлом или водородом, а также может вступать в реакцию со щелочными веществами.
Бром химически менее активный, чем хлор или фтор, но все же весьма ярко себя проявляет. Это обусловлено тем, что чаще всего бром Br используется в качестве жидкости, ведь в таком состоянии исходная степень концентрации при остальных одинаковых условиях выше, чем у Cl. Широко используется в химии, особенно органической. Может растворяться в h3O и реагировать с ней частично.
Галоген-элемент иод образует простое вещество I2 и способен вступать в реакции с h3O, растворяется в йодидах растворов, образуя при этом комплексные анионы. От большинства галогенов I отличается тем, что он не вступает в реакции с большинством представителей неметаллов и не спеша реагирует с металлами, при этом его необходимо нагревать. С водородом реагирует, лишь подвергаясь сильному нагреванию, а реакция является эндотермической.
Редкий галоген астат (At) проявляет реакционные способности меньше йода, однако может реагировать с металлами. В результате диссоциации возникают как анионы, так и катионы.
Соединения галогенов широко применяются человеком в самых разнообразных областях деятельности. Природный криолит (Na3AlF6) используют для получения Al. Бром и йод в качестве простых веществ часто используют фармацевтические и химические компании. При производстве запчастей для машин часто используют галогены. Фары – это одна из таких деталей. Качественно выбрать материал для данной составной части машины очень важно, так как фары освещают дорогу в ночное время и являются способом обнаружения как вас, так и других автомобилистов. Одним из лучших составных материалов для создания фар считается ксенон. Галоген тем не менее ненамного уступает по качеству этому инертному газу.

Хороший галоген – это фтор, добавка, широко используемая при производстве зубных паст. Он помогает предотвращать возникновение заболевания зубов – кариеса.
Такой элемент-галоген, как хлор (Cl), находит свое применение в получении HCl, часто используется при синтезе органических веществ, таких как пластмасса, каучук, синтетические волокна, красители и растворители и т. д. А также соединения хлора используют в качестве отбеливателей льняного и хлопчатобумажного материала, бумаги и как средство для борьбы с бактериями в питьевой воде.

Ввиду наличия очень высокой реакционной способности галогены по праву называются ядовитыми. Наиболее ярко способность к вступлению в реакции выражена у фтора. Галогены имеют ярко выраженные удушающие свойства и способны поражать ткани при взаимодействии.
Фтор в парах и аэрозолях считается одним из самых потенциально опасных форм галогенов, вредоносных для окружающих живых существ. Это связано с тем, что он слабо воспринимается обонянием и ощущается лишь по достижении большой концентрации.
Как мы видим, галогены являются очень важной частью периодической таблицы Менделеева, они имеют множество свойств, отличаются между собой по физическим и химическим качествам, атомному строению, степени окисления и способности реагировать с металлами и неметаллами. В промышленности используются разнообразным образом, начиная от добавок в средства личной гигиены и заканчивая синтезом веществ органической химии или отбеливателями. Несмотря на то что одним из лучших способов поддержания и создания света в фаре автомобиля является ксенон, галоген тем не менее ему практически не уступает и также широко используется и имеет свои преимущества.
Теперь вы знаете, что такое галоген. Сканворд с любыми вопросами об этих веществах для вас уже не помеха.
fb.ru
Атом водорода имеет электронную формулу внешнего (и единственного) электронного уровня 1s1. С одной стороны, по наличию одного электрона на внешнем электронном уровне атом водорода похож на атомы щелочных металлов. Однако, ему, так же как и галогенам не хватает до заполнения внешнего электронного уровня всего одного электрона, поскольку на первом электронном уровне может располагаться не более 2-х электронов. Выходит, что водород можно поместить одновременно как в первую, так и в предпоследнюю (седьмую) группу таблицы Менделеева, что иногда и делается в различных вариантах периодической системы:
С точки зрения свойств водорода как простого вещества, он, все-таки, имеет больше общего с галогенами. Водород, также как и галогены, является неметаллом и образует аналогично им двухатомные молекулы (h3).
В обычных условиях водород представляет собой газообразное, малоактивное вещество. Невысокая активность водорода объясняется высокой прочностью связи между атомами водорода в молекуле, для разрыва которой требуется либо сильное нагревание, либо применение катализаторов, либо и то и другое одновременно.
Из металлов водород реагирует только с щелочными и щелочноземельными! К щелочным металлам относятся металлы главной подгруппы I-й группы (Li, Na, K, Rb, Cs, Fr), а к щелочно-земельным — металлы главной подгруппы II-й группы, кроме бериллия и магния (Ca, Sr, Ba, Ra)
При взаимодействии с активными металлами водород проявляет окислительные свойства, т.е. понижает свою степень окисления. При этом образуются гидриды щелочных и щелочноземельных металлов, которые имеют ионное строение. Реакция протекает при нагревании:
Следует отметить, что взаимодействие с активными металлами является единственным случаем, когда молекулярный водород Н2 является окислителем.
Из неметаллов водород реагирует только c углеродом, азотом, кислородом, серой, селеном и галогенами!
Под углеродом следует понимать графит или аморфный углерод, поскольку алмаз — крайне инертная аллотропная модификация углерода.
При взаимодействии с неметаллами водород может выполнять только функцию восстановителя, то есть только повышать свою степень окисления:
Водород не реагирует с оксидами металлов, находящихся в ряду активности металлов до алюминия (включительно), однако, способен восстанавливать многие оксиды металлов правее алюминия при нагревании:
Из оксидов неметаллов водород реагирует при нагревании с оксидами азота, галогенов и углерода. Из всех взаимодействий водорода с оксидами неметаллов особенно следует отметить его реакцию с угарным газом CO.
Смесь CO и h3 даже имеет свое собственное название – «синтез-газ», поскольку из нее в зависимости от условий могут быть получены такие востребованные продукты промышленности как метанол, формальдегид и даже синтетические углеводороды:
С неорганическими кислотами водород не реагирует!
Из органических кислот водород реагирует только с непредельными, а также с кислотами, содержащими функциональные группы способные к восстановлению водородом, в частности альдегидные, кето- или нитрогруппы.
В случае водных растворов солей их взаимодействие с водородом не протекает. Однако при пропускании водорода над твердыми солями некоторых металлов средней и низкой активности возможно их частичное или полное восстановление, например:
Галогенами называют химические элементы VIIA группы (F, Cl, Br, I, At), а также образуемые ими простые вещества. Здесь и далее по тексту, если не сказано иное, под галогенами будут пониматься именно простые вещества.
Все галогены имеют молекулярное строение, что обусловливает низкие температуры плавления и кипения данных веществ. Молекулы галогенов двухатомны, т.е. их формулу можно записать в общем виде как Hal2.
| Галоген | Физические свойства |
| F2 | Светло-желтый газ с резким раздражающим запахом |
| Cl2 | Желто-зеленый газ с резким удушливым запахом |
| Br2 | Красно-бурая жидкость с резким зловонным запахом |
| I2 | Твердое вещество с резким запахом, образующее черно-фиолетовые кристаллы |
Следует отметить такое специфическое физическое свойство йода, как его способность к сублимации или, иначе говоря, возгонке. Возгонкой, называют явление, при котором вещество, находящееся в твердом состоянии, при нагревании не плавится, а, минуя жидкую фазу, сразу же переходит в газообразное состояние.
Электронное строение внешнего энергетического уровня атома любого галогена имеет вид ns2np7, где n – номер периода таблицы Менделеева, в котором расположен галоген. Как можно заметить, до восьмиэлектронной внешней оболочки атомам галогенов не хватает всего одного электрона. Из этого логично предположить преимущественно окисляющие свойства свободных галогенов, что подтверждается и на практике. Как известно, электроотрицательность неметаллов при движении вниз по подгруппе снижается, в связи с чем активность галогенов уменьшается в ряду:
F2 > Cl2 > Br2 > I2
Все галогены являются высокоактивными веществами и реагируют с большинством простых веществ. Однако, следует отметить, что фтор из-за своей чрезвычайно высокой реакционной способности может реагировать даже с теми простыми веществами, с которыми не могут реагировать остальные галогены. К таким простым веществам относятся кислород, углерод (алмаз), азот, платина, золото и некоторые благородные газы (ксенон и криптон). Т.е. фактически, фтор не реагирует лишь с некоторыми благородными газами.
Остальные галогены, т.е. хлор, бром и йод, также являются активными веществами, однако менее активными, чем фтор. Они реагируют практически со всеми простыми веществами, кроме кислорода, азота, углерода в виде алмаза, платины, золота и благородных газов.
При взаимодействии всех галогенов с водородом образуются галогеноводороды с общей формулой HHal. При этом, реакция фтора с водородом начинается самопроизвольно даже в темноте и протекает со взрывом в соответствии с уравнением:
Реакция хлора с водородом может быть инициирована интенсивным ультрафиолетовым облучением или нагреванием. Также протекает со взрывом:
Бром и йод реагируют с водородом только при нагревании и при этом, реакция с йодом является обратимой:
Взаимодействие фтора с фосфором приводит к окислению фосфора до высшей степени окисления (+5). При этом происходит образование пентафторида фосфора:
При взаимодействии хлора и брома с фосфором возможно получение галогенидов фосфора как в степени окисления + 3, так и в степени окисления +5, что зависит от пропорций реагирующих веществ:
При этом в случае белого фосфора в атмосфере фтора, хлора или жидком броме реакция начинается самопроизвольно.
Взаимодействие же фосфора с йодом может привести к образованию только триодида фосфора из-за существенно меньшей, чем у остальных галогенов окисляющей способности:
Фтор окисляет серу до высшей степени окисления +6, образуя гексафторид серы:
Хлор и бром реагируют с серой, образуя соединения, содержащие серу в крайне не свойственных ей степенях окисления +1 и +2. Данные взаимодействия являются весьма специфичными, и для сдачи ЕГЭ по химии умение записывать уравнения этих взаимодействий не обязательно. Поэтому три нижеследующих уравнения даны скорее для ознакомления:
Как уже было сказано выше, фтор способен реагировать со всеми металлами, даже такими малоактивными как платина и золото:
Остальные галогены реагируют со всеми металлами кроме платины и золота:
Более активные галогены, т.е. химические элементы которых расположены выше в таблице Менделеева, способны вытеснять менее активные галогены из образуемых ими галогеноводородных кислот и галогенидов металлов:
Аналогичным образом, бром и йод вытесняют серу из растворов сульфидов и или сероводорода:
Хлор является более сильным окислителем и окисляет сероводород в его водном растворе не до серы, а до серной кислоты:
Вода горит во фторе синим пламенем в соответствии с уравнением реакции:
Бром и хлор реагируют с водой иначе, чем фтор. Если фтор выступал в роли окислителя, то хлор и бром диспропорционируют в воде, образуя смесь кислот. При этом реакции обратимы:
Взаимодействие йода с водой протекает в настолько ничтожно малой степени, что им можно пренебречь и считать, что реакция не протекает вовсе.
Фтор при взаимодействии с водным раствором щелочи опять же выступает в роли окислителя:
Умение записывать данное уравнение не требуется для сдачи ЕГЭ. Достаточно знать факт о возможности такого взаимодействия и окислительной роли фтора в этой реакции.
В отличие от фтора, остальные галогены в растворах щелочей диспропорционируют, то есть одновременно и повышают и понижают свою степень окисления. При этом, в случае хлора и брома в зависимости от температуры возможно протекание по двум разным направлениям. В частности, на холоду реакции протекают следующим образом:
а при нагревании:
Йод реагирует с щелочами исключительно по второму варианту, т.е. с образованием йодата, т.к. гипоиодит не устойчив не только при нагревании, но также при обычной температуре и даже на холоду:
scienceforyou.ru


 МИНСКИЙ КОЛЛЕДЖ ТЕХНОЛОГИИ И ДИЗАЙНА ЛЕГКОЙ ПРОМЫШЛЕННОСТИ
МИНСКИЙ КОЛЛЕДЖ ТЕХНОЛОГИИ И ДИЗАЙНА ЛЕГКОЙ ПРОМЫШЛЕННОСТИРеферат
по дисциплине: Химия
Тема: «Водород и его соединения»
Подготовил:
Проверил: Минск 2009СодержаниеСтроение атома водорода в периодической системе
Степени окисления
Распространенность в природе
Водород как простое вещество
Соединения водорода
Список литературыСтроение атома водорода в периодической системеПервый элемент периодической системы (1-й период, порядковый номер 1). Не имеет полной аналогии с остальными химическими элементами и не принадлежит ни к какой группе, поэтому в таблицах условно помещается в IА группу и/или VIIA-группу.
Атом водорода наименьший по размерам и самый легкий среди атомов всех элементов. Электронная формула атома 1s1. Обычная форма существования элемента в свободном состоянии - двухатомная молекула.^ Атом водорода в соединениях с более электроотрицательными элементами проявляет степень окисления +1, например HF, h3O и др. А в соединениях с металлами - гидридах - степень окисления атома водорода равна -1, например NaH, Cah3 и др. Обладает значением электроотрицательности средним между типичными металлами и неметаллами. Способен каталитически восстанавливать в органических растворителях, таких как уксусная кислота или спирт, многие органические соединения: ненасыщенные соединения до насыщенных, некоторые соединения натрия-до аммиака или аминов.^ Природный водород состоит из двух стабильных изотопов - протия 1Н, дейтерия 2Н и трития 3Н. По-другому дейтерий обозначают как D, а тритий как Т. Возможны различные комбинации, например НТ, HD, TD, h3, D2, T2. Водород больше распространен в природе в виде различных соединений с серой (h3S), кислородом (в виде воды), углеродом, азотом и хлором. Реже в виде соединений с фосфором, йодом, бромом и другими элементами. Входит в состав всех растительных и животных организмов, нефти, ископаемых углей, природного газа, ряда минералов и пород. В свободном состоянии встречается очень редко в небольших количествах – в вулканических газах и продуктах разложения органических остатков. Водород является самым распространенным элементом во Вселенной (около 75%). Он входит в состав Солнца и большинства звезд, а также планет Юпитера и Сатурна, которые в основном состоят из водорода. На отдельных планетах водород может существовать в твердом виде.^ Молекула водорода состоит из двух атомов, связанных между собой ковалентной неполярной связью. Физические свойства - газ без цвета и запаха. Быстрее других газов распространяется в пространстве, проходит через мелкие поры, при высоких температурах сравнительно легко проникает сквозь сталь и другие материалы. Обладает высокой теплопроводностью.
^ . В обычном состоянии при низких температурах малоактивен, без нагревания реагирует с фтором и хлором (при наличии света).h3 + F2 2HF
h3 + Cl2 hv 2HClС неметаллами взаимодействует активнее, чем с металлами.2h3 + C = Ch5При взаимодействии с различными веществами может проявлять как окислительные, так и восстановительные свойства.
^ Одним из соединений водорода являются галогены. Они образуются при соединении водорода с элементами VIIA группы. HF, HCl, HBr и HI представляют собой бесцветные газы, хорошо растворимые в воде.Cl2 + h3OHClO + HCl; HClO-хлорная водаТак как HBr и HI типичные восстановители, то их нельзя получить по обменной реакции как HCl.CaF2 + h3SO4 = CaSO4 + 2HFВода - самое распространенное в природе соединение водорода.2Н2 + О2 = 2Н2ОНе имеет ни цвета, ни вкуса, ни запаха. Очень слабый электролит, но активно реагирует со многими металлами и неметаллами, основными и кислотными оксидами.2Н2О + 2Na = 2NaOH + h3
Н2О + BaO = Ba(OH)2
3 Н2О + P2O5 = 2h4PO4Тяжелая вода (D2O) – изотопная разновидность воды. Растворимость веществ в тяжелой воде значительно меньше чем в обычной. Тяжелая вода ядовита, так как замедляет биологические процессы в живых организмах. Накапливается в остатке электролиза при многоразовом электролизе воды. Используется как теплоноситель и замедлитель нейтронов в ядерных реакторах.
Гидриды – взаимодействие водорода с металлами (при высокой температуре)или менее электроотрицательными чем водород неметаллами.Si + 2h3 =Sih5
h3 + S = h3SСам же водород был открыт в первой половине 16в. Парацельсом. В 1776 Г. Кавендиш впервые исследовал его свойства, в 1783-1787 А. Лавуазье показал, что водород входит в состав воды, включил его в список химических элементов и предложил название «гидроген».Список литературы
shkolnie.ru