 Опубликовать
Опубликовать Опубликовать
ОпубликоватьРеферат на тему:
Синтетическая биология (Synthetic Biology) — термин, долго использовавшийся для описания подходов в биологии, стремящихся интегрировать различные области исследования для того, чтобы создать более целостный подход к пониманию концепции жизни.
В последнее время термин используется в другом значении, сигнализируя о новой области исследования, которая объединяет науку и инженерию с целью проектирования и построения новых (несуществующих в природе) биологических функций и систем.
Синтетическая биология — это новое направление генной инженерии. Развивается небольшой плеядой учёных. Главные цели следующие:
Более 100 лабораторий по всему миру занимаются синтетической биологией. Работы в этой области разобщены; над их систематизацией работает биолог Дрю Энди из Массачусетского технологического института. Это позволит проектировать живые системы, которые ведут себя предсказуемым (и заказанным по желанию) образом и используют взаимозаменяемые детали из стандартного набора генов. Учёные стремятся создать обширный генетический банк, позволяющий создавать любой нужный организм (по аналогии с созданием электронной схемы из промышленных транзисторов и диодов). Банк составляют биокирпичи (BioBrick) — фрагменты ДНК, чья функция строго определена и которые можно внедрить в геном клетки для синтеза заранее известного белка. Все отобранные биокирпичи спроектированы так, чтобы хорошо взаимодействовать со всеми другими на двух уровнях:
Сейчас в Массачусетском технологическом институте создали и систематизировали уже более 140 биокирпичей. Сложность заключается в том, что очень многие сконструированные фрагменты ДНК при внедрении в генетический код клетки-реципиента уничтожают её.
Синтетическая биология способна создать генинженерные бактерии, которые могут производить сложнейшие и дефицитные лекарства дёшево и в промышленных объёмах. Спроектированные геномы могут привести к появлению альтернативных источников энергии (синтез биотоплива) или к бактериям, которые помогут удалять излишний углекислый газ из атмосферы.
Корни синтетической биологии уходят в 1989 год, когда команда биологов из Цюриха под руководством Стивена Беннера (Steven Benner) синтезировала ДНК, содержащую две искусственных генетических буквы помимо четырёх известных (аденин, цитозин, гуанин и тимин), используемых всеми живыми организмами Земли.
Большинство учёных придерживается природных моделей; они пробуют создать клетки, которые окружены двухслойными мембранами и наполнены генетическим материалом в виде ДНК или РНК.
Некоторые сторонники синтетической биологии полагают, что все новые геномы, созданные учёными, должны становиться достоянием всего человечества и использоваться совершенно свободно, без прав какой-то отдельной группы на данные коды жизни.
Пэт Муни (Pat Mooney), директор канадской организации ETC Group, занимающейся вопросами биоэтики и опасности некоторых научных достижений для природы и общества, считает, что подобные исследования опасны, патент JCVI должен быть отозван, а все данные по этому геному закрыты.
Категории: Биоинформатика, Биотехнология, Биологическая кибернетика.
Текст доступен по лицензии Creative Commons Attribution-ShareAlike.wreferat.baza-referat.ru
Что такое «синтетическая биология»? Это новая и быстро развивающаяся отрасль молекулярной биологии, которая позволяет не только манипулировать с реальными генами и геномами, но и создавать совершенно новые последовательности ДНК и новые, никогда не существовавшие в природе биологические системы. Такие в прямом смысле сверхъестественные способности обязаны своим появлением стремительной эволюции молекулярных и компьютерных технологий, благодаря которым сегодня можно не только виртуально «сконструировать» любую генетическую последовательность, но и воплотить ее в жизнь. Так, еще в 2002 г. появился на свет первый полностью искусственный вирус, а еще через 8 лет – Синтия, первая жизнеспособная бактерия с полностью искусственным геномом. Эти достижения свидетельствуют о практически безграничных возможностях перепрограммирования ДНК, которые открывают не менее безграничные перспективы в самых разных областях науки и жизни, начиная от производства новых биотехнологических материалов до создания культурных растений с «улучшенным» фотосинтезом. Другое дело, что распорядиться этими «милостями не от природы» человечество должно с умом
 Сама идея синтетической биологии развивается «вокруг» геномной инженерии. За последние годы появились новые, крайне удобные молекулярные инструменты, с помощью которых можно каким угодно образом изменить геном практически любого организма. Да, это, может быть, дорого, можно при этом уткнуться в какую-то пока не известную проблему, но даже на текущем уровне развития технологий молекулярной биологии можно поэтапно за, условно говоря, «триллион долларов» слона превратить в мамонта, возродив этот прекрасный вымерший вид.
Сама идея синтетической биологии развивается «вокруг» геномной инженерии. За последние годы появились новые, крайне удобные молекулярные инструменты, с помощью которых можно каким угодно образом изменить геном практически любого организма. Да, это, может быть, дорого, можно при этом уткнуться в какую-то пока не известную проблему, но даже на текущем уровне развития технологий молекулярной биологии можно поэтапно за, условно говоря, «триллион долларов» слона превратить в мамонта, возродив этот прекрасный вымерший вид.
Другое дело, надо ли это делать? Ведь у синтетической биологии много других, намного более актуальных и важных задач, связанных, к примеру, с созданием средств диагностики, профилактики и лечения болезней человека, в том числе с применением персонализированного подхода, а также обеспечением продовольственной безопасности и повышения качества продуктов питания. Именно эти задачи легли в основу актуальных направлений исследований в рамках проекта САЕ «Синтетическая биология» Новосибирского государственного университета.
Когда речь зашла о заявке на прорывной проект от нашей САЕ, нам не пришлось долго думать: ее предметом стала разработка новых средств для геномного редактирования и их применение для направленного изменения человеческих клеток. Технологии геномного редактирования, появившись в последние несколько лет, произвели настоящую революцию как в науках о жизни, так и в практических областях, включая медицину, сельское хозяйство и промышленные биотехнологии. Без быстрого освоения подобных технологий Россия рискует оказаться в числе аутсайдеров.
Первый блок нашего проекта – фундаментальный – направлен на изучение процессов, происходящих в клетке в процессе ее «редактирования»; второй – на усовершенствование инструментов редактирования, включая разработку новых ферментов, способов доставки генетического материала и методов управления внутриклеточными процессами; третий – на получение практических результатов.
 Почему так важна эта первая, фундаментальная часть? Главная проблема геномного редактирования состоит в доступности и кажущейся легкости самой технологии, в результате чего темпы ее использования намного опередили темпы «понимания» ее механизмов. Целенаправленной модификацией генома любых организмов, от бактерий до человека, сейчас может заниматься практически любая хорошо оснащенная биологическая лаборатория. Однако не более двух десятков исследовательских групп в мире реально занимаются исследованием соответствующих молекулярных механизмов и клеточных процессов, пытаются разобраться, что в действительности происходит в клетке при редактировании генов. Говорят, что дьявол сидит в деталях. Недостаток понимания приводит к низкой эффективности, что приходится компенсировать деньгами. Условно говоря, сейчас, чтобы добиться поставленной цели, приходится буквально «тыкать наугад» и вместо десяти планшетов с клетками задействовать тысячу.
Почему так важна эта первая, фундаментальная часть? Главная проблема геномного редактирования состоит в доступности и кажущейся легкости самой технологии, в результате чего темпы ее использования намного опередили темпы «понимания» ее механизмов. Целенаправленной модификацией генома любых организмов, от бактерий до человека, сейчас может заниматься практически любая хорошо оснащенная биологическая лаборатория. Однако не более двух десятков исследовательских групп в мире реально занимаются исследованием соответствующих молекулярных механизмов и клеточных процессов, пытаются разобраться, что в действительности происходит в клетке при редактировании генов. Говорят, что дьявол сидит в деталях. Недостаток понимания приводит к низкой эффективности, что приходится компенсировать деньгами. Условно говоря, сейчас, чтобы добиться поставленной цели, приходится буквально «тыкать наугад» и вместо десяти планшетов с клетками задействовать тысячу.
Если говорить про самую популярную на сегодня систему геномного редактирования CRISPR/Cas9, то пока более-менее известно, и то не до конца, лишь как работает белок Cas9, который вносит разрыв в ДНК. В том числе не очень понятно, как этот фермент находит свою мишень в геноме, так как в пробирке Cas9 работает крайне неэффективно по сравнению с большинством других ферментов: реакция требует длительного времени и многократного избытка фермента по отношению к ДНК-мишени.
В ПЕРСПЕКТИВЕ – ИНСТИТУТ! В деятельность САЕ «Синтетическая биология» сейчас вовлечена практически вся биологическая часть факультета естественных наук НГУ. Одно из важнейших направлений работы – модернизация образования. В первую очередь это создание новых магистерских программ. Яркий пример – программа «Биотехнология», созданная под руководством заведующего лабораторией бионанотехнологии, микробиологии и вирусологии, чл.-корр. РАН С. В. Нетесова в сотрудничестве с ГНЦВБ «Вектор», Институтом химической и фундаментальной биологии СО РАН и Биотехнопарком Кольцово.
В мае 2016 г. началась работа по созданию магистерской программы «Структурная биоинформатика» под руководством заведующей лабораторией структурной биоинформатики и молекулярного моделирования НГУ А.Ю. Бакулиной. Эта деятельность оказалась настолько эффективной, что уже в сентябре были набраны первые магистранты, преимущественно выпускники механико-математического факультета НГУ. Междисциплинарный характер новых магистерских программ – не случайность, а одна из основных тенденций в развитии САЕ.
Обязательное условие программы САЕ – партнерство. НГУ всегда тесно взаимодействовал с СО РАН, но сейчас этого недостаточно. Очень важно привлечь к совместной работе представителей бизнеса, тем более что у нас есть такие соседи, как Технопарк Новосибирского академгородка и Биотехнопарк Кольцово. У нас много общих интересов в области науки и образования. Научное сообщество по-прежнему заинтересовано в повышении эффективности практического использования научных разработок. А представители бизнеса видят в НГУ источник квалифицированных кадров и готовы участвовать в разработке специализированных инжиниринговых магистерских программ. В результате САЕ должна стать неким сплавом науки, образования и бизнес-структур, привлекательным для студентов не только из нашей страны и ближнего зарубежья.
Сейчас мы занимаемся переоборудованием небольших учебных помещений, где будут располагаться лаборатории Центра перспективных биомедицинских исследований НГУ, а в более долгосрочных планах – создание при университете отдельного Института синтетической биологии
В деятельность САЕ «Синтетическая биология» сейчас вовлечена практически вся биологическая часть факультета естественных наук НГУ. Одно из важнейших направлений работы – модернизация образования. В первую очередь это создание новых магистерских программ. Яркий пример – программа «Биотехнология», созданная под руководством заведующего лабораторией бионанотехнологии, микробиологии и вирусологии, чл.-корр. РАН С. В. Нетесова в сотрудничестве с ГНЦВБ «Вектор», Институтом химической и фундаментальной биологии СО РАН и Биотехнопарком Кольцово.
В мае 2016 г. началась работа по созданию магистерской программы «Структурная биоинформатика» под руководством заведующей лабораторией структурной биоинформатики и молекулярного моделирования НГУ А.Ю. Бакулиной. Эта деятельность оказалась настолько эффективной, что уже в сентябре были набраны первые магистранты, преимущественно выпускники механико-математического факультета НГУ. Междисциплинарный характер новых магистерских программ – не случайность, а одна из основных тенденций в развитии САЕ.
Обязательное условие программы САЕ – партнерство. НГУ всегда тесно взаимодействовал с СО РАН, но сейчас этого недостаточно. Очень важно привлечь к совместной работе представителей бизнеса, тем более что у нас есть такие соседи, как Технопарк Новосибирского академгородка и Биотехнопарк Кольцово. У нас много общих интересов в области науки и образования. Научное сообщество по-прежнему заинтересовано в повышении эффективности практического использования научных разработок. А представители бизнеса видят в НГУ источник квалифицированных кадров и готовы участвовать в разработке специализированных инжиниринговых магистерских программ. В результате САЕ должна стать неким сплавом науки, образования и бизнес-структур, привлекательным для студентов не только из нашей страны и ближнего зарубежья.
Сейчас мы занимаемся переоборудованием небольших учебных помещений, где будут располагаться лаборатории Центра перспективных биомедицинских исследований НГУ, а в более долгосрочных планах – создание при университете отдельного Института синтетической биологии
к. х. н. П. Е. Воробьев
Следующий шаг при геномном редактировании – внесение в клетку нового генетического материала, который предполагается встроить в разрыв ДНК. На сегодня процесс генетической рекомбинации (перестройки ДНК) на основе такого нового искусственного олигонуклеотида – это настоящий «черный ящик». В принципе мы уже довольно много знаем о механизмах рекомбинации у человека, но только в «штатных» ситуациях. И знаем, что хотя рекомбинация при формировании половых клеток или при репарации («ремонте») поврежденной ДНК идет по одной и той же принципиальной схеме, детали этих механизмов совершенно различны. Чтобы разобраться в механизмах рекомбинации при геномном редактировании, узнать, насколько в них задействована система обычной рекомбинации, а насколько какие-то новые элементы, потребуется еще лет двадцать.
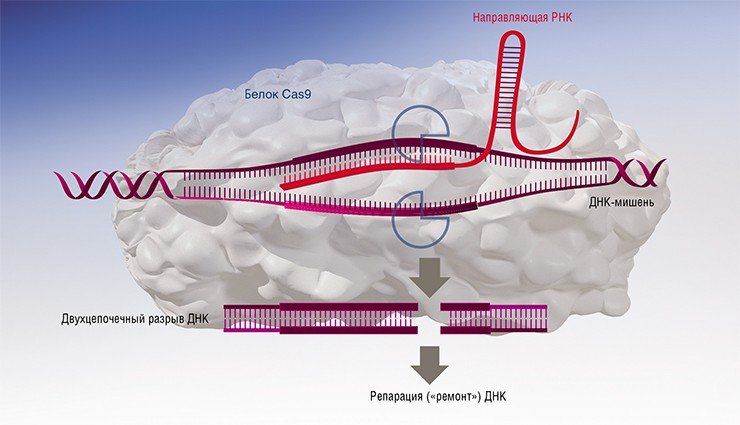
Но зато когда мы сможем во всем этом разобраться, то получим возможность регулировать сам путь, по которому идет редактирование. Как известно, целью обычно является выключение гена или изменение его функции. Выключить проще, потому что в данном случае достаточно внести разрыв, который клетка «заштопает», обычно с ошибками. Причем клетка предпочтет этот простой путь и тогда, когда мы планируем провести замену фрагмента с рекомбинацией: клеточные системы в этом случае «норовят» не заменить, а выключить мишень. Сейчас многие исследователи работают над решением этой проблемы, начиная с таких простых вещей, как ингибирование ферментов, которые в этом процессе участвуют. Например, оказалось, что один из таких ферментов ингибируется обычным кофеином, и если клетки получают такую «дозу», рекомбинация идет лучше.
Что касается усовершенствования инструментария редактирования генома, то я вижу здесь два принципиальных пути. Во-первых, можно каким-то образом модифицировать и улучшать уже известные ферменты, такие как Cas9. Структура этих белков хорошо изучена, и можно вносить в нее мутации для повышения их точности или эффективности. Кроме того, в качестве адресующих структур, которые ищут и распознают нужный фрагмент гена, можно использовать не обычные направляющие РНК, а модифицированные нуклеиновые кислоты, благодаря которым можно повысить скорость или точность поиска мишени. В нашем проекте над этой задачей будет работать группа под руководством чл.-кор. РАН Д. В.Пышного.
Второй путь – поиск принципиально новых способов геномного редактирования. Мы сейчас довольно много знаем о том, как белки взаимодействуют с ДНК, более того, с конца прошлого века накопилось довольно много описаний интересных феноменов в этой области, которые в то время были непоняты и не объяснены. Например, было обнаружено, что в клетках с определенной эффективностью будут происходить мутации и геномные замены даже в том случае, если их просто обработать олигонуклеотидами! Сейчас в наших руках есть все необходимые технологии, чтобы исследовать процессы, которые при этом происходят.
Ценность всех наших исследований, включая фундаментальные, еще и в том, что их результаты могут стать основой новых технологий, не подпадающих под уже имеющиеся патенты. Дело в том, что вся область геномного редактирования сейчас полностью «покрыта» патентами людей, которые эти технологии создали и чье финансирование исчисляется миллиардами долларов. В этом смысле нам с ними тягаться бесполезно – выгоднее попытаться найти собственные обходные пути.
Практическим выходом наших работ должен стать не возрожденный мамонт, на которого в любом случае денег не хватит, а вполне реальные новые клеточные линии, которые могут быть использованы в различных фармакологических исследованиях для поиска лекарств против таких широко распространенных заболеваний, как грипп, болезнь Паркинсона и рак молочной железы.
САЕ представляют собой своего рода научно-образовательные консорциумы, объединяющие многих участников. В случае «Синтетической биологии» партнерами НГУ стали все институты биологического профиля Сибирского отделения РАН, а также Сколковский институт науки и технологий (Москва), где работает один из лучших в России специалистов по геномному редактированию, профессор К. В. Северинов. Были привлечены и давние партнеры из Университета Париж-XI, специализирующегося на точных науках, который станет частью «суперуниверситета», создаваемого на основе нескольких парижских и провинциальных вузов в рамках французской академической реформыНапример, сегодня наиболее подходящей моделью для поисков и тестирования лекарств от гриппа считаются не лабораторные мыши, которые от него гибнут, а гораздо более крупные и требовательные животные – хорьки. У этих животных клетки легочного эпителия схожи с человеческими, поэтому они в высшей степени восприимчивы к вирусу гриппа человека и издавна используются фармакологами. Если нам удастся при помощи геномного редактирования создать линии человеческих клеток с разной чувствительностью к вирусам гриппа, это намного упростит поиск соответствующих лекарств.
 Еще одна подзадача – получение клеточных линий для тестирования токсичности новых химических соединений, которых ежегодно синтезируется сотни тысяч. Все эти вещества необходимо тестировать на безопасность для человека, для чего обычно предпочитают использовать лабораторных животных. Дело в том, что при тестировании на токсичность традиционно предпочитают «перебдеть, чем недобдеть», а результаты, полученные на стандартных клеточных линиях, обычно искажают показания в сторону меньшей токсичности по сравнению с данными, полученными на животных. Действительно, отдельные клетки оказываются более устойчивыми к негативным воздействиям, так как в организме, как правило, есть свое «слабое звено» – небольшие клеточные популяции особо «ранимых» клеток (например, стволовых), которые и будут определять устойчивость всей особи. Так как сейчас движение за отказ от использования животных в подобных исследованиях набирает обороты, новые генетически модифицированные линии клеток с повышенной восприимчивостью смогут стать адекватной заменой.
Еще одна подзадача – получение клеточных линий для тестирования токсичности новых химических соединений, которых ежегодно синтезируется сотни тысяч. Все эти вещества необходимо тестировать на безопасность для человека, для чего обычно предпочитают использовать лабораторных животных. Дело в том, что при тестировании на токсичность традиционно предпочитают «перебдеть, чем недобдеть», а результаты, полученные на стандартных клеточных линиях, обычно искажают показания в сторону меньшей токсичности по сравнению с данными, полученными на животных. Действительно, отдельные клетки оказываются более устойчивыми к негативным воздействиям, так как в организме, как правило, есть свое «слабое звено» – небольшие клеточные популяции особо «ранимых» клеток (например, стволовых), которые и будут определять устойчивость всей особи. Так как сейчас движение за отказ от использования животных в подобных исследованиях набирает обороты, новые генетически модифицированные линии клеток с повышенной восприимчивостью смогут стать адекватной заменой.
Если мы не выиграем конкурс прорывных проектов, это не означает, что вся наша деятельность в области геномного редактирования прекратится. Исследования, безусловно, будут развиваться, только меньшими темпами.
Уже в рамках текущего финансирования мы создали новую структуру под названием «Центр перспективных биомедицинских исследований», которая объединит шесть университетских лабораторий, имеющих отношение к геномному редактированию. И хотя на какие-либо фантастические результаты в этом случае рассчитывать не приходится, но, опираясь на интеллектуальные и материальные ресурсы институтов СО РАН, мы способны создать, возможно, лучший в России центр в этой области.
В этом смысле конкурентов у нас немного, за исключением того же Сколково, отечественных научных групп, занимающихся фундаментальными работами по геномному редактированию, очень мало.
Д.б.н., профессор РАН Д. О. Жарков

Среди всех участников САЕ НГУ «Синтетическая биология» мне хотелось бы в первую очередь отметить лабораторию структурной биоинформатики и молекулярного моделирования НГУ, возглавляемую А. Ю. Бакулиной, с которой мы поддерживаем тесное сотрудничество. Занимается она разработкой и применением технологий компьютерного моделирования применительно к биологическим макромолекулам – я считаю это направление одним из самых важных в современной синтетической биологии.
Традиционный подход в создании новых соединений состоит в том, что проводится много синтезов, получают массу вариантов, а из них уже выбирают подходящие. Благодаря же расчетным технологиям мы сначала можем спрогнозировать свойства будущего соединения, «спроектировать» его, а уже потом его создавать. То есть исследователь может заранее просчитать и оценить результат. Значимость этого трудно переоценить, когда речь идет о таких сложных молекулах, как производные олигонуклеотидов (коротких фрагментов нуклеиновых кислот), и вы хотите, к примеру, знать, будут ли они адекватно соответствовать структуре двойной спирали ДНК по размеру, прочности и другим структурным характеристикам.
Конкретная задача, которой занимаются физики из нашей лаборатории биомедицинской химии, – отработка методик и расчетов, которые лягут в основу таких компьютерных алгоритмов. И хотя полностью она еще не решена, успехи уже есть.
Нужно сказать, что технологии молекулярного докинга (метода молекулярного моделирования, позволяющего предсказать ориентацию и положение молекул, наиболее выгодные для образования устойчивого комплекса) в мире сейчас очень популярны, и в первую очередь в связи с поиском и созданием новых лекарственных соединений. Например, с помощью этих компьютерных технологий можно отобрать молекулы, способные с высокой эффективностью связываться с определенным участком белка-фермента и тем самым блокировать его работу.
Такие технологии, безусловно, нужно развивать, причем в более «глобальном» формате. Под последним я подразумеваю обращение к олигомерам (молекулам в виде цепочки из небольшого числа однотипных составных звеньев), тогда как в случае традиционного докинга речь идет, как правило, о низкомолекулярных соединениях. В качестве таких «среднемолекулярных» соединений могут выступать не только стандартные олигонуклеотиды, но и любые другие искусственно созданные молекулярные блоки в виде самых разных олигомерных цепочек. И в этом случае на первый план выходит компьютерное моделирование, так как число вариантов при этом резко возрастает.
Что касается химических методов получения искусственных олигомеров, то технический базис для этого у нас уже имеется. Хотя пока мы используем эти технологии с целью повысить функциональность тех же олигонуклеотидов для придания им дополнительной гидрофобности, введения репортерной метки и т. п. Ведь в этой области также есть еще много нерешенных вопросов, таких как доставка соединений в живые клетки. К примеру, для этой цели часто используется вариант, когда к олигонуклеотиду присоединяют специальные химические группировки (например, остаток холестерина), но это не всегда оправданно и эффективно. А ведь для модификации олигонуклеотидов можно использовать те же самые дополнительные ненуклеотидные цепочки, звенья которых сами по себе будут играть роль функциональных группировок с нужными свойствами.
Этот подход в перспективе может привести к созданию нового типа олигомерных агентов ненуклеотидной природы, для которых будет характерно огромное потенциальное разнообразие функциональных свойств отдельных звеньев, вероятно, даже большее, чем в случае использования аминокислот. И, конечно, есть задумка когда-нибудь окончательно отказаться от олигонуклеотидов и создать на основе уже хорошо «проработанной» нуклеотидной химии что-то совершенно новое вроде мультифункциональных олигомеров.
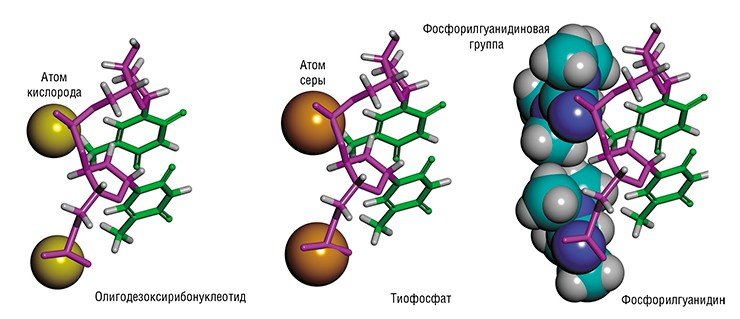
В качестве примера практических результатов в области синтетической биологии хочу привести фосфорилгуанидины – созданные в ИХБФМ СО РАН новые химические аналоги нуклеиновых кислот, прикладными приложениями которых сейчас активно занимаются в лаборатории химии нуклеиновых кислот (руководитель к. х. н. Д. А. Стеценко) и в нашей лаборатории биомедицинской химии.
В фосфорилгуанидинах – искусственных аналогах нуклеиновых кислот – «мостиками» между звеньями-нуклеотидами служат не отрицательно заряженные фосфатные группы, а «нейтральные» фосфорилгуанидиновые. Такая химическая трансформация облегчает им проникновение сквозь липидные мембраны живых клеток, придает устойчивость к разрушающему действию ферментов и способность образовывать прочные комплексы с клеточными ДНК и РНК. Благодаря этим свойствам фосфорилгуанидиновые олигонуклеотиды могут стать основой для создания средств медицинской диагностики и лекарственных препаратов нового поколенияТак, совместно с британскими учеными уже подана заявка на патент на использование этих соединений при терапии тяжелого генетического заболевания – мышечной дистрофии Дюшенна, которая приводит к полной потере способности двигаться и в итоге к смерти. Причина болезни – мутация, следствием которой служит нарушение процесса сплайсинга (вырезания фрагментов) при созревании информационной РНК, в результате чего в клетках синтезируется «неправильный» белок дистрофин, являющийся важным структурным компонентом мышечной ткани.
Корректировать этот патологический процесс можно с помощью олигонуклеотидов, и, как показали исследования на лабораторных животных, для этой цели хорошо подходят наши фосфорилгуанидины. Последние работают не хуже, чем морфолиновые олигомеры, совсем недавно разрешенные в США к практическому применению. В обоих этих случаях был реализован один и тот же принцип, хотя и на разных платформах. Конечно, такая терапия означает пожизненные уколы, но альтернативным вариантом является лишь редактирование генома, которое на сегодняшний день недоступно, хотя и становится все более реальным с течением времени.
На основе фосфорилгуанидинов можно создавать противобактериальные препараты нового поколения. Идея в том, что обычный антибиотик является низкомолекулярным соединением, к которому бактерии довольно быстро вырабатывают устойчивость. В случае же олигонуклеотидов и их аналогов, являющихся ген-направленными соединениями, мы воздействуем непосредственно на первопричину, т.е. на геном возбудителя. Работы по созданию таких антибиотиков, к которым бактериям не так просто выработать устойчивость, уже ведутсяСегодня мы сконцентрировались на еще одном очень важном практическом применении фосфорилгуанидинов – диагностике заболеваний. Есть тип диагностических сенсоров на основе полупроводниковых нанопроволок, работающих по принципу полевых транзисторов. Проводимость такого нанопроводника меняется, когда на его поверхности появляется заряд. Молекула же фосфорилгуанидинового олигонуклеотида, в отличие от обычного, сама по себе не имеет заряда. Иммобилизованный на поверхности проводника, такой олигонуклеотид способен специфично связаться с заряженной РНК-мишенью – нуклеотидным маркером того или иного заболевания. При этом детекция сигнала с проводника будет идти лишь в случае успешного связывания с мишенью, несущей электрический заряд. В экспериментах, проводимых совместно с новосибирским Институтом физики полупроводников им. А. В. Ржанова СО РАН было доказано, что с помощью сенсора, на который «посажены» производные фосфорилгуанидинов, можно действительно без дополнительных меток получать прямой диагностический сигнал.
Возвращаясь к технологиям компьютерного моделирования, напомню, что в состав «Центра перспективных биомедицинских исследований», созданного в НГУ в рамках САЕ «Синтетическая биология», войдет новая лаборатория белковой инженерии. Как видно из названия, она будет заниматься созданием новых ферментов и других белков с измененными свойствами, которые предполагается использовать для нужд биотехнологии либо в качестве терапевтических препаратов или молекулярных инструментов. Ведь виртуально «спроектировав» и изучив ту или иную нужную белковую молекулу, нужно затем обратиться к методам генной инженерии, чтобы начать ее реально производить. То есть встает конкретная задача синтезировать соответствующие генные последовательности – искусственные гены.
Чтобы «собрать» один такой ген, требуется в определенном порядке соединить несколько сотен искусственно синтезированных нуклеотидных цепочек! Отмечу, что в России подобных технологий практически нет, как нет и научных коллективов, которые занимаются этой проблематикой. Исключением служит группа к. х. н. А. Н. Синякова из нашей лаборатории, которая добилась немалых успехов в разработке методов синтеза олигонуклеотидов на поверхности специальных чипов – небольших кремниевых пластинок со множеством ячеек, где можно одновременно синтезировать большое число нуклеотидных последовательностей разного состава.
Наши исследователи совместно со специалистами из Института физики полупроводников им. А. В. Ржанова и Института автоматики и электрометрии СО РАН разработали и уже апробировали чиповую технологию синтеза олигонуклеотидов, основанную на использовании фотолабильных защитных групп или фотогенераторов кислот. В дальнейшем набор этих олигонуклеотидов подвергают ряду специальных обработок, чтобы в итоге получить целевую генную последовательность.
Заметим, что поскольку технологии эффективного синтеза искусственной ДНК открывают новые возможности не только в промышленности, медицине и сельском хозяйстве, но и в создании биологического оружия, в мире предпринимаются практические действия по ограничению их распространения. Это означает, что подобные установки в нашу страну экспортироваться не будут. Создание же отечественного микрочипового синтезатора – это наш реальный шаг к созданию искусственных генов, что является одним из краеугольных камней синтетической биологии. А от этого недалеко и до создания искусственных живых клеток, а в более отдаленной перспективе – и целых организмов.
Член-кор. РАН, д.х.н. Д. В. Пышный

Научно-исследовательское подразделение по исследованию защитных репарационных систем, которым я руковожу в рамках САЕ «Синтетическая биология» НГУ, фактически состоит из тех сотрудников трех лабораторий Института химической биологии и фундаментальной медицины СО РАН, которые наиболее тесно сотрудничают с университетом, – моей лаборатории биоорганической химии ферментов, лаборатории исследования модификации биополимеров (руководитель – д. х. н. О. С. Федорова) и лаборатории ферментов репарации (руководитель – д. х. н. Г. А. Невинский).
Мы занимаемся фундаментальными исследованиями систем репарации ДНК, результаты которых важны для понимания механизмов старения и могут стать основой для конструирования ингибиторов ферментов репарации («ремонта») ДНК, представляющих интерес для медицины. Все эти работы основаны на междисциплинарном сотрудничестве, которое раньше поддерживалось специальными интеграционными проектами СО РАН, а теперь переместилось на площадку университета. Этому очень важному вопросу посвятил свой доклад ректор НГУ, чл.-корр. РАН М. П. Федорук на последней научной сессии Общего собрания СО РАН. Он назвал такой переход новым вектором развития Новосибирского академгородка. САЕ позволяет не только более эффективно организовать междисциплинарное сотрудничество, но и активно включать в исследования студентов и магистров НГУ.
Возвращаясь к системам репарации ДНК, нужно сказать, что сейчас мы отчетливо понимаем, что все белки репарационной системы, ответственной за исправления повреждений ДНК, представляют собой потенциальные мишени для лекарственных препаратов. Универсальной мишенью является, к примеру, ядерный белок поли(АДФ-рибоза)-полимераза 1 (PARP1) – важнейший регулятор репарации ДНК, ингибирование которого может дать выраженный эффект при онкологических заболеваниях, а также ишемическом инсульте и других патологиях.
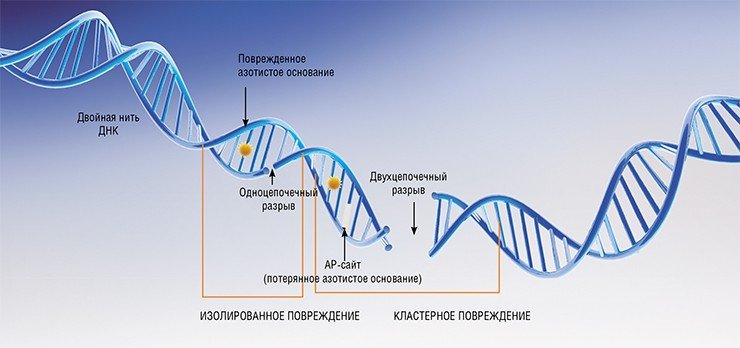
PARP1 является «сенсором» повреждений ДНК: он первым распознает ее разрывы и присоединяется к этим местам, начиная активно синтезировать олиго- или поли(АDP)-рибозные цепочки, которые ковалентно связываются с разными акцепторными белками и в том числе с самой PARP1. В результате в месте разрыва происходит деконденсация хроматина, что облегчает доступ ферментов репарации. Таким образом, PARP1 способствует восстановлению повреждений ДНК, в том числе и в раковых клетках при традиционной химио- или радиотерапии, что отрицательно сказывается на эффективности лечения.
Что касается случаев нарушения мозгового кровообращения в результате ишемии, то при множественных повреждениях генома гиперактивация PARP1 приводит к быстрому истощению имеющихся в них энергетических запасов в виде молекул АТФ, что чревато необратимой гибелью нейронов.
Идея ингибировать в подобных ситуациях активность PARP1 как универсального регулятора процессов репарации на первый взгляд представляется очень привлекательной. Но не надо забывать, что этот фермент является многофункциональным белком, и, как показывают многочисленные исследования, подавляя его репарационную активность, мы одновременно подавляем и другие его функции. Сегодня на основе ингибитора PARP-1 выпускается лекарство олапариб (линпарза), которое применяется для лечения некоторых видов рака, включая рак яичника. Тем не менее его рекомендовано применять с осторожностью из-за большого числа нежелательных побочных эффектов.
Поэтому в своих исследованиях мы работаем не только с этой универсальной, но и с другой, специфической мишенью – ферментом репарации тирозил-ДНК-фосфодиэстеразой 1 (Tdp1).
Дело в том, что в клетке существуют ферменты топоизомеразы, участвующие в динамичном поддержании определенной конформации двойной спирали ДНК. Топоизомеразы типа I вносят разрыв в цепь ДНК, ковалентно соединяясь с одним из его концов, после чего в дальнейшем происходит восстановление цепи. Противораковые препараты на основе камптотецина стабилизируют продукты этого ковалентного присоединения, не давая «залатать» повреждение, вносимое топоизомеразой, в результате чего опухолевая клетка погибает. Однако Tdp1 способен «снимать» эту стабилизацию, поэтому использование ингибиторов этого фермента даст возможность усилить эффективность основной противоопухолевой терапии.
Эта работа выполняется нами совместно с лабораторий физиологически активных веществ Новосибирского института органической химии им Н. Н. Ворожцова СО РАН (руководитель – д. х. н. Н. Ф. Салахутдинов), а также с группой к.б.н. Н. А. Поповой из Инстититута цитологии и генетики СО РАН. В экспериментах на лабораторных животных с привитой опухолью благодаря применению самого эффективного из разработанных ингибиторов удалось добиться значительного (до 50 %) уменьшения основной опухоли и практически полного исчезновения метастазов. Сейчас мы пытаемся получить финансирование для проведения уже клинических испытаний этого перспективного противоракового препарата.
И конечно, нужно отметить такое очень важное направление, как геномное редактирование с использованием системы CRISPR/Cas9, с помощью которого можно «выключать» сами гены, отвечающие за возникновение болезней. На этом переднем крае науки мы отстаем, тогда как в Европе и США уже создано множество коммерческих фирм, где эти технологии используются для создания нужных мутаций в целевых генах. Тем не менее, совершенно необходимо продолжать заниматься научно-исследовательскими разработками, которые повысят эффективность этого подхода.
Сегодня НГУ является не только «питомником» будущих исследователей – в его рамках активно идет развитие исследовательских структур. На мой взгляд, именно на таких университетских площадках и нужно создавать возможности для формирования новых научных подразделений под руководством перспективных молодых ученых. Почему, чтобы получить мегагранты, нам сегодня нужно приглашать специалистов из-за рубежа, зачастую наших бывших соотечественников, которые уже не могут там работать в силу своего возраста? В это же время лучшие представители нашей научной молодежи, не получая достаточного финансирования для своих работ, вынуждены искать себе место за границей. Почему мы не поддерживаем молодые таланты, которые выросли в нашей стране? Или мы собираемся вернуть их, когда они достигнут пенсионного возраста? Такой подход выглядит очень странным. Обратная сторона этого явления – невозможность пригласить на длительный срок молодого зарубежного специалиста, как это делается во всем мире. Сегодня нельзя организовать долгосрочную визу, рабочее место больше, чем на два-три месяца. В результате у нас нет нормального обмена молодыми кадрами с зарубежными лабораториями, и «зеленый свет» реально дан лишь в одну сторону – за границу. Поэтому и средства, которые наша страна вкладывает в образование, «отрабатывают» не у нас, а за рубежом. Эту проблему также пока никто не собирается серьезно решать. То же самое можно сказать и о многих других проблемах, связанных с обеспечением эффективности отечественных научных исследований (трудности с заказами реактивов и их своевременной поставкой из-за рубежа, непомерно высокие цены и т. д.). Надо начинать с фундамента – подвиги не могут длиться десятилетиямиВ рамках САЕ «Синтетическая биология» мы будем сотрудничать с НГУ как раз в этом направлении, конкретно – с лабораторией геномных технологий, которой заведует д.б.н. Д. О. Жарков. Одна из задач, решением которой будет заниматься к.х.н. Н.А. Кузнецов, касается исследования детальной кинетики функционирования белковых комплексов именно в этой системе геномного редактирования. Другими словами, предстоит изучить, как в термодинамическом режиме происходит на ДНК сборка комплекса CRISPR/Cas9 из отдельных компонентов. Это будет по-настоящему пионерная работа, так как в современном мире зачастую больше обращают внимание на конечный результат, а не на особенности самого процесса, что неправильно, так как понимание механизма помогает усовершенствовать практические технологии.
CRISPR/Cas9 – это, действительно, очень хороший инструмент для исследовательских и, безусловно, медицинских целей. В то же время нужно отдавать себе отчет, что результат не всегда будет однозначным, по крайней мере, не для всех болезней. Например, за возникновение раковых опухолей отвечает не один ген, поэтому попасть «в яблочко» в таких случаях не так просто. При своем появлении каждый новый метод всегда вызывает только восторженные отклики, но чем больше его применяют, тем больше вскрывается недостатков. Поэтому понимание механизмов, лежащих в его основе, будет далеко не лишним.
К примеру, разрыв нити ДНК в процессе «редактирования» – результат работы белка Cas9, может «залатываться» системами репарации, которыми мы занимаемся. Кстати, любой разрыв в ДНК очень эффективно распознает как раз та самая, интенсивно нами изучаемая PARP1. Этот фермент может влиять на процесс направленной модификации гена-мишени, так как он участвует в регуляции системы «ремонта» двойных разрывов нитей ДНК и влияет на соотношение процессов негомологичной и гомологичной рекомбинации. Поэтому исследования систем репарации очень важны для повышения эффективности работы систем редактирования генома, которые играют столь большую роль в современной синтетической биологии.
Член-кор. РАН, д.х.н. О. И. Лаврик
Литература
Власов В. В., Жарков Д. О., Пышный Д. В. Приручение древней молекулы // НАУКА из первых рук. 2014. № 3—4. С. 84—91.
Купрюшкин М. С., Пышный Д. В., Стеценко Д. А. Фосфорилгуанидины. Новый класс аналогов нуклеиновых кислот // Acta Naturae. 2014. Т. 6. № 4(23). С. 53—55.
Немудрый А. А., Валетдинова К. Р., Медведев С. П., Закиян С. М. Системы редактирования геномов TALEN и CRISPR/Cas – инструменты открытий // Acta Naturae. 2014. Т. 6. № 3. С. 20—42.
Пышный Д. В., Cтеценко Д. А. Фосфорилгуанидины – новые химические аналоги нуклеиновых кислот. // Наука из первых рук. 2014. № 5. C. 6—9.
Ширяева А. А., Северинов К. В. Системы CRISPR/Cas бактерий и архей. Как компоненты адаптивной иммунной системы прокариот стали универсальным и эффективным инструментом модификации геномов, исследования эпигеномов и управления транскрипцией генов? / Редактирование генов и геномов. Ред. С. М. Закиян, С. П. Медведев, Е. В. Дементьева, В. В. Власов Новосибирск: Издательство СО РАН, 2016. С. 133—169.
Barrangou R., Doudna J. A. Applications of CRISPR technologies in research and beyond // Nat. Biotechnol. 2016. V. 34. N. 9. P. 933—941.
scfh.ru
Эволюционное учение представляет собой крупнейшее теоретическое обобщение в современной биологии. Под биологической эволюцией понимают необратимый, поступательный и закономерный процесс исторического развития живой природы (начиная с момента абиогенного возникновения первых живых организмов на Земле до настоящего времени). В результате биологической эволюции на нашей планете возникло многообразие видов живых организмов и произошло возникновение биосоциального существа — человека.
Идеи о естественном происхождении живых существа, об их изменчивости существовали уже в трудах античных авторов. Правда, представления древних философов носили чисто умозрительный характер, отличались фрагментарностью и незавершенностью, нередко включая элементы очевидной фантазии.
С эпохи Возрождения начинается период бурного развития биологии, происходит накопление огромного фактического материала. Благодаря многочисленным географическим открытиям пополняются списки видов животных и растений, известных науке; расширяются представления о многообразии живых организмов. В этот период биология вооружается сравнительным и экспериментальными методами исследования, возникает микроскопия. Все это обусловило появление принципа градации, т.е. системы классификации живых организмов по степени их организационной сложности, что воплощалось в построение «лестниц существ» или «лестниц естественных тел». Так, Ш. Бонне в середине XVIII в. предложил свой вариант «лестницы», которая начинается с «тел неживой природы» — воздуха и воды. На следующих ступенях последовательно располагаются: металлы, камни, грибы, растения, насекомые, черви, рыбы, птицы, млекопитающие, обезьяны и человек. Ш. Бонне, как и многие другие авторы подобных построений, не связывал свою конструкцию с идеей о развитии природы. Речь шла лишь о градации «естественных тел».
В конце XVIII в. в биологии и философии получает распространение трансформизм: представление об изменении и превращении форм организмов, происхождении одних от других. Трансформизм сыграл прогрессивную роль в развитии естествознания, т.к. противостоял креационистским представлениям. Но в воззрениях трансформистов еще отсутствует идея эволюционизма, т.е. исторического (поступательного) процесса развития живой природы.
В начале XIX в. появляются первые эволюционные теории. Особое значение для дальнейшего развития эволюционной идеи имела теория Ж-Б. Ламарка (1809), в которой, помимо утверждения и обоснования идеи исторического развития живого, делается попытка объяснения причин и движущих сил эволюционного процесса. Отсылая читателя к школьному курсу общей биологии, где достаточно подробно излагается теория Ламарка, отметим лишь принципиально важные идеи, высказанные этим ученым. Вскрывая механизмы эволюции, Ламарк утверждал, что всем живым организмам свойственна изменчивость, которая проявляется в результате действия разнообразных факторов внешней среды. Наряду с этими рациональными и продуктивными идеями, в теории Ламарка содержались иррациональная идея о «внутреннем стремлении организмов к совершенствованию» и ошибочные утверждения («изменение органов в результате их упражнения или неупражнения», постулирование наследования приобретенных признаков). Тем те менее, теория Ж-Б. Ламарка получила широкое признание ученых XIX в., т.к. в ней утверждался принцип исторического развития органического мира и была предпринята попытка дать материалистическое объяснение механизмов эволюционного процесса. Историческая роль теории Ламарка заключается в том, что это была первая эволюционная теория. В ней содержались идеи, воспринятые и получившие развития в трудах других исследователей. Нетрудно заметить преемственность идей об изменчивости организмов и роли окружающей среды в эволюционном процессе в ряду:
Теория Ж-Б. Ламарка ® Теория Ч. Дарвина ® Синтетическая Теория Эволюции.
Крупнейшим событием в науке явилось появление научной теории исторического развития живой природы — эволюционной теории Ч. Дарвина (1859). Заслуга Дарвина заключается в том, что ему удалось, определив движущие силы эволюционного процесса, вскрыть его сущность и выстроить убедительную систему доказательств эволюции. Эта система представляет собой результат обобщения огромнейшего фактического материала не только биологии, но и других естественных и прикладных наук, социологии, демографии.
Выделим основные положения эволюционной теории Дарвина.
1. Искусственный отбор как движущий фактор происхождения и выведения новых сортов культурных растений и пород домашних животных. Разработка этой проблемы сыграла огромное значение для формирования идеи естественного отбора, являющейся центральным ядром дарвинизма.
2. Наличие у живых организмов определенной (ненаследственной) и неопределенной (наследственной) изменчивости. Исключительное значение наследственной изменчивости в эволюции живых организмов.
3. «Борьба за существование...», как писал сам Ч. Дарвин: «… в широком и метафорическом смысле, включая сюда зависимость одного существа от другого, а также подразумевая (что еще важнее) не только жизнь одной особи, но и успех ее в обеспечении себя потомством». Борьба за существование вытекает из геометрической прогрессии размножения организмов и многочисленных препятствий, сдерживающих неограниченное размножение. Дарвин особо подчеркивал, что «борьба за существование особенно упорна, когда она происходит между особями и разновидностями того же вида».
4. «Естественный отбор или переживание наиболее приспособленных», как «… сохранение полезных индивидуальных различий или изменений и уничтожение вредных». Дарвин считал, что «… естественный отбор действует только путем сохранения и накопления малых наследственных изменений, каждое из которых выгодно для сохраняемого существа».
5. Наследственная изменчивость, борьба за существование и естественный отбор — главные движущие силы, приводящие к образованию новых видов за счет «расхождения признаков». Первоначально «расхождение признаков» проявляется в возникновении разновидностей внутри старого вида, а по мере углубления различий происходит возникновение двух (или больше) новых видов (принцип дивергенции).
6. Естественный отбор служит причиной приспособленности видов, целесообразности строения и функций организмов. Другими словами: эволюция носит приспособительный характер. Органическая целесообразность универсальна (т.е. приспособленность присуща всем живым организмам, на всех стадиях их индивидуального развития), но она относительна, т.к. при изменении условий окружающей среды приспособленность организма в новых условиях не будет им соответствовать (например, задержка в выпадении снега с наступлением зимы, ставит в «сложное положение» животных, сменивших свой летний «наряд» на зимний — заяц-беляк и т.п.). Резкие климатические изменения на значительных территориях нашей планеты нередко приводили к вымиранию множества видов живых организмов (о чем свидетельствуют геологическая и палеонтологическая летописи).
7. Прогресс в развитии органического мира. Сущность прогрессивной эволюции заключается в том, что в каждую историческую эпоху среди форм, хорошо адаптированных к существующим условиям среды, появляются формы, обладающие принципиально новыми и более сложными типами строения. По данным палеонтологической летописи, с течением времени одни доминирующие группы организмов сменялись (или дополнялись) другими, имеющими более высокий уровень организации, чем их предшественники (таблица 13.3)
Таблица 13.3
| Эра | Растения | Позвоночные животные |
| Палеозой | Папоротники | Рыбы |
| Мезозой | Голосеменные | Динозавры и другие рептилии |
| Кайнозой | Покрытосеменные | Млекопитающие |
Последовательная смена доминирующих форм базируется не на частных адаптациях, а на приспособлениях более широкого характера, дающих организмам общие преимущества в борьбе за существование и являющихся признаками прогресса, определяющих группы. Накопление таких приспособлений и обеспечивает поступательный ход прогрессивной эволюции.
Теория эволюции Ч. Дарвина, охватив важнейшие проблемы биологии и дав им убедительное общее решение, послужила мощным толчком и заложила основы для дальнейшего развития биологии. Эта теория имеет неоспоримое мировоззренческое значение. Идеи эволюционизма распространились далеко за пределы биологии, проникли в другие области естествознания. Дарвинизм сегодня представлен Синтетической Теорией Эволюции (СТЭ), сложившейся к 40-м годам прошлого (ХХ) столетия.
СТЭ является непосредственным продолжением и развитием теории Дарвина. Взяв ее за основу, развив основные дарвинистские представления на базе достижений современных биологических наук и дисциплин (генетика, цитология, экология, молекулярная биология, биология развития и др.), СТЭ устранила некоторые недостатки теории Дарвина, обогатила ее новыми фактами, дополнила некоторыми важными идеями. Центральным ядром СТЭ, по-прежнему (как и у Дарвина), является идея о единстве происхождения и непрерывной эволюции живых организмов, о творческой роли естественного отбора.
В 1984 г. основные положения СТЭ были сведены Н.Н. Воронцовым в 11 постулатов. Рассмотрим эти постулаты.
1. Материалом для эволюции служат, как правило очень мелкие, однако дискретные изменения наследственности — мутации. Мутационная изменчивость поставляет материал для естественного отбора и носит случайный характер.
2. Ведущим движущим фактором эволюции является естественный отбор, основанный на селекции случайных и мелких мутаций. Отсюда наименование теории отбора — «селектогенез».
3. Наименьшая эволюционная единица — популяция, а не особь (как у Дарвина).
4. Эволюция в основном носит дивергентный характер, т.е. один вид (таксон) может стать предком нескольких дочерних видов (таксонов), но каждый вид имеет единственный предковый вид, единственную предковую популяцию.
5. Эволюция носит постепенный и длительный характер. Видообразование мыслится как поэтапная смена одной временной популяции чредой последующих временных популяций.
6. Вид состоит из множества соподчиненных морфологически, физиологически и генетически отличных, но репродуктивно не изолированных единиц — подвидов, популяций. Эта концепция носит название концепции широко политипического вида.
7. Обмен генами возможен лишь внутри вида. Если мутация имеет положительную селективную ценность на территории всего ареала вида, то она может распространяться по всем его подвидам и популяциям. Отсюда следует краткое определение вида как генетически целостной и замкнутой системы.
8. Поскольку критерием вида является его репродуктивная обособленность, то естественно, что этот критерий неприменим к формам без полового процесса, например к агамным и партеногенетическим организмам. Таким образом, СТЭ оставила вне видового статуса огромное множество прокариот, не имеющих полового процесса, а также некоторые специализированные формы высших эукариот, вторично утративших половой процесс.
9. Макроэволюция, или эволюция на уровне выше вида, идет лишь путем микроэволюции. Согласно СТЭ, не существует закономерностей макроэволюции, отличных от микроэволюционных, хотя есть явления (параллелизм, конвергенция, аналогия, гомология), которые легче исследовать на макроэволюционном уровне.
10. Каждая систематическая единица: вид, род и т.д., — должна иметь единственный корень, монофилетическое происхождение. Это обязательное условие для самого права на существование рассматриваемой группы. Ведь эволюционная систематика строит свою классификацию, исходя из их родства. А согласно четвертому постулату СТЭ, родственны только те группы, которые идут от одной эволюционной ветви. Если же у таксона вдруг обнаруживаются в предках две разные ветви, его следует разделить.
11. Исходя из всех упомянутых постулатов, ясно, что эволюция непредсказуема: она не направлена к некоей конечной цели, т.е. носит нефиналитический характер.
www.ronl.ru
Дмитрий Жарков, Дмитрий Пышный, Ольга Лаврик«Наука из первых рук» №5–6 (71–72), 2016

Что такое «синтетическая биология»? Это новая и быстро развивающаяся отрасль молекулярной биологии, которая позволяет не только манипулировать с реальными генами и геномами, но и создавать совершенно новые последовательности ДНК и новые, никогда не существовавшие в природе биологические системы. Такие в прямом смысле сверхъестественные способности обязаны своим появлением стремительной эволюции молекулярных и компьютерных технологий, благодаря которым сегодня можно не только виртуально «сконструировать» любую генетическую последовательность, но и воплотить ее в жизнь. Так, еще в 2002 г. появился на свет первый полностью искусственный вирус, а еще через 8 лет — Синтия, первая жизнеспособная бактерия с полностью искусственным геномом. Эти достижения свидетельствуют о практически безграничных возможностях перепрограммирования ДНК, которые открывают не менее безграничные перспективы в самых разных областях науки и жизни, начиная от производства новых биотехнологических материалов до создания культурных растений с «улучшенным» фотосинтезом. Другое дело, что распорядиться этими «милостями не от природы» человечество должно с умом.
 Об автореДмитрий Олегович Жарков — доктор биологических наук, профессор РАН, заведующий лабораторией геномной и белковой инженерии Института химической биологии и фундаментальной медицины СО РАН (Новосибирск). Профессор кафедры молекулярной биологии и заведующий лабораторией геномных технологий факультета естественных наук НГУ, научный руководитель САЕ «Синтетическая биология». |
Сама идея синтетической биологии развивается «вокруг» геномной инженерии. За последние годы появились новые, крайне удобные молекулярные инструменты, с помощью которых можно каким угодно образом изменить геном практически любого организма. Да, это, может быть, дорого, можно при этом уткнуться в какую-то пока не известную проблему, но даже на текущем уровне развития технологий молекулярной биологии можно поэтапно за, условно говоря, «триллион долларов» слона превратить в мамонта, возродив этот прекрасный вымерший вид.
Другое дело, надо ли это делать? Ведь у синтетической биологии много других, намного более актуальных и важных задач, связанных, к примеру, с созданием средств диагностики, профилактики и лечения болезней человека, в том числе с применением персонализированного подхода, а также обеспечением продовольственной безопасности и повышением качества продуктов питания. Именно эти задачи легли в основу актуальных направлений исследований в рамках проекта САЕ «Синтетическая биология» Новосибирского государственного университета.
Когда речь зашла о заявке на прорывной проект от нашей САЕ, нам не пришлось долго думать: ее предметом стала разработка новых средств для геномного редактирования и их применение для направленного изменения человеческих клеток. Технологии геномного редактирования, появившись в последние несколько лет, произвели настоящую революцию как в науках о жизни, так и в практических областях, включая медицину, сельское хозяйство и промышленные биотехнологии. Без быстрого освоения подобных технологий Россия рискует оказаться в числе аутсайдеров.
Первый блок нашего проекта — фундаментальный — направлен на изучение процессов, происходящих в клетке в процессе ее «редактирования»; второй — на усовершенствование инструментов редактирования, включая разработку новых ферментов, способов доставки генетического материала и методов управления внутриклеточными процессами; третий — на получение практических результатов.
Почему так важна эта первая, фундаментальная часть? Главная проблема геномного редактирования состоит в доступности и кажущейся легкости самой технологии, в результате чего темпы ее использования намного опередили темпы «понимания» ее механизмов. Целенаправленной модификацией генома любых организмов, от бактерий до человека, сейчас может заниматься практически любая хорошо оснащенная биологическая лаборатория. Однако не более двух десятков исследовательских групп в мире реально занимаются исследованием соответствующих молекулярных механизмов и клеточных процессов, пытаются разобраться, что в действительности происходит в клетке при редактировании генов. Говорят, что дьявол сидит в деталях. Недостаток понимания приводит к низкой эффективности, что приходится компенсировать деньгами. Условно говоря, сейчас, чтобы добиться поставленной цели, приходится буквально «тыкать наугад» и вместо десяти планшетов с клетками задействовать тысячу.
Если говорить про самую популярную на сегодня систему геномного редактирования CRISPR/Cas9, то пока более-менее известно, и то не до конца, лишь как работает белок Cas9, который вносит разрыв в ДНК. В том числе не очень понятно, как этот фермент находит свою мишень в геноме, так как в пробирке Cas9 работает крайне неэффективно по сравнению с большинством других ферментов: реакция требует длительного времени и многократного избытка фермента по отношению к ДНК-мишени.

Следующий шаг при геномном редактировании — внесение в клетку нового генетического материала, который предполагается встроить в разрыв ДНК. На сегодня процесс генетической рекомбинации (перестройки ДНК) на основе такого нового искусственного олигонуклеотида — это настоящий «черный ящик». В принципе мы уже довольно много знаем о механизмах рекомбинации у человека, но только в «штатных» ситуациях. И знаем, что хотя рекомбинация при формировании половых клеток или при репарации («ремонте») поврежденной ДНК идет по одной и той же принципиальной схеме, детали этих механизмов совершенно различны. Чтобы разобраться в механизмах рекомбинации при геномном редактировании, узнать, насколько в них задействована система обычной рекомбинации, а насколько какие-то новые элементы, потребуется еще лет двадцать.
Но зато когда мы сможем во всем этом разобраться, то получим возможность регулировать сам путь, по которому идет редактирование. Как известно, целью обычно является выключение гена или изменение его функции. Выключить проще, потому что в данном случае достаточно внести разрыв, который клетка «заштопает», обычно с ошибками. Причем клетка предпочтет этот простой путь и тогда, когда мы планируем провести замену фрагмента с рекомбинацией: клеточные системы в этом случае «норовят» не заменить, а выключить мишень. Сейчас многие исследователи работают над решением этой проблемы, начиная с таких простых вещей, как ингибирование ферментов, которые в этом процессе участвуют. Например, оказалось, что один из таких ферментов ингибируется обычным кофеином, и если клетки получают такую «дозу», рекомбинация идет лучше.

Что касается усовершенствования инструментария редактирования генома, то я вижу здесь два принципиальных пути. Во-первых, можно каким-то образом модифицировать и улучшать уже известные ферменты, такие как Cas9. Структура этих белков хорошо изучена, и можно вносить в нее мутации для повышения их точности или эффективности. Кроме того, в качестве адресующих структур, которые ищут и распознают нужный фрагмент гена, можно использовать не обычные направляющие РНК, а модифицированные нуклеиновые кислоты, благодаря которым можно повысить скорость или точность поиска мишени. В нашем проекте над этой задачей будет работать группа под руководством чл.-кор. РАН Д. В. Пышного.
Второй путь — поиск принципиально новых способов геномного редактирования. Мы сейчас довольно много знаем о том, как белки взаимодействуют с ДНК, более того, с конца прошлого века накопилось довольно много описаний интересных феноменов в этой области, которые в то время были непоняты и не объяснены. Например, было обнаружено, что в клетках с определенной эффективностью будут происходить мутации и геномные замены даже в том случае, если их просто обработать олигонуклеотидами! Сейчас в наших руках есть все необходимые технологии, чтобы исследовать процессы, которые при этом происходят.
Ценность всех наших исследований, включая фундаментальные, еще и в том, что их результаты могут стать основой новых технологий, не подпадающих под уже имеющиеся патенты. Дело в том, что вся область геномного редактирования сейчас полностью «покрыта» патентами людей, которые эти технологии создали и чье финансирование исчисляется миллиардами долларов. В этом смысле нам с ними тягаться бесполезно — выгоднее попытаться найти собственные обходные пути.
Практическим выходом наших работ должен стать не возрожденный мамонт, на которого в любом случае денег не хватит, а вполне реальные новые клеточные линии, которые могут быть использованы в различных фармакологических исследованиях для поиска лекарств против таких широко распространенных заболеваний, как грипп, болезнь Паркинсона и рак молочной железы.
Например, сегодня наиболее подходящей моделью для поисков и тестирования лекарств от гриппа считаются не лабораторные мыши, которые от него гибнут, а гораздо более крупные и требовательные животные — хорьки. У этих животных клетки легочного эпителия схожи с человеческими, поэтому они в высшей степени восприимчивы к вирусу гриппа человека и издавна используются фармакологами. Если нам удастся при помощи геномного редактирования создать линии человеческих клеток с разной чувствительностью к вирусам гриппа, это намного упростит поиск соответствующих лекарств.

Еще одна подзадача — получение клеточных линий для тестирования токсичности новых химических соединений, которых ежегодно синтезируется сотни тысяч. Все эти вещества необходимо тестировать на безопасность для человека, для чего обычно предпочитают использовать лабораторных животных. Дело в том, что при тестировании на токсичность традиционно предпочитают «перебдеть, чем недобдеть», а результаты, полученные на стандартных клеточных линиях, обычно искажают показания в сторону меньшей токсичности по сравнению с данными, полученными на животных. Действительно, отдельные клетки оказываются более устойчивыми к негативным воздействиям, так как в организме, как правило, есть свое «слабое звено» — небольшие клеточные популяции особо «ранимых» клеток (например, стволовых), которые и будут определять устойчивость всей особи. Так как сейчас движение за отказ от использования животных в подобных исследованиях набирает обороты, новые генетически модифицированные линии клеток с повышенной восприимчивостью смогут стать адекватной заменой.
Если мы не выиграем конкурс прорывных проектов, это не означает, что вся наша деятельность в области геномного редактирования прекратится. Исследования, безусловно, будут развиваться, только меньшими темпами.
Уже в рамках текущего финансирования мы создали новую структуру под названием «Центр перспективных биомедицинских исследований», которая объединит шесть университетских лабораторий, имеющих отношение к геномному редактированию. И хотя на какие-либо фантастические результаты в этом случае рассчитывать не приходится, но, опираясь на интеллектуальные и материальные ресурсы институтов СО РАН, мы способны создать, возможно, лучший в России центр в этой области.
В этом смысле конкурентов у нас немного, за исключением того же «Сколково», отечественных научных групп, занимающихся фундаментальными работами по геномному редактированию, очень мало.

 Об автореДмитрий Владимирович Пышный — член-корреспондент РАН, доктор химических наук, доцент, заместитель директора по научной работе и заведующий лабораторией биомедицинской химии Института химической биологии и фундаментальной медицины СО РАН (Новосибирск). Эксперт САЕ «Синтетическая биология». |
Среди всех участников САЕ НГУ «Синтетическая биология» мне хотелось бы в первую очередь отметить лабораторию структурной биоинформатики и молекулярного моделирования НГУ, возглавляемую А. Ю. Бакулиной, с которой мы поддерживаем тесное сотрудничество. Занимается она разработкой и применением технологий компьютерного моделирования применительно к биологическим макромолекулам — я считаю это направление одним из самых важных в современной синтетической биологии.
Традиционный подход в создании новых соединений состоит в том, что проводится много синтезов, получают массу вариантов, а из них уже выбирают подходящие. Благодаря же расчетным технологиям мы сначала можем спрогнозировать свойства будущего соединения, «спроектировать» его, а уже потом его создавать. То есть исследователь может заранее просчитать и оценить результат. Значимость этого трудно переоценить, когда речь идет о таких сложных молекулах, как производные олигонуклеотидов (коротких фрагментов нуклеиновых кислот), и вы хотите, к примеру, знать, будут ли они адекватно соответствовать структуре двойной спирали ДНК по размеру, прочности и другим структурным характеристикам.
Конкретная задача, которой занимаются физики из нашей лаборатории биомедицинской химии, — отработка методик и расчетов, которые лягут в основу таких компьютерных алгоритмов. И хотя полностью она еще не решена, успехи уже есть.
Нужно сказать, что технологии молекулярного докинга (метода молекулярного моделирования, позволяющего предсказать ориентацию и положение молекул, наиболее выгодные для образования устойчивого комплекса) в мире сейчас очень популярны, и в первую очередь в связи с поиском и созданием новых лекарственных соединений. Например, с помощью этих компьютерных технологий можно отобрать молекулы, способные с высокой эффективностью связываться с определенным участком белка-фермента и тем самым блокировать его работу.
Такие технологии, безусловно, нужно развивать, причем в более «глобальном» формате. Под последним я подразумеваю обращение к олигомерам (молекулам в виде цепочки из небольшого числа однотипных составных звеньев), тогда как в случае традиционного докинга речь идет, как правило, о низкомолекулярных соединениях. В качестве таких «среднемолекулярных» соединений могут выступать не только стандартные олигонуклеотиды, но и любые другие искусственно созданные молекулярные блоки в виде самых разных олигомерных цепочек. И в этом случае на первый план выходит компьютерное моделирование, так как число вариантов при этом резко возрастает.
Что касается химических методов получения искусственных олигомеров, то технический базис для этого у нас уже имеется. Хотя пока мы используем эти технологии с целью повысить функциональность тех же олигонуклеотидов для придания им дополнительной гидрофобности, введения репортерной метки и т. п. Ведь в этой области также есть еще много нерешенных вопросов, таких как доставка соединений в живые клетки. К примеру, для этой цели часто используется вариант, когда к олигонуклеотиду присоединяют специальные химические группировки (например, остаток холестерина), но это не всегда оправданно и эффективно. А ведь для модификации олигонуклеотидов можно использовать те же самые дополнительные ненуклеотидные цепочки, звенья которых сами по себе будут играть роль функциональных группировок с нужными свойствами.

Этот подход в перспективе может привести к созданию нового типа олигомерных агентов ненуклеотидной природы, для которых будет характерно огромное потенциальное разнообразие функциональных свойств отдельных звеньев, вероятно, даже большее, чем в случае использования аминокислот. И, конечно, есть задумка когда-нибудь окончательно отказаться от олигонуклеотидов и создать на основе уже хорошо «проработанной» нуклеотидной химии что-то совершенно новое вроде мультифункциональных олигомеров.
В качестве примера практических результатов в области синтетической биологии хочу привести фосфорилгуанидины — созданные в ИХБФМ СО РАН новые химические аналоги нуклеиновых кислот, прикладными приложениями которых сейчас активно занимаются в лаборатории химии нуклеиновых кислот (руководитель к. х. н. Д. А. Стеценко) и в нашей лаборатории биомедицинской химии.
Так, совместно с британскими учеными уже подана заявка на патент на использование этих соединений при терапии тяжелого генетического заболевания — мышечной дистрофии Дюшенна, которая приводит к полной потере способности двигаться и в итоге к смерти. Причина болезни — мутация, следствием которой служит нарушение процесса сплайсинга (вырезания фрагментов) при созревании информационной РНК, в результате чего в клетках синтезируется «неправильный» белок дистрофин, являющийся важным структурным компонентом мышечной ткани.
Корректировать этот патологический процесс можно с помощью олигонуклеотидов, и, как показали исследования на лабораторных животных, для этой цели хорошо подходят наши фосфорилгуанидины. Последние работают не хуже, чем морфолиновые олигомеры, совсем недавно разрешенные в США к практическому применению. В обоих этих случаях был реализован один и тот же принцип, хотя и на разных платформах. Конечно, такая терапия означает пожизненные уколы, но альтернативным вариантом является лишь редактирование генома, которое на сегодняшний день недоступно, хотя и становится все более реальным с течением времени.
Сегодня мы сконцентрировались на еще одном очень важном практическом применении фосфорилгуанидинов — диагностике заболеваний. Есть тип диагностических сенсоров на основе полупроводниковых нанопроволок, работающих по принципу полевых транзисторов. Проводимость такого нанопроводника меняется, когда на его поверхности появляется заряд. Молекула же фосфорилгуанидинового олигонуклеотида, в отличие от обычного, сама по себе не имеет заряда. Иммобилизованный на поверхности проводника, такой олигонуклеотид способен специфично связаться с заряженной РНК-мишенью — нуклеотидным маркером того или иного заболевания. При этом детекция сигнала с проводника будет идти лишь в случае успешного связывания с мишенью, несущей электрический заряд. В экспериментах, проводимых совместно с новосибирским Институтом физики полупроводников им. А. В. Ржанова СО РАН было доказано, что с помощью сенсора, на который «посажены» производные фосфорилгуанидинов, можно действительно без дополнительных меток получать прямой диагностический сигнал.
Возвращаясь к технологиям компьютерного моделирования, напомню, что в состав «Центра перспективных биомедицинских исследований», созданного в НГУ в рамках САЕ «Синтетическая биология», войдет новая лаборатория белковой инженерии. Как видно из названия, она будет заниматься созданием новых ферментов и других белков с измененными свойствами, которые предполагается использовать для нужд биотехнологии либо в качестве терапевтических препаратов или молекулярных инструментов. Ведь виртуально «спроектировав» и изучив ту или иную нужную белковую молекулу, нужно затем обратиться к методам генной инженерии, чтобы начать ее реально производить. То есть встает конкретная задача синтезировать соответствующие генные последовательности — искусственные гены.
Чтобы «собрать» один такой ген, требуется в определенном порядке соединить несколько сотен искусственно синтезированных нуклеотидных цепочек! Отмечу, что в России подобных технологий практически нет, как нет и научных коллективов, которые занимаются этой проблематикой. Исключением служит группа к. х. н. А. Н. Синякова из нашей лаборатории, которая добилась немалых успехов в разработке методов синтеза олигонуклеотидов на поверхности специальных чипов — небольших кремниевых пластинок со множеством ячеек, где можно одновременно синтезировать большое число нуклеотидных последовательностей разного состава.
Наши исследователи совместно со специалистами из Института физики полупроводников им. А. В. Ржанова и Института автоматики и электрометрии СО РАН разработали и уже апробировали чиповую технологию синтеза олигонуклеотидов, основанную на использовании фотолабильных защитных групп или фотогенераторов кислот. В дальнейшем набор этих олигонуклеотидов подвергают ряду специальных обработок, чтобы в итоге получить целевую генную последовательность.
Заметим, что поскольку технологии эффективного синтеза искусственной ДНК открывают новые возможности не только в промышленности, медицине и сельском хозяйстве, но и в создании биологического оружия, в мире предпринимаются практические действия по ограничению их распространения. Это означает, что подобные установки в нашу страну экспортироваться не будут. Создание же отечественного микрочипового синтезатора — это наш реальный шаг к созданию искусственных генов, что является одним из краеугольных камней синтетической биологии. А от этого недалеко и до создания искусственных живых клеток, а в более отдаленной перспективе — и целых организмов.

 Об автореОльга Ивановна Лаврик — член-корреспондент РАН, доктор химических наук, заведующая лабораторией биоорганической химии ферментов Института химической биологии и фундаментальной медицины СО РАН (Новосибирск) и совместной лаборатории защитных репарационных систем Новосибирского государственного университета, профессор кафедры молекулярной биологии факультета естественных наук НГУ. |
Научно-исследовательское подразделение по исследованию защитных репарационных систем, которым я руковожу в рамках САЕ «Синтетическая биология» НГУ, фактически состоит из тех сотрудников трех лабораторий Института химической биологии и фундаментальной медицины СО РАН, которые наиболее тесно сотрудничают с университетом, — моей лаборатории биоорганической химии ферментов, лаборатории исследования модификации биополимеров (руководитель — д. х. н. О. С. Федорова) и лаборатории ферментов репарации (руководитель — д. х. н. Г. А. Невинский).
Мы занимаемся фундаментальными исследованиями систем репарации ДНК, результаты которых важны для понимания механизмов старения и могут стать основой для конструирования ингибиторов ферментов репарации («ремонта») ДНК, представляющих интерес для медицины. Все эти работы основаны на междисциплинарном сотрудничестве, которое раньше поддерживалось специальными интеграционными проектами СО РАН, а теперь переместилось на площадку университета. Этому очень важному вопросу посвятил свой доклад ректор НГУ, чл.-корр. РАН М. П. Федорук на последней научной сессии Общего собрания СО РАН. Он назвал такой переход новым вектором развития Новосибирского академгородка. САЕ позволяет не только более эффективно организовать междисциплинарное сотрудничество, но и активно включать в исследования студентов и магистров НГУ.
Возвращаясь к системам репарации ДНК, нужно сказать, что сейчас мы отчетливо понимаем, что все белки репарационной системы, ответственной за исправления повреждений ДНК, представляют собой потенциальные мишени для лекарственных препаратов. Универсальной мишенью является, к примеру, ядерный белок поли(АДФ-рибоза)-полимераза 1 (PARP1) — важнейший регулятор репарации ДНК, ингибирование которого может дать выраженный эффект при онкологических заболеваниях, а также ишемическом инсульте и других патологиях.
PARP1 является «сенсором» повреждений ДНК: он первым распознает ее разрывы и присоединяется к этим местам, начиная активно синтезировать олиго- или поли(АDP)-рибозные цепочки, которые ковалентно связываются с разными акцепторными белками и в том числе с самой PARP1. В результате в месте разрыва происходит деконденсация хроматина, что облегчает доступ ферментов репарации. Таким образом, PARP1 способствует восстановлению повреждений ДНК, в том числе и в раковых клетках при традиционной химио- или радиотерапии, что отрицательно сказывается на эффективности лечения.
Что касается случаев нарушения мозгового кровообращения в результате ишемии, то при множественных повреждениях генома гиперактивация PARP1 приводит к быстрому истощению имеющихся в них энергетических запасов в виде молекул АТФ, что чревато необратимой гибелью нейронов.
Идея ингибировать в подобных ситуациях активность PARP1 как универсального регулятора процессов репарации на первый взгляд представляется очень привлекательной. Но не надо забывать, что этот фермент является многофункциональным белком, и, как показывают многочисленные исследования, подавляя его репарационную активность, мы одновременно подавляем и другие его функции. Сегодня на основе ингибитора PARP-1 выпускается лекарство олапариб (линпарза), которое применяется для лечения некоторых видов рака, включая рак яичника. Тем не менее его рекомендовано применять с осторожностью из-за большого числа нежелательных побочных эффектов.
Поэтому в своих исследованиях мы работаем не только с этой универсальной, но и с другой, специфической мишенью — ферментом репарации тирозил-ДНК-фосфодиэстеразой 1 (Tdp1).
Дело в том, что в клетке существуют ферменты топоизомеразы, участвующие в динамичном поддержании определенной конформации двойной спирали ДНК. Топоизомеразы типа I вносят разрыв в цепь ДНК, ковалентно соединяясь с одним из его концов, после чего в дальнейшем происходит восстановление цепи. Противораковые препараты на основе камптотецина стабилизируют продукты этого ковалентного присоединения, не давая «залатать» повреждение, вносимое топоизомеразой, в результате чего опухолевая клетка погибает. Однако Tdp1 способен «снимать» эту стабилизацию, поэтому использование ингибиторов этого фермента даст возможность усилить эффективность основной противоопухолевой терапии.
Эта работа выполняется нами совместно с лабораторий физиологически активных веществ Новосибирского института органической химии им Н. Н. Ворожцова СО РАН (руководитель — д. х. н. Н. Ф. Салахутдинов), а также с группой к. б. н. Н. А. Поповой из Института цитологии и генетики СО РАН. В экспериментах на лабораторных животных с привитой опухолью благодаря применению самого эффективного из разработанных ингибиторов удалось добиться значительного (до 50%) уменьшения основной опухоли и практически полного исчезновения метастазов. Сейчас мы пытаемся получить финансирование для проведения уже клинических испытаний этого перспективного противоракового препарата.
И конечно, нужно отметить такое очень важное направление, как геномное редактирование с использованием системы CRISPR/Cas9, с помощью которого можно «выключать» сами гены, отвечающие за возникновение болезней. На этом переднем крае науки мы отстаем, тогда как в Европе и США уже создано множество коммерческих фирм, где эти технологии используются для создания нужных мутаций в целевых генах. Тем не менее, совершенно необходимо продолжать заниматься научно-исследовательскими разработками, которые повысят эффективность этого подхода.
В рамках САЕ «Синтетическая биология» мы будем сотрудничать с НГУ как раз в этом направлении, конкретно — с лабораторией геномных технологий, которой заведует д. б. н. Д. О. Жарков. Одна из задач, решением которой будет заниматься к. х. н. Н. А. Кузнецов, касается исследования детальной кинетики функционирования белковых комплексов именно в этой системе геномного редактирования. Другими словами, предстоит изучить, как в термодинамическом режиме происходит на ДНК сборка комплекса CRISPR/Cas9 из отдельных компонентов. Это будет по-настоящему пионерная работа, так как в современном мире зачастую больше обращают внимание на конечный результат, а не на особенности самого процесса, что неправильно, так как понимание механизма помогает усовершенствовать практические технологии.
CRISPR/Cas9 — это, действительно, очень хороший инструмент для исследовательских и, безусловно, медицинских целей. В то же время нужно отдавать себе отчет, что результат не всегда будет однозначным, по крайней мере, не для всех болезней. Например, за возникновение раковых опухолей отвечает не один ген, поэтому попасть «в яблочко» в таких случаях не так просто. При своем появлении каждый новый метод всегда вызывает только восторженные отклики, но чем больше его применяют, тем больше вскрывается недостатков. Поэтому понимание механизмов, лежащих в его основе, будет далеко не лишним.
К примеру, разрыв нити ДНК в процессе «редактирования» — результат работы белка Cas9, может «залатываться» системами репарации, которыми мы занимаемся. Кстати, любой разрыв в ДНК очень эффективно распознает как раз та самая, интенсивно нами изучаемая PARP1. Этот фермент может влиять на процесс направленной модификации гена-мишени, так как он участвует в регуляции системы «ремонта» двойных разрывов нитей ДНК и влияет на соотношение процессов негомологичной и гомологичной рекомбинации. Поэтому исследования систем репарации очень важны для повышения эффективности работы систем редактирования генома, которые играют столь большую роль в современной синтетической биологии.
Литература 1. Власов В. В., Жарков Д. О., Пышный Д. В. Приручение древней молекулы // Наука из первых рук. 2014. № 3–4. С. 84–91.2. Купрюшкин М. С., Пышный Д. В., Стеценко Д. А. Фосфорилгуанидины. Новый класс аналогов нуклеиновых кислот // Acta Naturae. 2014. Т. 6. № 4(23). С. 53–55.3. Немудрый А. А., Валетдинова К. Р., Медведев С. П., Закиян С. М. Системы редактирования геномов TALEN и CRISPR/Cas — инструменты открытий // Acta Naturae. 2014. Т. 6. № 3. С. 20–42.4. Пышный Д. В., Стеценко Д. А. Фосфорилгуанидины — новые химические аналоги нуклеиновых кислот // Наука из первых рук. 2014. № 5. С. 6–9.5. Ширяева А. А., Северинов К. В. Системы CRISPR/Cas бактерий и архей. Как компоненты адаптивной иммунной системы прокариот стали универсальным и эффективным инструментом модификации геномов, исследования эпигеномов и управления транскрипцией генов? // Редактирование генов и геномов. Ред. С. М. Закиян, С. П. Медведев, Е. В. Дементьева, В. В. Власов. Новосибирск: Издательство СО РАН, 2016. С. 133–169.6. Barrangou R., Doudna J. A. Applications of CRISPR technologies in research and beyond // Nat. Biotechnol. 2016. V. 34. N. 9. P. 933–941.
elementy.ru
Статья на конкурс «био/мол/текст»: Недавно вышедшая статья от гарвардских биологов заставила многие информагентства выпустить заметки: ученые превратили кишечную палочку в биологический аналог компьютера, роль электрических сигналов в котором играют короткие молекулы РНК. В своей статье я хотел бы дать небольшой обзор достижений современных биоинженеров, а затем рассказать широкой публике о том, как же работают «биокомпьютеры» и чего мы от них ждем.

Эта работа опубликована в номинации «Свободная тема» конкурса «био/мол/текст»-2017.

Генеральный спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.

Спонсором приза зрительских симпатий и партнером номинации «Биомедицина сегодня и завтра» выступила фирма «Инвитро».

«Книжный» спонсор конкурса — «Альпина нон-фикшн»
На протяжении всего существования человечества основным способом узнать что-либо было наблюдение. Аристотель разбивал куриные яйца на разных стадиях инкубации и зарисовывал увиденное, в дальнейшем пытаясь это объяснить. С течением времени появился чуть более достоверный метод — эксперимент, в котором мы полностью управляем условиями наблюдения. Однако в последнее время ученым все больше хочется вмешаться в живые процессы, придумать новые полезные человечеству гены, или же просто что-нибудь там сломать и посмотреть, что будет.
В современной биологии вопросами вмешательства в живые системы занимаются синтетические биологи и биоинженеры. Они разрабатывают рациональные подходы к управлению и программированию клеточных функций; изучают методы создания искусственных генетических конструкций, схем и сетей. Можно как искать вдохновение в природе, перемещая гены между организмами, так и придумывать совершенно новые, не имеющие аналогов в живом мире системы.
Для лучшего понимания материала быстро освежим школьные знания.
Современные базовые положения молекулярной биологии кратко описываются так называемой центральной догмой (рис. 1): генетическая информация кодирует последовательность белка и в клетке хранится в виде ДНК, а РНК переносит информацию об аминокислотах к молекулярной машине синтеза белка — рибосоме. Необходимо ввести два термина: транскрипция — процесс синтеза РНК по матрице ДНК, — и трансляция — процесс синтеза белка из аминокислот по матрице РНК.
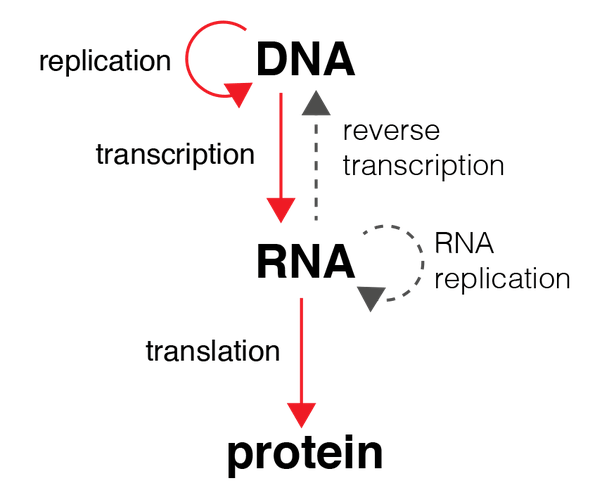
Рисунок 1. Центральная догма молекулярной биологии. На схеме показаны основные процессы передачи и реализации генетической информации в клетке.
Для того чтобы дать подробный обзор современных достижений синтетической биологии, потребовалась бы целая серия статей, так что я ограничусь несколькими избранными, наиболее полезными для человека, или же просто самыми захватывающими разработками.
Направленный мутагенез открывает сравнительно простой способ определить роль конкретного гена/белка в клеточных процессах — тот процесс, что перестал работать вследствие поломки этого гена или белка, очевидным образом зависит от их функции. Например, выключаем некий интересный нам ген у растения → вместо нормальных цветков видим только тычинки и пестики → вывод: ген участвует в формировании частей цветка. Казалось бы, в природе и так полно мутантов, зачем же создавать новых? Но найти, какой ген выключился у природного мутанта, гораздо сложнее, чем вручную сломать определенный нами же ген.
Вместо того чтобы заниматься выключением генов, можно попробовать внести в организм гены из других видов. Классические исследования в области генной модификации направлены на сельское хозяйство и скотоводство [1–3], но это не значит, что мы не можем решать и более интересные проблемы теми же методами.

Рисунок 2. Мутагенная цепная реакция на примере дрозофилы. Ферменты рекомбиназы в зиготе переводят мутацию в гомозиготный характер за счет изменения второй гомологичной хромосомы.
Тропические заболевания в последнее время привлекают все больше медийного внимания. Это и вирус Зика [4], [5], и лихорадка Денге, и малярия. И именно последняя инфекция вызывает больше всего опасений. В прошлом веке малярийный плазмодий стал устойчивым почти ко всем классическим препаратам [6]. Артемизинин, разработанный в 1970-е годы (за его разработку, кстати, вручили Нобелевскую премию 2015 года [7]), стал новой надеждой врачей и действительно привел к резкому снижению смертности от малярии за последние десятилетия. Сейчас артемизинин коммерчески производят [8] с использованием искусственного биохимического пути — ферменты, проводящие нужные реакции, собрали из разных бактерий в один модифицированный штамм. C точки зрения химиков-технологов это замечательное решение — мы не заботимся о выделении промежуточных продуктов, тратим меньше энергии на проведение реакций, да и выделить продукт легко — всего лишь отфильтровать бактерий.
Для решения проблемы заболеваний, переносимых насекомыми, есть другое решение — мутагенная цепная реакция [9], [10]. Название звучит страшновато, и это во многом соответствует действительности. Суть метода — сделать изменение в геноме распространяющимся в популяции, с потенциальной возможностью изменить в итоге абсолютно все организмы данного вида. На рисунке 2 показано, как мутантный тип (обозначен синим цветом) может стать доминирующим в популяции [11]. Мы нарушаем менделевские законы наследования с помощью внесения в геном модифицирующих его же ферментов.
С помощью мутагенной цепной реакции можно сделать комаров неспособными переносить малярию [12], причем все потомки модифицированного комара также будут не способны заражать людей.
У многих ученых мутагенная цепная реакция вызывает большие опасения. Мутация, однажды введенная в геном единственной особи, неконтролируемо распространяется в геномах детей, внуков, правнуков и всех последующих поколений популяции. Из-за этого «дикие» организмы могут исчезнуть с лица земли.
Менее радикальный, но очень похожий метод применяют уже сейчас. В Бразилии фабрики производят ГМ-комаров, потомство которых стерильно, и выпускают их в природу. Это помогает снизить количество комаров, переносящих Денге, Зика, малярию и тому подобное. Однако так как метод работает всего на двух поколениях, опасности, что что-то выйдет из под контроля, нет .
Рестриктазы — те самые ферменты, что редактировали геном комаров и дрозофил, — могут также помочь нам и в задачах нейронаук.
Метод Brainbow [13–15] позволил ученым-нейрологам покрасить каждый нейрон мозга (в данном случае крысы) в индивидуальный цвет. И дело тут не только в том, что выглядит это безумно красиво, но также и в том, что структура мозга стала различима еще на один уровень точнее: теперь мы можем проследить взаимосвязи нейронов, находящихся в одном слое коры, найти менее очевидные пути проведения сигналов, чуть-чуть приблизить нас к составлению коннектома — карты всех контактов нейронов в мозге. Работает это так: в геном встраивается несколько флуоресцентных белков разных цветов, и, когда клетка дифференцируется в нейрон, рестриктазы случайным образом выключают некоторые из них. Таким образом, каждый нейрон обладает своим цветом и четко выделяется на фоне остальных (рис. 3).

Рисунок 3. Срез гипоталамуса мозга крысы, окрашенный с помощью Brainbow.
Но не будем надолго останавливаться на модификациях и вставках одиночных (невзаимодействующих) генов, ведь вся сложность и запутанность живых систем обусловлена, в основном, огромным количеством и многообразием регуляторных систем, действующих как на уровне транскрипции, так и трансляции. Сейчас мы знаем о регуляции достаточно, чтобы пытаться создавать сети генов, работающие как и когда нам нужно.
Один из важных типов генных сетей — осцилляторы. Это системы, которые циклически переключаются между несколькими состояниями. К примеру, осцилляторные сети регулируют циркадные ритмы у животных [16], [17], суточные ритмы цианобактерий. Искусственные осцилляторы — одна из первых тем исследований биоинженеров. Бактерии, которые циклически меняют цвет в результате замкнутого круга активаций и выключений разных генов (видео), появились еще в 2008 году [18]. Обладание таким «временным» контролем производства белка может быть очень важно, ведь вся природа живет циклично.
Видео. Бактерии, которые осциллируют между флуоресцентным и бесцветным состоянием.
Другой «цветной» пример — бактерии, которые реагируют на свет, в результате окрашиваясь в тот цвет, которым их освещали [19]. Такое «бактериальное ТВ» (пример на рисунке 4) открывает для нас новый способ контроля за геномом бактерий, который не требует никакого химического воздействия на культуру. Действительно, разные длины волн света, облучающего клетки — нечто вроде кнопок на пульте, включающих синтез разных белков.

Рисунок 4. Ученые из Массачусетского технологического института изобразили логотип своего вуза на чашке Петри с модифицированными бактериями (слева вверху — изображение, которое проецировалось на колонию).
Не забыт ученым и другой тип макромолекул — рибонуклеиновые кислоты. Не будем сейчас останавливаться на всей важности РНК для клеток и ее роли в процессах появления жизни [20] и эволюции, а поговорим больше о практической стороне ее использования в синтетической биологии.
С одной стороны, РНК гораздо более многолика, чем ДНК и белки: множество конформаций (пространственных структур) позволяет РНК играть любую роль, начиная с носителя генетической информации, рецептора/сенсора, структурного каркаса, заканчивая даже ферментативной активностью.
С другой же — РНК максимально неустойчива в чистом виде , не живет в клетке продолжительное время, и работа с ней требует больше времени и сил.
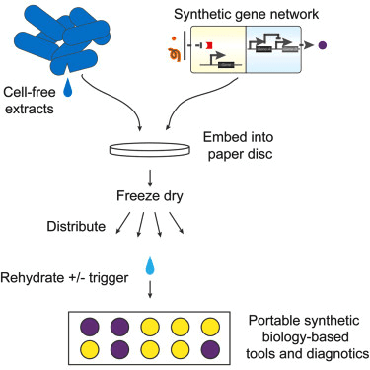
Рисунок 5. Графическое представление разработанных РНК-биосенсоров.
Тем не менее, и в этой области есть красивые и сложные разработки. Ученые из Гарвардского университета разработали РНК-биосенсоры [21]: модифицированные клетки нарабатывают распознающие РНК, которые потом в виде клеточного экстракта наносятся на бумагу. Такие тест-полоски высушиваются и могут храниться долгое время. При использовании на них наносят воду и образец, РНК-рецептор узнает некую мишень и запускает синтез цветного белка (рис. 5).
Так получаются недорогие, стойкие и точные анализаторы, которые могут с помощью капли слюны или крови идентифицировать болезнь или инфекцию за минуту вне лаборатории в любой точке мира.
От обзора общих достижений синтетической биологии теперь можно перейти к обещанному рассмотрению темы «биокомпьютеров». Впереди нас ждет самая сложная часть материала, но от этого она не становится менее интересной и красивой. Для начала вспомним, что же делают вычислительные устройства: они принимают некие сигналы на вход, производят их обработку (например, сравнивают, суммируют, выбирают один из нескольких), а затем выдают вывод, соответствующий входным данным.
Все живые организмы формально и являются биокомпьютерами: они на основании внешних условий (свет, наличие еды, плотность популяции и многих других) решают, какие синтезировать белки, в каком направлении двигаться, когда размножаться и делать запасы... Но вот только все эти действия — не то, что мы хотим получить. Синтетические биологи хотят сами определять сигналы, процесс «вычислений» и результат. Зачем нам это нужно? Применения «живым вычислениям» можно найти и в биотехнологии, и в медицине, и даже в самой научной деятельности. Они помогут нам добиться значительной автоматизации процессов, будь то анализ крови или мониторинг биотехнологического процесса. И сейчас это во многом реально воплотить в жизнь.
Важный элемент в вычислениях — это логические элементы (так называемые вентили), выполняющие базовые операции, такие как И, ИЛИ, НЕ, и так далее. Они позволяют уменьшить количество сигналов, дают возможность добавить ветвление (если... то... и т.д.) в будущую программу. Такие схемы могут быть реализованы как на уровне генов (рис. 6), так и на стадии трансляции с использованием коротких синтезированных молекул РНК [22–24]. Цепочки белков-активаторов и репрессоров вполне могут считаться транзисторами.

Рисунок 6. Основные логические элементы (а) со схемами их реализации на уровне генов (б).
Компьютер немыслим без памяти, и биологи понимают это. Первая статья, посвященная искусственной биологической памяти, была опубликована еще в 2000 году [25]. Используя внешний сигнал, ученые смогли переключать клетку между двумя стабильными состояниями (к примеру, между синтезами двух разных белков), формально являющимися единичным битом памяти (рис. 7).
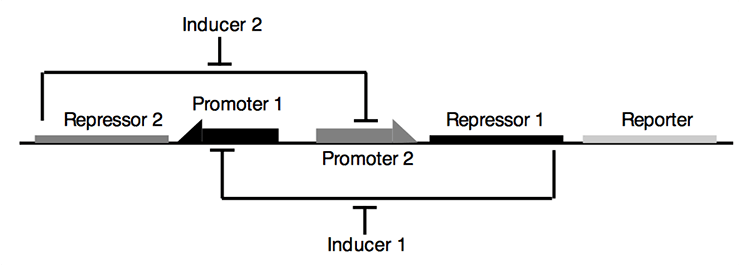
Рисунок 7. Схема генного переключателя. Индукторы 1 и 2 — управляющие сигналы, гены-репрессоры обеспечивают одновременную работу только одной половины (одного из двух состояний) системы.
Такие базовые элементы открывают огромный простор для фантазии — к примеру, существуют схемы, считающие количество событий [26], определяющие границу света и тени [27]... Но все же впереди еще долгий путь исследований, идей и прорывов.

В это верится с трудом, но у синтетической биологии довольно низкий порог вхождения (естественно только при наличии желания и знаний). Как это возможно? Путь лежит через соревнование iGEM (International Genetically Engineered Machine), основанное Массачусетским технологическим институтом в 2004 году. Сейчас участвовать могут команды до шести человек из школьников и студентов-бакалавров (есть также отдельная секция для всех кто «старше»).
iGEM представляет из себя настоящий биохакатон: ведь по духу соревнование очень близко движению биохакинга, набирающему популярность в течение последних 10 лет [28]. Весной команды регистрируются и придумывают идею проекта. За лето им предстоит научить бактерий (как самый стандартный и любимый объект) чему-нибудь новому и необычному.
Для этого, естественно, требуются наличие лаборатории, умение нетривиально мыслить, хорошая теоретическая подготовка и правильно поставленные лабораторные навыки.
А вот с реактивами и исходными материалами все гораздо интереснее: MIT содержит «реестр стандартных биологических запчастей» — базу простейших компонентов, таких как плазмиды, праймеры, промоторы, терминаторы, белки, белковые домены и многое другое (рис. 8), которые хранятся в формате молекул ДНК. Сейчас там содержится более 20 000 зарегистрированных частей, так что можно найти почти все что угодно, начиная с классических флуоресцентных белков, заканчивая сенсорами тяжелых металлов и знаменитым CRISPR/Cas. После того как оргкомитет одобряет проект зарегистрировавшейся команды, им высылают все необходимые компоненты из реестра.
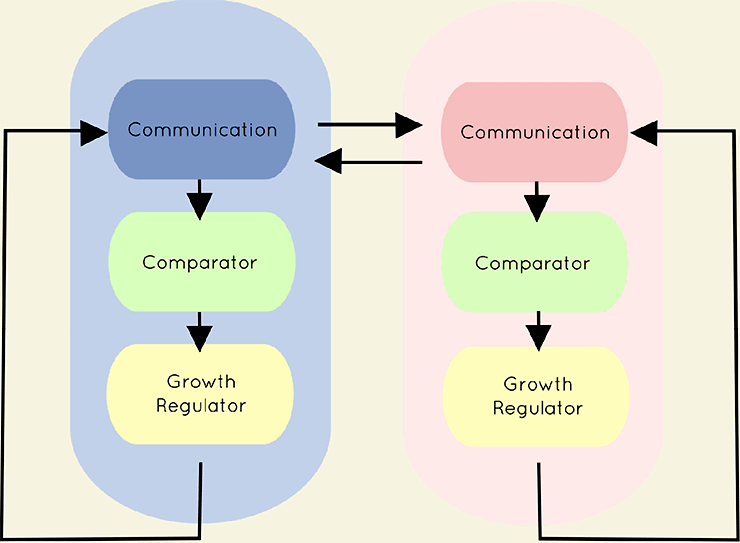
Рисунок 8. Упрощенная схема проекта команды Imperial College London.
Победителя выбирает коллегия из 120 признанных ученых на ежегодной осенней конференции в Бостоне.
Для примера расскажу об одном из проектов студентов Имперского колледжа Лондона (Imperial College London), выигравшем Гранд-приз в 2016 году. Основная идея — регулировать видовое соотношение бактерий в совместных культурах. Это в дальнейшем может позволить по полной реализовать потенциал целых синтетических экосистем. Студенты скомбинировали систему бактериального чувства кворума (с помощью которой бактерии общаются и координируют свое поведение внутри вида), вычислительные схемы из РНК, которые сравнивали кворум-сигналы разных видов, и белки, ингибирующие рост (общая схема показана на рис. 8). Таким образом бактерии всегда в курсе численности всех видов, и за счет ингибиторов роста имеют возможность сохранять ее соотношение постоянным. РНК-компараторы были разработаны с нуля, и также был представлен софт для записи и анализа данных роста совместных культур.
Мероприятие это довольно популярно в университетских кругах, количество участников достигает пяти тысяч человек, и даже в России недавно снова появилась своя команда.
Казалось бы, это все игрушки, ведь кому сейчас могут понадобиться такие «запрограммированные» бактерии? Они все-таки подвержены мутациям, зашумлению «сигнала» (из-за общей стохастичности внутриклеточных процессов) и довольно медлительны. Но ведь точно так же говорили и об обычных компьютерах в 1940–1950-е годы! Однако сейчас компьютеры используют в областях, немыслимых лет 40 назад. Можно лишь предположить возможные будущие применения биокомпьютеров:
biomolecula.ru
Синтетическая биология (англ. Synthetic Biology) — термин, долго использовавшийся для описания подходов в биологии, стремящихся интегрировать различные области исследования для того, чтобы создать более целостный подход к пониманию концепции жизни.[источник не указан 1817 дней]
В последнее время термин используется в другом значении, сигнализируя о новой области исследования, которая объединяет науку и инженерию с целью проектирования и построения новых (несуществующих в природе) биологических функций и систем.[источник не указан 1817 дней]
Синтетическая биология — это новое направление генной инженерии. Развивается небольшой плеядой учёных. Главные цели следующие[источник не указан 1817 дней]:
Более 100 лабораторий по всему миру занимаются синтетической биологией. Работы в этой области разобщены; над их систематизацией работает биолог Дрю Энди из Массачусетского технологического института. Это позволит проектировать живые системы, которые ведут себя предсказуемым (и заказанным по желанию) образом и используют взаимозаменяемые детали из стандартного набора генов. Учёные стремятся создать обширный генетический банк, позволяющий создавать любой нужный организм (по аналогии с созданием электронной схемы из промышленных транзисторов и диодов). Банк составляют биокирпичи (BioBrick) — фрагменты ДНК, чья функция строго определена и которые можно внедрить в геном клетки для синтеза заранее известного белка. Все отобранные биокирпичи спроектированы так, чтобы хорошо взаимодействовать со всеми другими на двух уровнях:
Сейчас в Массачусетском технологическом институте создали и систематизировали уже более 140 биокирпичей. Сложность заключается в том, что очень многие сконструированные фрагменты ДНК при внедрении в генетический код клетки-реципиента уничтожают её.
Синтетическая биология способна создать генинженерные бактерии, которые могут производить сложнейшие и дефицитные лекарства дёшево и в промышленных объёмах. Спроектированные геномы могут привести к появлению альтернативных источников энергии (синтез биотоплива) или к бактериям, которые помогут удалять излишний углекислый газ из атмосферы.
 Править
ПравитьКорни синтетической биологии уходят в 1989 год, когда команда биологов из Цюриха под руководством Стивена Беннера (Steven Benner) синтезировала ДНК, содержащую две искусственных генетических буквы помимо четырёх известных (аденин, цитозин, гуанин и тимин), используемых всеми живыми организмами Земли.
Большинство учёных придерживается природных моделей; они пробуют создать клетки, которые окружены двухслойными мембранами и наполнены генетическим материалом в виде ДНК или РНК.
 Править
ПравитьНекоторые сторонники синтетической биологии полагают, что все новые геномы, созданные учёными, должны становиться достоянием всего человечества и использоваться совершенно свободно, без прав какой-то отдельной группы на данные коды жизни.
Пэт Муни (англ. Pat Mooney), директор канадской организации ETC Group, занимающейся вопросами биоэтики и опасности некоторых научных достижений для природы и общества, считает, что подобные исследования опасны, патент JCVI должен быть отозван, а все данные по этому геному закрыты.
 Править
Правитьru.science.wikia.com