|
|
|
|
 Far Far |
 WinNavigator WinNavigator |
 Frigate Frigate |
 Norton
Commander Norton
Commander |
 WinNC WinNC |
 Dos
Navigator Dos
Navigator |
 Servant
Salamander Servant
Salamander |
 Turbo
Browser Turbo
Browser |
|
|
 Winamp,
Skins, Plugins Winamp,
Skins, Plugins |
 Необходимые
Утилиты Необходимые
Утилиты |
 Текстовые
редакторы Текстовые
редакторы |
 Юмор Юмор |
|
|
|
File managers and best utilites |
Реферат на тему Физико химические методы анализа их классификация и основные при мы. Физико химические методы анализа реферат
Физико-химические методы анализа, их классификация и основные приёмы
Физик-химические методы анализа, их классификация и основные приёмы
Физико-химические методы анализа (ФХМА) основаны на использовании зависимости физических свойств веществ (например, светопоглощения, электрической проводимости и т.д.) от их химического состава. Иногда в литературе от ФХМА отделяют физические методы анализа, подчёркивая тем самым, что в ФХМА используется химическая реакция, а в физических - нет. Физические методы анализа и ФХМА, главным образом в западной литературе, называют инструментальными, так как они обычно требуют применения приборов, измерительных инструментов. Инструментальные методы анализа в основном имеют свою собственную теорию, отличную от теории методов химического (классического) анализа (титриметрии и гравиметрии). Базисом этой теории является взаимодействие вещества с потоком энергии.
При использовании ФХМА для получения информации о химическом составе вещества исследуемый образец подвергают воздействию какого-либо вида энергии. В зависимости от вида энергии в веществе происходит изменение энергетического состояния составляющих его частиц (молекул, ионов, атомов), выражающееся в изменении того или иного свойства (например окраски, магнитных свойств и т.п.). Регистрируя изменение этого свойства как аналитический сигнал, получают информацию о качественном и количественном составе исследуемого объекта или о его структуре.
По виду энергии возмущения и измеряемого свойства (аналитического сигнала) ФХМА можно классифицировать следующим образом (табл.2.1.1).
Кроме перечисленных в таблице существует множество других частных ФХМА, не подпадающих под данную классификацию.
Наибольшее практическое применение имеют оптические, хроматографические и потенциометрические методы анализа.
Таблица 2.1.1.
Вид энергии возмущения | Измеряемое свойство | Название метода | Название группы методов |
Поток электронов (эле-ктрохимические реак-ции в растворах и на электродах) | Напряжение, потенциал | Потенциометрия | Электрохимические |
Ток поляризации электродов | Вольтамперо - метрия, полярография | ||
Сила тока | Амперометрия | ||
Сопротивление, проводимость | Кондуктометрия | ||
Импеданс (сопротивление переменному току, ёмкость) | Осциллометрия, высокочастотная кондуктометрия | ||
Количество электричества | Кулонометрия | ||
Масса продукта электрохимической реакции | Электрограви-метрия | ||
Диэлектрическая проницаемость | Диэлкометрия | ||
Электромагнитное излучение | Длина волны и интенсивность спектральной линии в инфракрасной, видимой и ультрафиолетовой частях спектра =10-3...10-8 м | Оптические методы (ИК - спектро-скопия, атомно-эмиссионный анализ, атомно-абсорбционный анализ, фотомет-рия, люминис - центный анализ, турбидиметрия, нефелометрия) | Спектральные |
То же, в рентгеновской области спектра =10-8...10-11 м | Рентгеновская фотоэлектронная, оже-спектроско-пия | ||
Времена релаксации и химический сдвиг | Спектроскопия ядерномагнитного (ЯМР) и электронного парамагнитного (ЭПР) резонанса | ||
Теплота | Температура | Термический анализ | Тепловые |
Термограви - метрия | |||
Количество теплоты | Калориметрия | ||
Энтальпия | Термометрический анализ (энтальпиметрия) | ||
Механические свойства | Дилатометрия | ||
Энергия химических и физических (Ван-дер-Ваальсо-вые силы) взаимодействий | Электропроводность Теплопроводность Ток ионизации | Газовая, жидкостная, осадочная, ионообменная, гельпроникающая хроматографии | Хроматографические |
По сравнению с классическими химическими методами ФХМА отличаются меньшим пределом обнаружения, временем и трудоёмкостью. ФХМА позволяют проводить анализ на расстоянии, автоматизировать процесс анализа и выполнять его без разрушения образца (недеструктивный анализ).
По способам определения различают прямые и косвенные ФХМА. В прямых методах количество вещества находят непосредственным пересчётом измеренного аналитического сигнала в количество вещества (массу, концентрацию) с помощью уравнения связи. В косвенных методах аналитический сигнал используется для установления конца химической реакции (как своеобразный индикатор), а количество определяемого вещества, вступившего в реакцию, находят с помощью закона эквивалентов, т.е. по уравнению, непосредственно не связанному с названием метода.
По способу количественных определений различают без эталонные и эталонные инструментальные методы анализа.
Без эталонные методы основаны на строгих закономерностях, формульное выражение которых позволяет пересчитать интенсивность измеренного аналитического сигнала непосредственно в количестве определяемого вещества с привлечением только табличных величин. В качестве такой закономерности может выступать, например, закон Фарадея, позволяющий по току и времени электролиза рассчитать количество определяемого вещества в растворе при кулонометрическом титровании. Безэталонных методов очень мало, поскольку каждое аналитическое определение представляет собой систему сложных процессов, в которых невозможно теоретически учесть влияние каждого из многочисленных действующих факторов на результат анализа. В связи с этим при анализах пользуются определёнными приёмами, позволяющими экспериментально учесть эти влияния. Наиболее распространённым приёмом является применение эталонов, т.е. образцов веществ или материалов с точно известным содержанием определяемого элемента (или нескольких элементов). При проведении анализа измеряют определяемое вещество исследуемого образца и эталона, сравнивают полученные данные и по известному содержанию элемента в эталоне рассчитывают содержание этого элемента в анализируемом образце. Эталоны могут быть изготовлены промышленным способом (стандартные образцы, стали-нормали) или приготовляются в лаборатории непосредственно перед проведением анализа (образцы сравнения). Если в качестве стандартных образцов применяют химически чистые вещества (примесей меньше 0.05%), то их называют стандартными веществами.
На практике количественные определения инструментальными методами осуществляют по одному из трёх способов: градуировочной функции (стандартных серий), стандартов (сравнения) или стандартных добавок.
При работе по методу градуировочной функции с помощью стандартных веществ или стандартных образцов получают ряд образцов (или растворов), содержащих различные, но точно известные количества определяемого компонента. Иногда этот ряд называют стандартной серией. Затем проводят анализ этой стандартной серии и по полученным данным вычисляют значение чувствительности К (в случае линейной градуировочной функции). После этого измеряют интенсивность аналитического сигнала А в исследуемом объекте и вычисляют количество (массу, концентрацию) искомого компонента с помощью уравнения связи или находят по градуировочному графику (см. рис.2.1.1).
или находят по градуировочному графику (см. рис.2.1.1).
Метод сравнения (стандартов) применим только для линейной градуировочной функции. Определение данного компонента проводят в стандартном образце (стандартном веществе) и получают
 .
.
Потом определяют в анализируемом объекте

 .
.
Делением первого уравнения на второе исключают чувствительность
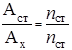
и вычисляют результат анализа
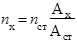 .
.
Метод стандартных добавок применим тоже только к линейной градуировочной функции. В этом методе сначала проводят анализ навески исследуемого объекта и получают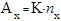 , затем к навеске добавляют известное количество (массу, объём раствора) определяемого компонента и после анализа получают
, затем к навеске добавляют известное количество (массу, объём раствора) определяемого компонента и после анализа получают
 .
.
Делением первого уравнения на второе исключают К и получают формулу для расчёта результатов анализа:
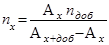 .
.
Спектр вещества получают, воздействуя на него температурой, потоком электронов, световым потоком (электромагнитной энергией) с определённой длиной волны (частоты излучения) и другими способами. При определённой величине энергии воздействия вещество способно перейти в возбуждённое состояние. При этом происходят процессы, приводящие к появлению в спектре излучения с определённой длиной волны (табл.2.2.1).
Излучение, поглощение, рассеяние или рефракция электромагнитного излучения может рассматриваться как аналитический сигнал, несущий информацию о качественном и количественном составе вещества или о его структуре. Частота (длина волны) излучения определяется составом исследуемого вещества, а интенсивность излучения пропорциональна числу частиц, вызвавших его появление, т.е. количеству вещества или компонента смеси.
Каждый из аналитических методов обычно использует не полный спектр вещества, охватывающий диапазон длин волн от рентгеновских излучений до радиоволн, а только определённую его часть. Спектральные методы обычно различают по диапазону длин волн спектра, являющемуся рабочим для данного метода: ультрафиолетовые (УФ), рентгеновские, инфракрасные (ИК), микроволновые и т.д.
Методы, работающие в УФ, видимом и ИК диапазоне называют оптическими. Они больше всего применяются в спектральных методах вследствие сравнительной простоты оборудования для получения и регистрации спектра.
Атомно-эмиссионный анализ (АЭА) основан на качественном и количественном определении атомного состава вещества путём получения и изучения спектров эмиссии атомов, входящих в состав вещества.
Пи АЭА анализируемая проба вещества вводится в источник возбуждения спектрального прибора. В источнике возбуждения данная проба подвергается сложным процессам, заключающимся в плавлении, испарении, диссоциации молекул, ионизации атомов, возбуждении атомов и ионов.
Возбуждённые атомы и ионы через очень короткое время (~10-7-108с) самопроизвольно возвращаются из неустойчивого возбуждённого состояния в нормальное или промежуточное состояние. Это приводит к излучению света с частотой и появлению спектральной линии.
Общую схему атомной эмиссии можно представить так:
А + Е А* А + h
Степень и интенсивность протекания этих процессов зависит от энергии источника возбуждения (ИВ).
Наиболее распространёнными ИВ являются: газовое пламя, дуговые и искровые разряды, индукционно связанная плазма (ИСП). Их энергетической характеристикой можно считать температуру.
Количественный АЭА основан на зависимости между концентрацией элемента и интенсивностью его спектральных линий, которая определяется формулой Ломакина:
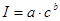 ,
,
где I - интенсивность спектральной линии определяемого элемента; c - концентрация; a и b - константы.
Величины a и b зависят от свойств аналитической линии, ИВ, соотношения концентраций элементов в пробе, поэтому зависимость обычно устанавливается эмпирически для каждого элемента и каждого образца. На практике обычно пользуются методом сравнения с эталоном.
обычно устанавливается эмпирически для каждого элемента и каждого образца. На практике обычно пользуются методом сравнения с эталоном.
При количественных определениях используют в основном фотографический способ регистрации спектра. Интенсивность спектральной линии, получаемой на фотопластинке, характеризуется ее почернением:
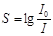 ,
,
где S - степень почернения фотопластинки; I0 - интенсивность света проходящего через незачерненную часть пластинки, а I - через зачерненную, т.е. спектральную линию. Измерение почернения спектральной линии проводят по сравнению с почернением фона или по отношению к интенсивности линии сравнения. Полученная разность почернений (S) прямо пропорциональна логарифму концентрации (с):
S = K lgc.
При методе трех эталонов на одной фотопластинке фотографируют спектры трех эталонов с известным содержанием элементов и спектр анализируемого образца. Измеряют почернение выбранных линий. Строят градуировочный график, по которому находят содержание изучаемых элементов.
В случае анализа однотипных объектов применяют метод постоянного графика, который строят по большому числу эталонов. Затем в строго одинаковых условиях снимают спектр образца и одного из эталонов. По спектру эталона проверяют не произошло ли смещение графика. Если смещения нет, то неизвестную концентрацию находят по постоянному графику, а если есть, то величину смещения учитывают с помощью спектра эталона.
При количественном АЭА погрешность определения содержания основы составляет 1-5%, а примеси - до 20%. Визуальный метод регистрации спектра быстрее, но менее точен, чем фотографический.
По аппаратурному оформлению можно выделить АЭА с визуальной, фотографической и фотоэлектрической регистрацией и измерением интенсивности спектральных линий.
Визуальные методы (регистрация с помощью глаза) можно использовать только для исследования спектров с длинами волн в области 400 - 700 нм. Средняя спектральная чувствительность глаза максимальна для желто-зеленого света с длиной волны 550 нм. Визуально можно с достаточной точностью установить равенство интенсивностей линий с ближайшими длинами волн или определить наиболее яркую линию. Визуальные методы делятся на стилоскопические и стилометрические.
Стилоскопический анализ основан на визуальном сравнении интенсивностей спектральных линий анализируемого элемента (примеси) и близлежащих линий спектра основного элемента пробы. Например, при анализе сталей обычно сравнивают интенсивности спектральных линий примеси и железа. При этом используют заранее известные стилоскопические признаки, в которых равенству интенсивности линий определенной аналитической пары соответствует определенная концентрация анализируемого элемента.
Стилоскопы используют для экспресс-анализа, для которого не требуется высокой точности.6-7 элементов определяют за 2-3 мин. Чувствительность анализа 0,01-0,1%. Для анализа применяют как стационарные стилоскопы СЛ-3... СЛ-12, так и переносные СЛП-1... СЛП-4.
Стилометрический анализ отличается от стилоскопического тем, что более яркую линию аналитической пары ослабляют при помощи специального устройства (фотометра) до установления равенства интенсивностей обеих линий. Кроме того, стилометры позволяют сближать в поле зрения аналитическую линию и линию сравнения, что значительно повышает точность измерений. Для анализа применяют стилометры СТ-1... СТ-7.
Относительная погрешность визуальных измерений 1 – 3%. Их недостатками являются ограниченность видимой области спектра, утомительность, отсутствие объективной документации о проведении анализа.
Фотографические методы основаны на фотографической регистрации спектра с помощью специальных приборов-спектрографов. Рабочая область спектрографов ограничена длиной волны 1000 нм, т.е. их можно использовать в видимой области и УФ. Интенсивность спектральных линий измеряют по степени почернения их изображения на фотопластинке или фотопленке.
superbotanik.net
Курсовая работа - Физико-химические методы анализа, их классификация и основные приёмы
Физик-химические методы анализа, их классификация и основные приёмы
Физико-химические методы анализа (ФХМА) основаны на использовании зависимости физических свойств веществ (например, светопоглощения, электрической проводимости и т.д.) от их химического состава. Иногда в литературе от ФХМА отделяют физические методы анализа, подчёркивая тем самым, что в ФХМА используется химическая реакция, а в физических — нет. Физические методы анализа и ФХМА, главным образом в западной литературе, называют инструментальными, так как они обычно требуют применения приборов, измерительных инструментов. Инструментальные методы анализа в основном имеют свою собственную теорию, отличную от теории методов химического (классического) анализа (титриметрии и гравиметрии). Базисом этой теории является взаимодействие вещества с потоком энергии.
При использовании ФХМА для получения информации о химическом составе вещества исследуемый образец подвергают воздействию какого-либо вида энергии. В зависимости от вида энергии в веществе происходит изменение энергетического состояния составляющих его частиц (молекул, ионов, атомов), выражающееся в изменении того или иного свойства (например окраски, магнитных свойств и т.п.). Регистрируя изменение этого свойства как аналитический сигнал, получают информацию о качественном и количественном составе исследуемого объекта или о его структуре.
По виду энергии возмущения и измеряемого свойства (аналитического сигнала) ФХМА можно классифицировать следующим образом (табл.2.1.1).
Кроме перечисленных в таблице существует множество других частных ФХМА, не подпадающих под данную классификацию.
Наибольшее практическое применение имеют оптические, хроматографические и потенциометрические методы анализа.
Таблица 2.1.1.
Вид энергии возмущения | Измеряемое свойство | Название метода | Название группы методов |
Поток электронов (эле-ктрохимические реак-ции в растворах и на электродах) | Напряжение, потенциал | Потенциометрия | Электрохимические |
Ток поляризации электродов | Вольтамперо — метрия, полярография | ||
Сила тока | Амперометрия | ||
Сопротивление, проводимость | Кондуктометрия | ||
Импеданс (сопротивление переменному току, ёмкость) | Осциллометрия, высокочастотная кондуктометрия | ||
Количество электричества | Кулонометрия | ||
Масса продукта электрохимической реакции | Электрограви-метрия | ||
Диэлектрическая проницаемость | Диэлкометрия | ||
Электромагнитное излучение | Длина волны и интенсивность спектральной линии в инфракрасной, видимой и ультрафиолетовой частях спектра =10-3...10-8 м | Оптические методы (ИК — спектро-скопия, атомно-эмиссионный анализ, атомно-абсорбционный анализ, фотомет-рия, люминис — центный анализ, турбидиметрия, нефелометрия) | Спектральные |
То же, в рентгеновской области спектра =10-8...10-11 м | Рентгеновская фотоэлектронная, оже-спектроско-пия | ||
Времена релаксации и химический сдвиг | Спектроскопия ядерномагнитного (ЯМР) и электронного парамагнитного (ЭПР) резонанса | ||
Теплота | Температура | Термический анализ | Тепловые |
Термограви — метрия | |||
Количество теплоты | Калориметрия | ||
Энтальпия | Термометрический анализ (энтальпиметрия) | ||
Механические свойства | Дилатометрия | ||
Энергия химических и физических (Ван-дер-Ваальсо-вые силы) взаимодействий | Электропроводность Теплопроводность Ток ионизации | Газовая, жидкостная, осадочная, ионообменная, гельпроникающая хроматографии | Хроматографические |
По сравнению с классическими химическими методами ФХМА отличаются меньшим пределом обнаружения, временем и трудоёмкостью. ФХМА позволяют проводить анализ на расстоянии, автоматизировать процесс анализа и выполнять его без разрушения образца (недеструктивный анализ).
По способам определения различают прямые и косвенные ФХМА. В прямых методах количество вещества находят непосредственным пересчётом измеренного аналитического сигнала в количество вещества (массу, концентрацию) с помощью уравнения связи. В косвенных методах аналитический сигнал используется для установления конца химической реакции (как своеобразный индикатор), а количество определяемого вещества, вступившего в реакцию, находят с помощью закона эквивалентов, т.е. по уравнению, непосредственно не связанному с названием метода.
По способу количественных определений различают без эталонные и эталонные инструментальные методы анализа.
Без эталонные методы основаны на строгих закономерностях, формульное выражение которых позволяет пересчитать интенсивность измеренного аналитического сигнала непосредственно в количестве определяемого вещества с привлечением только табличных величин. В качестве такой закономерности может выступать, например, закон Фарадея, позволяющий по току и времени электролиза рассчитать количество определяемого вещества в растворе при кулонометрическом титровании. Безэталонных методов очень мало, поскольку каждое аналитическое определение представляет собой систему сложных процессов, в которых невозможно теоретически учесть влияние каждого из многочисленных действующих факторов на результат анализа. В связи с этим при анализах пользуются определёнными приёмами, позволяющими экспериментально учесть эти влияния. Наиболее распространённым приёмом является применение эталонов, т.е. образцов веществ или материалов с точно известным содержанием определяемого элемента (или нескольких элементов). При проведении анализа измеряют определяемое вещество исследуемого образца и эталона, сравнивают полученные данные и по известному содержанию элемента в эталоне рассчитывают содержание этого элемента в анализируемом образце. Эталоны могут быть изготовлены промышленным способом (стандартные образцы, стали-нормали) или приготовляются в лаборатории непосредственно перед проведением анализа (образцы сравнения). Если в качестве стандартных образцов применяют химически чистые вещества (примесей меньше 0.05%), то их называют стандартными веществами.
На практике количественные определения инструментальными методами осуществляют по одному из трёх способов: градуировочной функции (стандартных серий), стандартов (сравнения) или стандартных добавок.
При работе по методу градуировочной функции с помощью стандартных веществ или стандартных образцов получают ряд образцов (или растворов), содержащих различные, но точно известные количества определяемого компонента. Иногда этот ряд называют стандартной серией. Затем проводят анализ этой стандартной серии и по полученным данным вычисляют значение чувствительности К (в случае линейной градуировочной функции). После этого измеряют интенсивность аналитического сигнала А в исследуемом объекте и вычисляют количество (массу, концентрацию) искомого компонента с помощью уравнения связи  или находят по градуировочному графику (см. рис.2.1.1).
или находят по градуировочному графику (см. рис.2.1.1).
Метод сравнения (стандартов) применим только для линейной градуировочной функции. Определение данного компонента проводят в стандартном образце (стандартном веществе) и получают
 .
.
Потом определяют в анализируемом объекте

 .
.
Делением первого уравнения на второе исключают чувствительность

и вычисляют результат анализа
 .
.
Метод стандартных добавок применим тоже только к линейной градуировочной функции. В этом методе сначала проводят анализ навески исследуемого объекта и получают  , затем к навеске добавляют известное количество (массу, объём раствора) определяемого компонента и после анализа получают
, затем к навеске добавляют известное количество (массу, объём раствора) определяемого компонента и после анализа получают
 .
.
Делением первого уравнения на второе исключают К и получают формулу для расчёта результатов анализа:
 .
.
Спектр вещества получают, воздействуя на него температурой, потоком электронов, световым потоком (электромагнитной энергией) с определённой длиной волны (частоты излучения) и другими способами. При определённой величине энергии воздействия вещество способно перейти в возбуждённое состояние. При этом происходят процессы, приводящие к появлению в спектре излучения с определённой длиной волны (табл.2.2.1).
Излучение, поглощение, рассеяние или рефракция электромагнитного излучения может рассматриваться как аналитический сигнал, несущий информацию о качественном и количественном составе вещества или о его структуре. Частота (длина волны) излучения определяется составом исследуемого вещества, а интенсивность излучения пропорциональна числу частиц, вызвавших его появление, т.е. количеству вещества или компонента смеси.
Каждый из аналитических методов обычно использует не полный спектр вещества, охватывающий диапазон длин волн от рентгеновских излучений до радиоволн, а только определённую его часть. Спектральные методы обычно различают по диапазону длин волн спектра, являющемуся рабочим для данного метода: ультрафиолетовые (УФ), рентгеновские, инфракрасные (ИК), микроволновые и т.д.
Методы, работающие в УФ, видимом и ИК диапазоне называют оптическими. Они больше всего применяются в спектральных методах вследствие сравнительной простоты оборудования для получения и регистрации спектра.
Атомно-эмиссионный анализ (АЭА) основан на качественном и количественном определении атомного состава вещества путём получения и изучения спектров эмиссии атомов, входящих в состав вещества.
Пи АЭА анализируемая проба вещества вводится в источник возбуждения спектрального прибора. В источнике возбуждения данная проба подвергается сложным процессам, заключающимся в плавлении, испарении, диссоциации молекул, ионизации атомов, возбуждении атомов и ионов.
Возбуждённые атомы и ионы через очень короткое время (~10-7-108с) самопроизвольно возвращаются из неустойчивого возбуждённого состояния в нормальное или промежуточное состояние. Это приводит к излучению света с частотой и появлению спектральной линии.
Общую схему атомной эмиссии можно представить так:
А + Е А* А + h
Степень и интенсивность протекания этих процессов зависит от энергии источника возбуждения (ИВ).
Наиболее распространёнными ИВ являются: газовое пламя, дуговые и искровые разряды, индукционно связанная плазма (ИСП). Их энергетической характеристикой можно считать температуру.
Количественный АЭА основан на зависимости между концентрацией элемента и интенсивностью его спектральных линий, которая определяется формулой Ломакина:
 ,
,
где I — интенсивность спектральной линии определяемого элемента; c — концентрация; a и b — константы.
Величины a и b зависят от свойств аналитической линии, ИВ, соотношения концентраций элементов в пробе, поэтому зависимость  обычно устанавливается эмпирически для каждого элемента и каждого образца. На практике обычно пользуются методом сравнения с эталоном.
обычно устанавливается эмпирически для каждого элемента и каждого образца. На практике обычно пользуются методом сравнения с эталоном.
При количественных определениях используют в основном фотографический способ регистрации спектра. Интенсивность спектральной линии, получаемой на фотопластинке, характеризуется ее почернением:
 ,
,
где S — степень почернения фотопластинки; I0 — интенсивность света проходящего через незачерненную часть пластинки, а I — через зачерненную, т.е. спектральную линию. Измерение почернения спектральной линии проводят по сравнению с почернением фона или по отношению к интенсивности линии сравнения. Полученная разность почернений (S) прямо пропорциональна логарифму концентрации (с):
S = K lgc.
При методе трех эталонов на одной фотопластинке фотографируют спектры трех эталонов с известным содержанием элементов и спектр анализируемого образца. Измеряют почернение выбранных линий. Строят градуировочный график, по которому находят содержание изучаемых элементов.
В случае анализа однотипных объектов применяют метод постоянного графика, который строят по большому числу эталонов. Затем в строго одинаковых условиях снимают спектр образца и одного из эталонов. По спектру эталона проверяют не произошло ли смещение графика. Если смещения нет, то неизвестную концентрацию находят по постоянному графику, а если есть, то величину смещения учитывают с помощью спектра эталона.
При количественном АЭА погрешность определения содержания основы составляет 1-5%, а примеси — до 20%. Визуальный метод регистрации спектра быстрее, но менее точен, чем фотографический.
По аппаратурному оформлению можно выделить АЭА с визуальной, фотографической и фотоэлектрической регистрацией и измерением интенсивности спектральных линий.
Визуальные методы (регистрация с помощью глаза) можно использовать только для исследования спектров с длинами волн в области 400 — 700 нм. Средняя спектральная чувствительность глаза максимальна для желто-зеленого света с длиной волны 550 нм. Визуально можно с достаточной точностью установить равенство интенсивностей линий с ближайшими длинами волн или определить наиболее яркую линию. Визуальные методы делятся на стилоскопические и стилометрические.
Стилоскопический анализ основан на визуальном сравнении интенсивностей спектральных линий анализируемого элемента (примеси) и близлежащих линий спектра основного элемента пробы. Например, при анализе сталей обычно сравнивают интенсивности спектральных линий примеси и железа. При этом используют заранее известные стилоскопические признаки, в которых равенству интенсивности линий определенной аналитической пары соответствует определенная концентрация анализируемого элемента.
Стилоскопы используют для экспресс-анализа, для которого не требуется высокой точности.6-7 элементов определяют за 2-3 мин. Чувствительность анализа 0,01-0,1%. Для анализа применяют как стационарные стилоскопы СЛ-3… СЛ-12, так и переносные СЛП-1… СЛП-4.
Стилометрический анализ отличается от стилоскопического тем, что более яркую линию аналитической пары ослабляют при помощи специального устройства (фотометра) до установления равенства интенсивностей обеих линий. Кроме того, стилометры позволяют сближать в поле зрения аналитическую линию и линию сравнения, что значительно повышает точность измерений. Для анализа применяют стилометры СТ-1… СТ-7.
Относительная погрешность визуальных измерений 1 – 3%. Их недостатками являются ограниченность видимой области спектра, утомительность, отсутствие объективной документации о проведении анализа.
Фотографические методы основаны на фотографической регистрации спектра с помощью специальных приборов-спектрографов. Рабочая область спектрографов ограничена длиной волны 1000 нм, т.е. их можно использовать в видимой области и УФ. Интенсивность спектральных линий измеряют по степени почернения их изображения на фотопластинке или фотопленке.
www.ronl.ru
Реферат на тему Физико химические методы анализа их классификация и основные при мы
Физик-химические методы анализа, их классификация и основные приёмы
Физико-химические методы анализа (ФХМА) основаны на использовании зависимости физических свойств веществ (например, светопоглощения, электрической проводимости и т.д.) от их химического состава. Иногда в литературе от ФХМА отделяют физические методы анализа, подчёркивая тем самым, что в ФХМА используется химическая реакция, а в физических - нет. Физические методы анализа и ФХМА, главным образом в западной литературе, называют инструментальными, так как они обычно требуют применения приборов, измерительных инструментов. Инструментальные методы анализа в основном имеют свою собственную теорию, отличную от теории методов химического (классического) анализа (титриметрии и гравиметрии). Базисом этой теории является взаимодействие вещества с потоком энергии. При использовании ФХМА для получения информации о химическом составе вещества исследуемый образец подвергают воздействию какого-либо вида энергии. В зависимости от вида энергии в веществе происходит изменение энергетического состояния составляющих его частиц (молекул, ионов, атомов), выражающееся в изменении того или иного свойства (например окраски, магнитных свойств и т.п.). Регистрируя изменение этого свойства как аналитический сигнал, получают информацию о качественном и количественном составе исследуемого объекта или о его структуре. По виду энергии возмущения и измеряемого свойства (аналитического сигнала) ФХМА можно классифицировать следующим образом (табл.2.1.1). Кроме перечисленных в таблице существует множество других частных ФХМА, не подпадающих под данную классификацию. Наибольшее практическое применение имеют оптические, хроматографические и потенциометрические методы анализа.Таблица 2.1.1.
| Вид энергии возмущения | Измеряемое свойство | Название метода | Название группы методов |
| Поток электронов (эле-ктрохимические реак-ции в растворах и на электродах) | Напряжение, потенциал | Потенциометрия | Электрохимические |
| Ток поляризации электродов | Вольтамперо - метрия, полярография | ||
| Сила тока | Амперометрия | ||
| Сопротивление, проводимость | Кондуктометрия | ||
| Импеданс (сопротивление переменному току, ёмкость) | Осциллометрия, высокочастотная кондуктометрия | ||
| Количество электричества | Кулонометрия | ||
| Масса продукта электрохимической реакции | Электрограви-метрия | ||
| Диэлектрическая проницаемость | Диэлкометрия | ||
| Электромагнитное излучение | Длина волны и интенсивность спектральной линии в инфракрасной, видимой и ультрафиолетовой частях спектра =10-3...10-8 м | Оптические методы (ИК - спектро-скопия, атомно-эмиссионный анализ, атомно-абсорбционный анализ, фотомет-рия, люминис - центный анализ, турбидиметрия, нефелометрия) | Спектральные |
| То же, в рентгеновской области спектра =10-8...10-11 м | Рентгеновская фотоэлектронная, оже-спектроско-пия | ||
| Времена релаксации и химический сдвиг | Спектроскопия ядерномагнитного (ЯМР) и электронного парамагнитного (ЭПР) резонанса | ||
| Теплота | Температура | Термический анализ | Тепловые |
| Термограви - метрия | |||
| Количество теплоты | Калориметрия | ||
| Энтальпия | Термометрический анализ (энтальпиметрия) | ||
| Механические свойства | Дилатометрия | ||
| Энергия химических и физических (Ван-дер-Ваальсо-вые силы) взаимодействий | Электропроводность Теплопроводность Ток ионизации | Газовая, жидкостная, осадочная, ионообменная, гельпроникающая хроматографии | Хроматографические |
 или находят по градуировочному графику (см. рис.2.1.1). Метод сравнения (стандартов) применим только для линейной градуировочной функции. Определение данного компонента проводят в стандартном образце (стандартном веществе) и получают
или находят по градуировочному графику (см. рис.2.1.1). Метод сравнения (стандартов) применим только для линейной градуировочной функции. Определение данного компонента проводят в стандартном образце (стандартном веществе) и получают . Потом определяют в анализируемом объекте
. Потом определяют в анализируемом объекте
 . Делением первого уравнения на второе исключают чувствительность
. Делением первого уравнения на второе исключают чувствительность и вычисляют результат анализа
и вычисляют результат анализа . Метод стандартных добавок применим тоже только к линейной градуировочной функции. В этом методе сначала проводят анализ навески исследуемого объекта и получают
. Метод стандартных добавок применим тоже только к линейной градуировочной функции. В этом методе сначала проводят анализ навески исследуемого объекта и получают  , затем к навеске добавляют известное количество (массу, объём раствора) определяемого компонента и после анализа получают
, затем к навеске добавляют известное количество (массу, объём раствора) определяемого компонента и после анализа получают . Делением первого уравнения на второе исключают К и получают формулу для расчёта результатов анализа:
. Делением первого уравнения на второе исключают К и получают формулу для расчёта результатов анализа:  . Спектр вещества получают, воздействуя на него температурой, потоком электронов, световым потоком (электромагнитной энергией) с определённой длиной волны (частоты излучения) и другими способами. При определённой величине энергии воздействия вещество способно перейти в возбуждённое состояние. При этом происходят процессы, приводящие к появлению в спектре излучения с определённой длиной волны (табл.2.2.1). Излучение, поглощение, рассеяние или рефракция электромагнитного излучения может рассматриваться как аналитический сигнал, несущий информацию о качественном и количественном составе вещества или о его структуре. Частота (длина волны) излучения определяется составом исследуемого вещества, а интенсивность излучения пропорциональна числу частиц, вызвавших его появление, т.е. количеству вещества или компонента смеси. Каждый из аналитических методов обычно использует не полный спектр вещества, охватывающий диапазон длин волн от рентгеновских излучений до радиоволн, а только определённую его часть. Спектральные методы обычно различают по диапазону длин волн спектра, являющемуся рабочим для данного метода: ультрафиолетовые (УФ), рентгеновские, инфракрасные (ИК), микроволновые и т.д. Методы, работающие в УФ, видимом и ИК диапазоне называют оптическими. Они больше всего применяются в спектральных методах вследствие сравнительной простоты оборудования для получения и регистрации спектра. Атомно-эмиссионный анализ (АЭА) основан на качественном и количественном определении атомного состава вещества путём получения и изучения спектров эмиссии атомов, входящих в состав вещества. Пи АЭА анализируемая проба вещества вводится в источник возбуждения спектрального прибора. В источнике возбуждения данная проба подвергается сложным процессам, заключающимся в плавлении, испарении, диссоциации молекул, ионизации атомов, возбуждении атомов и ионов. Возбуждённые атомы и ионы через очень короткое время (~10-7-108с) самопроизвольно возвращаются из неустойчивого возбуждённого состояния в нормальное или промежуточное состояние. Это приводит к излучению света с частотой и появлению спектральной линии. Общую схему атомной эмиссии можно представить так: А + Е А* А + h Степень и интенсивность протекания этих процессов зависит от энергии источника возбуждения (ИВ). Наиболее распространёнными ИВ являются: газовое пламя, дуговые и искровые разряды, индукционно связанная плазма (ИСП). Их энергетической характеристикой можно считать температуру. Количественный АЭА основан на зависимости между концентрацией элемента и интенсивностью его спектральных линий, которая определяется формулой Ломакина:
. Спектр вещества получают, воздействуя на него температурой, потоком электронов, световым потоком (электромагнитной энергией) с определённой длиной волны (частоты излучения) и другими способами. При определённой величине энергии воздействия вещество способно перейти в возбуждённое состояние. При этом происходят процессы, приводящие к появлению в спектре излучения с определённой длиной волны (табл.2.2.1). Излучение, поглощение, рассеяние или рефракция электромагнитного излучения может рассматриваться как аналитический сигнал, несущий информацию о качественном и количественном составе вещества или о его структуре. Частота (длина волны) излучения определяется составом исследуемого вещества, а интенсивность излучения пропорциональна числу частиц, вызвавших его появление, т.е. количеству вещества или компонента смеси. Каждый из аналитических методов обычно использует не полный спектр вещества, охватывающий диапазон длин волн от рентгеновских излучений до радиоволн, а только определённую его часть. Спектральные методы обычно различают по диапазону длин волн спектра, являющемуся рабочим для данного метода: ультрафиолетовые (УФ), рентгеновские, инфракрасные (ИК), микроволновые и т.д. Методы, работающие в УФ, видимом и ИК диапазоне называют оптическими. Они больше всего применяются в спектральных методах вследствие сравнительной простоты оборудования для получения и регистрации спектра. Атомно-эмиссионный анализ (АЭА) основан на качественном и количественном определении атомного состава вещества путём получения и изучения спектров эмиссии атомов, входящих в состав вещества. Пи АЭА анализируемая проба вещества вводится в источник возбуждения спектрального прибора. В источнике возбуждения данная проба подвергается сложным процессам, заключающимся в плавлении, испарении, диссоциации молекул, ионизации атомов, возбуждении атомов и ионов. Возбуждённые атомы и ионы через очень короткое время (~10-7-108с) самопроизвольно возвращаются из неустойчивого возбуждённого состояния в нормальное или промежуточное состояние. Это приводит к излучению света с частотой и появлению спектральной линии. Общую схему атомной эмиссии можно представить так: А + Е А* А + h Степень и интенсивность протекания этих процессов зависит от энергии источника возбуждения (ИВ). Наиболее распространёнными ИВ являются: газовое пламя, дуговые и искровые разряды, индукционно связанная плазма (ИСП). Их энергетической характеристикой можно считать температуру. Количественный АЭА основан на зависимости между концентрацией элемента и интенсивностью его спектральных линий, которая определяется формулой Ломакина:  , где I - интенсивность спектральной линии определяемого элемента; c - концентрация; a и b - константы. Величины a и b зависят от свойств аналитической линии, ИВ, соотношения концентраций элементов в пробе, поэтому зависимость
, где I - интенсивность спектральной линии определяемого элемента; c - концентрация; a и b - константы. Величины a и b зависят от свойств аналитической линии, ИВ, соотношения концентраций элементов в пробе, поэтому зависимость  обычно устанавливается эмпирически для каждого элемента и каждого образца. На практике обычно пользуются методом сравнения с эталоном. При количественных определениях используют в основном фотографический способ регистрации спектра. Интенсивность спектральной линии, получаемой на фотопластинке, характеризуется ее почернением:
обычно устанавливается эмпирически для каждого элемента и каждого образца. На практике обычно пользуются методом сравнения с эталоном. При количественных определениях используют в основном фотографический способ регистрации спектра. Интенсивность спектральной линии, получаемой на фотопластинке, характеризуется ее почернением:  , где S - степень почернения фотопластинки; I0 - интенсивность света проходящего через незачерненную часть пластинки, а I - через зачерненную, т.е. спектральную линию. Измерение почернения спектральной линии проводят по сравнению с почернением фона или по отношению к интенсивности линии сравнения. Полученная разность почернений (S) прямо пропорциональна логарифму концентрации (с): S = K lgc. При методе трех эталонов на одной фотопластинке фотографируют спектры трех эталонов с известным содержанием элементов и спектр анализируемого образца. Измеряют почернение выбранных линий. Строят градуировочный график, по которому находят содержание изучаемых элементов. В случае анализа однотипных объектов применяют метод постоянного графика, который строят по большому числу эталонов. Затем в строго одинаковых условиях снимают спектр образца и одного из эталонов. По спектру эталона проверяют не произошло ли смещение графика. Если смещения нет, то неизвестную концентрацию находят по постоянному графику, а если есть, то величину смещения учитывают с помощью спектра эталона. При количественном АЭА погрешность определения содержания основы составляет 1-5%, а примеси - до 20%. Визуальный метод регистрации спектра быстрее, но менее точен, чем фотографический. По аппаратурному оформлению можно выделить АЭА с визуальной, фотографической и фотоэлектрической регистрацией и измерением интенсивности спектральных линий. Визуальные методы (регистрация с помощью глаза) можно использовать только для исследования спектров с длинами волн в области 400 - 700 нм. Средняя спектральная чувствительность глаза максимальна для желто-зеленого света с длиной волны 550 нм. Визуально можно с достаточной точностью установить равенство интенсивностей линий с ближайшими длинами волн или определить наиболее яркую линию. Визуальные методы делятся на стилоскопические и стилометрические. Стилоскопический анализ основан на визуальном сравнении интенсивностей спектральных линий анализируемого элемента (примеси) и близлежащих линий спектра основного элемента пробы. Например, при анализе сталей обычно сравнивают интенсивности спектральных линий примеси и железа. При этом используют заранее известные стилоскопические признаки, в которых равенству интенсивности линий определенной аналитической пары соответствует определенная концентрация анализируемого элемента. Стилоскопы используют для экспресс-анализа, для которого не требуется высокой точности.6-7 элементов определяют за 2-3 мин. Чувствительность анализа 0,01-0,1%. Для анализа применяют как стационарные стилоскопы СЛ-3... СЛ-12, так и переносные СЛП-1... СЛП-4. Стилометрический анализ отличается от стилоскопического тем, что более яркую линию аналитической пары ослабляют при помощи специального устройства (фотометра) до установления равенства интенсивностей обеих линий. Кроме того, стилометры позволяют сближать в поле зрения аналитическую линию и линию сравнения, что значительно повышает точность измерений. Для анализа применяют стилометры СТ-1... СТ-7. Относительная погрешность визуальных измерений 1 – 3%. Их недостатками являются ограниченность видимой области спектра, утомительность, отсутствие объективной документации о проведении анализа. Фотографические методы основаны на фотографической регистрации спектра с помощью специальных приборов-спектрографов. Рабочая область спектрографов ограничена длиной волны 1000 нм, т.е. их можно использовать в видимой области и УФ. Интенсивность спектральных линий измеряют по степени почернения их изображения на фотопластинке или фотопленке.
, где S - степень почернения фотопластинки; I0 - интенсивность света проходящего через незачерненную часть пластинки, а I - через зачерненную, т.е. спектральную линию. Измерение почернения спектральной линии проводят по сравнению с почернением фона или по отношению к интенсивности линии сравнения. Полученная разность почернений (S) прямо пропорциональна логарифму концентрации (с): S = K lgc. При методе трех эталонов на одной фотопластинке фотографируют спектры трех эталонов с известным содержанием элементов и спектр анализируемого образца. Измеряют почернение выбранных линий. Строят градуировочный график, по которому находят содержание изучаемых элементов. В случае анализа однотипных объектов применяют метод постоянного графика, который строят по большому числу эталонов. Затем в строго одинаковых условиях снимают спектр образца и одного из эталонов. По спектру эталона проверяют не произошло ли смещение графика. Если смещения нет, то неизвестную концентрацию находят по постоянному графику, а если есть, то величину смещения учитывают с помощью спектра эталона. При количественном АЭА погрешность определения содержания основы составляет 1-5%, а примеси - до 20%. Визуальный метод регистрации спектра быстрее, но менее точен, чем фотографический. По аппаратурному оформлению можно выделить АЭА с визуальной, фотографической и фотоэлектрической регистрацией и измерением интенсивности спектральных линий. Визуальные методы (регистрация с помощью глаза) можно использовать только для исследования спектров с длинами волн в области 400 - 700 нм. Средняя спектральная чувствительность глаза максимальна для желто-зеленого света с длиной волны 550 нм. Визуально можно с достаточной точностью установить равенство интенсивностей линий с ближайшими длинами волн или определить наиболее яркую линию. Визуальные методы делятся на стилоскопические и стилометрические. Стилоскопический анализ основан на визуальном сравнении интенсивностей спектральных линий анализируемого элемента (примеси) и близлежащих линий спектра основного элемента пробы. Например, при анализе сталей обычно сравнивают интенсивности спектральных линий примеси и железа. При этом используют заранее известные стилоскопические признаки, в которых равенству интенсивности линий определенной аналитической пары соответствует определенная концентрация анализируемого элемента. Стилоскопы используют для экспресс-анализа, для которого не требуется высокой точности.6-7 элементов определяют за 2-3 мин. Чувствительность анализа 0,01-0,1%. Для анализа применяют как стационарные стилоскопы СЛ-3... СЛ-12, так и переносные СЛП-1... СЛП-4. Стилометрический анализ отличается от стилоскопического тем, что более яркую линию аналитической пары ослабляют при помощи специального устройства (фотометра) до установления равенства интенсивностей обеих линий. Кроме того, стилометры позволяют сближать в поле зрения аналитическую линию и линию сравнения, что значительно повышает точность измерений. Для анализа применяют стилометры СТ-1... СТ-7. Относительная погрешность визуальных измерений 1 – 3%. Их недостатками являются ограниченность видимой области спектра, утомительность, отсутствие объективной документации о проведении анализа. Фотографические методы основаны на фотографической регистрации спектра с помощью специальных приборов-спектрографов. Рабочая область спектрографов ограничена длиной волны 1000 нм, т.е. их можно использовать в видимой области и УФ. Интенсивность спектральных линий измеряют по степени почернения их изображения на фотопластинке или фотопленке. bukvasha.ru
Доклад - Физико-химические методы анализа их классификация и основные приёмы
Физик-химические методы анализа, их классификация и основные приёмы
Физико-химические методы анализа (ФХМА) основаны на использовании зависимости физических свойств веществ (например, светопоглощения, электрической проводимости и т.д.) от их химического состава. Иногда в литературе от ФХМА отделяют физические методы анализа, подчёркивая тем самым, что в ФХМА используется химическая реакция, а в физических — нет. Физические методы анализа и ФХМА, главным образом в западной литературе, называют инструментальными, так как они обычно требуют применения приборов, измерительных инструментов. Инструментальные методы анализа в основном имеют свою собственную теорию, отличную от теории методов химического (классического) анализа (титриметрии и гравиметрии). Базисом этой теории является взаимодействие вещества с потоком энергии.
При использовании ФХМА для получения информации о химическом составе вещества исследуемый образец подвергают воздействию какого-либо вида энергии. В зависимости от вида энергии в веществе происходит изменение энергетического состояния составляющих его частиц (молекул, ионов, атомов), выражающееся в изменении того или иного свойства (например окраски, магнитных свойств и т.п.). Регистрируя изменение этого свойства как аналитический сигнал, получают информацию о качественном и количественном составе исследуемого объекта или о его структуре.
По виду энергии возмущения и измеряемого свойства (аналитического сигнала) ФХМА можно классифицировать следующим образом (табл.2.1.1).
Кроме перечисленных в таблице существует множество других частных ФХМА, не подпадающих под данную классификацию.
Наибольшее практическое применение имеют оптические, хроматографические и потенциометрические методы анализа.
Таблица 2.1.1.
Вид энергии возмущения
Измеряемое свойство
Название метода
Название группы методов
Поток электронов (эле-ктрохимические реак-ции в растворах и на электродах)
Напряжение, потенциал
Потенциометрия
Электрохимические
Ток поляризации электродов
Вольтамперо — метрия, полярография
Сила тока
Амперометрия
Сопротивление, проводимость
Кондуктометрия
Импеданс (сопротивление переменному току, ёмкость)
Осциллометрия, высокочастотная кондуктометрия
Количество электричества
Кулонометрия
Масса продукта электрохимической реакции
Электрограви-метрия
Диэлектрическая проницаемость
Диэлкометрия
Электромагнитное излучение
Длина волны и интенсивность спектральной линии в инфракрасной, видимой и ультрафиолетовой частях спектра =10-3...10-8 м
Оптические методы (ИК — спектро-скопия, атомно-эмиссионный анализ, атомно-абсорбционный анализ, фотомет-рия, люминис — центный анализ, турбидиметрия, нефелометрия)
Спектральные
То же, в рентгеновской области спектра =10-8...10-11 м
Рентгеновская фотоэлектронная, оже-спектроско-пия
Времена релаксации и химический сдвиг
Спектроскопия ядерномагнитного (ЯМР) и электронного парамагнитного (ЭПР) резонанса
Теплота
Температура
Термический анализ
Тепловые
Термограви — метрия
Количество теплоты
Калориметрия
Энтальпия
Термометрический анализ (энтальпиметрия)
Механические свойства
Дилатометрия
Энергия химических и физических (Ван-дер-Ваальсо-вые силы) взаимодействий
Электропроводность Теплопроводность Ток ионизации
Газовая, жидкостная, осадочная, ионообменная, гельпроникающая хроматографии
Хроматографические
По сравнению с классическими химическими методами ФХМА отличаются меньшим пределом обнаружения, временем и трудоёмкостью. ФХМА позволяют проводить анализ на расстоянии, автоматизировать процесс анализа и выполнять его без разрушения образца (недеструктивный анализ).
По способам определения различают прямые и косвенные ФХМА. В прямых методах количество вещества находят непосредственным пересчётом измеренного аналитического сигнала в количество вещества (массу, концентрацию) с помощью уравнения связи. В косвенных методах аналитический сигнал используется для установления конца химической реакции (как своеобразный индикатор), а количество определяемого вещества, вступившего в реакцию, находят с помощью закона эквивалентов, т.е. по уравнению, непосредственно не связанному с названием метода.
По способу количественных определений различают без эталонные и эталонные инструментальные методы анализа.
Без эталонные методы основаны на строгих закономерностях, формульное выражение которых позволяет пересчитать интенсивность измеренного аналитического сигнала непосредственно в количестве определяемого вещества с привлечением только табличных величин. В качестве такой закономерности может выступать, например, закон Фарадея, позволяющий по току и времени электролиза рассчитать количество определяемого вещества в растворе при кулонометрическом титровании. Безэталонных методов очень мало, поскольку каждое аналитическое определение представляет собой систему сложных процессов, в которых невозможно теоретически учесть влияние каждого из многочисленных действующих факторов на результат анализа. В связи с этим при анализах пользуются определёнными приёмами, позволяющими экспериментально учесть эти влияния. Наиболее распространённым приёмом является применение эталонов, т.е. образцов веществ или материалов с точно известным содержанием определяемого элемента (или нескольких элементов). При проведении анализа измеряют определяемое вещество исследуемого образца и эталона, сравнивают полученные данные и по известному содержанию элемента в эталоне рассчитывают содержание этого элемента в анализируемом образце. Эталоны могут быть изготовлены промышленным способом (стандартные образцы, стали-нормали) или приготовляются в лаборатории непосредственно перед проведением анализа (образцы сравнения). Если в качестве стандартных образцов применяют химически чистые вещества (примесей меньше 0.05%), то их называют стандартными веществами.
На практике количественные определения инструментальными методами осуществляют по одному из трёх способов: градуировочной функции (стандартных серий), стандартов (сравнения) или стандартных добавок.
При работе по методу градуировочной функции с помощью стандартных веществ или стандартных образцов получают ряд образцов (или растворов), содержащих различные, но точно известные количества определяемого компонента. Иногда этот ряд называют стандартной серией. Затем проводят анализ этой стандартной серии и по полученным данным вычисляют значение чувствительности К (в случае линейной градуировочной функции). После этого измеряют интенсивность аналитического сигнала А в исследуемом объекте и вычисляют количество (массу, концентрацию) искомого компонента с помощью уравнения связи />или находят по градуировочному графику (см. рис.2.1.1).
Метод сравнения (стандартов) применим только для линейной градуировочной функции. Определение данного компонента проводят в стандартном образце (стандартном веществе) и получают
/>.
Потом определяют в анализируемом объекте
/>/>.
Делением первого уравнения на второе исключают чувствительность
/>
и вычисляют результат анализа
/>.
Метод стандартных добавок применим тоже только к линейной градуировочной функции. В этом методе сначала проводят анализ навески исследуемого объекта и получают />, затем к навеске добавляют известное количество (массу, объём раствора) определяемого компонента и после анализа получают
/>.
Делением первого уравнения на второе исключают К и получают формулу для расчёта результатов анализа:
--PAGE_BREAK--/>.
Спектр вещества получают, воздействуя на него температурой, потоком электронов, световым потоком (электромагнитной энергией) с определённой длиной волны (частоты излучения) и другими способами. При определённой величине энергии воздействия вещество способно перейти в возбуждённое состояние. При этом происходят процессы, приводящие к появлению в спектре излучения с определённой длиной волны (табл.2.2.1).
Излучение, поглощение, рассеяние или рефракция электромагнитного излучения может рассматриваться как аналитический сигнал, несущий информацию о качественном и количественном составе вещества или о его структуре. Частота (длина волны) излучения определяется составом исследуемого вещества, а интенсивность излучения пропорциональна числу частиц, вызвавших его появление, т.е. количеству вещества или компонента смеси.
Каждый из аналитических методов обычно использует не полный спектр вещества, охватывающий диапазон длин волн от рентгеновских излучений до радиоволн, а только определённую его часть. Спектральные методы обычно различают по диапазону длин волн спектра, являющемуся рабочим для данного метода: ультрафиолетовые (УФ), рентгеновские, инфракрасные (ИК), микроволновые и т.д.
Методы, работающие в УФ, видимом и ИК диапазоне называют оптическими. Они больше всего применяются в спектральных методах вследствие сравнительной простоты оборудования для получения и регистрации спектра.
Атомно-эмиссионный анализ (АЭА) основан на качественном и количественном определении атомного состава вещества путём получения и изучения спектров эмиссии атомов, входящих в состав вещества.
Пи АЭА анализируемая проба вещества вводится в источник возбуждения спектрального прибора. В источнике возбуждения данная проба подвергается сложным процессам, заключающимся в плавлении, испарении, диссоциации молекул, ионизации атомов, возбуждении атомов и ионов.
Возбуждённые атомы и ионы через очень короткое время (~10-7-108с) самопроизвольно возвращаются из неустойчивого возбуждённого состояния в нормальное или промежуточное состояние. Это приводит к излучению света с частотой и появлению спектральной линии.
Общую схему атомной эмиссии можно представить так:
А + Е А* А + h
Степень и интенсивность протекания этих процессов зависит от энергии источника возбуждения (ИВ).
Наиболее распространёнными ИВ являются: газовое пламя, дуговые и искровые разряды, индукционно связанная плазма (ИСП). Их энергетической характеристикой можно считать температуру.
Количественный АЭА основан на зависимости между концентрацией элемента и интенсивностью его спектральных линий, которая определяется формулой Ломакина:
/>,
где I — интенсивность спектральной линии определяемого элемента; c — концентрация; a и b — константы.
Величины a и b зависят от свойств аналитической линии, ИВ, соотношения концентраций элементов в пробе, поэтому зависимость />обычно устанавливается эмпирически для каждого элемента и каждого образца. На практике обычно пользуются методом сравнения с эталоном.
При количественных определениях используют в основном фотографический способ регистрации спектра. Интенсивность спектральной линии, получаемой на фотопластинке, характеризуется ее почернением:
/>,
где S — степень почернения фотопластинки; I0 — интенсивность света проходящего через незачерненную часть пластинки, а I — через зачерненную, т.е. спектральную линию. Измерение почернения спектральной линии проводят по сравнению с почернением фона или по отношению к интенсивности линии сравнения. Полученная разность почернений (S) прямо пропорциональна логарифму концентрации (с):
S = K lgc.
При методе трех эталонов на одной фотопластинке фотографируют спектры трех эталонов с известным содержанием элементов и спектр анализируемого образца. Измеряют почернение выбранных линий. Строят градуировочный график, по которому находят содержание изучаемых элементов.
В случае анализа однотипных объектов применяют метод постоянного графика, который строят по большому числу эталонов. Затем в строго одинаковых условиях снимают спектр образца и одного из эталонов. По спектру эталона проверяют не произошло ли смещение графика. Если смещения нет, то неизвестную концентрацию находят по постоянному графику, а если есть, то величину смещения учитывают с помощью спектра эталона.
При количественном АЭА погрешность определения содержания основы составляет 1-5%, а примеси — до 20%. Визуальный метод регистрации спектра быстрее, но менее точен, чем фотографический.
По аппаратурному оформлению можно выделить АЭА с визуальной, фотографической и фотоэлектрической регистрацией и измерением интенсивности спектральных линий.
Визуальные методы (регистрация с помощью глаза) можно использовать только для исследования спектров с длинами волн в области 400 — 700 нм. Средняя спектральная чувствительность глаза максимальна для желто-зеленого света с длиной волны 550 нм. Визуально можно с достаточной точностью установить равенство интенсивностей линий с ближайшими длинами волн или определить наиболее яркую линию. Визуальные методы делятся на стилоскопические и стилометрические.
Стилоскопический анализ основан на визуальном сравнении интенсивностей спектральных линий анализируемого элемента (примеси) и близлежащих линий спектра основного элемента пробы. Например, при анализе сталей обычно сравнивают интенсивности спектральных линий примеси и железа. При этом используют заранее известные стилоскопические признаки, в которых равенству интенсивности линий определенной аналитической пары соответствует определенная концентрация анализируемого элемента.
Стилоскопы используют для экспресс-анализа, для которого не требуется высокой точности.6-7 элементов определяют за 2-3 мин. Чувствительность анализа 0,01-0,1%. Для анализа применяют как стационарные стилоскопы СЛ-3… СЛ-12, так и переносные СЛП-1… СЛП-4.
Стилометрический анализ отличается от стилоскопического тем, что более яркую линию аналитической пары ослабляют при помощи специального устройства (фотометра) до установления равенства интенсивностей обеих линий. Кроме того, стилометры позволяют сближать в поле зрения аналитическую линию и линию сравнения, что значительно повышает точность измерений. Для анализа применяют стилометры СТ-1… СТ-7.
Относительная погрешность визуальных измерений 1 – 3%. Их недостатками являются ограниченность видимой области спектра, утомительность, отсутствие объективной документации о проведении анализа.
Фотографические методы основаны на фотографической регистрации спектра с помощью специальных приборов-спектрографов. Рабочая область спектрографов ограничена длиной волны 1000 нм, т.е. их можно использовать в видимой области и УФ. Интенсивность спектральных линий измеряют по степени почернения их изображения на фотопластинке или фотопленке.
www.ronl.ru
Реферат - Физико-химические методы анализа их классификация и основные приёмы
Физик-химические методы анализа, их классификация и основные приёмы
Физико-химические методы анализа (ФХМА) основаны на использовании зависимости физических свойств веществ (например, светопоглощения, электрической проводимости и т.д.) от их химического состава. Иногда в литературе от ФХМА отделяют физические методы анализа, подчёркивая тем самым, что в ФХМА используется химическая реакция, а в физических — нет. Физические методы анализа и ФХМА, главным образом в западной литературе, называют инструментальными, так как они обычно требуют применения приборов, измерительных инструментов. Инструментальные методы анализа в основном имеют свою собственную теорию, отличную от теории методов химического (классического) анализа (титриметрии и гравиметрии). Базисом этой теории является взаимодействие вещества с потоком энергии.
При использовании ФХМА для получения информации о химическом составе вещества исследуемый образец подвергают воздействию какого-либо вида энергии. В зависимости от вида энергии в веществе происходит изменение энергетического состояния составляющих его частиц (молекул, ионов, атомов), выражающееся в изменении того или иного свойства (например окраски, магнитных свойств и т.п.). Регистрируя изменение этого свойства как аналитический сигнал, получают информацию о качественном и количественном составе исследуемого объекта или о его структуре.
По виду энергии возмущения и измеряемого свойства (аналитического сигнала) ФХМА можно классифицировать следующим образом (табл.2.1.1).
Кроме перечисленных в таблице существует множество других частных ФХМА, не подпадающих под данную классификацию.
Наибольшее практическое применение имеют оптические, хроматографические и потенциометрические методы анализа.
Таблица 2.1.1.
Вид энергии возмущения
Измеряемое свойство
Название метода
Название группы методов
Поток электронов (эле-ктрохимические реак-ции в растворах и на электродах)
Напряжение, потенциал
Потенциометрия
Электрохимические
Ток поляризации электродов
Вольтамперо — метрия, полярография
Сила тока
Амперометрия
Сопротивление, проводимость
Кондуктометрия
Импеданс (сопротивление переменному току, ёмкость)
Осциллометрия, высокочастотная кондуктометрия
Количество электричества
Кулонометрия
Масса продукта электрохимической реакции
Электрограви-метрия
Диэлектрическая проницаемость
Диэлкометрия
Электромагнитное излучение
Длина волны и интенсивность спектральной линии в инфракрасной, видимой и ультрафиолетовой частях спектра =10-3...10-8 м
Оптические методы (ИК — спектро-скопия, атомно-эмиссионный анализ, атомно-абсорбционный анализ, фотомет-рия, люминис — центный анализ, турбидиметрия, нефелометрия)
Спектральные
То же, в рентгеновской области спектра =10-8...10-11 м
Рентгеновская фотоэлектронная, оже-спектроско-пия
Времена релаксации и химический сдвиг
Спектроскопия ядерномагнитного (ЯМР) и электронного парамагнитного (ЭПР) резонанса
Теплота
Температура
Термический анализ
Тепловые
Термограви — метрия
Количество теплоты
Калориметрия
Энтальпия
Термометрический анализ (энтальпиметрия)
Механические свойства
Дилатометрия
Энергия химических и физических (Ван-дер-Ваальсо-вые силы) взаимодействий
Электропроводность Теплопроводность Ток ионизации
Газовая, жидкостная, осадочная, ионообменная, гельпроникающая хроматографии
Хроматографические
По сравнению с классическими химическими методами ФХМА отличаются меньшим пределом обнаружения, временем и трудоёмкостью. ФХМА позволяют проводить анализ на расстоянии, автоматизировать процесс анализа и выполнять его без разрушения образца (недеструктивный анализ).
По способам определения различают прямые и косвенные ФХМА. В прямых методах количество вещества находят непосредственным пересчётом измеренного аналитического сигнала в количество вещества (массу, концентрацию) с помощью уравнения связи. В косвенных методах аналитический сигнал используется для установления конца химической реакции (как своеобразный индикатор), а количество определяемого вещества, вступившего в реакцию, находят с помощью закона эквивалентов, т.е. по уравнению, непосредственно не связанному с названием метода.
По способу количественных определений различают без эталонные и эталонные инструментальные методы анализа.
Без эталонные методы основаны на строгих закономерностях, формульное выражение которых позволяет пересчитать интенсивность измеренного аналитического сигнала непосредственно в количестве определяемого вещества с привлечением только табличных величин. В качестве такой закономерности может выступать, например, закон Фарадея, позволяющий по току и времени электролиза рассчитать количество определяемого вещества в растворе при кулонометрическом титровании. Безэталонных методов очень мало, поскольку каждое аналитическое определение представляет собой систему сложных процессов, в которых невозможно теоретически учесть влияние каждого из многочисленных действующих факторов на результат анализа. В связи с этим при анализах пользуются определёнными приёмами, позволяющими экспериментально учесть эти влияния. Наиболее распространённым приёмом является применение эталонов, т.е. образцов веществ или материалов с точно известным содержанием определяемого элемента (или нескольких элементов). При проведении анализа измеряют определяемое вещество исследуемого образца и эталона, сравнивают полученные данные и по известному содержанию элемента в эталоне рассчитывают содержание этого элемента в анализируемом образце. Эталоны могут быть изготовлены промышленным способом (стандартные образцы, стали-нормали) или приготовляются в лаборатории непосредственно перед проведением анализа (образцы сравнения). Если в качестве стандартных образцов применяют химически чистые вещества (примесей меньше 0.05%), то их называют стандартными веществами.
На практике количественные определения инструментальными методами осуществляют по одному из трёх способов: градуировочной функции (стандартных серий), стандартов (сравнения) или стандартных добавок.
При работе по методу градуировочной функции с помощью стандартных веществ или стандартных образцов получают ряд образцов (или растворов), содержащих различные, но точно известные количества определяемого компонента. Иногда этот ряд называют стандартной серией. Затем проводят анализ этой стандартной серии и по полученным данным вычисляют значение чувствительности К (в случае линейной градуировочной функции). После этого измеряют интенсивность аналитического сигнала А в исследуемом объекте и вычисляют количество (массу, концентрацию) искомого компонента с помощью уравнения связи />или находят по градуировочному графику (см. рис.2.1.1).
Метод сравнения (стандартов) применим только для линейной градуировочной функции. Определение данного компонента проводят в стандартном образце (стандартном веществе) и получают
/>.
Потом определяют в анализируемом объекте
/>/>.
Делением первого уравнения на второе исключают чувствительность
/>
и вычисляют результат анализа
/>.
Метод стандартных добавок применим тоже только к линейной градуировочной функции. В этом методе сначала проводят анализ навески исследуемого объекта и получают />, затем к навеске добавляют известное количество (массу, объём раствора) определяемого компонента и после анализа получают
/>.
Делением первого уравнения на второе исключают К и получают формулу для расчёта результатов анализа:
--PAGE_BREAK--/>.
Спектр вещества получают, воздействуя на него температурой, потоком электронов, световым потоком (электромагнитной энергией) с определённой длиной волны (частоты излучения) и другими способами. При определённой величине энергии воздействия вещество способно перейти в возбуждённое состояние. При этом происходят процессы, приводящие к появлению в спектре излучения с определённой длиной волны (табл.2.2.1).
Излучение, поглощение, рассеяние или рефракция электромагнитного излучения может рассматриваться как аналитический сигнал, несущий информацию о качественном и количественном составе вещества или о его структуре. Частота (длина волны) излучения определяется составом исследуемого вещества, а интенсивность излучения пропорциональна числу частиц, вызвавших его появление, т.е. количеству вещества или компонента смеси.
Каждый из аналитических методов обычно использует не полный спектр вещества, охватывающий диапазон длин волн от рентгеновских излучений до радиоволн, а только определённую его часть. Спектральные методы обычно различают по диапазону длин волн спектра, являющемуся рабочим для данного метода: ультрафиолетовые (УФ), рентгеновские, инфракрасные (ИК), микроволновые и т.д.
Методы, работающие в УФ, видимом и ИК диапазоне называют оптическими. Они больше всего применяются в спектральных методах вследствие сравнительной простоты оборудования для получения и регистрации спектра.
Атомно-эмиссионный анализ (АЭА) основан на качественном и количественном определении атомного состава вещества путём получения и изучения спектров эмиссии атомов, входящих в состав вещества.
Пи АЭА анализируемая проба вещества вводится в источник возбуждения спектрального прибора. В источнике возбуждения данная проба подвергается сложным процессам, заключающимся в плавлении, испарении, диссоциации молекул, ионизации атомов, возбуждении атомов и ионов.
Возбуждённые атомы и ионы через очень короткое время (~10-7-108с) самопроизвольно возвращаются из неустойчивого возбуждённого состояния в нормальное или промежуточное состояние. Это приводит к излучению света с частотой и появлению спектральной линии.
Общую схему атомной эмиссии можно представить так:
А + Е А* А + h
Степень и интенсивность протекания этих процессов зависит от энергии источника возбуждения (ИВ).
Наиболее распространёнными ИВ являются: газовое пламя, дуговые и искровые разряды, индукционно связанная плазма (ИСП). Их энергетической характеристикой можно считать температуру.
Количественный АЭА основан на зависимости между концентрацией элемента и интенсивностью его спектральных линий, которая определяется формулой Ломакина:
/>,
где I — интенсивность спектральной линии определяемого элемента; c — концентрация; a и b — константы.
Величины a и b зависят от свойств аналитической линии, ИВ, соотношения концентраций элементов в пробе, поэтому зависимость />обычно устанавливается эмпирически для каждого элемента и каждого образца. На практике обычно пользуются методом сравнения с эталоном.
При количественных определениях используют в основном фотографический способ регистрации спектра. Интенсивность спектральной линии, получаемой на фотопластинке, характеризуется ее почернением:
/>,
где S — степень почернения фотопластинки; I0 — интенсивность света проходящего через незачерненную часть пластинки, а I — через зачерненную, т.е. спектральную линию. Измерение почернения спектральной линии проводят по сравнению с почернением фона или по отношению к интенсивности линии сравнения. Полученная разность почернений (S) прямо пропорциональна логарифму концентрации (с):
S = K lgc.
При методе трех эталонов на одной фотопластинке фотографируют спектры трех эталонов с известным содержанием элементов и спектр анализируемого образца. Измеряют почернение выбранных линий. Строят градуировочный график, по которому находят содержание изучаемых элементов.
В случае анализа однотипных объектов применяют метод постоянного графика, который строят по большому числу эталонов. Затем в строго одинаковых условиях снимают спектр образца и одного из эталонов. По спектру эталона проверяют не произошло ли смещение графика. Если смещения нет, то неизвестную концентрацию находят по постоянному графику, а если есть, то величину смещения учитывают с помощью спектра эталона.
При количественном АЭА погрешность определения содержания основы составляет 1-5%, а примеси — до 20%. Визуальный метод регистрации спектра быстрее, но менее точен, чем фотографический.
По аппаратурному оформлению можно выделить АЭА с визуальной, фотографической и фотоэлектрической регистрацией и измерением интенсивности спектральных линий.
Визуальные методы (регистрация с помощью глаза) можно использовать только для исследования спектров с длинами волн в области 400 — 700 нм. Средняя спектральная чувствительность глаза максимальна для желто-зеленого света с длиной волны 550 нм. Визуально можно с достаточной точностью установить равенство интенсивностей линий с ближайшими длинами волн или определить наиболее яркую линию. Визуальные методы делятся на стилоскопические и стилометрические.
Стилоскопический анализ основан на визуальном сравнении интенсивностей спектральных линий анализируемого элемента (примеси) и близлежащих линий спектра основного элемента пробы. Например, при анализе сталей обычно сравнивают интенсивности спектральных линий примеси и железа. При этом используют заранее известные стилоскопические признаки, в которых равенству интенсивности линий определенной аналитической пары соответствует определенная концентрация анализируемого элемента.
Стилоскопы используют для экспресс-анализа, для которого не требуется высокой точности.6-7 элементов определяют за 2-3 мин. Чувствительность анализа 0,01-0,1%. Для анализа применяют как стационарные стилоскопы СЛ-3… СЛ-12, так и переносные СЛП-1… СЛП-4.
Стилометрический анализ отличается от стилоскопического тем, что более яркую линию аналитической пары ослабляют при помощи специального устройства (фотометра) до установления равенства интенсивностей обеих линий. Кроме того, стилометры позволяют сближать в поле зрения аналитическую линию и линию сравнения, что значительно повышает точность измерений. Для анализа применяют стилометры СТ-1… СТ-7.
Относительная погрешность визуальных измерений 1 – 3%. Их недостатками являются ограниченность видимой области спектра, утомительность, отсутствие объективной документации о проведении анализа.
Фотографические методы основаны на фотографической регистрации спектра с помощью специальных приборов-спектрографов. Рабочая область спектрографов ограничена длиной волны 1000 нм, т.е. их можно использовать в видимой области и УФ. Интенсивность спектральных линий измеряют по степени почернения их изображения на фотопластинке или фотопленке.
www.ronl.ru
Реферат - Физико-химические методы анализа, их классификация и основные приёмы
Физик-химические методы анализа, их классификация и основные приёмы
Физико-химические методы анализа (ФХМА) основаны на использовании зависимости физических свойств веществ (например, светопоглощения, электрической проводимости и т.д.) от их химического состава. Иногда в литературе от ФХМА отделяют физические методы анализа, подчёркивая тем самым, что в ФХМА используется химическая реакция, а в физических — нет. Физические методы анализа и ФХМА, главным образом в западной литературе, называют инструментальными, так как они обычно требуют применения приборов, измерительных инструментов. Инструментальные методы анализа в основном имеют свою собственную теорию, отличную от теории методов химического (классического) анализа (титриметрии и гравиметрии). Базисом этой теории является взаимодействие вещества с потоком энергии.
При использовании ФХМА для получения информации о химическом составе вещества исследуемый образец подвергают воздействию какого-либо вида энергии. В зависимости от вида энергии в веществе происходит изменение энергетического состояния составляющих его частиц (молекул, ионов, атомов), выражающееся в изменении того или иного свойства (например окраски, магнитных свойств и т.п.). Регистрируя изменение этого свойства как аналитический сигнал, получают информацию о качественном и количественном составе исследуемого объекта или о его структуре.
По виду энергии возмущения и измеряемого свойства (аналитического сигнала) ФХМА можно классифицировать следующим образом (табл.2.1.1).
Кроме перечисленных в таблице существует множество других частных ФХМА, не подпадающих под данную классификацию.
Наибольшее практическое применение имеют оптические, хроматографические и потенциометрические методы анализа.
Таблица 2.1.1.
Вид энергии возмущения | Измеряемое свойство | Название метода | Название группы методов |
Поток электронов (эле-ктрохимические реак-ции в растворах и на электродах) | Напряжение, потенциал | Потенциометрия | Электрохимические |
Ток поляризации электродов | Вольтамперо — метрия, полярография | ||
Сила тока | Амперометрия | ||
Сопротивление, проводимость | Кондуктометрия | ||
Импеданс (сопротивление переменному току, ёмкость) | Осциллометрия, высокочастотная кондуктометрия | ||
Количество электричества | Кулонометрия | ||
Масса продукта электрохимической реакции | Электрограви-метрия | ||
Диэлектрическая проницаемость | Диэлкометрия | ||
Электромагнитное излучение | Длина волны и интенсивность спектральной линии в инфракрасной, видимой и ультрафиолетовой частях спектра =10-3...10-8 м | Оптические методы (ИК — спектро-скопия, атомно-эмиссионный анализ, атомно-абсорбционный анализ, фотомет-рия, люминис — центный анализ, турбидиметрия, нефелометрия) | Спектральные |
То же, в рентгеновской области спектра =10-8...10-11 м | Рентгеновская фотоэлектронная, оже-спектроско-пия | ||
Времена релаксации и химический сдвиг | Спектроскопия ядерномагнитного (ЯМР) и электронного парамагнитного (ЭПР) резонанса | ||
Теплота | Температура | Термический анализ | Тепловые |
Термограви — метрия | |||
Количество теплоты | Калориметрия | ||
Энтальпия | Термометрический анализ (энтальпиметрия) | ||
Механические свойства | Дилатометрия | ||
Энергия химических и физических (Ван-дер-Ваальсо-вые силы) взаимодействий | Электропроводность Теплопроводность Ток ионизации | Газовая, жидкостная, осадочная, ионообменная, гельпроникающая хроматографии | Хроматографические |
По сравнению с классическими химическими методами ФХМА отличаются меньшим пределом обнаружения, временем и трудоёмкостью. ФХМА позволяют проводить анализ на расстоянии, автоматизировать процесс анализа и выполнять его без разрушения образца (недеструктивный анализ).
По способам определения различают прямые и косвенные ФХМА. В прямых методах количество вещества находят непосредственным пересчётом измеренного аналитического сигнала в количество вещества (массу, концентрацию) с помощью уравнения связи. В косвенных методах аналитический сигнал используется для установления конца химической реакции (как своеобразный индикатор), а количество определяемого вещества, вступившего в реакцию, находят с помощью закона эквивалентов, т.е. по уравнению, непосредственно не связанному с названием метода.
По способу количественных определений различают без эталонные и эталонные инструментальные методы анализа.
Без эталонные методы основаны на строгих закономерностях, формульное выражение которых позволяет пересчитать интенсивность измеренного аналитического сигнала непосредственно в количестве определяемого вещества с привлечением только табличных величин. В качестве такой закономерности может выступать, например, закон Фарадея, позволяющий по току и времени электролиза рассчитать количество определяемого вещества в растворе при кулонометрическом титровании. Безэталонных методов очень мало, поскольку каждое аналитическое определение представляет собой систему сложных процессов, в которых невозможно теоретически учесть влияние каждого из многочисленных действующих факторов на результат анализа. В связи с этим при анализах пользуются определёнными приёмами, позволяющими экспериментально учесть эти влияния. Наиболее распространённым приёмом является применение эталонов, т.е. образцов веществ или материалов с точно известным содержанием определяемого элемента (или нескольких элементов). При проведении анализа измеряют определяемое вещество исследуемого образца и эталона, сравнивают полученные данные и по известному содержанию элемента в эталоне рассчитывают содержание этого элемента в анализируемом образце. Эталоны могут быть изготовлены промышленным способом (стандартные образцы, стали-нормали) или приготовляются в лаборатории непосредственно перед проведением анализа (образцы сравнения). Если в качестве стандартных образцов применяют химически чистые вещества (примесей меньше 0.05%), то их называют стандартными веществами.
На практике количественные определения инструментальными методами осуществляют по одному из трёх способов: градуировочной функции (стандартных серий), стандартов (сравнения) или стандартных добавок.
При работе по методу градуировочной функции с помощью стандартных веществ или стандартных образцов получают ряд образцов (или растворов), содержащих различные, но точно известные количества определяемого компонента. Иногда этот ряд называют стандартной серией. Затем проводят анализ этой стандартной серии и по полученным данным вычисляют значение чувствительности К (в случае линейной градуировочной функции). После этого измеряют интенсивность аналитического сигнала А в исследуемом объекте и вычисляют количество (массу, концентрацию) искомого компонента с помощью уравнения связи  или находят по градуировочному графику (см. рис.2.1.1).
или находят по градуировочному графику (см. рис.2.1.1).
Метод сравнения (стандартов) применим только для линейной градуировочной функции. Определение данного компонента проводят в стандартном образце (стандартном веществе) и получают
 .
.
Потом определяют в анализируемом объекте

 .
.
Делением первого уравнения на второе исключают чувствительность

и вычисляют результат анализа
 .
.
Метод стандартных добавок применим тоже только к линейной градуировочной функции. В этом методе сначала проводят анализ навески исследуемого объекта и получают  , затем к навеске добавляют известное количество (массу, объём раствора) определяемого компонента и после анализа получают
, затем к навеске добавляют известное количество (массу, объём раствора) определяемого компонента и после анализа получают
 .
.
Делением первого уравнения на второе исключают К и получают формулу для расчёта результатов анализа:
 .
.
Спектр вещества получают, воздействуя на него температурой, потоком электронов, световым потоком (электромагнитной энергией) с определённой длиной волны (частоты излучения) и другими способами. При определённой величине энергии воздействия вещество способно перейти в возбуждённое состояние. При этом происходят процессы, приводящие к появлению в спектре излучения с определённой длиной волны (табл.2.2.1).
Излучение, поглощение, рассеяние или рефракция электромагнитного излучения может рассматриваться как аналитический сигнал, несущий информацию о качественном и количественном составе вещества или о его структуре. Частота (длина волны) излучения определяется составом исследуемого вещества, а интенсивность излучения пропорциональна числу частиц, вызвавших его появление, т.е. количеству вещества или компонента смеси.
Каждый из аналитических методов обычно использует не полный спектр вещества, охватывающий диапазон длин волн от рентгеновских излучений до радиоволн, а только определённую его часть. Спектральные методы обычно различают по диапазону длин волн спектра, являющемуся рабочим для данного метода: ультрафиолетовые (УФ), рентгеновские, инфракрасные (ИК), микроволновые и т.д.
Методы, работающие в УФ, видимом и ИК диапазоне называют оптическими. Они больше всего применяются в спектральных методах вследствие сравнительной простоты оборудования для получения и регистрации спектра.
Атомно-эмиссионный анализ (АЭА) основан на качественном и количественном определении атомного состава вещества путём получения и изучения спектров эмиссии атомов, входящих в состав вещества.
Пи АЭА анализируемая проба вещества вводится в источник возбуждения спектрального прибора. В источнике возбуждения данная проба подвергается сложным процессам, заключающимся в плавлении, испарении, диссоциации молекул, ионизации атомов, возбуждении атомов и ионов.
Возбуждённые атомы и ионы через очень короткое время (~10-7-108с) самопроизвольно возвращаются из неустойчивого возбуждённого состояния в нормальное или промежуточное состояние. Это приводит к излучению света с частотой и появлению спектральной линии.
Общую схему атомной эмиссии можно представить так:
А + Е А* А + h
Степень и интенсивность протекания этих процессов зависит от энергии источника возбуждения (ИВ).
Наиболее распространёнными ИВ являются: газовое пламя, дуговые и искровые разряды, индукционно связанная плазма (ИСП). Их энергетической характеристикой можно считать температуру.
Количественный АЭА основан на зависимости между концентрацией элемента и интенсивностью его спектральных линий, которая определяется формулой Ломакина:
 ,
,
где I — интенсивность спектральной линии определяемого элемента; c — концентрация; a и b — константы.
Величины a и b зависят от свойств аналитической линии, ИВ, соотношения концентраций элементов в пробе, поэтому зависимость  обычно устанавливается эмпирически для каждого элемента и каждого образца. На практике обычно пользуются методом сравнения с эталоном.
обычно устанавливается эмпирически для каждого элемента и каждого образца. На практике обычно пользуются методом сравнения с эталоном.
При количественных определениях используют в основном фотографический способ регистрации спектра. Интенсивность спектральной линии, получаемой на фотопластинке, характеризуется ее почернением:
 ,
,
где S — степень почернения фотопластинки; I0 — интенсивность света проходящего через незачерненную часть пластинки, а I — через зачерненную, т.е. спектральную линию. Измерение почернения спектральной линии проводят по сравнению с почернением фона или по отношению к интенсивности линии сравнения. Полученная разность почернений (S) прямо пропорциональна логарифму концентрации (с):
S = K lgc.
При методе трех эталонов на одной фотопластинке фотографируют спектры трех эталонов с известным содержанием элементов и спектр анализируемого образца. Измеряют почернение выбранных линий. Строят градуировочный график, по которому находят содержание изучаемых элементов.
В случае анализа однотипных объектов применяют метод постоянного графика, который строят по большому числу эталонов. Затем в строго одинаковых условиях снимают спектр образца и одного из эталонов. По спектру эталона проверяют не произошло ли смещение графика. Если смещения нет, то неизвестную концентрацию находят по постоянному графику, а если есть, то величину смещения учитывают с помощью спектра эталона.
При количественном АЭА погрешность определения содержания основы составляет 1-5%, а примеси — до 20%. Визуальный метод регистрации спектра быстрее, но менее точен, чем фотографический.
По аппаратурному оформлению можно выделить АЭА с визуальной, фотографической и фотоэлектрической регистрацией и измерением интенсивности спектральных линий.
Визуальные методы (регистрация с помощью глаза) можно использовать только для исследования спектров с длинами волн в области 400 — 700 нм. Средняя спектральная чувствительность глаза максимальна для желто-зеленого света с длиной волны 550 нм. Визуально можно с достаточной точностью установить равенство интенсивностей линий с ближайшими длинами волн или определить наиболее яркую линию. Визуальные методы делятся на стилоскопические и стилометрические.
Стилоскопический анализ основан на визуальном сравнении интенсивностей спектральных линий анализируемого элемента (примеси) и близлежащих линий спектра основного элемента пробы. Например, при анализе сталей обычно сравнивают интенсивности спектральных линий примеси и железа. При этом используют заранее известные стилоскопические признаки, в которых равенству интенсивности линий определенной аналитической пары соответствует определенная концентрация анализируемого элемента.
Стилоскопы используют для экспресс-анализа, для которого не требуется высокой точности.6-7 элементов определяют за 2-3 мин. Чувствительность анализа 0,01-0,1%. Для анализа применяют как стационарные стилоскопы СЛ-3… СЛ-12, так и переносные СЛП-1… СЛП-4.
Стилометрический анализ отличается от стилоскопического тем, что более яркую линию аналитической пары ослабляют при помощи специального устройства (фотометра) до установления равенства интенсивностей обеих линий. Кроме того, стилометры позволяют сближать в поле зрения аналитическую линию и линию сравнения, что значительно повышает точность измерений. Для анализа применяют стилометры СТ-1… СТ-7.
Относительная погрешность визуальных измерений 1 – 3%. Их недостатками являются ограниченность видимой области спектра, утомительность, отсутствие объективной документации о проведении анализа.
Фотографические методы основаны на фотографической регистрации спектра с помощью специальных приборов-спектрографов. Рабочая область спектрографов ограничена длиной волны 1000 нм, т.е. их можно использовать в видимой области и УФ. Интенсивность спектральных линий измеряют по степени почернения их изображения на фотопластинке или фотопленке.
www.ronl.ru
Реферат: физико-химические методы исследования - n1.docx
Реферат: физико-химические методы исследованияскачать (36 kb.)Доступные файлы (1):n1.docx
План:1.Введение
2. Основные физико-химические методы анализа
3. Спектральные и оптические методы анализа
3.1. Эмиссионный спектральный анализ. Фотометрия пламени
3.2. Атомно-абсорбционный анализ
3.3. Молекулярно-абсорбционный анализ
3.4. Люминесцентный анализ
4. Электрохимические методы
4.1. Вольтамперометрия
4.2. Потенциометрия
4.3. Кондуктометрический анализ
4.4. Полярографический анализ
4.5. Кулонометрия
4.6. Кондуктометрия
5. Хроматографичегкие методы анализа
5.1. Жидкостная ионообменная хроматография
5.2. Газовая хроматография
6. Термические методы
6.1. Методы термического анализа
1.Введение
Физико-химические или инструментальные методы анализа основаны на измерении с помощью приборов (инструментов) физических параметров анализируемой системы, которые возникают или изменяются в ходе выполнения аналитической реакции.
Бурное развитие физико-химических методов анализа было вызвано тем, что классические методы химического анализа (гравиметрия, титриметрия) уже не могли удовлетворять многочисленные запросы химической, фармацевтической, металлургической, полупроводниковой, атомной и других отраслей промышленности, требовавших повышения чувствительности методов до 10-8 – 10-9 %, их селективности и экспрессности, что позволило бы управлять технологическими процессами по данным химического анализа, а также выполнять их в автоматическом режиме и дистанционно.
Ряд современных физико-химических методов анализа позволяют одновременно в одной и той же пробе выполнять как качественный, так и количественный анализ компонентов. Точность анализа современных физико-химических методов сопоставима с точностью классических методов, а в некоторых, например в кулонометрии, она существенно выше.
К недостаткам некоторых физико-химических методов следует отнести дороговизну используемых приборов, необходимость применения эталонов. Поэтому классические методы анализа по-прежнему не потеряли своего значения и применяются там, где нет ограничений в скорости выполнения анализа и требуется высокая его точность при высоком содержании анализируемого компонента.
[1. http://www.ftchemistry.dsmu.edu.ua/ana_him/lek_13.html]2. Основные физико-химические методы анализа
В группе физико-химических методов анализа иногда выделяют физические методы. Однако достаточно строгого и однозначного критерии для этого нет, поэтому выделение физических методов принципиального значения не имеет.
Общее число физико-химических методов анализа довольно велико — оно составляет несколько десятков. Наибольшее практическое значение среди них имеют следующие:
- спектральные и другие оптические методы;
- электрохимические методы;
- хроматографические методы анализа.
Среди указанных трех групп наиболее обширной по числу методов и важной по практическому значению является группа спектральных и других оптических методов анализа Она включает методы эмиссионной атомной спектроскопии, атомно-абсорбционной спектроскопии, инфракрасной спектроскопии, спектрофотомерии, люминесценции и другие методы, основанные на измерении различных эффектов при взаимодействии вещества с электромагнитным излучением.
Группа электрохимических методов анализа, основанная на измерении электрической проводимости, потенциалов и других свойств, включает методы кондуктометрии, потенциометрии, вольтамперометрии и т.д.
В группу хроматографических методов входят методы газовой и газожидкостной хроматографии, жидкостной распределительной, тонкослойной, ионообменной и других видов хроматографии
[2. Аналитическая химия в 2-х частях, 1989]
3. Спектральные и оптические методы анализа
Оптические и спектральные методы анализа основаны на измерении параметров, характеризующих эффекты взаимодействия электромагнитного излучения с веществами: интенсивности излучения возбужденных атомов, поглощения монохроматического излучения, показателя преломления света, угла вращения плоскости поляризованного луча света и др. Все эти параметры являются функцией концентрации вещества в анализируемом объекте.
[3. Физико-химические методы анализа, 1999]3.1. Эмиссионный спектральный анализ. Фотометрия пламени
Фотометрия пламени представляет собой разновидность эмиссионного спектрального анализа. Метод основан на термическом возбуждении атомов в пламени и прямом измерении интенсивности их излучения при помощи фотоэлемента или фотоумножителя. Используя монохроматор или соответствующий светофильтр, выделяют наиболее яркую спектральную линию.
При общей оценке методов эмиссионной спектроскопии необходимо, прежде всего, отмстить их низкий предел обнаружения, точность, быстроту выполнения анализов и универсальность. Многочисленные применения нашел спектральный анализ и в других отраслях народного хозяйства и техники (геологии, химической промышленности, сельском хозяйстве, космохимии и т. д.).
Метод применяют для определения щелочных, щелочноземельных, а также некоторых других металлов. Пределы обнаружения щелочных металлов составляют 0,1-0,001 мкг/мл, остальных - 0,1-5 мкг/мл; относительное, стандартное отклонение 0,02-0,04.
[4. Методы анализа по фотометрии пламени, 1967]3.2. Атомно-абсорбционный анализ
Атомно-абсорбционный анализ основан на поглощении невозбужденными атомами излучения от внешнего источника. Атомизация исследуемого вещества происходит в плазме – пламени газовой горелки (пропан – воздух, кислород – ацетилен и др.) или электротермическом атомизаторе. Обычно используется резонансное поглощение электромагнитных колебаний атомами, которое наблюдается при минимальной для данного элемента энергии возбуждения и подчиняется экспоненциальному закону поглощения.
Атомно-абсорбционный спектральный анализ получил широкое распространение в практике вследствие многих своих достоинств. Важным достоинством атомно-абсорбционного метода является наличие менее жестких требований, чем в эмиссионной спектроскопии, к условиям получения поглощающей плазмы, поскольку аналитический сигнал зависит от числа невозбужденных атомов, которое сравнительно мало меняется при небольших колебаниях температуры. Погрешность определения обычно составляет примерно 5 % и в зависимости от различных условий "зменнется в пределах от 3 до 10%.
Метод имеет также ряд ограничений. Атомно-абсорбционным методом не определяются элементы, резонансные линии которых ежат в далеком ультрафиолете (углерод, фосфор, галогены). Необходимость растворения пробы также можно рассматривать как недостаток, поскольку эта операция удлиняет измерение. Однако работа с растворами упрощает эталонирование и обеспечивает высокую воспроизводимость результатов. К существенным недостаткам метода относится невозможность одновременного определения нескольких элементов, хотя для этого имеются все предпосылки. Необходимо отметить также, что помимо чисто аналитического применения атомно-абсорбцнонная спектроскопия используется для определения силы осциллятора, коэффициентов диффузии, давления насыщенных паров и т. д.
[5.http://www.ftchemistry.dsmu.edu.ua/ana_him/lek_16.html]3.3. Молекулярно-абсорбционный анализ
Данный вид анализа основан на исследовании спектров поглощения электромагнитного излучения молекулами различных веществ. Излучение источника света в виде пучка с определенными волновыми характеристиками направляется на газообразное, твердое исследуемое вещество или его раствор.
Молекулярно-абсорбционный спектральный анализ включает в себя спектрофотометрический и фотоколориметрический виды анализа.
Спектрофотометрический анализ основан на определении спектра поглощения или измерении светопоглощения при строго определенной длине волны, которая соответствует максимуму кривой поглощения исследуемого вещества.
Фотоколориметрический анализ базируется на сравнении интенсивности окрасок исследуемого окрашенного и стандартного окрашенного растворов определенной концентрации.
[6.Руководство для следователей, 2005]3.4. Люминесцентный анализ
Люминесцентный анализ, метод исследования различных объектов, основанный на наблюдении их люминесценции. При люминесцентном анализе наблюдают либо собственное свечение исследуемых объектов (например, паров исследуемого газа), либо свечение специальных люминофоров, которыми обрабатывают исследуемый объект. Аппаратура, применяемая для люминесцентного анализа, содержит источник возбуждения люминесценции и регистрирующее устройство. Чаще всего возбуждают фотолюминесценцию объекта, однако в некоторых случаях наблюдают катодолюминесценцию, радиолюминесценцию и хемилюминесценцию. Фотовозбуждение обычно производится кварцевыми ртутными лампами, причём с помощью светофильтров из их спектра обычно вырезается ультрафиолетовая часть. Кроме ртутных ламп, в качестве источника света в люминесцентном анализе применяют ксеноновые лампы, искры в воздухе, лазеры. Регистрация люминесценции обычно осуществляется визуально или с помощью фотоэлектронных приборов, которые повышают точность люминесцентного анализа.
Люминесцентный анализ находит применение также в криминалистике (для определения подлинности документов, обнаружения следов токсических веществ и т.п.), реставрационных работах, дефектоскопии. Находит применение в гигиене (определение качества некоторых продуктов, питьевой воды) и промышленно-санитарной химии (определение содержания вредных веществ в воздухе) и т.п.
[7.Люминесцентный анализ, 1961]4. Электрохимические методы
Электрохимические методы анализа основаны на измерении электрических параметров: силы тока, напряжения, равновесных электродных потенциалов, электрической проводимости, количества электричества, величины которых пропорциональны содержанию вещества в анализируемом объекте.
[8. Аналитическая химия. Физико-химические методы анализа, 1991]
4.1. Вольтамперометрия основана на исследовании зависимости тока поляризации от напряжения, прикладываемого к электрохимической ячейке, когда потенциал рабочего электрода значительно отличается от равновесного значения. По разнообразию методов вольтамперометрия — самая многочисленная группа из всех электрохимических методов анализа, широко используемая для определения веществ в растворах и расплавах (например, полярография, амперометрия).
[9. Теоретические основы электрохимического анализа, 1974]4.2. Потенциометрия
Потенциометрический метод анализа основан на использовании зависимости электродвижущей силы (ЭДС) электрохимической цепи от активности (концентрации) анализируемого иона.
Потенциометрические методы анализа подразделяются на два вида:- прямая потенциометрия, или ионометрия;- потенциометрическое титрование.Прямая потенциометрия - метод основан на определении концентрации йона непосредственно по измеренной ЭДС электрохимической цепи, содержащей соответствующий ионоселективный электрод.
Потенциометрическое титрование - метод основан на определении точки эквивалентности по резкому изменению в ней ЭДС электрохимической цепи, содержащей индикаторный электрод.
[10. http://www.ftchemistry.dsmu.edu.ua/ana_him/lek_16.html]
4.3. Кондуктометрический анализ
К кондуктометрии относятся методы, в которых измеряют электропроводность электролитов (водных и неводных растворов, коллоидных систем, расплавов, твёрдых веществ). Кондуктометрический анализ основан на изменении концентрации вещества или химического состава среды в межэлектродном пространстве; он не связан с потенциалом электрода, который обычно близок к равновесному значению. Кондуктометрия включает прямые методы анализа (используемые, например, в солемерах) и косвенные (например, в газовом анализе) с применением постоянного или переменного тока (низкой и высокой частоты), а также хронокондуктометрию, низкочастотное и высокочастотное титрование.
[11. Теоретические основы электрохимических методов анализа, 1975]4.4. Полярографический анализ
Как вытекает из самого названия, полярография основана на явлении поляризации электродов при прохождении электрического тока через проводники второго рода (растворы электролитов). Поляризация электродов обусловлена замедленностью электродных процессов. Она складывается в основном из трех видов: электрохимической, концентрационной и омической.
[12. http://revolution.allbest.ru/chemistry/00095510_0.html]4.5. Кулонометрия
Кулонометрия объединяет методы анализа, основанные на измерении количества вещества, выделяющегося на электроде в процессе электрохимической реакции в соответствии с Фарадея законами. При кулонометрии потенциал рабочего электрода отличается от равновесного значения. Различают потенциостатическую и гальваностатическую кулонометрию, причём последняя включает прямой и инверсионный методы, электроанализ и кулонометрическое титрование.
[ 13. Физико-химические методы исследования и анализа, 2011]4.6.Кондуктометрия
К кондуктометрии относятся методы, в которых измеряют электропроводность электролитов (водных и неводных растворов, коллоидных систем, расплавов, твёрдых веществ). Кондуктометрический анализ основан на изменении концентрации вещества или химического состава среды в межэлектродном пространстве; он не связан с потенциалом электрода, который обычно близок к равновесному значению. Кондуктометрия включает прямые методы анализа (используемые, например, в солемерах) и косвенные (например, в газовом анализе) с применением постоянного или переменного тока (низкой и высокой частоты), а также хронокондуктометрию, низкочастотное и высокочастотное титрование.
[13. Физико-химические методы исследования и анализа, 2011]5. Хроматографичегкие методы анализа
Хроматография - наиболее часто используемый аналитический метод. Новейшими хроматографическими методами можно проанализировать газообразные, жидкие и твердые вещества с различной молекулярной массой. Это могут быть изотопы водорода, ионы металлов, полимеры, белки, нефть и др. С помощью хроматографии получена обширная информация о строении и свойствах многих классов органических соединений. Применение хроматографических методов для разделения белков оказало огромное влияние на развитие современной биохимии. Хроматографию с успехом применяют в исследовательских и клинических целях в самых разных областях биологии и медицины, в фармацевтике и криминалистике: для терапевтического мониторинга в связи с ростом нелегального употребления наркотиков, идентификации антибиотиков и отнесения их к той или иной группе антибактериальных препаратов, для анализа отдельных наиболее важных классов пестицидов. Такие достоинства, как универсальность, экспрессность и чувствительность делают хроматографию важнейшим аналитическим методом.
Различные методы хроматографии можно классифицировать по агрегатному состоянию фаз, способу их относительного перемещения, аппаратурному оформлению процесса и т. д.
[14. http://www.ftchemistry.dsmu.edu.ua/ana_him/lek_16.html]5.1. Жидкостная ионообменная хроматография
Основана на различной способности разделяемых ионов к ионному обмену с фиксироваными ионами сорбента, образующимися в результате диссоциации ионогенных групп последнего. Для разделения катионов используют катиониты, для разделения анионов – аниониты.
[15. Ионный обмен в технологии и анализе неорганических веществ, 1980]5.2. Газовая хроматография
Газовая хроматография — разновидность хроматографии, метод разделения летучих компонентов, при котором подвижной фазой служит инертный газ (газ-носитель), протекающий через неподвижную фазу с большой поверхностью. В качестве подвижной фазы используют водород, гелий, азот, аргон, углекислый газ. Газ-носитель не реагирует с неподвижной фазой и разделяемыми веществами.Различают газо-твёрдофазную и газо-жидкостную хроматографию. В первом случае неподвижной фазой является твёрдый носитель (силикагель, уголь, оксид алюминия), во втором — жидкость, нанесённая на поверхность инертного носителя.
Разделение основано на различиях в летучести и растворимости (или адсорбируемости) компонентов разделяемой смеси.Этот метод можно использовать для анализа газообразных, жидких и твёрдых веществ с молекулярной массой меньше 400, которые должны удовлетворять определённым требованиям, главные из которых — летучесть, термостабильность, инертность, лёгкость получения. Этим требованиям в полной мере удовлетворяют, как правило, органические вещества, поэтому газовую хроматографию широко используют как серийный метод анализа органических соединений.
[16. Основы аналитической химии, 2000]6. Термические методы
Методы основаны на взаимодействии вещества с тепловой энергией. В них какой-либо параметр исследуемой системы измеряют в зависимости от температуры. Наибольшее применение в аналитической химии находят тепловые эффекты, которые являются причиной или следствием химических реакций. В меньшей степени применяются методы, основанные на выделении или поглощении теплоты в результате физических процессов. Это процессы, связанные с переходом вещества из одной модификации в другую, с изменением агрегатного состояния и другими изменениями межмолекулярного взаимодействия, например, происходящими при растворении или разбавлении.
[17. Физико-химические методы анализа, 2008]6.1. Методы термического анализа
| Название метода | Регистрируемый параметр | Измерительный прибор |
| Термогравиметрия (ТГА) | Изменение массы | Термовесы |
| Термогравиметрия по производной (ДТГ) | Скорость изменения массы | Термовесы |
| Термический (ТА) и дифференциальный термический анализ (ДТА) | Выделяемая или поглощаемая теплота | Аппаратура дифференциального термического анализа |
| Дифференциальная сканирующая калориметрия (ДСК) | Выделяемая или поглощаемая теплота | Дифференциальный сканирующий калориметр |
| Термометрическое титрование | Изменение температуры | Адиабатический калориметр |
| Энтальпиметрия | Выделяемая или поглощаемая теплота | Адиабатический калориметр |
| Дилатометрия | Изменение температуры | Дилатометры |
| Катарометрия | Изменения температуры | Катарометры |
Список использованной литературы:1. http://www.ftchemistry.dsmu.edu.ua/ana_him/lek_13.html;
2. Аналитическая химия в 2-х частях, В.П. Васильев, 2 часть, 1989;
3. Физико-химические методы анализа, Н.М. Дубова, Т.М. Гиндуллина и др., 1999;
4. Полуэктов Н.С., Методы анализа по фотометрии пламени, 2 изд., M., 1967;
5. http://www.ftchemistry.dsmu.edu.ua/ana_him/lek_16.html;
6. Руководство для следователей / Под общ. ред. В.В. Мозякова. тельство «Экзамен», 2005. — 912 с.;
7. Люминесцентный анализ. Сборник статей под редакцией М. А. Константиновой-Шлезингер, М., 1961. Э. А. Свириденков;
8. Е.Н. Дорохова, Г.В. Прохорова, Аналитическая химия. Физико-химические методы анализа, 1991;
9. Галюс 3., Теоретические основы электрохимического анализа, пер. с польск., М., 1974;
10. http://www.ftchemistry.dsmu.edu.ua/ana_him/lek_16.html;
11. Лопатин Б. А., Теоретические основы электрохимических методов анализа, М., 1975;
12. http://revolution.allbest.ru/chemistry/00095510_0.html;
13. Е.И. Короткова, О.А. Воронова, Физико-химические методы исследования и анализа, 2011;
14. http://www.ftchemistry.dsmu.edu.ua/ana_him/lek_16.html;
15. Сенявин М. М., Ионный обмен в технологии и анализе неорганических веществ, М., 1980;
16. Основы аналитической химии. / Ю. А. Золотов, Е. Н. Дорохова, В. И. Фадеева и др. Под ред. Ю. А. Золотова. — М.: Высш. шк., 2000;
17. Луцик, В.И. Физико-химические методы анализа: учебн. пос. / В.И. Луцик, А.Е. Соболев, Ю.В. Чурсанов. 1-е изд. Тверь: ТГТУ, 2008, 208 с.
nashaucheba.ru
|
|
..:::Счетчики:::.. |
|
|
|
|
|
|
|
|


