Инструкция
по приготовлению и контролю качества растворов глюкозы 5%. 10%, 20%, 25% для инъекций в условиях аптек.
I. Характеристика готового продукта
Раствор глюкозы 5%, 10%, 20%, 25% для инъекций.
Препарат представляет собой, 5%, 10%, 20%, 25% раствор глюкозы в воде для инъекций, стабилизированный 0,1 моль/дм3 хлористоводородной кислоты с хлоридом натрия.
Состав: Глюкозы безводной 50 г, 100 г, 200 г, 250 г. Раствора хлористоводородной кислоты 0,1 моль/дм3 до рН 3,0-4,1. Натрия хлорида 0,26 г, 0,26 г, 0,26 г, 0,26 г.
Воды для инъекций до 1 л. Бес цветная или слегка желтоватая прозрачная жидкость сладкого вкуса без запаха; рН 3,0-4,1.
Препарат по стерильности, апирогенности и отсутствию механических примесей должен выдерживать требования указанные в ст. 286 ГФ X. Содержание глюкозы в 1 мл препарата соответствен-о быть 0,0485—0,0515 г; 0,097—0,103 г; 0,194—0,206 г ,242—0,258 г (ГФ X стр. 312).
Выпускают во флаконах разной вместимости, укупоренных резиновыми пробками 25 П, ИР-21 под обкатку алюминиевыми колпачками.
Хранят препарат при комнатной температуре, срок хранения 1 месяц.
Изотонические растворы (5%) вводят под кожу, в вену (капельно) и в клизмах.
Гипертонические растворы глюкозы (10%, 20%, 25%) вводят внутривенно.
2. Характеристика сырья и материалов.
Таблица 1
| № п/п | Наименование сырья, полупродуктов | Нормативно – техническая документация | Квалификация | Содержание основного вещества в % |
| 1. 2. 3. 4. 1. 2. 3. 4. 5. 6. 7. 8. 9. 10. 11. 12. | I. Сырьё Вода очищенная Глюкоза кристаллическая медицинская Натрия хлорид Кислота хлористоводородная разведенная II. Материалы Марля медицинская Вата медицинская Бумага фильтровальная лабораторная Бумага универсальная индикаторная Ткани хлопчатобумажные бязевой группы Бельтинг хлопчатобумажный Шелковая туаль Колпачки алюминиевые Пробки резиновые Пергамент Флаконы стеклянные Мерная посуда для приготовления растворов и др. | ГФ Х ст. 74 ГФ Х ст. 311 ГФ Х ст. 425 ГФ Х ст. 18 ГОСТ 9412-77 ГОСТ 5556-75 ГОСТ 12026-76 ТУ 6-09-1181-71 ГОСТ 116-80-76 ГОСТ 332-69 ГОСТ 20722-75 ОСТ 64-7-85-79 ТУ 38-006269-80 | Для инъекций Гигроскопическая Гигроскопическая Фильтровальный Арт. 12008 100 % натурального шелка 25П, ИР-21 | Не менее 99,5 % |
3. Перечень оборудования
Таблица 2
| № п/п | Наименование оборудования | Нормативно – техническая документация |
| 1. 2. 3. 4. 5. 6. | Аквадистилляторы различных марок Сборник для очищенной или обессоленной воды Мерник смеситель для приготовления инъекционных растворов или другая емкость Мешалки для приготовления растворов (настольного и напольного типов МИ-02) Аппарат для фильтрования растворов прямого типа АФРП или аналоговый Фильтрующие воронки со стеклянными фильтрами, воронки стеклянные или разъемные фильтр – воронка Ф - 30 |
4. Изложение технологического процесса.
Технологический процесс козы для инъекций состоят из 6 стадий:
1. Подготовительные работы.
2. Приготовление раствора.
3. Фильтрование и фасовка раствора.
4. Стерилизация раствора.
5. Контроль готовой продукции.
6. Оформление.
Стадия 1. Подготовительные работы
1.1. Подготовка помещения, персонала вспомогательного материала, оборудования, тароукупорочных средств проводят в соответствии с действующим приказом МЗ и СЗ ПМР.
Вспомогательный материал, сосуды для приготовления растворов, мерные колбы, цилиндры, воронки, стеклянные фильтры, тароукупорочные средства (сосуды резиновые пробки) обрабатывают и стерилизуют в со ответствии с действующей «Инструкцией по приготовлению раствора для инъекций в аптеках».
Аллюминиевые колпачки выдерживают 15 мин 1—2% растворе моющих средств, подогретом до 70— 80°С, моют, затем раствор сливают, а колпачки промывают проточной водопроводной водой
Чистые колпачки сушат в биксах в воздушных стерилизаторах.
1.2. Подготовка сырья. Исходным сырьем для получения 5%, 10%, 20%, 25% раствора глюкозы является глюкоза, соответствующая требованиям ГФ X ст. 311.
Брутто формула глюкозы С6Н12О6-Н2О. М. м. 198,17.
При изготовлении раствора для инъекций глюкозу берут в большем количестве, чем указано в прописи, с учетом содержания кристаллизационной воды по расчету:
где:
а — количество безводной глюкозы, указанное в прописи;
б— процентное содержание воды в препарате по анализу.
Кислота хлористоводородная 0,1 моль/дм3.
Для приготовления 1 л 0,1 моль/дм3 хлористоводородной кислоты необходимо взять 44 мл разбавленной хлористоводородной кислоты с плотностью 1,038—1,039.
Натрия хлорид.
Брутто-формула NaCl. М. м. 58,44. С целью разрушения пирогенных веществ натрий хлорид перед изготовлением растворов напревают в открытых стеклянных или фарфоровых емкостях в воздушных стелиризаторах при 180°С— 2 часа при толщине слоя порошка не более 6—7 см и используют в течение 24 часов.
Стадия 2. Приготовление раствора
Загрузка сырья, растворение, анализ пробы. Раствор глюкозы для инъекций готовят весообъемным методом. В мерник-смеситель или другую емкость загружают кристалическую глюкозу, (в пересчете на безводную) добавляют воды для инъекций приблизительно 2/3 нужного количества и с помощью мешалки раствор, перемешивают до полного растворения глюкозы в течении 2—3 мин.
Для стабилизации раствора глюкозы добавляют 0,26 г. натрия хлорида и 5 мл раствора 0,1 моль/дм3 хлористоводородной кислоты на каждый литр раствора. Можно стабилизатор приготовить заранее и добавить его в количестве 5% от общего объёма раствора.*
* Стабилизатор готовят еx tempore по следующей прописи: натрия хлорида 5,2 г, разведенной хлористоводородной кислоты 4,4 мл, воды для инъекций до 1 литра.
Затем добавляют воду для инъекций до заданного объёма, перемешивают 2-3 минуты.
Раствор контролируют на содержание глюкозы, стабилизатора (натрия хлорида, хлористоводородной кислотой) и по РН.
Подлинность.
1. К 1 мл препарата прибавляют 5 мл реактива Фелинга и нагревают до кипения; образуется кирпично-красный осадок.
2.2 Выпаривают 2-3 капли раствора на водяной бане. После охлаждения к сухому остатку прибавляют 0,01 г. тимола, 5—6 капель концентрированной серной кислоты и 1-2 капли воды; появляется красно-фиолетовое окрашивание.
Определение количественного содержания глюкозы.
На призму рефрактометра наносят несколько капель воды очищенной и по шкале находят показатель преломления. Вытирают призму досуха наносят на нее несколько капель испытуемого раствора и находят показатель преломления, который определяют 3-4 раза, который раз беря новую порцию препарата. Для расчета берут среднее из всех определений.
Содержание глюкозы (Х) вычисляют по формуле:
где:
n - показатель преломления препарата;
n 0 - показатель преломления воды очищенной.
0,00142 - величина прироста показателя преломления при увеличении концентрации глюкозы на 1%.
Определение количественного содержания стабилизатора в глюкозе.
1) Определение хлористоводородной кислоты.
К 25 мл. раствора прибавляют 1 каплю метилового красного и титруют 0,02 моль/дм3 раствора едкого натра** от красного до желтого окрашивания (А мл.).
1 мл. 0,02 моль/дм3 раствора едкого натра соответствует 0,0007292 г. хлористого водорода. Содержание 0,1 моль/дм3 раствора хлористоводородной кислоты в миллилитрах (Х) вычисляют по формуле:
где: 0,3646 – содержание хлористого водорода в 100 мл. 0,1 моль/дм3 в граммах.
2) Определенние натрия хлорида и хлористоводородной кислоты.
К 2 мл. раствора прибавляют 1-2 капли раствора калия хромата и тетруют 0,02 моль/дм3 раствора серебра нитрата до оранжево-желтого окрашивания (Б мл.).
Количество миллилитров 0,02 моль/дм3 раствора серебра нитрата, израсходованного на титрование натрия хлорида вычисляют по разности:
1 мл. 0,02 моль/дм3 серебра нитрата соответствует 0,0011688 г. натрия хлорида. Определение РН раствора проводят с помощью потенциометра или универсальной индикаторной бумаги.
Стадия 3. Фильтрование и фасовка раствора
3.1 Фильтрование, розлив, укупорка пробками, первичный контроль на отсутствие механических загрязнений. При удовлетворительном результате анализа раствор фильтруют под давлением столба жидкости или при разряжении 4,15—0,25 кгс/см2 с использованием приборов указанных в таблице 2.
Для фильтрования используют фильтрующие воронки со стеклянными фильтрами ПОР 10 (размер пор 3-10мкм) . ПОР 16 (размер пор 10—16 мкм), разъемные фильтр -воронки Ф-30 или стеклянные воронки в сочетании с различными фильтровальными материалами, указанными в таблице1.
Первые порции фильтрата подвергаются повторному фильтрованию. Фильтрование раствора сочетают с одновременным розливом его в подготовленные стеклянные флаконы, которые укупоривают пробками и тут
** 0,02 моль/дм3 раствора едкого натра готовят по еx tempore на свежеприготовленной воде очищенной. Сохраняют в склянках с притертыми пробками. Срок хранения раствора 2 суток.
же проводят первичный контроль раствора на отсутствие механических загрязнений.
При обнаружении механических загрязнений раствор перефильтровывают.
Если раствор фильтруют в большую емкость, то далее его разливают в подготовленные стерильные флаконы, укупоривают стерильными пробками, после чего проводят первичный контроль на отсутствие механических загрязнений*.
3.2. Укупорка, маркировка.
Сосуды с раствором закрывают металлическими колпачками с помощью обкаточного приспособления, маркируют путем надписи, штамповки, используя жетоны и др., затем передают на стерилизацию.
Стадия 4. Стерилизация раствора
Раствор во флаконах стерилизуют в паровом стерилизаторе насыщенным водяным паром при избыточном давлении 0,11 МПа (1,1 кгс/см2) и температуре 120°С. Раствор во флаконах вместимостью до 100 мл стерилизуют в течение 8 мин., от 100 мл до 500 мл. – 12 мин.
Стадия 5. Контроль готовой продукции
5.1. Раствор во флаконах контролируют на отсутствие механических загрязнений (см. п. 3. 1.)
5.2. От каждой серии отбирают 1 флакон для контроля по всем физико-химическим показателям**. Определяют внешний вид раствора, рН, подлинность, количественное содержание глюкозы, соляной кислоты, натрия хлорида в соответствии с методиками, изложенными в разделе «Стадия 2».
Бактериологический контроль на стерильность и контроль на отсутствие пирогенных веществ осуществляют в соответствии с действующими приказами МЗ и СЗ ПМР.
5.3. Бракераж. Раствор во флаконе считают забракованным при несоответствии его физико-химическим показателям, содержании видимых
* Целесообразно перед разливом из большой емкости отобрать пробу во флакон для предварительного контроля на отсутствие механических загрязнений.
** За одну серию раствора считают продукцию, полученную в одной емкости от одной загрузки препарата
механических загрязнений, не стерильности и пирогенности раствора, нарушения герметичности укупорки, недостаточности объема заполнения флакона.
Стадия 6. Оформление
Флаконы с растворами оформляют согласно действующему приказу МЗ и СЗ ПМР.
Техника безопасности
При приготовлении растворов для инъекций следует руководствоваться Правилами но устройству, эксплуатации, технике (безопасности и производственной санитарии при работе в аптеках, и правилами по эксплуатации и технике безопасности при работе на автоклавах.
Инструкция
по приготовлению и контролю качества растворов глюкозы 5%. 10%, 20%, 25% для инъекций (без стабилизатора) в условиях аптек.
СОСТАВ: Глюкозы безводной (ФС 42-3102-94) или Глюкозы (в пересчете на без водную) (ФС 42-2419-96) - 50 г, 100 г, 200 г, 250 г. Воды для инъекций (ФС 42-2620-97) - до 1 л
КРАТКАЯ ТЕХНОЛОГИЯ. Раствор готовят в асептических условиях массо-объемным способом. Глюкозу растворяют приблизительно в 2/3 объема воды для инъекций, доводят водой для инъекций до нужного объема, перемешивают.
Раствор фильтруют*, разливают в бутылки, укупоривают резиновыми пробками, обкатывают металлическими колпачками и стерилизуют насыщенным водным паром под давлением при 120 град. С в течение 12 мин.
* Оптимально раствор фильтровать через мембранный микрофильтр типа "Владипор" с размером пор 0,22 - 0,45 мкм.
Примечания.
1. Недопустимо оставлять бутылки с раствором глюкозы в паровом стерилизаторе до полного охлаждения (на ночь).
2. С целью уменьшения времени теплового воздействия на растворы глюкозы при использовании парового стерилизатора без принудительного (форсированного) охлаждения, целесообразно помещать бутылки в биксы и вынимать биксы из парового стерилизатора после окончания цикла стерилизации.
Описание. Бесцветная или слегка желтоватая прозрачная жидкость.
Подлинность.
1. К 1 мл препарата прибавляют 5 мл реактива Фелинга и нагревают до кипения: образуется кирпично - красный осадок.
2. Выпаривают 2-3 капли препарата на водяной бане. После охлаждения к сухому остатку прибавляют 0,01 г тимола, 5-6 капель кислоты серной концентрированной и 1-2 капли воды; появляется красно - фиолетовое окрашивание.
Прозрачность. Раствор должен быть прозрачным (ГФ XI, вып. 1, с. 198).
Цветность. Окраска раствора не должна быть интенсивнее эталона 5б (ГФ XI, вып. 2, с. 194).
рН*. 3,8-6,5 (потенциометрически или с помощью индикаторной бумаги РИФАН).
5-Оксиметилфурфурол и родственные вещества. **
Точно отмеренный объем раствора, эквивалентный 1 г глюкозы, разбавляют водой в мерной колбе до 250 мл измеряют оптическую плотность полученного раствора на спектрофотометре при длине волны 284 нм в кювете с толщиной слоя 10 мм. В качестве контрольного раствора используют воду. Оптическая плотность полученного раствора должна быть не более 0,25.
* Определяют в растворе, предварительно разведенном водой до 5 %. На 100 мл раствора добавляют 0,3 мл насыщенного раствора калия хлорида.
** Определение проводят при наличии спектрофотометра.
Определение объёма раствора, механических включений.
Отклонение от номинального объема +/-5%. Контролируют выборочно 5 бутылок из каждой серии путем измерения объема раствора мерным цилиндром.
Контроль на механические включения проводят по Инструкции по контролю растворов для инъекций, изготовленных в аптеках, на чистоту от механических включений.
Стерильность. Препарат должен быть стерильным (ГФ XI, вып. 2, с. 187 "Испытания на стерильность").
Пирогенность. Препарат должен быть апирогенным (ГФ XI, вып. 1, с. 183).
Тест - доза для 5% и 10% растворов - 10 мл на 1 кг массы животного, для 20% и 25% - 10 мл раствора, предварительно разведенного до 10% апирогенной водой, на 1 кг массы животного.
Количественное определение.
Измеряют показатель преломления исследуемого раствора (n) и воды (n0).
Содержание глюкозы безводной в 1 мл препарата в граммах (X) вычисляют по формуле:
Где 0,00142 - фактор, равный величине прироста показателя преломления раствора глюкозы безводной при увеличении концентрации на 1%.
Упаковка. По 200 или 400 мл в бутылки из стекла НС-2 или НС-2А, укупоренных пробками из резины и обжатых алюминиевыми колпачками.
Контроль на фиксированность укупорки проводят в соответствии с требованиями действующей Инструкции по контролю качества лекарственных средств, изготовляемых в аптеках.
Маркировка. Бутылка с раствором (до стерилизации) маркируют путем надписей, штамповки, используя жетоны и другое. Оформление бутылок с раствором к отпуску согласно действующим единым правилам оформления лекарств, приготовляемых в аптеках.
На этикетке следует указать, что раствор "без стабилизатора".
Хранение. При температуре от +5 град. С до +30 град. С.
Срок годности: 2 месяца*.
ПРИМЕНЕНИЕ. Инфузионный раствор.
* Промежуточные концентрации растворов глюкозы, не указанные в данной инструкции, имеют такой же метод приготовления, контроля, режим стерилизации и срок годности.
Примечания.
1. Изготовление раствора проводится в соответствии с требованиями Общей статьи ГФ XI "Инфекционные лекарственные формы. Лекарственные средства для парентерального применения" (вып. 2, с. 140) и Методических указаний по изготовлению стерильных растворов в аптеках.
2. Подготовка оборудования, инвентаря, упаковочных и укупорочных средств, используемых при изготовлении раствора, правила оформления к отпуску, а также осуществление его контроля (в том числе на механические включения) и оценка качества изготовления проводятся в соответствии с требованиями действующих Инструкций, утверждены приказами МЗ и СЗ ПМР.
3. При изготовлении раствора для инъекций следует руководствоваться Правилами по устройству, эксплуатации, технике безопасности и производственной санитарии при работе в аптеках, действующими Правилами по эксплуатации и технике безопасности при работе на автоклавах.
4. Титрованные растворы, индикаторы и реактивы, приведенные в настоящей инструкции, описаны в ГФ XI, вып. 2, с. 61-133.
gigabaza.ru
УТВЕРЖДАЮЗаместитель министра здравоохраненияРоссийской ФедерацииА.Е.Вилькенот 25.12.97
Состав:Глюкозы безводной (ФС 42-3102-94) или Глюкозы (в пересчете на безводную) (ФС 42-2419-86) - 50 г, 100 г, 200 г или 400 г.Натрия хлорида (ФС 42-2572-95) - 0,26 г.Раствора кислоты хлористоводородной 0,1 М (ГФ XI, вып.2, с.77) - до рН 3,0-4,1 (около 5 мл).Воды для инъекций (ФС 42-2620-97) - до 1 л.Краткая технология. Раствор готовят в асептических условиях массо-объемным способом. Глюкозу растворяют приблизительно в 2/3 объема воды для инъекций, добавляют при перемешивании натрия хлорид и 0,1 М раствор кислоты хлористоводородной до рН 3,0-4,1 (4,8-5,2 мл), объем раствора доводят водой для инъекций до требуемого объема.Раствор фильтруют*, разливают в бутылки для крови, укупоривают резиновыми пробками, обкатывают металлическими колпачками и стерилизуют насыщенным водяным паром под давлением при 120°С в течение 12 мин.
________________
* Оптимально раствор фильтровать через мембранный микрофильтр типа "Владипор" с размером пор 0,22-0,45 мкм.Примечания: 1. Недопустимо оставлять бутылки с раствором глюкозы в паровом стерилизаторе до полного охлаждения (на ночь).
2. С целью уменьшения времени теплового воздействия на растворы глюкозы при использовании парового стерилизатора без принудительного (форсированного) охлаждения целесообразно помещать бутылки в биксы и вынимать биксы из парового стерилизатора после окончания цикла стерилизации.Описание. Бесцветная или слегка желтоватая прозрачная жидкость.Подлинность. 1. К 0,5 мл препарата прибавляют 1 мл реактива Фелинга и нагревают до кипения. Образуется кирпично-красный осадок (глюкоза).
2. Выпаривают 0,2 мл препарата на водяной бане. После охлаждения к сухому остатку прибавляют 0,01 г тимола, 0,2 мл кислоты серной концентрированной и 1-2 капли воды. Появляется красно-фиолетовое окрашивание (глюкоза).
3. К 1 мл препарата прибавляют 0,1 мл кислоты азотной разведенной и 0,1 мл раствора серебра нитрата. Образуется белый творожистый осадок, растворимый в растворе аммиака (хлориды).
4. Графитовую палочку смачивают раствором и вносят в бесцветное пламя. Наблюдается окрашивание пламени в желтый цвет (натрий).
5. К 3 мл препарата прибавляют 1 каплю раствора метилового красного. Раствор окрашивается в красный цвет (кислотность).
6. К 3 мл препарата прибавляют 1 каплю раствора метилового оранжевого. Раствор окрашивается в розовый цвет (кислотность).Цветность. Окраска препарата не должна быть интенсивнее эталона 5б (ГФ XI, вып.1, с.194).Прозрачность. Препарат должен быть прозрачным (ГФ XI, вып.1, с.198).рН* 3,0-4,1. Определяют потенциометрически (ГФ XI, вып.1, с.113) или с помощью индикаторной бумаги РИФАН (ГФ XI, вып.2, с.99).
________________
* Определяют в растворе, предварительно разведенном водой до 5%.Посторонние примеси (5-гидроксиметилфурфурол и родственные соединения*).
________________
* Определение проводят при наличии спектрофотометра.Точно отмеренный объем препарата, эквивалентный 1 г глюкозы, разбавляют водой в мерной колбе до 250 мл. Измеряют оптическую плотность полученного раствора на спектрофотометре при длине волны 284 нм в кювете с толщиной слоя 10 мм. В качестве контрольного раствора используют воду. Оптическая плотность полученного раствора должна быть не более 0,25.Определение объема препарата. Допустимое отклонение от номинального объема ± 5%. Контролируют выборочно 5 бутылок от каждой серии путем измерения объема препарата мерным цилиндром.Механические включения. Препарат должен выдерживать требования "Инструкции по контролю инъекционных и офтальмологических растворов и глазных капель, изготовленных в аптеках, на механические включения".Пирогенность. Препарат должен быть апирогенным (ГФ XI, вып.2, с.183). Тест-доза для 5 и 10% раствора - 10 мл на 1 кг массы животного.Тест-доза для 25 и 40% - 10 мл раствора, предварительно разведенного до 10% апирогенной водой, на 1 кг массы животного.Стерильность. Препарат должен быть стерильным (ГФ XI, вып.2, с.187).
1. Измеряют показатель преломления исследуемого препарата (n) и воды () при температуре 20°С.Содержание глюкозы безводной в 1 мл препарата в граммах (X) вычисляют по формуле:
X = (n - ) : (0,00142 х 100),
где 0,00142 - фактор, равный величине прироста показателя преломления раствора глюкозы безводной при увеличении концентрации на 1%.В 1 мл препарата должно быть соответственно 0,0485-0,0515 г, 0,097-0,103 г, 0,194-0,206 г или 0,388-0,412 г глюкозы безводной.
2. Титруют 25 мл препарата 0,1 М раствором серебра нитрата до оранжево-желтого окрашивания (индикатор - калия хромат).1 мл 0,1 М раствора серебра нитрата соответствует 0,0097 г суммы натрия хлорида и кислоты хлористоводородной, которых в 1 мл препарата должно быть 0,00043-0,00053 г.На титрование 25 мл препарата должно быть израсходовано 1,12-1,36 мл 0,1 М раствора серебра нитрата*.
________________
* При изготовлении раствора глюкозы для инъекций (любой концентрации) можно использовать приготовленный заранее стабилизатор, содержащий натрия хлорида 5,2 г; кислоты хлористоводородной разведенной 4,4 мл в 1 л воды для инъекций и проверенный полным химическим контролем. Стабилизатор добавляют в количестве 5% от общего объема изготовляемого раствора.Упаковка. По 200 или 400 мл в бутылки для крови из стекла НС-2 или НС-2А по ГОСТ 10782-85, укупоренные пробками из резины 52-369/1 по ТУ 38-006269-95, 52-599/1, 52-599/3 по ТУ 38-106618-95 и обжатые алюминиевыми колпачками по ТУ 9467-003-05749470-94.Контроль на фиксированность укупорки проводят в соответствии с требованиями действующей "Инструкции по контролю качества лекарственных средств, изготовляемых в аптеках".Маркировка. Бутылки с раствором (до стерилизации) маркируют путем надписей, штамповки, используя жетоны и др. Оформление бутылок с раствором к отпуску согласно действующим единым правилам оформления лекарств, приготовляемых в аптеках.Хранение. При температуре от 5 до 30°С.Срок годности*. 3 месяца.
________________
* Промежуточные концентрации раствора глюкозы, не указанные в данных МУ, имеют такой же метод приготовления, контроля качества, режим стерилизации и срок годности.Инфузионный раствор.Примечания. 1. Изготовление раствора проводится в соответствии с требованиями Общей статьи ГФ XI "Инъекционные лекарственные формы. Лекарственные средства для парентерального применения" (вып.2, с.140) и "Методических указаний по изготовлению стерильных растворов в аптеках" (24.08.94).
2. Подготовка оборудования, инвентаря, упаковочных и укупорочных средств, используемых при изготовлении раствора, правила оформления к отпуску, а также осуществление его контроля (в т.ч. на механические включения) и оценка качества изготовления проводятся в соответствии с требованиями действующих Инструкций, утв. приказами Минздрава СССР N 581* от 30.04.85, N 96** от 03.04.91, N 276*** от 27.09.91, N 530"**** от 04.06.82, N 583"**** от.19.07.72.
________________
* Приказ Минздрава СССР от 30.04.85 N 581 "Об утверждении Инструкции по санитарному режиму аптек" отменен приказом Минздрава России от 21.10.97 N 309 (опубликован в журнале "Новая Аптека", 1998, октябрь).** Приказ Минздрава СССР от 03.04.91 N 96 "О контроле качества лекарственных средств, изготовляемых в аптеках" отменен приказом Минздрава России от 16.07.97 N 214 (опубликован в журнале "Новая Аптека", 1999, N 1).*** Приказ Минздрава СССР от 27.09.91 N 276 "О нормах отклонений, допустимых при изготовлении лекарственных форм и фасовке промышленной продукции в аптеках" отменен приказом Минздрава России от 16.10.97 N 305 (опубликован в журнале "Новая Аптека", 1998, июль).**** В настоящее время действуют Единые правила оформления лекарств, приготовляемых в аптечных учреждениях (предприятиях) различных форм собственности (Методические рекомендации), утв. Минздравом России от 24.07.97.
3. При изготовлении раствора для инъекций следует руководствоваться правилами по устройству, эксплуатации, технике безопасности и производственной санитарии при работе в аптеках, действующими правилами по эксплуатации и технике безопасности при работе на автоклавах.
4. Титрованные растворы, индикаторы и реактивы, приведенные в настоящих МУ, описаны в ГФ XI, вып.2.
СОГЛАСОВАНОНачальник Управления Государственногоконтроля лекарственных средстви медицинской техники Минздрава РоссииР.У.Хабриев25.12.97
Начальник Управления научныхи образовательных медицинскихучреждений Минздрава РоссииВ.И.Сергиенко
Текст документа сверен по:"Новая аптека", N 7, 1999 год
docs.cntd.ru
Отчёт по лабораторной работе«Фармакопейный анализ углеводов».
Цель работы: Освоить методы оценки качества углеводов
Объекты исследования: Раствор глюкозы 5 % для инъекций – Solutio Glucosi 5 % pro injectionibus
Оборудование:1) Электронные весы2) Поляриметр3) Рефрактометр
Посуда: пробирки, пипетки, бюретки, мерные колбы, колбы для титрования, химические стаканы, мензурки
Реактивы:1. Вода очищенная2. Гидроксид аммония3. 0,1 М раствор иода4. 10 % раствор гидроксида натрия5. Кислота хлористоводородная разведенная6. 0,1 М раствор тиосульфата натрия
Индикаторы: крахмал
Ход работы:
I.Описание.
На анализ поступил объект – раствор глюкозы для инъекций 5 %.
Раствор глюкозы 5 % для инъекций представляет собой бесцветную прозрачную жидкость, что соответствует требованиям НД.
II. Количественное определение
1. Ознакомились с поляриметрическим методом количественного определения:
Объем исследуемого раствора, эквивалентный 2,5 г глюкозы (50 мл 5 %), поместили в мерную колбу вместимостью 100 мл, прибавили 0,2 мл раствора гидроксида аммония, довели объем раствора до метки, перемешали и оставили на 40 минут.
При измерении оптического вращения на поляриметре сначала устанавливают нулевую точку прибора и определяют величину поправки с трубкой, заполненной растворителем (водой очищенной). После этого проводят основное измерение не менее 3 раз.
Содержание глюкозы в 1 мл в граммах (Х):Х = α ∙ 100/52,8 ∙ v ∙ l
где: α – угол вращения испытуемого раствора, в градусах
l – толщина слоя, в дм
52,8 – удельное вращение глюкозы
v – объем исследуемого раствора, взятый для определения, в мл
2. Рефрактометрическое определение:
На призму рефрактометра нанесли несколько капель воды и салфеткой аккуратно вытерли ее, тем самым проводя очистку и подготовку прибора к работе. Данное действие повторили несколько раз. Затем пипеткой на призму нанесли несколько капель воды очищенной и по шкале нашли показатель преломления (no = 1, 3323), установили границу отсчета. Осторожно вытерли призму насухо как в начале испытания. Затем нанесли на призму несколько капель испытуемого раствора – раствор глюкозы для инъекций 5 % – и нашли показатель преломления ( n = 1,3413).
Содержание глюкозы в 1 мл в граммах (Х):Х = n – no/ 0,00142 ∙ 100
где 0,00142 – фактор показателя преломления безводной глюкозы
Результат: Х = 1,3413 – 1, 3323/0,00142 ∙ 100 = 0,0633803
Отклонение по ФС должно быть ± 10%
5% – 0,05
х% – 0,06 → х = 5 ∙ 0,06/ 0,05 = 6%, что соответствует требованиям НД.
3. Иодиметрическое определение 5 % раствора глюкозы для инъекциий
Для проведения испытания градуированной пипеткой отобрали 1,0 мл 5% раствора глюкозы и поместили в мензурку.. Довели объем раствора в мензурке до 10 мл водой очищенной, премешали. Затем перенесли раствор из мензурки в колбу для титрования. В колбу пипеткой добавили 10,0 мл 0,1 М раствора иода, 2,0 мл 10 % раствора гидроксида натрия, закрыли колбу пробкой и реакционную смесь оставили стоять в темном месте 5 минут. Далее пипеткой прибавили 5,0 мл кислоты хлористоводородной разведенной и титровали 0,1 М раствором тиосульфата натрия до обесцвечивания раствора (индикатор – крахмал). Параллельно проводили контрольный опыт.
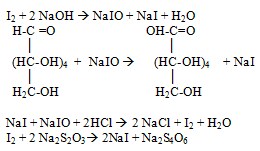
Объём титранта в основном опыте составил 0,8 мл.
Объём титранта в контрольном опыте составил 4,6 мл.
fэ = 1/2
Мэ= М ∙ fэ = 180,0/2 = 90 г/моль∙экв.
Т = Сэ ∙ Мэ / 1000 = 0,1 ∙ 90/1000 = 0,009 г/мл
ω = (Vк.о. – V2 )∙ K∙ T ∙100 ∙ / а ∙ = ( 4,6 – 0,8)∙ 0,009 ∙ 100/ 1 = 3,42%
где Vк.о. – объем титранта, пошедшего на титрование контрольного опыта, мл;
V2 – объем титранта, пошедшего на титрование избытка титранта, мл
K – поправочный коэффициент титранта;
T – количество анализируемого вещества, г, соответствующее 1 мл титранта;
a – масса вещества, взятая для анализа, г
3,42% / 100 = 0,0342 г
0.0292 – 0.0392 г. – не соответствует требованиям НД
5% – 0,05
0,05± 10%
0,05± 0,005
По НД содержание глюкозы 0,045-0,055 г
Вывод: В ходе проделанной работы были освоены способы оценки качества углеводов. Был проведен анализ препарата – раствор глюкозы 5 % для инъекций. Было установлено соответствие образца 5 % раствора глюкозы для инъекций требованиям НД по показателям: описание, количественное определение методом рефрактометрии, – и несоответствие по показателю количественное определение иодиметрическим методом, а также сделан вывод о неудовлетворительном качестве представленного образца.
farmf.ru
Флакон оранжевого стекла укупоривают плотно пластмассовой пробкой с навинчивающейся крышкой. Наклеивают номер рецепта и этикетки «Внутреннее», «Хранить в прохладном месте», «Беречь от детей».
74.Возьми:Калия бромида 3,0
Глюкозы 5,0
Воды очищенной 200 мл
Смешай.Выдай.Обозначь: По 1 столовой ложке 3 раза в день.
Решение:
Recipe: Kalii bromidi 3,0
Glucosi 5,0
Aquae purificatae 200 ml
M.D.S.По 1 столовой ложке 3 раза в день.
Выписана жидкая лекарственная форма для внутреннего применения, представляющая собой истинный раствор.
Оборотная сторона
Калия бромид 3,0, КУО=0,27
Глюкозы 5.0 КУО=0,69
Глюкоза с учетом влажности
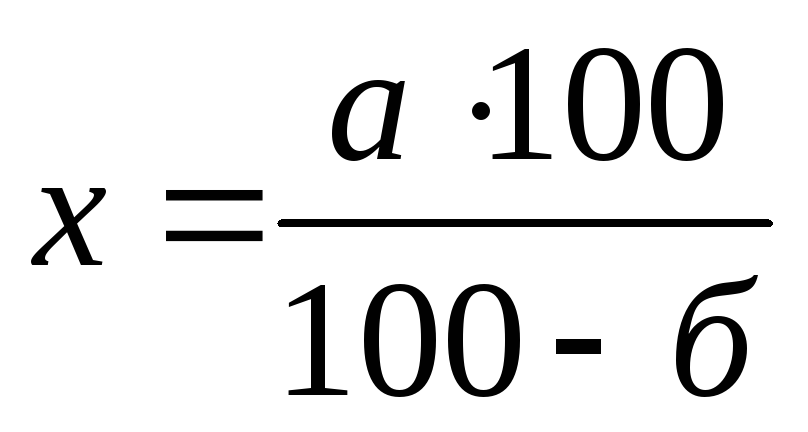 ,
,
где: х – масса глюкозы, необходимая для изготовления раствора, г;
а – масса безводной глюкозы, требуемая для изготовления
раствора, г;
б – содержание влаги в глюкозе, %.
5х100
Х=----------------=5,5
100-10
Содержание сухих веществ (3,0+5,5)/200=0,0426 или 4,25%
Очищенной воды 200 - (3,0х0,27+5,5х0,69)=195,4мл
Общий объем 200 мл
Поскольку количество сухих веществ превышает 3% от объема раствора, лекарственную форму готовят с учет КУО.
В подставку отмеривают 195,4 мл воды очищенной. На весах ВР-10 отвешивают 5,5 глюкозы водной, на весах ВР-5 отвешиваю 3,0 калия бромида, последовательно добавляют в воду очищенную и тщательно перемешивают, фильтруют в отпускной флакон через бумажный фильтр, укупоривают и оформляют к отпуску.
ППК
Лицевая сторона
Дата № рецепта
Aquae purificatae 195,4 ml
Glucosi 5,5
Kalii bromidi 3,0
Vобщ= 200 мл
Приготовил
Проверил
Отпустил
Флакон бесцветного стекла укупоривают плотно пластмассовой пробкой с навинчивающейся крышкой. Наклеивают номер рецепта и этикетки «Внутреннее», «Хранить в прохладном месте», «Беречь от детей».
81.Возьми:Натрия бромида 3,0
Раствора кальция хлорида 5% - 200 мл
Адонизида 5 мл
Смешай.Выдай.Обозначь: По 1 столовой ложке 4 раза в день.
1.Recipe Natrii bromidi 3,0
Sol. Саlciichloridi5% 200ml
Аdonisidi5ml
M.D.S.По 1 столовой ложке 4 раза в день.
Выписана жидкая лекарственная форма для внутреннего применения, представляющая собой микстуру.
Оборотная сторона
Кальция хлорида 10,0, КУО=0,37
Натрия бромида 3,0, КУО=0,26
Содержание сухих веществ (10,0+3,0)/205=0,063 или 6,3%
Очищенной воды 200-10х0,37-3х0.26=195,5 мл
Адонизида 5 мл
Общий объем 200+5=205 мл
Поскольку количество сухих веществ превышает 3% от объема раствора, лекарственную форму готовят с учет КУО.
В подставку отмеривают 195,5 мл воды очищенной. На весах ВР-10 отвешивают 10,0 кальция хлорида, на весах ВР-5 3,0 натрия бромида, последовательно добавляют в воду очищенную и тщательно перемешивают, фильтруют в отпускной флакон через бумажный фильтр. В отдельный стаканчик отмеривают 5 мл адонизида, смешивают с примерно равным количеством «солевого» раствора, затем частями при перемешивании добавляют в склянку для отпуска. Стаканчик ополаскивают готовой микстурой. Отпускной флакон взбалтывают и оформляют к отпуску.
ППК
Лицевая сторона
Дата № рецепта
Aquae purificatae 195,5 ml
Natrii bromidi 3,0
Саlcii chloridi 10,0
Аdonisidi 5ml
Vобщ= 205 ml
Приготовил
Проверил
Отпустил
studfiles.net
Cтраница 1
Стандартные растворы глюкозы [ 1 т безводной глюкозы, перекристаллизованной из спирта, количественно переносят в мерную колбу вместимостью 100 мл и добавляют дистиллированной воды до метки при 20 С. Полученный раствор перемешивают и от него отбирают 10 мл в мерную колбу вместимостью 100 мл и доливают дистиллированную воду до метки. Получают рабочий раствор, из которого готовят стандартные растворы концентрацией 10, 30 и 60 мкг в 1 мл раствора. Для этого берут три колбы вместимостью по 100 мл, в одну колбу наливают 1 мл, в другую 3 и в третью 6 мл рабочего раствора. К содержимому колб приливают раствор бензойной кислоты ( 2 7 г бензойной кислоты в 1 л дистиллированной воды) до метки при 20 С. Получают три стандартных раствора глюкозы необходимой концентрации. Такие растворы могут храниться в холодильнике в течение 1 года. [1]
Использу я стандартные растворы глюкозы с содержанием 10, ЗС, 60, 90 и 150 миг на 1 мл раствора, строят калибровочную кривую так же, как при применении о-дианизидина. [2]
Для построения калибровочной кривой используют стандартные растворы глюкозы, содержащие в 1 см3 50, 100 и 150 мкг глюкозы. [3]
Одновременно выполняется контрольное определение на стандартном растворе глюкозы и гултаминовой кислоты. [4]
Одновременно выполняется контрольное определение на стандартном растворе глюкозы и глутаминовой кислоты. [5]
При пользовании фотоколориметром его следует откалибровать по стандартным растворам глюкозы. [6]
Для этого в сухие мерные колбы вместимостью 100 см3 с помощью бюретки наливают стандартный раствор глюкозы в объемах, приведенных в табл. 3, и доливают до метки 0 5 % - ным раствором гидроокиси натрия. [7]
Параллельно с исследуемыми растворами ставят контрольную пробу с дистиллированной водой и пробы со стандартными растворами глюкозы. [8]
Для измерения концентрации глюкозы с помощью энзимного электрода на основе глюкозооксидазы последний необходимо калибровать по стандартным растворам глюкозы, подобно другим ионоселективным мембранным электродам. [10]
Например, на предварительное титрование реакционной жидкости пошло 0 80 мл, необходимо добавить в раствор 0 80 - 0 10 0 70 мл стандартного раствора глюкозы, тогда дистиллированной воды приливают 2 50 - 0 701 8 мл. [11]
Количество глюкозы в опытных пробах рассчитывают по калибровочному графику. Ввиду того что сернокислый цинк и щелочь частично ингибируют глюкозооксидазу, пробы со стандартным раствором глюкозы обрабатывают так же, как и опытные. Объем проб доводят дистиллированной водой до 3 мл, в контрольную пробу ( без глюкозы) вносят 3 мл дистиллированной воды. Осадок гидроокиси цинка удаляют центрифугированием или фильтрованием. Из каждой пробы отбирают по 0 5 мл раствора в чистые и сухие пробирки, приливают по 0 5 мл дистиллированной воды и по 3 мл рабочего реактива, перемешивают и фотометрируют развившуюся синюю окраску при 630 нм. [12]
Употребляют только свежеприготовленный реактив. Продажный препарат антрона надо дважды перекристаллизовать из бензола или ледяной уксусной кислоты; б) стандартный раствор глюкозы: в 1 л кипящей воды растворяют 2 5 г бензойной кислоты. На аналитических весах отвешивают 1 г глюкозы. [13]
В коническую колбу на 50 - 70 мл наливают 2 5 мл испытуемого раствора, в котором должно быть не более 0 15 % редуцирующих углеводов, добавляют 2 5 мл дистиллированной воды, 5 мл раствора Фелинга I и 5 мл раствора Фелинга II. Колбу с реакционной смесью помещают на электроплитку, содержимое доводят до кипения и предварительно титруют стандартным раствором глюкозы из микробюретки с Z-образным наконечником. Отсчитывают количество израсходованного раствора. После этого проводят основное титрование, на которое берут по 5 мл растворов Фелинга I и II, 2 5 мл испытуемого раствора и добавляют столько раствора глюкозы, сколько пошло его на предварительное титрование, за вычетом 0 10 - 0 15 мл. Затем к раствору добавляют такое количество дистиллированной воды, чтобы в сумме с раствором глюкозы получилось 2 5 мл. [14]
Пентозы образуют только фурфурол ( но не формальдегид) и определению гексоз не мешают. Смешивают 1 мл раствора, содержащего 50 - 300 мгк гексозы, с 5 мл 0 2 % - ного раствора хро-мотроповой кислоты в 15 М h3SO4 и нагревают 30 мин при 100 С. После охлаждения до комнатной температуры вводят 9 М h3SO4 до объема 10 мл и измеряют оптическую плотность при 570 нм. Калибровочный график строят, используя стандартные растворы глюкозы. [15]
Страницы: 1 2
www.ngpedia.ru
Приготовление стандартных растворов глюкозы. Для приготовления используют перекристаллизованную из спирта безводную глюкозу, которую хранят в эксикаторе над хлористым кальцием. Для приготовления раствора отвешивают на аналитических весах 100 мг глюкозы с точностью до четвертого знака после запятой и растворяют ее в 100 мл насыщенного раствора бензойной кислоты (для приготовления насыщенного раствора бензойной кислоты 2,7 г бензойной кислоты растворяют дистиллированной водой в мерной колбе вместимостью 1000 мл). Из этого раствора отбирают 5, 10, 15 мл в мерные колбы вместимостью 100 мл и доводят объем до метки бензойной кислотой. Полученные растворы с содержанием 50, 100 и 150 мкг глюкозы в 1 мл используются для построения градуировочной кривой. [c.288]
Приготовление стандартных растворов. В небольших химических стаканчиках на аналитических весах отвешивают 2, 4, 6, 8, 10, 12 г глюкозы, добавляют немного воды и получившийся сироп количественно переносят в мерные колбочки на 50 мл. Добавляют до метки дистиллированной воды и тщательно перемешивают, многократно переворачивая колбочку. [c.149]
Приготовление раствора стандартного образца глюкозы (5 мг/мл) 0,5 г глюкозы, предварительно высушенной до постоянной массы при температуре 37 °С, растворяют в насыщенном растворе бензойной кислоты в мерной колбе вместимостью 100 мл и доводят объем раствора до метки раствором бензойной кислоты. Срок годности раствора 3 мес при температуре от 8 до 10°С. [c.181]
Реактивы о-толуидиновый реактив ТХУ, 3%-ный раствор глюкоза, стандартный раствор 5,5 ммоль/л (приготовлен разбавлением 27,75 ммоль/л раствора). [c.131]
Хотя при производстве листов хроматографической бумаги изготовители проявляют особую тщательность, все же для таких сложных структур, как бумага, будут встречаться различия между отдельными листами. Эти различия резче выражены в ТСХ, где большинство исследователей для приготовления пластинок пользуются ручным распределением сорбента по поверхности. Как уже сообщалось, результаты, полученные при развитии хроматограммы, в условиях, когда на бумагу наносят одинаковые количества вещества, могут немного различаться. Как бы то ни было, при количественном анализе всегда возникает следующая проблема можно ли результаты исследований со стандартными растворами достаточно надежно распространить на результаты, полученные с неизвестным и совершенно отличным количеством анализируемой пробы. Возникает еще и другой вопрос является ли постоянным для одного листа хроматографической бумаги наклон линии регрессии, связывающей количество вещества, найденного в конечной зоне, с количеством вещества, нанесенным в точку на линии старта. И если это условие выполняется, то сохраняется ли постоянным наклон линии регрессии при развитии хроматограмм на других листах бумаги в одинаковых условиях хроматографического опыта Авторы работ [3, 4, 7] уже показали, что наклон линии регрессии ие всегда постоянен, но, поскольку в этих работах источники ошибок обусловлены процессом нанесения начальных пятен, было решено изучить эту проблему заново, используя устройство, предназначенное для точного измерения начальных объемов. На каждый из 10 листов хроматографической бумаги наносили по 10 проб радиоактивной глюкозы, содержащих от 20 до 100 мкг глюкозы. Затем проводили процесс развития хроматограмм как с одним листом, так и с серией из четырех листов одновременно в одной камере при температуре 18°, поддерживаемой с помощью водяной бани. Описания линий регрессии для каждого листа приведены в табл. 4, а две наиболее отклоняющиеся [c.21]
СИ, что может вызвать тяжелые ожоги при попадании на кожу или в глаза. Необходимо пользоваться защитными очками и перчатками. Нельзя насасывать раствор в пипетку ртом. Необходимо знать меры по оказанию первой помощи при попадании кислот на кожу и в глаза.) Пробирки помещают на 15 мин в водяную баню с температурой 25 °С и затем снимают показания оптической плотности в каждой пробе при 488 нм против контрольного образца, приготовленного без глюкозы (разд. 16.1.1). Концентрацию глюкозы в пробах определяют по стандартной калибровочной кривой, отражающей зависимость между оптической плотностью стандартных растворов и концентрацией глюкозы. [c.296]
Рабочий раствор Фелинга I [основной раствор Фелинга I разбав-ляют примерно в 20 раз (5 мл разбавляют до 100 мл)]. Титр рабочего раствора должен быть точным и содержать 0,003463 г uS04-5h30 в 1 л. Его проверяют по стандартному 1,0%-ному раствору перекристаллизованной глюкозы, приготовленному за 4—5 ч до анализа. Для проверки титра раствор глюкозы разбавляют в 25 раз (4 мл стандартного раствора в мерной колбе на 100 мл доливают дистиллированной водой до метки при 20° С) и определяют в нем содержание сахаров по методу Бертрана (для определения точного содержания сахара в растворе) и микрометодом (для установления количества основного раствора Фелинга I необходимого для приготовления рабочего). [c.135]
Приготовление стандартного раствора глюкозы. В мерную колбу па 100 мл вносят 1 г глюкозы, растворяют ее в небольшом объеме дистиллированной воды, а затем доводят до метки 1 мл прнго-товлеппого раствора содержит 10 мг глюкозы. [c.113]
Снижение концентрации сахара обусловлено повышением гликогенообразоеательной функции печени и мышц и увеличением интенсивности окислительного распада глюкозы. За единицу инсулина принята специфическая биологическая активность 0,045 мг стандартного кристаллического препарата, приготовленного Лабораторией по государственному контролю органопрепаратов в Москве. Это количество инсулина в течение часа снижает содержание сахара в крови кролика весом 2 кг, предварительно голодавшего 24 часа, до 45 мг% и вызывает у него вознинно вение судорог. [c.177]
Одним из показателей, определяемых цри установлении ПДКд веществ в воде водоемов, является их пороговая концентрация, не влияющая на санитарный режим водоемов. При определении этого показателя учитывалось влияние ПЖ на процессы биохимического потребления кислорода (БОК), нитрификации и развития простейших организмов /6/. Для приготовления растворов кислоты использовали ПМДА, соответствующий Т7 38.10227-80. Пороговой концентрацией вещества, существенно не влияющей на баланс растворенного кислоро -да, тем самым и на общий санитарный режим водоемов, является та, которая изменяет БПК не более чем на 10-15/ по сравнению с контрольной пробой. Определение ЕПК проводили методом разбавления /7/, стандартный фон загрязнений в разбавляющей воде создавали введением глюкозы, вещества хорошо биологически окисляемого /8/. [c.92]
chem21.info
Зам. руководителя Департамента государственного контроля качества, эффективности, безопасности лекарственных средств и медицинской техники МЗ РФ А.А. Топорков 17.07.2001 г.
Рекомендована к утверждению Комиссией по лабораторным реагентам Комитета по новой медицинской технике МЗ РФ (протокол № 9 от 30.10.2000 г.)
ИНСТРУКЦИЯ
по применению набора реагентов для определения глюкозы в биологических жидкостях глюкозооксидазным методом
НАЗНАЧЕНИЕ
Набор предназначен для количественного и качественного колориметрического определения концентрации глюкозы в сыворотке и плазме крови, цельной крови и моче человека глюкозооксидазным методом в клинико-диагностических и биохимических лабораториях и в научно-исследовательской практике. Набор рассчитан на проведение 400 определений при расходе 1,0 мл рабочего раствора на один анализ.
ПРИНЦИП ДЕЙСТВИЯ
Глюкозоксидаза окисляет D-глюкозу до глюкуроновой кислоты с образованием перекиси водорода; последняя под действием пероксидазы реагирует с 4-аминоантипирином и фенолом с образованием соединения красного цвета, интенсивность окраски которого пропорциональна концентрации глюкозы в анализируемом образце и измеряется фотометрически при длине волны 510 (470–540) нм.
СОСТАВ НАБОРА
1. Концентрат буфера с фенолом (фенол — 20,7 г/л, калий фосфорнокислый двузамещенный 3-водный — 137 г/л, калий фосфорнокислый однозамещенный — 55 г/л), 10 мл — 2 флакона.
2. Субстратно-ферментная смесь сухая (4-аминоантипирин — 0,032 г, глюкозооксидаза — 3000 МЕ, пероксидаза — 300 МЕ) — 2 флакона.
3. Антикоагулянт сухой (натрий хлористый — 4,2 г, натрий фтористый — 0,11 г, этилендиамин-N,N,N`,N`-тетрауксусной кислоты динатриевая соль 2-водная — 0,2 г) — 1 упаковка.
4. Калибровочный раствор глюкозы (глюкоза — 10 ммоль/л, бензойная кислота — 1,8 г/л), 2,0 мл — 1 флакон.
АНАЛИТИЧЕСКИЕ ХАРАКТЕРИСТИКИ НАБОРА
Линейная область определения концентрации глюкозы — в диапазоне от 2 до 20 ммоль/л, отклонение от линейности — не более 5%.
Чувствительность определения — не более 1 ммоль/л.
Воспроизводимость: коэффициент вариации не более 5%.
Нормальные величины концентрации глюкозы составляют:
— для сыворотки крови и плазмы крови 3,9–6,1 ммоль/л;
— для цельной крови 3,3–5,5 ммоль/л;
— для мочи не более 0,5 ммоль/л.
Качество набора можно оценивать по контрольным сывороткам отечественного или зарубежного производства, аттестованными данным методом. Рекомендуется в каждой лаборатории уточнить диапазон нормальных величин у обследуемого контингента.
МЕРЫ ПРЕДОСТОРОЖНОСТИ
При работе с набором необходимо соблюдать правила техники безопасности, рекомендуемые при работе с кровью в соответствии с «Инструкцией по мерам профилактики распространения инфекционных заболеваний при работе в клинико-диагностических лабораториях лечебных и профилактических учреждений», утвержденной Минздравом СССР от 17.01.91 г. и «Правила устройства, техники безопасности, производственной санитарии, противоэпидемического режима и личной гигиены при работе в лабораториях (отделениях, отделах) санитарно-эпидемиологических учреждений системы Министерства здравоохранения СССР» (М., 1981 г.). При работе с набором следует надевать одноразовые резиновые или пластиковые перчатки, так как образцы крови человека следует рассматривать как потенциально инфицированные, способные длительное время сохранять или передавать ВИЧ, вирус гепатита или любой другой возбудитель вирусной инфекции. Все компоненты набора в используемых концентрациях являются нетоксичными.
ОБОРУДОВАНИЕ И РЕАГЕНТЫ
— Спектрофотометр, длина волны 510 нм, или фотоэлектроколориметр, длина волны 470–540 нм (зеленый светофильтр), кювета с толщиной поглощающего свет слоя 10 или 5 мм;
— пипетки, позволяющие отбирать объем жидкости 0,01 и 1,0 мл;
— колбы мерные вместимостью 200 и 500 мл;
— пробирки центрифужные вместимостью 5–10 мл;
— термостат, обеспечивающий температуру +37° С;
— центрифуга лабораторная на 3000 об/мин;
— секундомер; — вода дистиллированная;
— перчатки резиновые или пластиковые.
АНАЛИЗИРУЕМЫЕ ОБРАЗЦЫ
Негемолизированная сыворотка или плазма крови, цельная кровь, моча.
ПОДГОТОВКА РЕАГЕНТОВ ДЛЯ АНАЛИЗА
Рабочий раствор. В мерной колбе вместимостью 200 мл последовательно растворить в дистиллированной воде содержимое одного флакона концентрата буфера с фенолом и одного флакона сухой субстратно-ферментной смеси, затем довести объем дистиллированной водой до метки. Рабочий раствор можно хранить в темном месте в плотно укупоренной посуде при температуре +2–8° С не более 1 месяца.
Антикоагуляционный раствор (для определения глюкозы в цельной крови). Содержимое упаковки с сухим антикоагулянтом количественно перенести в мерную колбу вместимостью 500 мл, растворить в дистиллированной воде и довести объем дистиллированной водой до метки. Антикоагуляционный раствор можно хранить в плотно укупоренной посуде при температуре +2–8° С не более 3 месяцев.
Калибровочный раствор глюкозы готов к применению.
ПРОВЕДЕНИЕ АНАЛИЗА
1. Определение глюкозы в сыворотке (плазме) крови и моче.
Компоненты реакционной смеси внести в пробирки в количествах, указанных в таблице 1.
Таблица 1
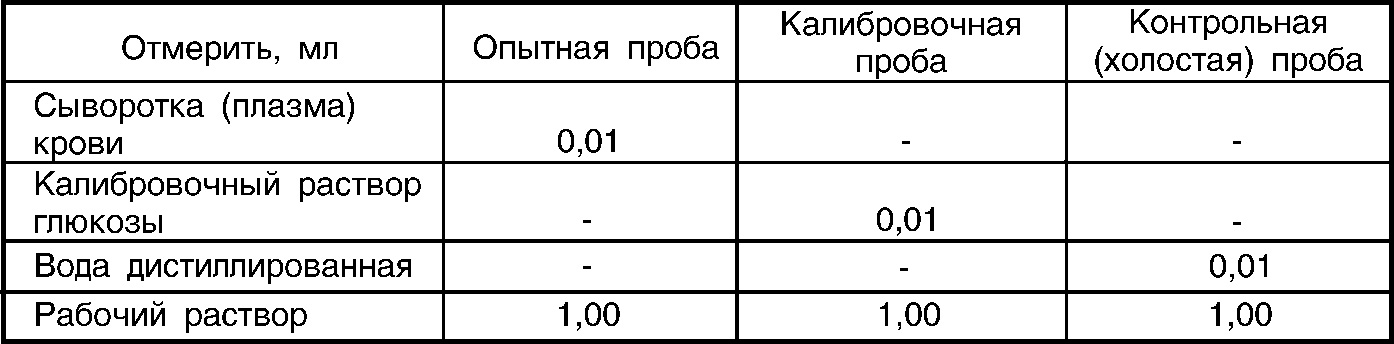
Содержимое пробирок тщательно перемешать и инкубировать в течение 15 минут при температуре +37° С или в течение 30 минут при комнатной температуре (+18–25° С). Через 5–10 минут после начала инкубации пробирки интенсивно встряхнуть. После окончания инкубации измерить величину оптической плотности калибровочной и опытных проб против контрольной (холостой) пробы при длине волны 510 (470–540) нм в кювете с толщиной поглощающего свет слоя 10 или 5 мм. Окраска устойчива в течение 1 часа после окончания инкубации.
Концентрацию глюкозы рассчитать по формуле:
Eо
С = ------------------ х 10 ,
Eк
где: С — концентрация глюкозы в опытной пробе, ммоль/л;
Eо — оптическая плотность опытной пробы, ед.опт.плотн.;
Eк — оптическая плотность калибровочной пробы, ед.опт.плотн.;
10 — концентрация глюкозы в калибровочном растворе, ммоль/л.
Примечание: при использовании кювет другого объема расход реагентов может быть пропорционально изменен с сохранением соотношения объема анализируемого образца к объему рабочего раствора 1:100.
2. Определение глюкозы в цельной крови.
Компоненты реакционной смеси внести в пробирки в количествах, указанных в таблице 2.
Таблица 2
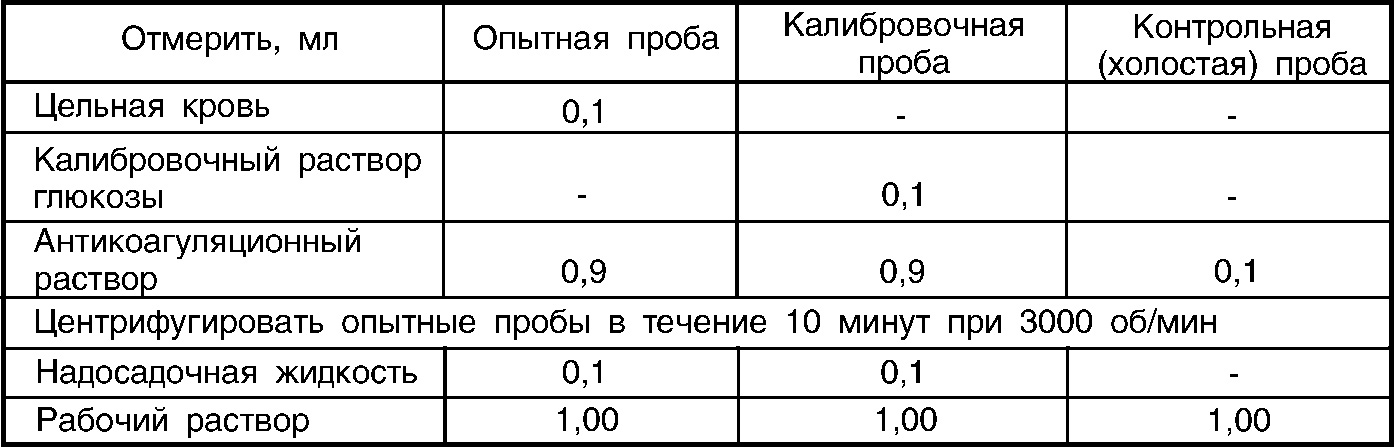
Дальше определение, измерение оптической плотности и расчеты проводить так, как это указано для сыворотки (плазмы) крови.
3. Качественное определение глюкозы в моче.
В центрифужной пробирке смешать 0,2 мл рабочего раствора, 0,02 мл мочи и инкубировать в течение 15–20 минут при комнатной температуре (+18–25° С). Пробы мочи, вызывающие покраснение реакционной смеси, считать положительными.
УСЛОВИЯ ХРАНЕНИЯ И ЭКСПЛУАТАЦИИ НАБОРА
Набор должен храниться в упаковке предприятия-изготовителя при температуре +2–8° С в течение всего срока годности. Допускается хранение наборов при температуре +25° С не более 5 суток. Срок годности набора — 2 года. Рабочий раствор может хранится в темном месте в плотно укупоренной посуде при температуре +2–8° С не более 1 месяца. Антикоагуляционный раствор может храниться в плотно укупоренной посуде при температуре +2–8° С не 3 трех месяцев. Калибровочный раствор глюкозы после вскрытия флакона может храниться в укупоренном виде при температуре +2–8° С не 3 трех месяцев. При получении значений концентрации глюкозы выше 20 ммоль/л анализируемый образец необходимо развести дистиллированной водой в соотношении 1:1, повторить анализ и полученный результат умножить на 2.
По вопросам, касающимся приобретения наборов и их качества, просим обращаться по адресу: 105173, г. Москва, ул. Западная, д. 2, стр. 1, ООО «Агат—Мед». Телефон для справок: (495) 777-41-92.
Инструкция составлена: к.б.н. И.В. Смирновым — зав. лабораторией ГНЦ РАМН, В.В. Майоровой — научным сотрудником ООО «Агат-Мед».www.agat.ru