Реферат на тему "Вода и её биологическое значение". Вода и ее биологическое значение реферат
Реферат на тему "Вода и её биологическое значение" страница 4
Это интересно. Талая вода и её польза. В последнее время распространены различные формы и виды, рекомендации по оздоровлению организма. Одно из них, это применение талой воды. При замерзании воды конфигурация системы биомолекул не нарушается и жизненная функция после оттаивания сохраняется. Вода в твёрдом состоянии имеет иную упорядоченность молекул, чем в жидком. После замерзания и оттаивания она приобретает иные биологические свойства. Это и стало причиной использования воды путем применения талой воды с лечебной целью. (Вода в кастрюле ставится на два часа в морозильную камеру. Затем незамерзшая вода сливается, а лед остается для таяния.) . После оттаивания вода имеет более упорядоченную структуру, с зародышами клатратов льда, что позволяет ей взаимодействовать с биологическими компонентами и растворёнными веществами, например с другой скоростью. При употреблении талой воды в оганизм попадают мелкие центры льдоподобной структуры, которые в дальнейшем могут разрастись и перевести воду во льдоподобное состояние и тем самым произвести оздоравливающее действие.
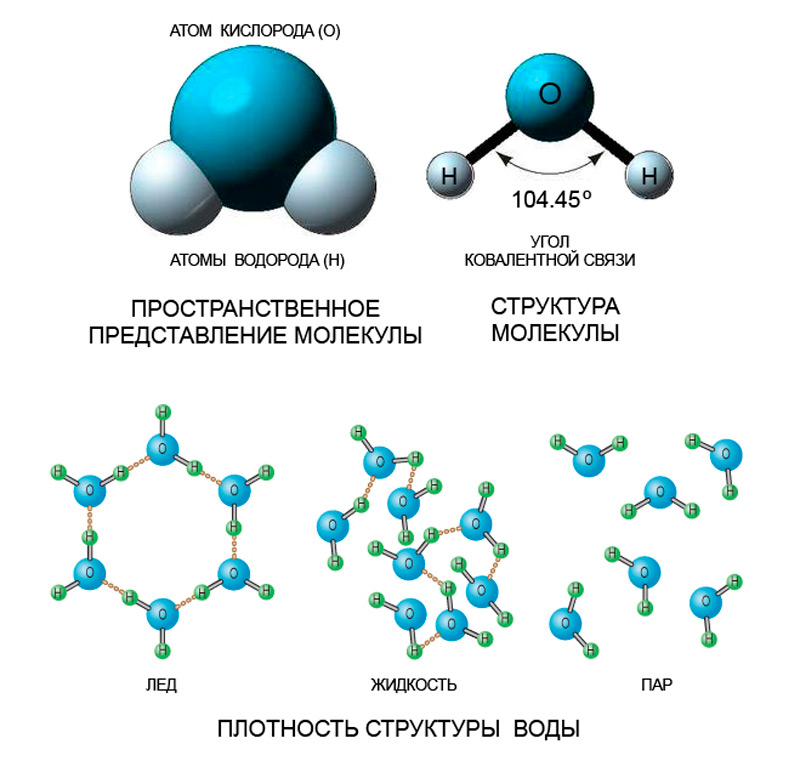
Строение молекулы воды.
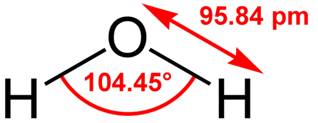
Вода - уникальное вещество и все её аномальные свойства: высокая температура кипения, значительная растворяющая и диссоциирующая способность, малая теплопроводность, высокая теплота испарения и другие обусловлены строением её молекулы и пространственной структурой. В молекуле воды два атома водорода соединены с атомом кислорода так, что их связь образует угол около 105О. О2-
Вследствие этого положительные и отрицательные
заряды распределены неравномерно и сосредото- Н+ 105О Н+
чены в противоположных концах
молекулы. На рис. 1 Схема строения молекулы воды
Такие молекулы называют полярными, или диполями. Исследования привели к тому, что жидкая вода наряду с обыкновенными молекулами Н2О содержит более сложные частицы . Состав их выражается формулой ( Н2О )п,где п =2,3 и т.д.. Такое взаимодействие одинаковых молекул , не изменяющее их химической природы, называется ассоциацией молекул.
Диэлектрик. Опытным путем установлено, что химически чистая вода не проводит электрический ток (является диэлектриком). Проводником воду делают растворенные в ней соли, то есть положительные и отрицательные ионы.
Климат и погода. Вода – важнейший фактор климатообразования. Поглощая тепло из атмосферы, и отдавая его обратно, вода регулирует климатические процессы. Вода играла и играет определяющую роль в геологической истории Земли, в формировании климата и погоды, в круговороте веществ, в физиологической и биологической сферах жизни.
Водные ресурсы Земли.
Общее количество воды на земле оценивается в 14000 млн.км3. Однако стационарные запасы пресных вод, пригодных для использования составляют всего 0,3 % объема гидросферы. Вода на нашей планете находится в состоянии круговорота. Круговорот – это постоянный обмен элементами между воздухом, водой, землей, растениями и животными. Под действием солнечной энергии вода испаряется с поверхности мирового океана и суши, а затем выпадает в виде атмосферных осадков. Все эти процессы дают возможность всему живому на Земле жить и развиваться. Вода также имеет лечебные свойства . Минеральные воды содержат большое количество полезных свойств. Возле таких источников создают санатории. Вода занимает 79,8 % всей поверхности планеты, а на долю суши остается лишь 29,2%. Водную оболочку нашей планеты называют гидросферой. Вода появилась на нашей планете около 3,5 млрд. лет назад в виде паров, которые образовались в результате дегазации мантии. В настоящее время вода – это самый важный элемент в биосфере Земли, поскольку ее нельзя заменить ничем. К счастью, водные ресурсы считаются неисчерпаемыми, поскольку ученые придумали способ опреснения соленых вод. Главное назначение воды как природного ресурса – поддержание жизнедеятельности всего живого – растений, животных и человека. Она – основа всего живого на нашей планете, главный поставщик кислорода в самом важном процессе на Земле – фотосинтезе. Невозможно не отметить роль водных источников в видоизменении нашей планеты. Люди испокон веков селились возле водоемов и источников воды. Вода служит одним из главных средств сообщения. Почти три четверти поверхности Земли покрыто океанами и морями. Это источники влаги, которая, испаряясь, поднимается в атмосферу и образует облака. Моря и океаны оказывают большое влияние на погоду во всем мире, так как воздушные потоки , проходящие над ними, нагреваются или охлаждаются. Водные ресурсы нашей планеты – это запасы всей воды. Это: океаны, озера, реки, моря, болота, подземные воды, искусственные водоемы, ледники и снежники ( Антарктида, Арктика и высокогорья), вода, содержащаяся в растениях и животных, пары атмосферы.
infourok.ru
Реферат по теме Вода и ее биологическое значение
ООО Учебный центр «ПРОФЕССИОНАЛ» Реферат по дисциплине: «Химия: теория и методика преподавания в образовательной организации» По теме: «Вода и её биологическое значение» Исполнитель: Мелентьева Ольга Геннадьевна Москва 2017 год Содержание Введение (с. 3) Физические и химические свойства воды (c. 4) Строение воды (с. 8) Биологическая роль воды (с. 9) Заключение (с. 12) Список литературы (с. 14) Введение Без воды жизнь на нашей планете не могла бы существовать. Вода важна для живых организмов по двум причинам. Во-первых, она является необходимым компонентом живых клеток, и, во-вторых, для многих организмов она служит еще и средой обитания. Цель данной работы – изучение воды как уникального минерального ресурса планеты, ее физико-химические свойства и как следствие значение для всех живых организмов. Вода является основным компонентом большинства растительных клеток и тканей. Содержание воды в клетках варьирует в зависимости от типа клеток и физиологических условий. Например, в корне моркови содержится около 85 % воды, тогда как молодые листья салата на 95 % состоят из воды. В некоторых сухих семенах и спорах содержание воды составляет всего лишь 10 %; однако, для того чтобы они стали метаболически активными, содержание воды в них должно существенно увеличиться. Вода является средой, в которой происходит диффузия растворенных соединений по клеткам растения; представляет собой вещество, необычайно удобное для регуляции температуры; служит растворителем необходимым для протекания многих биохимических реакций; наконец, вода довольно мало сжимаема при давлениях, существующих в организме, что подчеркивает ее роль в поддержании структуры растения. Минеральные вещества, необходимые для роста, и органические соединения, синтезируемые в ходе фотосинтеза – все они транспортируются по растению в виде водных растворов. У активно растущих растений существует непрерывный водный поток из почвы через тело растения к листьям, где вода испаряется в основном через устьица. Вода представляет собой один из необходимых метаболитов, т.е. непосредственно участвует в метаболизме. Она служит источником кислорода, выделяемого в ходе фотосинтеза, и водорода, используемого для восстановления углекислого газа. При образовании АТФ – важного макроэргического соединения – из АДФ и фосфата происходит отщепление воды, иными словами, подобное фосфорилирование есть не что иное, как процесс дегидратации, происходящий в водном растворе в биологических условиях; вода участвует в реакциях гидролиза. Таким образом, знание уникальных свойств воды имеет громадное значение для общего понимания физиологии растений. Если оба атома водорода заменить на атомы дейтерия (2Н), то мы получим тяжелую воду, или окись дейтерия с молекулярной массой 20. В воду можно также ввести атом трития (3Н), который радиоактивен и имеет период полураспада 12,4 г. Такая вода оказалась полезным инструментом в изучении скорости ее диффузии в тканях растений. Возможно пометить воду замещая обычный изотоп воды 16О на тяжелый изотоп 18О. Этот тип метки был использован для доказательства того, что кислород, выделяемый в ходе фотосинтеза, происходит из воды, а не из углекислого газа. [7] Сегодня уже не надо доказывать, какую роль играет вода в жизнедеятельности человека: от ее качества зависит состояние здоровья людей, уровень их санитарно-эпидемиологического благополучия, степень комфортности и, как следствие, социальная стабильность общества в целом.Физические и химические свойства воды. Молекулы воды обнаружены в межзвёздном пространстве. Вода входит в состав комет, большинства планет солнечной системы и их спутников. Изотопный состав. Существуют девять устойчивых изотопных разновидностей воды. Содержание их в пресной воде в среднем следующее: 1Н216О – 99,73%, 1Н218О – 0,2%, 1Н217О – 0,04%, 1h3Н16О – 0,03%. Остальные пять изотопных разновидностей присутствуют в воде в ничтожно малых количествах. Строение молекулы. Как известно, свойства химических соединений зависят от того, из каких элементов состоят их молекулы, и изменяются закономерно. Воду можно рассматривать как оксид водорода или как гидрид кислорода. Атомы водорода и кислорода в молекуле воды расположены в углах равнобедренного треугольника с длиной связи О – Н 0,957 нм; валентный угол Н – О – Н 104o 27’. Физические свойства воды аномальны, что объясняется приведёнными выше данными о взаимодействии между молекулами воды. Вода – единственное вещество на Земле, которое существует в природе во всех трёх агрегатных состояниях – жидком, твёрдом и газообразном. Плавление льда при атмосферном давлении сопровождается уменьшением объёма на 9%. Плотность жидкой воды при температуре, близкой к нулю, больше, чем у льда. При 00С 1 грамм льда занимает объём 1,0905 кубических сантиметров, а 1 грамм жидкой воды занимает объём 1,0001 кубических сантиметров. И лёд плавает, оттого и не промерзают обычно насквозь водоёмы, а лишь покрываются ледяным покровом. Температурный коэффициент объёмного расширения льда и жидкой воды отрицателен при температурах соответственно ниже - 2100 С и + 3,980 С. Теплоёмкость при плавлении возрастает почти вдвое и в интервале от 00 С до 1000 С почти не зависит от температуры. Вода имеет незакономерно высокие температуры плавления и кипения в сравнении с другими водородными соединениями элементов главной подгруппы VI группы таблицы Менделеева. Вода, несмотря на все её аномальные свойства, является эталоном для измерения температуры, массы ( веса), количества тепла, высоты местности. Шведский физик Андерс Цельсий, член Стокгольмской академии наук, создал в 1742 году стоградусную шкалу термометра, которой в настоящее время пользуются почти повсеместно. Точка кипения воды обозначена 100 , а точка таяния льда 0 . [1] Из химических свойств воды особенно важны способность её молекул диссоциировать (распадаться) на ионы и способность воды растворять вещества разной химической природы. Роль воды как главного и универсального растворителя определяется прежде всего полярностью её молекул и, как следствие, её чрезвычайно высокой диэлектрической проницаемостью. Разноимённые электрические заряды, и в частности ионы, притягиваются друг к другу в воде в 80 раз слабее, чем притягивались бы в воздухе. Силы взаимного притяжения между молекулами или атомами погружённого в воду тела также слабее, чем в воздухе. Тепловому движению в этом случае легче разбить молекулы. Оттого и происходит растворение, в том числе многих труднорастворимых веществ: капля камень точит. Электролитическая диссоциация воды – причина гидролиза солей слабых кислот и (или) оснований. Степень электролитической диссоциации заметно возрастает при повышении температуры. Образование воды из элементов по реакции: Н2 + 1/2 О2 = Н2О -242 кДж/моль для пара -286 кДж/моль для жидкой воды -при низких температурах в отсутствии катализаторов происходит крайне медленно, но скорость реакции резко возрастает при повышении температуры, и при 5500 С она происходит со взрывом. При понижении давления и повышении температуры равновесие сдвигается влево. Под действием ультрафиолетового излучения происходит фотодиссоциация воды на ионы Н+ и ОН- .При пропускании паров воды через раскалённый уголь она разлагается и образуется так называемый водяной газ: Н2О + С = СО + Н2При повышенной температуре в присутствии катализатора вода реагирует с СО; СН4 и другими углеводородами, например: Н2О + СО = СО2 + Н2 Н2О + СН4 = СО + 3Н2 Эти реакции используют для промышленного получения водорода. Фосфор при нагревании с водой под давлением в присутствии катализатора окисляется в метафосфорную кислоту: 6Н2О + 3Р = 2НРО3 + 5Н2 Вода взаимодействует со многими металлами с образованием Н2 и сответствующего гидроксида. Со щелочными и щелочно-земельными металлами ( кроме Мg ) эта реакция протекает уже при комнатной температуре. Менее активные металлы разлагают воду при повышенной температуре, например, Мg и Zn – выше 1000 С; Fe – выше 6000 С :2Fe + 3h3O = Fe2O 3 + 3h3 При взаимодействии с водой многих оксидов образуются кислоты или основания. Вода может служить катализатором, например, щелочные металлы и водород реагируют с CI2 только в присутствии следов воды. Иногда вода – каталитический яд, например, для железного катализатора при синтезе Nh4. Способность молекул воды образовывать трёхмерные сетки водородных связей позволяет ей давать с инертными газами, углеводородами, СО2, CI2, (Ch3)2O, CHCI3 и многими другими веществами газовые гидраты. [2] Строение воды. Вода - уникальное вещество и все её аномальные свойства: высокая температура кипения, значительная растворяющая и диссоциирующая способность, малая теплопроводность, высокая теплота испарения и другие обусловлены строением её молекулы и пространственной структурой. У отдельно взятой молекулы воды есть качество, которое проявляется только в присутствии других молекул: способность образовывать водородные мостики между атомами кислорода двух оказавшихся рядом молекул, так, что атом водорода располагается на отрезке, соединяющем атомы кислорода. Свойство образовывать такие мостики обусловлено наличием особого межмолекулярного взаимодействия, в котором существенную роль играет атом водорода. Это взаимодействие называется водородной связью. [5] Каждая из присоединённых к данной молекул воды сама способна к присоединению дальнейших молекул. Этот процесс можно называть "полимеризацией". Если только одна из двух возможных связей участвует в присоединении следующей молекулы, а другая остаётся вакантной, то "полимеризация" приведёт к образованию либо зигзагообразной цепи, либо замкнутого кольца. Наименьшее кольцо, по-видимому, может состоять из четырёх молекул, но величина угла 90° делает водородные связи крайне напряжёнными. Практически ненапряжёнными должны быть пятизвенные кольца (угол 108° ), а шестизвенные (угол 120° ), также как и семизвенные - напряжённые. [2] Рассмотрение реальных структур гидратов показывает, что, действительно, наиболее устойчиво шестизвенное кольцо, находимое в структурах льдов. Плоские кольца являются привилегией клатратных гидратов, причём во всех известных структурах чаще всего встречаются плоские пятизвенные кольца из молекул воды. Они, как правило, чередуются во всех структурах клатратных гидратов с шестизвенными кольцами, очень редко с четырёхзвенными, а в одном случае - с плоским семизвенным. [4] В целом структура воды представляется как смесь всевозможных гидратных структур, которые могут в ней образоваться. В прикладном аспекте это, например, имеет важное значение для понимания действия лекарственных веществ. Как было показано Л. Полингом структурированная клатратная форма воды в межсинаптических образованиях мозга обеспечивает, с одной стороны, передачу импульсов с нейрона на нейрон, а, с другой стороны при попадании в эти участки наркозного вещества такая передача нарушается, то есть наблюдается явление наркоза. Гидратация некоторых структур мозга является одной из основ реализации действия наркотических анальгетиков (морфина). Биологическая роль воды. Биологическое значение воды можно показать на примере медузы. Если высушить медузу, то остаток составит 0,1% ее живой массы. Организм форели на 84% состоит из воды, лягушки на 80%. За 9 - 10 дней вода проходит через весь организм. Вода известна как хороший растворитель - она растворяет многие вещества. Кроме того, вода является той физико-химической средой, благодаря которой может осуществляться большинство реакций обмена веществ, обеспечивающих непрерывный процесс разрушения и восстановления живых тканей. Таким образом, вода является основной биологической жидкостью. Она не только инертная среда, она может также вступать в соединение с другими компонентами живой материи. Необходимо особо подчеркнуть это ее значение в биологическом круговороте. Одновременно вода играет роль в регулировании температуры организма и необходима для орошения его тканей. Взрослый человек должен выпивать около 2,5 л воды в сутки. За 60 лет своей жизни он выпивает целую цистерну пресной воды (50 т). Пить очень пресные воды вредно, ибо это вызывает выщелачивание кальция из организма, особенно детского. Жажда является естественной потребностью, ее вызывает повышение осмотического давления внутри организма. Это так называемая " тканевая жажда ", которую невозможно утолить, смазывая слизистую оболочку рта, эту потребность можно удовлетворить только введением жидкости в организм. В течение суток в пищеварительный канал поступает 9 -10 л жидкости, которая впитывается слизистой оболочкой. Из этого количества жидкости извне поступает только 2,5 л, а остальное количество распределяется следующим образом: 1,5 л слюны, столько же желудочного сока, 3 л кишечного сока, 0,7 л сока поджелудочной железы и 0,5 л желчи. В ухе у нас есть так называемый лабиринт, наполненный жидкостью, при ходьбе он регулирует равновесие нашего тела. Питьевой центр в нашем организме - это командный пункт, ведающий водным балансом человеческого тела. Он контролирует и регулирует беспрерывный обмен воды между отдельными органами. В среднем в сутки из организма человека выделяется 2 - 2,5 л воды. Чтобы поддержать водный баланс в организме необходимо вводить в него такое же количество воды. Отсюда, очевидно то огромное значение, которое имеет вода для всех живых существ. Функции воды: 1) Обеспечивает подержание структуры, 2) служит растворителем и средой для диффузии. 3) участвует в реакциях гидролиза 4) является средой, где происходит оплодотворение, 5) обеспечивает распространение семян, 6) обуславливает осмос, 7) участвует в фотосинтезе 8) транспортирует неорганические ионы и органические молекулы 9) обеспечивает прорастание семян 10) обеспечивает транспорт веществ 11) обеспечивает осморегуляцию12) способствует охлаждению 13) служит одним из компонентов смазки 14) служит опорой некоторым организмам 15) выполняет защитную функцию 16) способствует миграции организмов. Заключение. Вода - сок жизни. Такое определение дал воде Леонардо да Винчи. В воде зародилась жизнь, без воды не возможно вообще существование - ни растений, ни животных, ни людей. Академик Ферсман назвал воду " самым важным минералом на земле, без которого нет жизни ". Вода - это величайшая ценность не только для жителей пустыни, но и для каждого человека. Восточная поговорка гласит: "где вода, там жизнь. Где кончается вода, там кончается земля". Все живое вещество нашей планеты на 2/3 состоит из воды. Без воздуха жизнь возможна (анаэробные организмы), без воды – нет. Недаром академик Вернадский считал, что «вода и живое вещество – генетически связанные части организованности земной коры», а немецкий физиолог Эмиль Дюбуа писал: «Жизнь – это одушевленная вода». Без воды человек не может жить и 3 дней. Вода составляет 60% массы человека к 50 годам. Основная часть воды, около 70%, сосредоточена внутри клеток, а 30% - это внеклеточная вода, которая разделяется на две части: меньшая часть, около 7%, - это кровь и лимфа (она является фильтром крови), а большая часть – межтканевая, омывающая клетки. Без воды невозможно питание и развитие организма. Для жизни необходимо, чтобы питательные вещества попадали в кровь, которая разносит их по всему организму. Сама кровь, как показано, также содержит большое количество воды. В каждом органе нашего тела, в каждой живой клетке идут превращения одних веществ в другие. Из поступающей в организм пищи вырабатываются сложные вещества, необходимые для его нормальной работы. Все эти превращения возможны только тогда, когда различные вещества в организме находятся в растворе. Вот почему так много воды в нашем теле. [6] Среди многих полезных свойств воды едва ли не самым важным является ее способность утолять жажду. «Вода…- это живая кровь, которая создает жизнь там, где ее не было» (А.А.Карпинский). Человек очень быстро ощущает нарушение водного баланса. Если количество воды в человеческом организме уменьшится на 1-2% (0,5-1л) против нормы, человек испытывает жажду; при уменьшении на 5-8% (2-3 л) его кожа сморщивается, во рту пересыхает, сознание затемняется, могут появиться галлюцинации; потеря 10% влаги (~5 л) вызывает расстройство психического аппарата, нарушение глотательного рефлекса; при потере 14-15% (7-8 л) человек умирает. Таким образом, очевидно, что жизнедеятельность человеческого организма прочно связана с водой. Список литературы. Антонченко В. Я., Ильин В. В. Проблемные вопросы физики воды и гомеопатии. Вестник биофизической медицины, 1992 №1, с.11-13. Андреев В. Г. Влияние протонного обменного взаимодействия на строение молекулы воды и прочность водородной связи. Материалы V Международной конференции «Актуальные проблемы науки в России». — Кузнецк 2008, т.3 С. 58-62. Бышевский А. Ш., Терсенов О. А. Биохимия для врача, Екатеринбург: изд. "Уральский рабочий", 1994. - 378 с. Гидробионты в самоочищении вод и биогенной миграции элементов. — М.: МАКС-Пресс. 2008. 200 с. Предисловие члена-корр. РАН В. В. Малахова. (Серия: Наука. Образование. Инновации. Выпуск 9). Дерпгольц В. Ф. Вода во вселенной. - Л.: "Недра", 2000. – 287 с. Коробкин В. И., Передельский Л. В. Экология. Учебное пособие для вузов. - Ростов /на/Дону. Феникс, 2005. – 423 с. О некоторых вопросах поддержания качества воды и её самоочищения // Водные ресурсы. 2005. т. 32. № 3. С. 337—347. http://www.studfiles.ru/preview/5694910/page:6/weburok.com
Реферат на тему "Вода и её биологическое значение" страница 2
Состав воды. Что собой вообще представляет вода? На этот вопрос можно ответить, лишь разложив воду на её составные части, производя её анализ. При разложении воды электрическим током образуются газы: водород – 2 объема и кислород 1 – объем. Зная, что 1 л кислорода при нормальных условиях имеет массу - 1,429 г, а 1 л водорода - 0,089 г, можно высчитать массовые отношения выделившихся газов: (0,089*2) : 1,429 =1:8 . Так как в молекуле воды не может быть меньше одного атома кислорода (16 а.е.м.), а простейшее массовое отношение водорода к кислороду равно 1: 8 то в молекуле воды должно быть 2 атома водорода ( 2 а.е.м.). Следовательно, формула воды Н2О. Наряду с электролизом есть и другие возможности разложения воды. В большинстве случаев это достигается путем реакции восстановления , при которой от воды действием сильного восстановителя отнимается кислород, а водород выделяется в элементарном виде. И так, при установлении качественного и количественного состава вещества и последующего вывода химических формул , обычно применяют 2 способа: разложение сложного вещества на простые и получение его из простых веществ. Рассматривая химические и физические свойства воды, ученые пришли к выводу, что они обусловлены главным образом малыми размерами молекул воды, их полярностью и способностью соединяться друг с другом водородными связями. На основе этой особенности воды, и вникая в важность биологических процессов, рассмотрим следующие свойства.
Вода -растворитель. Вода - является универсальным растворителем ряда неорганических соединений и органических веществ, в среде которого протекают все элементарные акты жизнедеятельности. Это качество объясняется особым строением молекулы воды. Молекулы сильно поляризованы, благодаря чему легко входят во взаимодействие с молекулами других веществ. Именно свойство сильного растворителя затрудняет получение абсолютно химически чистой воды. При помощи воды происходят основные биохимические превращения. Большая часть химических реакций протекает в водных растворах. К примеру, в основу современной классификации витаминов положена их способность растворяться в воде (В,С,РР). В воде растворяются газы, жидкости и твердые тела. Присущие воде свойства растворителя означают также, что вода служит средой для транспорта различных веществ. Эту роль она выполняет в крови, в лимфатической и экскреторной системах, в пищеварительном тракте и во флоэме и ксилеме растений. Молекулы растворяющегося вещества , испытывая притяжение со стороны молекул воды , отрываются от поверхности вещества и распределяются по всему объему жидкости. Растворение многих веществ в воде часто сопровождается охлаждением образующегося раствора. Это наблюдается в случаях растворения хлористого натрия, калийной селитры и других веществ. Понижение температуры объясняют затратой энергии, необходимой для раздробления вещества до мельчайших частиц ( молекул или ионов) и распределения их по всему объему жидкости. При растворении других веществ, например, едкого натра, едкого кали, обнаруживают значительное разогревание раствора. Следовательно, в этих случаях, помимо растворения ,идет какой-то процесс, сопровождающийся выделением теплоты. Великий химик Д.И.Менделеев разработал теорию растворов, согласно которой растворение является процессом не только физическим, во многих случаях его надо рассматривать и как химическое взаимодействие растворяющегося вещества с водой, сопровождающееся образованием так называемых гидратов. Одним из доказательств справедливости представлений Д.Т.Менделеева о растворах является существование кристаллогидратов, т.е. веществ, содержащих кристаллизационную воду. К ним относят медный купорос СuSO4 * 5h3O, железный купорос Fe SO4 * 7h3O, гипс CaSO4 * 2h3O и др. Физические и химические свойства воды. Уникальные свойства воды интересуют людей с древнейших времен. Это единственное вещество на Земле, которое при нормальных для человека условиях может находиться сразу в трех агрегатных состояниях - жидком, твердом и газообразном. Чистая вода не имеет запаха. Она бесцветна и прозрачна в тонком слое. В слоях значительной толщины она ярко-голубого цвета. Реальные физические свойства воды резко отличаются от свойств других гидридов (соединений с водородом). Проще говоря, в отличие от других веществ, свойства воды нельзя вычислить на основании ее положения в периодической таблице химических элементов Менделеева. Теоретически, исходя из своего положения в таблице, вода - это есть гидрид кислорода - должна переходить в твердую фазу, превращаться в лед. Вода замерзает при 0оС и кипит при 100 оС (давление 1 атм), наибольшую плотность имеет при +4о С ,т.е.1 л воды при +4 о С весит больше, чем 1 л воды при более высокой и более низкой температурах. При замерзании вода расширяется и из 92 объёмов её получается 100 объемов льда. Таким образом , лёд легче воды (при замерзании плотность воды уменьшается, поэтому лед всплывает); удельный вес его равен 0,92. Благодаря этому лед остается на поверхности водоёма и предотвращает промерзание воды до дна. Благодаря этому уникальному свойству воды озера и реки не промерзают до дна, и водные обитатели могут пережить зиму. Уменьшение плотности льда происходит вследствие увеличения объема. Именно поэтому замерзающая вода рвет водопроводные трубы.Вода может быть переохлаждена до отрицательных температур без перехода в твердое состояние. Однако при малейшем сотрясении или попадании каких-либо частиц переохлажденная вода быстро превращается в лед. Посторонние частицы, пузырьки воздуха в этом случае становятся центрами кристаллизации. Молекулы воды очень устойчивы. Лишь при температуре выше 1000о С водяной пар начинает распадаться на водород и кислород. Тем не менее, вода является химически активным веществом. Она легко вступает в химическое взаимодействие со многими другими веществами. Вода служит катализатором для многих химических процессов, в частности реакций горения некоторых веществ.
infourok.ru
Реферат по теме «Вода и её биологическое значение»
ООО Учебный центр «ПРОФЕССИОНАЛ» Реферат по дисциплине: « Общая и теоретическая химия » По теме: «Вода и её биологическое значение» Исполнитель: Речкунова Ольга Васильевна Москва 2017год Содержание Введение 3 Вода – самое удивительное вещество на Земле 4 Строение воды 5 Биологическое значение воды 6 Вода - ценнейший природный ресурс 8 Вода и здоровье 10 Заключение 15 Список литературы 16 Введение Никого из нас не удивляет дождь или падающий снег, гладь плавно текущей реки или озера. Другое дело – огромные просторы морей и океанов, водопады, гигантские ледники, сползающие с заоблачных высот, струи гейзеров, подобно фонтанам бьющие из-под земли. От этих красот у любого захватит дух. Но редко кто задумывается над тем, откуда взялись моря или реки, дождь или снег, каковы свойства воды, предстающей в таком разнообразном виде. Вода – самая загадочная жидкость на Земле. Певцы древних степных народов издавна воспевали её, поэты посвящали ей удивительные строки. Даже о капле воды написано множество страниц. А ученые по сей день, как и сотни лет назад, не могут дать точного ответа на, казалось бы, несложный вопрос: что такое вода? «Вода, у тебя нет ни цвета, ни вкуса, ни запаха, тебя невозможно описать, тобой наслаждаются, не ведая, что ты такое. Нельзя сказать, что необходимо для жизни: ты сама жизнь.Ты исполняешь нас с радостью, которую не объяснишь нашими чувствами.С тобой возвращаются к нам силы, с которыми мы уже простились.По твоей милости в нас вновь начинают бурлить высохшие родники нашего сердца.» (А. де Сент-Экзюпери. Планета людей) Я выбрала эту тему для реферата потому что – это самая актуальная тема, так как вода это самое важное вещество на Земле без которого не может существовать ни один живой организм и не могут протекать никакие биологические, химические реакции, и технологические процессы. Вода – одно из самых распространённых веществ в природе (гидросфера занимает 71 % поверхности Земли). Воде принадлежит важнейшая роль в геологии, истории планеты. Без воды невозможно существование живых организмов. Дело в том, что тело человека почти на 63% - 68% состоит из воды. Практически все биохимические реакции в каждой живой клетке – это реакции в водных растворах… В растворах же (преимущественно водных) протекает большинство технологических процессов на предприятиях химической промышленности, в производстве лекарственных препаратов и пищевых продуктов. И в металлургии вода чрезвычайно важна, причём не только для охлаждения. Не случайно гидрометаллургия – извлечение металлов из руд и концентратов с помощью растворов различных реагентов – стала важной отраслью промышленности. Вода – самое удивительное вещество на Земле Вода – вещество привычное и необычное. Известный советский учёный академик И. В. Петрянов свою научно-популярную книгу о воде назвал "самое необыкновенное вещество в мире". А "Занимательная физиология", написанная доктором биологических наук Б. Ф. Сергеевым, начинается с главы о воде – "Вещество, которое создало нашу планету". Учёные абсолютно правы: нет на Земле вещества, более важного для нас, чем обыкновенная вода, и в тоже время не существует другого такого вещества, в свойствах которого было бы столько противоречий и аномалий, сколько в её свойствах. Почти? поверхности нашей планеты занято океанами и морями. Твёрдой водой – снегом и льдом – покрыто 20% суши. От воды зависит климат планеты.Геофизики утверждают, что Земля давно бы остыла и превратилась в безжизненный кусок камня, если бы не вода. У неё очень большая теплоёмкость. Нагреваясь, она поглощает тепло; остывая, отдаёт его. Земная вода и поглощает, и возвращает очень много тепла и тем самым "выравнивает" климат. А от космического холода предохраняет Землю те молекулы воды, которые рассеяны в атмосфере – в облаках и в виде паров… без воды обойтись нельзя – это самое важное вещество на Земле. Строение воды Вода - уникальное вещество и все её аномальные свойства: высокая температура кипения, значительная растворяющая и диссоциирующая способность, малая теплопроводность, высокая теплота испарения и другие обусловлены строением её молекулы и пространственной структурой. У отдельно взятой молекулы воды есть качество, которое проявляется только в присутствии других молекул: способность образовывать водородные мостики между атомами кислорода двух оказавшихся рядом молекул, так, что атом водорода располагается на отрезке, соединяющем атомы кислорода. Свойство образовывать такие мостики обусловлено наличием особого межмолекулярного взаимодействия, в котором существенную роль играет атом водорода. Это взаимодействие называется водородной связью. Каждая из присоединённых к данной молекул воды сама способна к присоединению дальнейших молекул. Этот процесс можно называть "полимеризацией". Если только одна из двух возможных связей участвует в присоединении следующей молекулы, а другая остаётся вакантной, то "полимеризация" приведёт к образованию либо зигзагообразной цепи, либо замкнутого кольца. Наименьшее кольцо, по-видимому, может состоять из четырёх молекул, но величина угла 90° делает водородные связи крайне напряжёнными. Практически ненапряжёнными должны быть пятизвенные кольца (угол 108° ), а шестизвенные (угол 120° ), также как и семизвенные - напряжённые. Рассмотрение реальных структур гидратов показывает, что, действительно, наиболее устойчиво шестизвенное кольцо, находимое в структурах льдов. Плоские кольца являются привилегией клатратных гидратов, причём во всех известных структурах чаще всего встречаются плоские пятизвенные кольца из молекул воды. Они, как правило, чередуются во всех структурах клатратных гидратов с шестизвенными кольцами, очень редко с четырёхзвенными, а в одном случае - с плоским семизвенным. В целом структура воды представляется как смесь всевозможных гидратных структур, которые могут в ней образоваться. В прикладном аспекте это, например, имеет важное значение для понимания действия лекарственных веществ. Как было показано Л. Полингом структурированная клатратная форма воды в межсинаптических образованиях мозга обеспечивает, с одной стороны, передачу импульсов с нейрона на нейрон, а, с другой стороны при попадании в эти участки наркозного вещества такая передача нарушается, то есть наблюдается явление наркоза. Гидратация некоторых структур мозга является одной из основ реализации действия наркотических анальгетиков (морфина). Биологическое значение воды Биологическое значение воды можно показать на примере медузы. Если высушить медузу, то остаток составит 0,1% ее живой массы. Организм форели на 84% состоит из воды, лягушки на 80%. За 9 - 10 дней вода проходит через весь организм. Вода известна как хороший растворитель - она растворяет многие вещества. Кроме того, вода является той физико-химической средой, благодаря которой может осуществляться большинство реакций обмена веществ, обеспечивающих непрерывный процесс разрушения и восстановления живых тканей. Таким образом, вода является основной биологической жидкостью. Она не только инертная среда, она может также вступать в соединение с другими компонентами живой материи. Необходимо особо подчеркнуть это ее значение в биологическом круговороте. Одновременно вода играет роль в регулировании температуры организма и необходима для орошения его тканей. Взрослый человек должен выпивать около 2,5 л воды в сутки. За 60 лет своей жизни он выпивает целую цистерну пресной воды (50 т). Пить очень пресные воды вредно, ибо это вызывает выщелачивание кальция из организма, особенно детского. Жажда является естественной потребностью, ее вызывает повышение осмотического давления внутри организма. Это так называемая ” тканевая жажда “, которую невозможно утолить, смазывая слизистую оболочку рта, эту потребность можно удовлетворить только введением жидкости в организм. В течение суток в пищеварительный канал поступает 9 -10 л жидкости, которая впитывается слизистой оболочкой. Из этого количества жидкости извне поступает только 2,5 л, а остальное количество распределяется следующим образом: 1,5 л слюны, столько же желудочного сока, 3 л кишечного сока, 0,7 л сока поджелудочной железы и 0,5 л желчи. В ухе у нас есть так называемый лабиринт, наполненный жидкостью, при ходьбе он регулирует равновесие нашего тела. Питьевой центр в нашем организме - это командный пункт, ведающий водным балансом человеческого тела. Он контролирует и регулирует беспрерывный обмен воды между отдельными органами. В среднем в сутки из организма человека выделяется 2 - 2,5 л воды. Чтобы поддержать водный баланс в организме необходимо вводить в него такое же количество воды. Отсюда, очевидно, то огромное значение, которое имеет вода для всех живых существ. Чтобы ответить на этот вопрос, обратимся к продуктам, которые мы повседневно употребляем. Потребность организма в воде удовлетворяется приемом пищи и напитков. Некоторая доля воды образуется в организме за счет сгорания водорода, т. е. соединения его с вдыхаемым кислородом. Что касается образования кислорода, то уже определенно известно, что кислород атмосферы - продукт разложения воды, а не углекислого газа в процессе фотосинтеза, производимого растениями. Таким образом, без воды не может быть и дыхания - первого и непременного условия жизни. Больше всего воды в грибах, овощах и фруктах - почти 90%. Когда мы съедаем килограмм овощей, наш организм получает столько жидкости, сколько дает литр выпитого молока. Ученые считают молоко лучшим продуктом питания. В нем есть все, что нужно человеческому организму: сахар и белок, жир, минеральные соли и вода. Если взвесить твердые вещества, содержащиеся в молоке, то окажется что в нем 85 - 90% воды. Но есть растение, которое не менее ценно, чем молоко, - это соевые бобы. Смолотые и сваренные соевые бобы дают соевое молоко, из которого делают масло, потому что в них только 10% воды, тогда как масло коровье содержит 14% воды. В коровьем мясе находится столько воды, сколько в нашем собственном теле. Следовательно, в любом продукте питания содержится то или иное количество воды и, таким образом, мы убеждаемся в том, что воду можно есть. Вода - ценнейший природный ресурс Вода - ценнейший природный ресурс. Она играет исключительную роль в процессах обмена веществ, составляющих основу жизни. Огромное значение вода имеет в промышленном и сельскохозяйственном производстве. Общеизвестна необходимость ее для бытовых потребностей человека, всех растений и животных. Для многих живых существ она служит средой обитания. Рост городов, бурное развитие промышленности, интенсификация сельского хозяйства, значительное расширение площадей орошаемых земель, улучшение культурно-бытовых условий и ряд других факторов все больше усложняет проблемы обеспечения водой.Потребности в воде огромны и ежегодно возрастают. Ежегодный расход воды на земном шаре по всем видам водоснабжения составляет 3300-3500 км3. При этом 70% всего водопотребления используется в сельском хозяйстве.Много воды потребляют химическая и целлюлозно-бумажная промышленность, черная и цветная металлургия. Развитие энергетики также приводит к резкому увеличению потребности в воде. Значительное кол-во воды расходуется для потребностей отрасли животноводства, а также на бытовые потребности населения. Большая часть воды после ее использования для хозяйственно-бытовых нужд возвращается в реки в виде сточных вод. Дефицит пресной воды уже сейчас становится мировой проблемой. Все более возрастающие потребности промышленности и сельского хозяйства в воде заставляют все страны, ученых мира искать разнообразные средства для решения этой проблемы. На современном этапе определяются такие направления рационального использования водных ресурсов: более полное использование и расширенное воспроизводство ресурсов пресных вод; разработка новых технологических процессов, позволяющих предотвратить загрязнение водоемов и свести к минимуму потребление свежей воды. Ученые подсчитали, что 97.5% всех запасов воды на планете Земля приходится на соленые воды морей и океанов. Иными словами, пресная вода составляет только 2.5% мировых запасов.Если учесть, что 75% пресной воды “заморожено” в горных ледниках и полярных шапках, еще 24% находится под землей в виде грунтовых вод, а еще 0.5% “рассредоточено” в почве в виде влаги, то получается, что на наиболее доступный и дешевый источники воды — реки, озера и прочие наземные водоемы приходится чуть больше 0.01% мировых запасов воды.Принимая во внимание то значение, которое вода имеет для жизнедеятельности человека и всего живого на Земле, приведенные цифры наглядно подтверждают сакраментальный тезис о том, что вода — одно из самых драгоценных сокровищ нашей планеты. Вода и здоровье Проблема чистой воды стала одной из важнейших в наше время. Научный прогресс, значительно облегчив нашу жизнь, породил другую проблему – загрязнения окружающей среды. Попить воды просто из–под крана сегодня решится далеко не каждый и правильно сделает. Конечно, все может обойтись и без фатальных последствий, но это уже очень напоминает игру в «русскую рулетку». Итак, что же за опасности подстерегают нас в воде из-под крана? К наиболее распространенным загрязнениям воды можно отнести железо, марганец, сульфиды, фториды, соли кальция и магния, различные органические соединения. Присутствие железа в воде здоровью не угрожает, однако, при повышении содержания железа в воде (более 0,3 мг/л) в виде гидрокарбонатов, сульфатов, хлоридов органических комплексных соединений придает воде неприятную красно – коричневую окраску и вызывает ухудшение вкуса. При длительном употреблении внутрь воды с содержанием железа выше нормы, человек рискует приобрести различные заболевания печени, крови, аллергические реакции, нарушения репродуктивной функции. Повышенное содержание марганца приводит к анемии, нарушению функционального состояния центральной нервной системы. Некоторые врачи говорят о мутагенном влиянии на человека повышенного содержания марганца в воде, при беременности увеличивается вероятность патогенных родов, мертворождения. При повышенном содержании солей серной и соляной кислот (сульфаты и хлориды) вода приобретает неприятный соленый или горько – соленый привкус. Употребление такой воды приводит к нарушениям работы желудочно-кишечного тракта. Вода, в которой содержится более 350 мг хлоридов, а сульфатов более 500 мг на литр, считается неблагоприятной для здоровья. Содержание в воде катионов кальция и магния придает воде так называемую жесткость. Оптимальный уровень жесткости – 3,0 – 3,5 мг экв/л ( = моль/ метр кубический). Постоянное употребление воды с повышенной жесткостью ведет к накоплению солей в организме, а в конечном итоге к заболеваниям суставов (артриты, полиартриты), образованию камней в почках, желчном и мочевом пузырях. Повышенное содержание фтора приводит к крапчатости эмали зубов, увеличивается выведение кальция с мочой, уменьшается содержание кальция и фосфора в костях (приводит к их хрупкости), подавляется иммунная реактивность, происходят морфофункциональные изменения в почках и печени. Однако, низкое содержание фтора тоже не слишком хорошо - вода отвечает за состояние зубов человека. От того, сколько фтора в ней содержится, зависит частота заболевания кариесом. Считается, что фторирование воды способствует профилактике кариеса, особенно для детей. Для того, чтобы вода не нанесла вред, содержание фтора в ней должно быть в пределах 0,7 – 1,5 мг/л.Наличие в воде сульфидов (сероводорода) придает воде неприятный запах и вызывает раздражение кожи. Мышьяк вызывает расстройства центральной и периферической нервной системы, с последующим развитием полиневритов. Длительное поступление стронция в организм в больших количествах (более 7 мг/л) приводит к функциональным изменениям печени.Алюминий, накапливаясь в организме, может стать причиной старческого слабоумия, повышенной возбудимости, неврологические изменения, связанные с болезнью Паркинсона. У детей алюминий вызывает нарушения моторных реакций, анемию, головные боли, заболевание почек, печени, колиты. Это все так называемые химические загрязнения. А ведь есть еще и органическое. Это бактерии, которые вызывают различные заболевания. Например, через загрязненную воду передаются такие болезни, как брюшной тиф, дизентерия, водная лихорадка, полиомиелит. Да и элементарное расстройство желудка – не самая приятная вещь. К счастью, бактерии погибают при простом кипячении. В течение многих лет для обеззараживания воды применялся хлор, считавшийся самым эффективным средством. Однако хлор не только уничтожает бактерии, но и вступает в химические реакции с другими веществами, образуя при этом не менее опасные для здоровья соединения. Именно эти хлорорганические соединения (образующиеся при кипячении хлорированной воды, в частности) могут приводить к хроническим нефритам и гепатитам, токсикозам беременности, развитию диатеза у детей. Кроме того, хлор, как более активный элемент, вытесняет из организма йод, ослабляя тем самым функциональное состояние щитовидной железы. И это еще не весь перечень веществ, который может оказаться в вашем стакане. Список можно продолжать до бесконечности. Вы еще не передумали пить воду из–под крана? Вода - сок жизни. Такое определение дал воде Леонардо да Винчи. В воде зародилась жизнь, без воды не возможно вообще существование - ни растений, ни животных, ни людей. Академик Ферсман назвал воду ” самым важным минералом на земле, без которого нет жизни “. Вода - это величайшая ценность не только для жителей пустыни, но и для каждого человека. Восточная поговорка гласит: “где вода, там жизнь. Где кончается вода, там кончается земля”. Все живое вещество нашей планеты на 2/3 состоит из воды. Без воздуха жизнь возможна (анаэробные организмы), без воды – нет. Недаром академик Вернадский считал, что «вода и живое вещество – генетически связанные части организованности земной коры», а немецкий физиолог Эмиль Дюбуа писал: «Жизнь – это одушевленная вода». Без воды человек не может жить и 3 дней. Вода составляет 60% массы человека к 50 годам. Основная часть воды, около 70%, сосредоточена внутри клеток, а 30% - это внеклеточная вода, которая разделяется на две части: меньшая часть, около 7%, - это кровь и лимфа (она является фильтром крови), а большая часть – межтканевая, омывающая клетки. Без воды невозможно питание и развитие организма. Для жизни необходимо, чтобы питательные вещества попадали в кровь, которая разносит их по всему организму. Сама кровь, как показано, также содержит большое количество воды. В каждом органе нашего тела, в каждой живой клетке идут превращения одних веществ в другие. Из поступающей в организм пищи вырабатываются сложные вещества, необходимые для его нормальной работы. Все эти превращения возможны только тогда, когда различные вещества в организме находятся в растворе. Вот почему так много воды в нашем теле. Среди многих полезных свойств воды едва ли не самым важным является ее способность утолять жажду. «Вода…- это живая кровь, которая создает жизнь там, где ее не было» (А.А.Карпинский). Человек очень быстро ощущает нарушение водного баланса. Если количество воды в человеческом организме уменьшится на 1-2% (0,5-1л) против нормы, человек испытывает жажду; при уменьшении на 5-8% (2-3 л) его кожа сморщивается, во рту пересыхает, сознание затемняется, могут появиться галлюцинации; потеря 10% влаги (~5 л) вызывает расстройство психического аппарата, нарушение глотательного рефлекса; при потере 14-15% (7-8 л) человек умирает. Говоря о чудесных свойствах воды и ее незаменимости в живом организме, нельзя не остановиться на замечательной способности самого организма регулировать водный баланс. Как известно, по норме человек потребляет 2,5 л воды в сутки. Эта вода является жизненно необходимой для существования человека – она растворяет питательные вещества для их проникания в клетку, участвует в химических процессах при пищеварении, а также вымывает продукты жизнедеятельности и уходит из организма через почки и кожу, унося с собой вредные вещества. Если поступление воды в организм прекратилось, она продолжает выделяться через почки и кожу. При этом постоянно происходит сгущение крови. Для того чтобы прекратить дальнейшее ее сгущение, необходимо вызвать чувство жажды в «руководстве» организма. Сгущенная кровь, дойдя до головного мозга, раздражает центр, регулирующий водно-солевой баланс, оттуда поступает сигнал в кору головного мозга приблизительно следующего содержания: «Уважаемый хозяин! Надо выпить воды». Если же нет возможности утолить жажду, из названного выше центра поступает сигнал в маленькую железу, находящуюся под головным мозгом (гипофиз). На сигнал «сверху» гипофиз выделяет гормон, который кровью доставляется в почки и приказывает им в целях экономии сократить выделение воды с мочой. Такое состояние организма позволяет выиграть некоторое время, необходимое для поиска воды. Таким образом, очевидно, что жизнедеятельность человеческого организма прочно связана с водой. Заключение Вода - самое распространенное среди неорганических веществ на нашей планете. Она содержится практически везде: на земной поверхности и в её недрах, в мантии и в горных породах, в высоких слоях атмосферы и даже в космосе. Таким образом, вода – самая удивительная жидкость на Земле, свойства которой превосходят всякую фантазию. Уникальные свойства воды позволяют ей выполнять не менее уникальные биологические функции. Вода, такое привычное вещество обладает совершенно удивительными свойствами. Только благодаря этим свойствам воды стала возможна жизнь на Земле. При поиске жизни на других планетах один из важнейших вопросов – есть ли там достаточное количество воды. Уникальное значение воды для биологических систем обусловлено количественным содержанием ее в живых организмах. Вода участвует в регуляции температуры тела человека и поддержании кислотно-щелочного равновесия, кроме того, вода участвует во всех протекающих в организме химических реакциях. Нерациональное использование воды и ее возрастающее загрязнение становятся день ото дня все более и более серьезными проблемами, которые способны довести человечество до катастрофы. Жизненно необходимо осознание каждым человеком личной и социальной ответственности за сохранение водных ресурсов и овладение практическими способами сбережения и улучшения качества воды. Спаси себя, человече, Сыне, родимый, спаси! Чтоб реки текли, а не речи По нашей великой Руси! (М.Рудаков) Список литературы Бышевский А. Ш., Терсенов О. А. Биохимия для врача, Екатеринбург: изд. "Уральский рабочий", 1994. - 378 с. Грин Н., Стаут У., Тейлор Д. Биология, т. 1.: Пер. с англ. - М.: Мир, 1993. - 368 с. Габуда С. П. Связанная вода. Факты и гипотезы, Новосибирск: Наука, 1982. - 159 с. Зенин С. В. Водная среда как информационная матрица биологических процессов. В кн. Тезисы докладов 1 Международного симпозиума, Пущино, 1997, с. 12-13. КриксуновЕ.А., Пасечник В.В. “Экология. 10-11 класс”, “Дрофа”, 2000 Садовничая Л. П. с соавт. Биофизическая химия, К.: Вища школа, 1986. - 271 с. Сб. Структура и роль воды в живом организме, Л.: Изд. ЛГУ, 1966. - 208 с.schoolfiles.net
Реферат на тему "Вода и ее биологическое значение" страница 3
Хотя в целом молекула воды электронейтральна, она имеет два полюса, заряженных противоположно. На кислородном конце вследствие неполного уравновешивания электронов всегда возникает отрицательный заряд, а на водородном – положительный. Такие молекулы носят название активный диполь («ди» - два).
Однако электроны, входящие в состав атомов водорода, не удовлетворяются взаимодействием только со своим атомом кислорода, а стремятся также воздействовать на соседние кислородные атомы. Т.е. между собой диполи образуют спонтанные соединения – одна молекула воды отрицательно заряженным концом может притянуть к себе другую молекулу за ее положительный край. В результате молекулы воды соединяются еще и дополнительными связями, получившими название водородные. Ковалентные связи О – Н внутри молекулы отличаются устойчивостью, они не рвутся при переходах воды из одного состояния в другое: вода – пар – лед. Их разрушение требует больших энергетических затрат: электролиз, нагревание воды и т.п. В отличие от них водородные связи короткоживущие и гораздо менее прочные – они в несколько десятков раз слабее ковалентных связей. При таянии льда, снега, водородные связи в образующейся воде сохраняются только частично, а в водяном паре они все разорваны.
Несмотря на то, что в процессе теплового движения молекул водородные связи рвутся, взамен им тут же возникают новые. В результате молекулы Н2О в воде оказываются прочно связанными друг с другом и образуют характерную молекулярную конструкцию, которая достаточно устойчива к любым разрушающим воздействиям (тепловым, механическим, электрическим). По этой причине, например, необходимо затратить много тепла, чтобы превратить воду в пар. В связи с тем, что разрушение межмолекулярных водородных связей в воде требует дополнительных энергозатрат, h3O имеет более высокую температуру кипения – 100°C – по сравнению с прочими водородными соединениями элементов подгруппы кислорода (h3S, h3Se, h3Te).
Высокая растворяющая способность воды обусловлена также наличием водородных связей, поскольку растворимость в значительной степени зависит от способности соединения давать водородные связи с растворителем. В результате содержащие ОН – группы такие вещества, как сахар, глюкоза, спирты, карбоновые кислоты, как правило, хорошо растворимы в воде.
В ходе многочисленных исследований было выявлено удивительное обстоятельство: внутренняя структура воды очень близка структуре льда. Благодаря наличию водородных связей каждая молекула h3O во льду окружена четырьмя ближайшими к ней молекулами, находящимися на одинаковых расстояниях от неё, и размещённых в вершинах правильного тетраэдра. Структура льда представляет собой ажурный решетчатый каркас. Ажурная кристаллическая структура льда приводит к тому, что его плотность ниже плотности воды при той же температуре.
В воде, так же, как и во льду, каждая молекула h3O окружена четырьмя другими молекулами воды. Между ними имеются пустоты, превосходящие по размерам сами молекулы. Чем их больше, тем меньше плотность льда и воды. Ажурная решетчатая структура воды сохраняется до 30-40°С. При расплавлении льда количество пустот уменьшается, и плотность воды возрастает. Тепловые колебания приводят к изгибу и разрыву водородных связей. Сошедшие с равновесных положений молекулы воды попадают в соседние пустоты структуры и на некоторое время задерживаются там. Это ведет к образованию дефектов решетки, наличие которых обусловливает аномальные свойства воды.
infourok.ru


