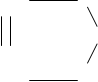 HCC ==O
HCC ==OСодержание
Роль катализа в промышленности и экологии.
Определение катализа.
Селективность.
Общие представления о понятии «механизм химической реакции».
Классификация каталитических систем по фазам.
Классификация катализаторов по типам реакций.
Адсорбция.
Основные требования к промышленным катализаторам.
Роль катализа в промышленности и экологии
Основным потребителем катализаторов являются нефтепереработка, нефтехимия, химия и экология.
Маркет катализаторов в год составляет около 700 тысяч тонн. Примерно половина – катализаторы каталитического крекинга. Потребности химической промышленности – около одной трети, экологии – десятая часть.
Если средняя стоимость катализаторов – 4$ за килограмм, а средняя доля в себестоимости – 0,3%, то с помощью катализаторов производят продуктов на сумму не менее 1000 миллиардов $.
Катализ позволяет экономить сырье и энергию, а также не загрязнять окружающую среду.
Определение катализа
Катализ – это ускорение одного или нескольких возможных направлений превращения химических веществ.
Термодинамика дает ответ на вопрос, как далеко может пройти конкретная химическая реакция. Этот ответ не зависит от пути реакции. На вопрос, с какой скоростью будет достигаться это конечное состояние, отвечает кинетика.
Скорость зависит от пути реакции!
Например, смесь 1,5 % бутана с воздухом при бесконечном по времени их контакте при температуре 4500С превратится в смесь диоксида углерода, воды и остатка воздуха. В присутствии катализатора, состоящего из смеси V, P и O, в течение 2-3 секунд примерно половина бутан окислится в малеиновый ангидрид.
Катализаторы ускоряют один или несколько термодинамически возможных превращений участников реакции, создавая, как правило, новый, энергетически более выгодный путь.
СН3 ---СН2 ---СН2 — СН3 + 3,5 О2 ==
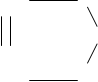 HCC ==O
HCC ==O
O
HCC ==O
Новый путь появляется за счет того, что реагенты образуют химические (промежуточные) соединения с катализатором.
Селективность
Если превращения этих соединений протекает через более низкие энергетические барьеры, то каталитический путь может оказаться быстрее, чем некаталитический.
Путь, по которому превращаются или образуются интересующие нас вещества, часто называю механизмом.
Что значит «более низкие энергетические барьеры»?

Число соударений молекул газа между собой при атмосферном давлении в 1 см3 в 1 сек из кинетической теории газов равно примерно 1030.
Число ударов молекул газа при атмосферном давлении об 1 см2 поверхности в 1 сек равно примерно 1023. Если внешняя поверхность гранул катализатора в 1 см3 равна 100 см2, то для того, чтобы каталитический путь был более быстрым, необходимо, чтобы Екат было бы примерно на 60 кДж/моль меньше, чем Енк .
| Реакция | Е нк, кДж/моль | Е кат, кДж/моль | Кат-р |
2HJ ® h3 + J2 2N2 O ® 2N2 + O2 | 184 245 | 105 59 121 134 | Au Pt Au Pt |
Общие представления о понятии «механизм химической реакции»
Лимитирующая стадия.
Схемы механизма – химическая, физическая и кинетическая.
 |
Микрокинетическая модель паровой конверсии метана.
 |

Классификация каталитических систем по фазам.
| Катализатор | Реактанты |
| Гомогенная | |
газообразный жидкий | газообразные жидкие |
| Гетерогенная | |
жидкий твердый твердый твердый твердый | газообразные жидкие газообразные жидкие + газообразные твердые |
Классификация катализаторов по типам реакций.
| Реакции | Катализатор | |
Металлы Полупроводниковые оксиды и сульфиды Изоляторы Кислоты | Гидрирование Дегидрирование Гидрогенолиз Алкилирование Окисление Окисление Дегидрирование Гидродесульфирование Дегидрирование Алкилирование Гидратация Крекинг | Ni, Cu, Pd, Pt, Fe Ni, Cu, Pd, Pt Pd, Pt Ni, Cu Cu, Ag Bi-Mo-O, Fe-Mo-O, Fe-Sn-O, V-P-O Cr-O, Fe-Cr-O Ni-Mo-S, Co-Mo-S Al-O, Si-O, Mg-O h3 SO4 h4 PO4 Цеолиты |
Адсорбция
Роль адсорбции в катализе. Физическая и химическая адсорбции. Их характерные различия и общие черты
· зависимость от природы адсорбента,
· от температуры,
· покрытия поверхности,
· тепловой эффект,
· влияние на электропроводность.
Энергетическая диаграмма при химической адсорбции.
Теплота и термодинамика адсорбции.
Изотермы адсорбции.
Модель идеальной поверхности Ленгмюра.
Вывод изотермы Ленгмюра.

Физический смысл констант.
Вид изотермы при устремлении Р к нулю или бесконечности.
Связь между энергиями активации стадий адсорбции и десорбции и теплотой адсорбции.
Модели биографической и индуцированной неоднороднных поверхностей.
Вывод изотермы Темкина.

Физический смысл констант.
Вид изотермы при устремлении Р к нулю или бесконечности. Область средних покрытий.
Основные требования к промышленным катализаторам
Химические требования
· термическая стабильность,
· стойкость к отравлению «ядами»,
· легкая регенерируемость,
· высокая избирательность,
· активность при доступных температурах и давлениях.
Механические требования
· прочность,
· малое гидравлическое сопротивление,
· однородность,
· оптимальная пористая структура.
www.ronl.ru
Реферат на тему:
Ката́лиз (греч. κατάλυσις восходит к καταλύειν — разрушение) — избирательное ускорение одного из возможных термодинамически разрешенных направлений химической реакции под действием катализатора(ов), который многократно вступает в промежуточное химическое взаимодействие с участниками реакции и восстанавливает свой химический состав после каждого цикла промежуточных химических взаимодействий.[1]
Термин «катализ» был введён в 1835 году шведским учёным Йёнсом Якобом Берцелиусом.
Явление катализа распространено в природе (большинство процессов, происходящих в живых организмах, являются каталитическими) и широко используется в технике (в нефтепереработке и нефтехимии, в производстве серной кислоты, аммиака, азотной кислоты и др.). Большая часть всех промышленных реакций — это каталитические.
Катализатор изменяет механизм реакции на энергетически более выгодный, то есть снижает энергию активации. Катализатор образует с молекулой одного из реагентов промежуточное соединение, в котором ослаблены химические связи. Это облегчает его реакцию со вторым реагентом. Важно отметить, что катализаторы ускоряют обратимые реакции, как в прямом, так и в обратном направлениях.
Катализ может быть положительным (когда скорость реакции увеличивается) и отрицательным (когда скорость реакции уменьшается). Для обозначения отрицательного катализа часто используют термин ингибирование.
Катализ бывает гомогенным и гетерогенным (контактным). В гомогенном катализе катализатор состоит в той же фазе, что и реактивы реакции, в то время, как гетерогенные катализаторы отличаются фазой.
Примером гомогенного катализа является разложение пероксида водорода в присутствии ионов йода. Реакция протекает в две стадии:
h3О2 + I → h3О + IO h3О2 + IO → h3О + О2 + IПри гомогенном катализе действие катализатора связано с тем, что он вступает во взаимодействие с реагирующими веществами с образованием промежуточных соединений, это приводит к снижению энергии активации.
При гетерогенном катализе ускорение процесса обычно происходит на поверхности твердого тела — катализатора, поэтому активность катализатора зависит от величины и свойств его поверхности. На практике катализатор обычно наносят на твердый пористый носитель.
Механизм гетерогенного катализа сложнее, чем у гомогенного. Механизм гетерогенного катализа включает пять стадий, причем все они обратимы.
Примером гетерогенного катализа является окисление SO2 в SO3 на катализаторе V2O5 при производстве серной кислоты (контактный метод).
Химия катализа изучает вещества, изменяющие скорость химических реакций. Вещества, замедляющие реакции, называются ингибиторами. Ферменты — это биологические катализаторы. Катализатор не находится в стехиометрических отношениях с продуктами и регенерируется после каждого цикла превращения реагентов в продукты. Несмотря на появление новых способов активации молекул (плазмохимия, радиационное и лазерное воздействия и другие), катализ − основа химических производств (относительная доля каталитических процессов составляет 80-90 %).
Реакция, накормившая человечество (решение проблемы связанного азота) — цикл Габера-Боша. Аммиак получают с катализатором — пористым железом. Протекает при Р = 30 МПа и Т = 420—500 °C
3Н2 + N2 = 2Nh4
Водород для синтеза Nh4 получают путем двух последовательных каталитических процессов: конверсии СН4(СН4 + Н2О → СО + 3Н2) на Ni−катализаторах и конверсии образующегося оксида углерода (СО + Н2О → СО2 + Н2). Для достижения высоких степеней превращения последнюю реакцию осуществляют в две стадии: высокотемпературная (315—480 °C) — на Fe−Cr−оксидных катализаторах и низкотемпературная (200—350 °C) — на Cu−Zn−оксидных катализаторах. Из аммиака получают азотную кислоту и другие соединения азота — от лекарств и удобрений до взрывчатых веществ.
Различают катализы ''гомогенный, гетерогенный, межфазный, мицеллярный, ферментативный.
Энергия активации E каталитических реакций значительно меньше, чем для той же реакций в отсутствие катализатора. Например, для некаталитического разложения Nh4 на N2 + Н2 E ~ 320 кДж/моль, для того же разложения в присутствии Pt Е ~ 150 кДж/моль. Благодаря снижению E обеспечивается ускорение каталитических реакций по сравнению с некаталитическими.
wreferat.baza-referat.ru
Классификации катализаторов
Существуют различные типы классификации катализаторов, в основе которых лежит определенная совокупность свойств или характеристик. Наиболее широко используется классификация по типу веществ, которые являются катализаторами. Она включает следующие группы катализаторов:
Металлы (массивные, чистые, сплавы, скелетные, нанесенные) – гетерогенные катализаторы.
Так, например, металлы VIII группы (Fe, Ni, Co, Pt, Pd) используются в качестве катализаторов гидрирования ненасыщенных соединений (главным образом алкенов и алкинов). Серебро является катализатором окисления и окислительного дегидрирования (напр., синтез формальдегида из метанола).
Металлические катализаторы могут быть компактными, скелетными, нанесенными.
Pt-сетка (компактный металл в виде переплетенных нитей) – Кт окисления диоксида серы в триоксид (получение серной кислоты). Или известный катализатор гидрирования – Никель Ренея (это скелетный катализатор, который получается при выщелачивании сплава никель-алюминий).
Нанесенные катализаторы – палладий на угле (Pd/C), палладий на оксиде алюминия (Pd/Al2O3) и т.д.
Твердые бинарные соединения металлов МmЭn, где Э – О, S, Se, Te, As, P, C, N, Si, B, гетерогенные катализаторы. Из этой группы чаще всего используются оксиды или халькогениды металлов полупроводникового типа. Примерами служат оксиды MgO, ZnO, Fe2O3, Cr2O3, WO3, MoO3, V2O5 и др.
Так, в синтезе серной кислоты в настоящее время используется V2O5.
Катализаторы этого типа широко применяются в процессах гидрирования. Например в синтезе метанола из СО и водорода по реакции:
CO+ h3→ Ch4OH
катализатором служит смесь оксидов:
Cr2O3+ZnO (I Kt, суммарное давление газов 250-300 атм, температура 300-4000С ), Cr2O3+ZnO+CuO (II Kt, условия более мягкие: суммарное давление 50-100 атм., температура 220-2700С, однако, в отличие от предыдущего, катализатор чрезвычайно чувствителен к наличию серосодержащих примесей в исходных газах).
Смесь оксидов молибдена, висмута и фосфора состава MoO3∙Bi2O3∙P2O5 – катализатор окислительного аммонолиза пропилена в акрилонитрил:
Ch3=CH-Ch4+ Nh4+ 1.5 O2→ Ch3=CH-CN + 3h3O
Сульфиды молибдена и вольфрама состава MoxSy+WxSy являются хорошими катализаторами в процессах гидроочистки (обессеривания) нефтяных фракций –– в присутствии этих катализаторов происходит восстановление серосодержащих органических соединений до элементарной серы или сероводорода.
3. Кислоты и основания (гомогенные и гетерогенные катализаторы) – протонные кислоты Бренстеда (НА) в водных и неводных средах, апротонные кислоты Льюиса – Усановича (BF3, RI), протонные и апротонные центры твердых оксидов (оксиды алюминия, алюмосиликаты), любые типы оснований (в том числе твердые – МgO, CaCO3, ионообменные смолы).
На таких катализаторах протекают реакции кислотно-основного катализа, а именно крекинг нефтяных фракций (на алюмосиликатах и цеолитах), дегидратация и гидратация, синтез аминов из спиртов (на Al2O3), этерификация спиртов и кислот, конденсация альдегидов и кетонов.
Комплексы металлов, включая соли (гомогенные и гетерогенные катализаторы). Следует отметить, что соли переходных металлов – это, как правило, комплексные соединения.
Рассмотрим, например, Вакер-процесс (окисление этилена в ацетальдегид), который протекает в присутствии катализатора PdCl2/CuCl2. На самом деле PdCl2 является линейным полимером, в котором атомы металла связаны хлоридными мостиками:
/>
В растворе к присутствии хлорид-ионов, он деполимеризуется с образованием плоско-квадратных анионных комплексов палладия
/>
и именно эти анионные комплексы являются составной частью катализатора и участвуют в каталитическом цикле.
В гидрировании алкинов и алкенов катализатором служат фосфиновые комплексы родия состава RhCl(PPh4)3.
В процессе карбонилирования метанола в уксусную кислоту (процесс фирмы Монсанто) в качестве предшественника катализатора используют смесь карбонильных комплексов Rh(I) и иодистого метила (MeI).
Катализаторы реакции Реппе (карбонилирование алкинов в присутствии воды (гидрокарбоксилирование), спиртов или аминов) является тетракарбонил никеля состава Ni(CO)4 – довольно лабильный комплекс, имеющий тетраэдрическое строение.
Ферменты (гомогенные и гетерогенные).
Ферменты (энзимы) – биологические катализаторы обладают уникальными свойствами: высокой производительностью в расчете на один реакционный центр и селективностью, связанной со специфичностью действия. Работают ферменты в очень мягких условиях, при атмосферном давлении и температуре до 40о. В биологических системах отсутствуют неводные растворители и сильные кислоты и основания ( рН ≈ 7 ). Например фермент уреаза гидролизует только молекулы мочевины, не обращая внимания на другие амиды, и делает это гораздо эффективнее обычных кислотных катализаторов (табл. ).
Таблица
Реакция и субстрат
Катализатор
Константа ско-рости второго по-рядка, моль-1∙с-1
Температура, оС
Гидролиз сложных эфиров
Этилбензоат
Этиловый эфир N-бензоил-L-тирозина
Н3О+
Химотрипсин
9,0∙10-5
1,9∙104
54
25
Гидролиз аденозин-трифосфата (АТФ )
Н3О+
Миозин
4,7∙10-6
8,2∙106
40
25
Гидролиз амидов
Бензамид
Амид N-бензоил- L-тирозина
Мочевина
Н3О+
Химотрипсин
Н3О+
Уреаза
2,4∙10-6
14,9
7,4∙10-6
5,0∙106
52
25
62
21
--PAGE_BREAK--II. Классификация катализаторов по степени дискретности и коллективности действия
Взаимодействие катализатора с реагентами в газовой и жидкой фазе носит в основном дискретный характер (взаимодействие с одним реакционным центром катализатора) (гомогенный катализ). Взаимодействие реагентов с активными центрами на поверхности гетерогенного катализатора подвергается влиянию специфических эффектов твердого тела (большое количество ядер и электронов). Здесь главную роль играют коллективные эффекты. Поэтому катализаторы можно классифицировать по степени дискретности.
Коллективные эффекты выражены сильно в: а) массивных металлах, б) твердых растворах (сплавах).
Коллективные эффекты выражены слабее в: а) полупроводниковых оксидах, б) солях металлов в кристаллическом состоянии (HgCl2, MoS2, PdCl2, CuCl).
Дискретные свойства выражены сильно в: а) кислотных катализаторах в растворах, б) комплексах металлов в растворах, в) комплексах металлов, химически связанных с поверхностью носителя.
Фактически в ряду металлы → оксиды металлов → кислотные катализаторы и комплексные соединения происходит уменьшение влияния коллективных эффектов и увеличение влияния дискретных свойств. Такое деление не полностью совпадает с делением на гомогенные и гетерогенные катализаторы.
III. Классификация по специфике электронного строения
d–Катализаторы – катализаторы на основе переходных металлов, имеющие d–электроны и энергетически выгодные d–орбитали.
s,p-Катализаторы – катализаторы, в активном центре которых находится элемент, имеющий валентные S и P – орбитали(электроны). Это протонные и апротонные кислоты (НХ, RX, R+, BF3, оксиды алюминия, алюмосиликаты), а также основания Бренстеда (O, N, S, P, Hal – содержащие ионы и молекулы.
Металлы побочных подгрупп I и II групп Периодической системы относятся к промежуточному типу.
Группа d–катализаторов обладает несомненно более широким спектром каталитического действия из-за большего числа энергетически доступных орбиталей:
(n-1) d, n s, n p и электронов, участвующих в элементарных стадиях каталитических процессов.
Из группы d-катализаторов особенно широким спектром каталитических свойств обладают металлокомплексные катализаторы (как в растворах, так и на поверхности). Именно исследование металлокомплексных катализаторов позволило установить механизм многих каталитических процессов на “молекулярном уровне”.
Особенно следует отметить, что появление металлокластерных катализаторов позволило «перебросить мостик» между металлокомплексными катализаторами в растворе и гетерогенными катализаторами на носителе.
Фактически кластерные катализаторы сочетают в себе
— с одной стороны – свойства дискретной молекулы, дополненные взаимодействием между металлами на молекулярном уровне,
— с другой стороны – свойства ансамбля из атомов металла, ограниченные рамками одной молекулы.
Представления о том, как происходит превращение субстрата (или нескольких субстратов) на поверхности катализатора и является главным подходом к пониманию механизма каталитических процессов.
Но, фактически, такие превращения – это превращения, протекающие в координационной сфере атома металла и они подчиняются всем закономерностям, которые наблюдаются в координационной химии.
Поэтому, прежде чем обсуждать механизмы активации молекул катализатором (что, собственно говоря, и является “интимным” механизмом катализа), необходимо вспомнить основные понятия координационной химии
www.ronl.ru
 (Назад)
(Назад) (Cкачать работу)
(Cкачать работу)
Функция "чтения" служит для ознакомления с работой. Разметка, таблицы и картинки документа могут отображаться неверно или не в полном объёме!
26
Оглавление:Оглавление...................................................................................1Введение........................................................................................2
Видные деятели химии о катализе.............................................5
Немного о промышленном катализе........................................7
Роль катализа в экологии..........................................................11
Энергетический барьер..............................................................12
Прохождение через энергетический барьер............................14
Гомогенный катализ..................................................................17
Гетерогенный катализ...............................................................19
Катализ в биохимии..................................................................20
Приложения(графики и схемы)..............................................22-25
Список литературы...................................................................26
Введение.
КАТАЛИЗ - процесс, заключающийся в изменении скорости химических реакций в присутствии веществ, называемых катализаторами.
Катализаторы - вещества, изменяющие скорость химической реакции, которые могут участвовать в реакции, входить в состав промежуточных продуктов, но не входят в состав конечных продуктов реакции и после окончания реакции остаются неизменными.
Каталитические реакции - реакции, протекающие в присутствии катализаторов.
Положительным называют катализ, при котором скоость реакции возрастает, отрицательным (ингибированием) - при котором она убывает. Примером положительного катализа может служить процесс окисления аммиака на платине при получении азотной кислоты. Примером отрицательного - снижение скорости коррозии при введении в жидкость, в которой эксплуатируется металл, нитрита натрия, хромата и дихромата калия.
Катализаторы, замедляющие химическую реакцию, называются ингибиторами.
В зависимости от того, находится катализатор в той же фазе, что и реагирующие вещества, или образует самостоятельную фазу, говорят о гомогенном или гетерогенном катализе.
Примером гомогенного катализа является разложение пероксида водорода в присутствии ионов йода. Реакция протекает в две стадии:
Н О + I = H O + IO
Н O + IO = Н O + O + I
При гомогенном катализе действие катализатора связано с тем, что он вступает во взаимодействие с реагирующими веществами с образованием промежуточных соединений, это приводит к снижению энергии активации.
При гетерогенном катализе ускорение процесса обычно происходит на поверхности твердого тела - катализатора, поэтому активность катализатора зависит от величины и свойств его поверхности. На практике катализатор обычно наносят на твердый пористый носитель. Механизм гетерогенного катализа сложнее, чем у гомогенного.
Механизм гетерогенного катализа включает пять стадий, причем все они обратимы.
1. Диффузия реагирующих веществ к поверхности твердого вещества.
2. Физическая адсорбция на активных центрах поверхности твердого вещества реагирующих молекул и затем хемосорбция их.
3. Химическая реакция между реагирующими молекулами.
4. Десорбция продуктов с поверхности катализатора.
5. Диффузия продукта с поверхности катализатора в общий поток.
Примером гетерогенного катализа является окисление SO2 в SO3 на катализаторе V2O5 при производстве серной кислоты (контактный метод).
Промоторы (или активаторы) - вещества, повышающие активность катализатора. При этом промоторы могут сами и не обладать каталитическими свойствами.
Каталитические яды - посторонние примеси в реакционной смеси, приводящие к частичной или полной потере активности катализатора. Так, следы мышьяка, фосфора вызывают быструю потерю катализатором V O активности (контактный метод производства h3 SO4 ).
Многие важнейшие химические производства, такие, как получение серной кислоты, аммиака, азотной кислоты, синтетического каучука, ряда полимеров и др., проводятся в присутствии катализаторов.
Биохимические реакции в растительных и животных организмах ускоряются биохимическими катализаторами - ферментами.
Скорость процесса - чрезвычайно важный фактор, определяющий производительность оборудования химических производств. Поэтому одна из основных задач, поставленных перед химией научно-технической революцией, это поиск путей увеличения скорости реакций. Другая важ- ная задача современной химии, обусловленная резко возрастающими масштабами производства химических продуктов,- повышение избирательности химических превращений в полезные продукты, уменьшение количества выбросов и отходов. С этим связана, кроме того, и охрана окружающей среды и более рациональное использование истощающихся, к сожалению, природных ресурсов.
Для достижения всех этих целей нужны верные средства, и такими средствами служат прежде всего катализаторы. Однако изыскивать их не так просто. B процессе познания внутреннего устройства окружающих нас вещей ученые установили определенную градацию, иерархию уровней микромира. Мир, описываемый в нашей книге,- это мир молекул, взаимные превращения которых составляют предмет химии. Нас будет интересовать не вся химия, а только часть ее, посвященная изучению динамики изменения химической структуры молекул. Видимо нет надобности говорить о том, что молекулы построены из атомов, а последние- из ядра и окружающей его электронной оболочки; что свойства молекул зависят от природы составляющих их атомов и последовательности соединения их друг с другому что химические и физические свойства веществ зависят от свойств молекул и характера их взаимосвязи.Будем считать, что все это в общих чертах известно читателю, и потому главный упор сделаем на вопросах, связанных с представлением о скорости химических реакций.
Взаимные превращения молекул протекают с самой различной скоростью. Скорость можно изменять, нагревая или охлаждая смесь реагирующих молекул. При нагревании скорость реакции, как правило, возрастает, но это не единственное средство ускорения химических превращений. Существует еще один, более эффективный способ - каталитический, широко используемый в наше время в производстве самых разнообразных продуктов.
Первые научные представления о катализе возникли одновременно с развитием атомной теории строения вещества. В 1806 г., через год после того, как один из создателей современной атомистической теории Дальтон сформулировал в «Записках Манчестерского литературного и философского общества» закон кратных отношений, Клеман и Дезорм опубликовали подробные данные об ускорении процесса окисления сернистого газа в присутствии окислов азота при камерном производстве серной кислоты. Шесть лет спустя в «Технологическом журнале» Кирхгоф изложил результаты своих наблюдений об ускоряющем действии разбавленных минеральных кислот на гидролиз крахмала до глюкозы. Этими двумя наблюдениями была открыта эпоха экспериментального изуче- ния необычных для того времени химических явлений, которым шведский химик Берцелиус дал в 1835 г. общее название «катализ» от греческого слова «каталоо» - разрушать. Такова, в двух словах, история открытия ка- тализа, который с полным основанием следует отнести к одному из фундаментальных явлений природы.
Теперь нам следует дать современное и наиболее общепринятое определение катализа, а затем и некоторую общую классификацию каталитических процессов, так как именно с этого начинается любая точная наука. Как известно, «физика - это то, чем занимаются физики (то же самое можно сказать и о химии)». Следуя этому наставлению Бергмана, можно было бы ограничиться утверждением, что «катализ - это то, чем занимаются и химики и физики». Но, естественно, такого шутливого объяснения недостаточно, и со времен Берцелиуса давалось множество научных определений понятию «катализ». На наш взгляд наилучшее определение сформулировано Г. К. Вересковым: «Феноменологически катализ можно определить как возбуждение химических реакций или изменение их скорости под действием веществ - катализаторов, многократно вступающих в промежуточные химические взаимодействия с участниками реакции и восстанавливающих после каждого цикла промежуточных взаимодействий свой химический состав».
referat.co
Содержание
Роль катализа в промышленности и экологии.
Определение катализа.
Селективность.
Общие представления о понятии «механизм химической реакции».
Классификация каталитических систем по фазам.
Классификация катализаторов по типам реакций.
Адсорбция.
Основные требования к промышленным катализаторам.
Роль катализа в промышленности и экологии
Основным потребителем катализаторов являются нефтепереработка, нефтехимия, химия и экология.
Маркет катализаторов в год составляет около 700 тысяч тонн. Примерно половина – катализаторы каталитического крекинга. Потребности химической промышленности – около одной трети, экологии – десятая часть.
Если средняя стоимость катализаторов – 4$ за килограмм, а средняя доля в себестоимости – 0,3%, то с помощью катализаторов производят продуктов на сумму не менее 1000 миллиардов $.
Катализ позволяет экономить сырье и энергию, а также не загрязнять окружающую среду.
Определение катализа
Катализ – это ускорение одного или нескольких возможных направлений превращения химических веществ.
Термодинамика дает ответ на вопрос, как далеко может пройти конкретная химическая реакция. Этот ответ не зависит от пути реакции. На вопрос, с какой скоростью будет достигаться это конечное состояние, отвечает кинетика.
Скорость зависит от пути реакции!
Например, смесь 1,5 % бутана с воздухом при бесконечном по времени их контакте при температуре 4500С превратится в смесь диоксида углерода, воды и остатка воздуха. В присутствии катализатора, состоящего из смеси V, P и O, в течение 2-3 секунд примерно половина бутан окислится в малеиновый ангидрид.
Катализаторы ускоряют один или несколько термодинамически возможных превращений участников реакции, создавая, как правило, новый, энергетически более выгодный путь.
СН3 ---СН2 ---СН2 — СН3 + 3,5 О2 ==
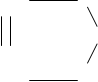 HCC ==O
HCC ==O
O
HCC ==O
Новый путь появляется за счет того, что реагенты образуют химические (промежуточные) соединения с катализатором.
Селективность
Если превращения этих соединений протекает через более низкие энергетические барьеры, то каталитический путь может оказаться быстрее, чем некаталитический.
Путь, по которому превращаются или образуются интересующие нас вещества, часто называю механизмом.
Что значит «более низкие энергетические барьеры»?

Число соударений молекул газа между собой при атмосферном давлении в 1 см3 в 1 сек из кинетической теории газов равно примерно 1030.
Число ударов молекул газа при атмосферном давлении об 1 см2 поверхности в 1 сек равно примерно 1023. Если внешняя поверхность гранул катализатора в 1 см3 равна 100 см2, то для того, чтобы каталитический путь был более быстрым, необходимо, чтобы Екат было бы примерно на 60 кДж/моль меньше, чем Енк .
| Реакция | Е нк, кДж/моль | Е кат, кДж/моль | Кат-р |
2HJ ® h3 + J2 2N2 O ® 2N2 + O2 | 184 245 | 105 59 121 134 | Au Pt Au Pt |
Общие представления о понятии «механизм химической реакции»
Лимитирующая стадия.
Схемы механизма – химическая, физическая и кинетическая.
 |
Микрокинетическая модель паровой конверсии метана.
 |

Классификация каталитических систем по фазам.
| Катализатор | Реактанты |
| Гомогенная | |
газообразный жидкий | газообразные жидкие |
| Гетерогенная | |
жидкий твердый твердый твердый твердый | газообразные жидкие газообразные жидкие + газообразные твердые |
Классификация катализаторов по типам реакций.
| Реакции | Катализатор | |
Металлы Полупроводниковые оксиды и сульфиды Изоляторы Кислоты | Гидрирование Дегидрирование Гидрогенолиз Алкилирование Окисление Окисление Дегидрирование Гидродесульфирование Дегидрирование Алкилирование Гидратация Крекинг | Ni, Cu, Pd, Pt, Fe Ni, Cu, Pd, Pt Pd, Pt Ni, Cu Cu, Ag Bi-Mo-O, Fe-Mo-O, Fe-Sn-O, V-P-O Cr-O, Fe-Cr-O Ni-Mo-S, Co-Mo-S Al-O, Si-O, Mg-O h3 SO4 h4 PO4 Цеолиты |
Адсорбция
Роль адсорбции в катализе. Физическая и химическая адсорбции. Их характерные различия и общие черты
· зависимость от природы адсорбента,
· от температуры,
· покрытия поверхности,
· тепловой эффект,
· влияние на электропроводность.
Энергетическая диаграмма при химической адсорбции.
Теплота и термодинамика адсорбции.
Изотермы адсорбции.
Модель идеальной поверхности Ленгмюра.
Вывод изотермы Ленгмюра.

Физический смысл констант.
Вид изотермы при устремлении Р к нулю или бесконечности.
Связь между энергиями активации стадий адсорбции и десорбции и теплотой адсорбции.
Модели биографической и индуцированной неоднороднных поверхностей.
Вывод изотермы Темкина.

Физический смысл констант.
Вид изотермы при устремлении Р к нулю или бесконечности. Область средних покрытий.
Основные требования к промышленным катализаторам
Химические требования
· термическая стабильность,
· стойкость к отравлению «ядами»,
· легкая регенерируемость,
· высокая избирательность,
· активность при доступных температурах и давлениях.
Механические требования
· прочность,
· малое гидравлическое сопротивление,
· однородность,
· оптимальная пористая структура.
www.ronl.ru
Содержание
Роль катализа в промышленности и экологии.
Определение катализа.
Селективность.
Общие представления о понятии "механизм химической реакции".
Классификация каталитических систем по фазам.
Классификация катализаторов по типам реакций.
Адсорбция.
Основные требования к промышленным катализаторам.
Роль катализа в промышленности и экологии
Основным потребителем катализаторов являются нефтепереработка, нефтехимия, химия и экология.
Маркет катализаторов в год составляет около 700 тысяч тонн. Примерно половина – катализаторы каталитического крекинга. Потребности химической промышленности – около одной трети, экологии – десятая часть.
Если средняя стоимость катализаторов – 4$ за килограмм, а средняя доля в себестоимости – 0,3%, то с помощью катализаторов производят продуктов на сумму не менее 1000 миллиардов $.
Катализ позволяет экономить сырье и энергию, а также не загрязнять окружающую среду.
Определение катализа
Катализ – это ускорение одного или нескольких возможных направлений превращения химических веществ.
Термодинамика дает ответ на вопрос, как далеко может пройти конкретная химическая реакция. Этот ответ не зависит от пути реакции. На вопрос, с какой скоростью будет достигаться это конечное состояние, отвечает кинетика.
Скорость зависит от пути реакции!
Например, смесь 1,5 % бутана с воздухом при бесконечном по времени их контакте при температуре 4500С превратится в смесь диоксида углерода, воды и остатка воздуха. В присутствии катализатора, состоящего из смеси V, P и O, в течение 2-3 секунд примерно половина бутан окислится в малеиновый ангидрид.
Катализаторы ускоряют один или несколько термодинамически возможных превращений участников реакции, создавая, как правило, новый, энергетически более выгодный путь.
СН3---СН2---СН2--- СН3+ 3,5 О2==
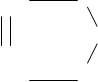 HCC ==O
HCC ==O
O
HCC ==O
Новый путь появляется за счет того, что реагенты образуют химические (промежуточные) соединения с катализатором.
Селективность
Если превращения этих соединений протекает через более низкие энергетические барьеры, то каталитический путь может оказаться быстрее, чем некаталитический.
Путь, по которому превращаются или образуются интересующие нас вещества, часто называю механизмом.
Что значит «более низкие энергетические барьеры»?
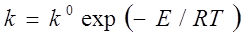
Число соударений молекул газа между собой при атмосферном давлении в 1 см3в 1 сек из кинетической теории газов равно примерно 1030.
Число ударов молекул газа при атмосферном давлении об 1 см2поверхности в 1 сек равно примерно 1023. Если внешняя поверхность гранул катализатора в 1 см3равна 100 см2, то для того, чтобы каталитический путь был более быстрым, необходимо, чтобы Екатбыло бы примерно на 60 кДж/моль меньше, чем Енк.
| Реакция | Енк, кДж/моль | Екат, кДж/моль | Кат-р |
2HJ ® h3+ J2 2N2O ® 2N2+ O2 | 184 245 | 105 59 121 134 | Au Pt Au Pt |
Общие представления о понятии «механизм химической реакции»
Лимитирующая стадия.
Схемы механизма – химическая, физическая и кинетическая.
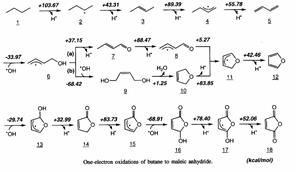 |
Микрокинетическая модель паровой конверсии метана.
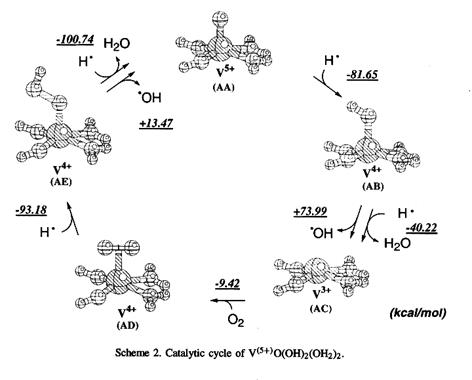 |

Классификация каталитических систем по фазам.
| Катализатор | Реактанты |
| Гомогенная | |
газообразный жидкий | газообразные жидкие |
| Гетерогенная | |
жидкий твердый твердый твердый твердый | газообразные жидкие газообразные жидкие + газообразные твердые |
Классификация катализаторов по типам реакций.
| Реакции | Катализатор | |
Металлы Полупроводниковые оксиды и сульфиды Изоляторы Кислоты | Гидрирование Дегидрирование Гидрогенолиз Алкилирование Окисление Окисление Дегидрирование Гидродесульфирование Дегидрирование Алкилирование Гидратация Крекинг | Ni, Cu, Pd, Pt, Fe Ni, Cu, Pd, Pt Pd, Pt Ni, Cu Cu, Ag Bi-Mo-O, Fe-Mo-O, Fe-Sn-O, V-P-O Cr-O, Fe-Cr-O Ni-Mo-S, Co-Mo-S Al-O, Si-O, Mg-O h3SO4 h4PO4 Цеолиты |
Адсорбция
Роль адсорбции в катализе. Физическая и химическая адсорбции. Их характерные различия и общие черты
· зависимость от природы адсорбента,
· от температуры,
· покрытия поверхности,
· тепловой эффект,
· влияние на электропроводность.
Энергетическая диаграмма при химической адсорбции.
Теплота и термодинамика адсорбции.
Изотермы адсорбции.
Модель идеальной поверхности Ленгмюра.
Вывод изотермы Ленгмюра.
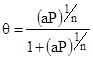
Физический смысл констант.
Вид изотермы при устремлении Р к нулю или бесконечности.
Связь между энергиями активации стадий адсорбции и десорбции и теплотой адсорбции.
Модели биографической и индуцированной неоднороднных поверхностей.
Вывод изотермы Темкина.

Физический смысл констант.
Вид изотермы при устремлении Р к нулю или бесконечности. Область средних покрытий.
Основные требования к промышленным катализаторам
Химические требования
· термическая стабильность,
· стойкость к отравлению «ядами»,
· легкая регенерируемость,
· высокая избирательность,
· активность при доступных температурах и давлениях.
Механические требования
· прочность,
· малое гидравлическое сопротивление,
· однородность,
· оптимальная пористая структура.
superbotanik.net
- 1 -
Содержание
Роль катализа в промышленности и экологии.
Определение катализа.
Селективность.
Общие представления о понятии "механизм химической реакции".
Классификация каталитических систем по фазам.
Классификация катализаторов по типам реакций.
Адсорбция.
Основные требования к промышленным катализаторам.
Роль катализа в промышленности и экологии
Основным потребителем катализаторов являются нефтепереработка, нефтехимия, химия и экология.
Маркет катализаторов в год составляет около 700 тысяч тонн. Примерно половина - катализаторы каталитического крекинга. Потребности химической промышленности - около одной трети, экологии - десятая часть.
Если средняя стоимость катализаторов - 4$ за килограмм, а средняя доля в себестоимости - 0,3%, то с помощью катализаторов производят продуктов на сумму не менее 1000 миллиардов $.
Катализ позволяет экономить сырье и энергию, а также не загрязнять окружающую среду.
Определение катализа
Катализ - это ускорение одного или нескольких возможных направлений превращения химических веществ.
Термодинамика дает ответ на вопрос, как далеко может пройти конкретная химическая реакция. Этот ответ не зависит от пути реакции. На вопрос, с какой скоростью будет достигаться это конечное состояние, отвечает кинетика.
Скорость зависит от пути реакции!
Например, смесь 1,5 % бутана с воздухом при бесконечном по времени их контакте при температуре 4500 С превратится в смесь диоксида углерода, воды и остатка воздуха. В присутствии катализатора, состоящего из смеси V, P и O, в течение 2-3 секунд примерно половина бутан окислится в малеиновый ангидрид.
Катализаторы ускоряют один или несколько термодинамически возможных превращений участников реакции, создавая, как правило, новый, энергетически более выгодный путь.
СН3---СН2---СН2--- СН3 + 3,5 О2 ==
HC C ==O
O
HC C ==O
Новый путь появляется за счет того, что реагенты образуют химические (промежуточные) соединения с катализатором.
Селективность
Если превращения этих соединений протекает через более низкие энергетические барьеры, то каталитический путь может оказаться быстрее, чем некаталитический.
Путь, по которому превращаются или образуются интересующие нас вещества, часто называю механизмом.
Что значит «более низкие энергетические барьеры»?
Число соударений молекул газа между собой при атмосферном давлении в 1 см3 в 1 сек из кинетической теории газов равно примерно 1030.
Число ударов молекул газа при атмосферном давлении об 1 см2 поверхности в 1 сек равно примерно 1023. Если внешняя поверхность гранул катализатора в 1 см3 равна 100 см2, то для того, чтобы каталитический путь был более быстрым, необходимо, чтобы Екат было бы примерно на 60 кДж/моль меньше, чем Енк.
Реакция | Е нк, кДж/моль | Е кат, кДж/моль | Кат-р | |
2HJ h3 + J2 2N2O 2N2 + O2 | 184 245 | 105 59 121 134 | Au Pt Au Pt |
Общие представления о понятии «механизм химической реакции»
Лимитирующая стадия.
Схемы механизма - химическая, физическая и кинетическая.
Физико-химический механизм реакции окисления бутана в малеиновый ангидрид.
Микрокинетическая модель паровой конверсии метана.
Классификация каталитических систем по фазам.
Катализатор | Реактанты | |
Гомогенная | ||
| газообразный жидкий | газообразные жидкие | |
Гетерогенная | ||
| жидкийтвердыйтвердыйтвердый твердый | газообразныежидкиегазообразныежидкие + газообразные твердые |
Реакции | Катализатор | ||
| МеталлыПолупроводниковые оксиды и сульфидыИзоляторы Кислоты | ГидрированиеДегидрированиеГидрогенолизАлкилированиеОкислениеОкислениеДегидрированиеГидродесульфированиеДегидрированиеАлкилированиеГидратация Крекинг | Ni, Cu, Pd, Pt, FeNi, Cu, Pd, PtPd, PtNi, CuCu, AgBi-Mo-O, Fe-Mo-O,Fe-Sn-O, V-P-OCr-O, Fe-Cr-ONi-Mo-S, Co-Mo-SAl-O, Si-O, Mg-Oh3SO4h4PO4 Цеолиты |
Основные требования к промышленным катализаторам
Химические требования
· термическая стабильность,
· стойкость к отравлению «ядами»,
· легкая регенерируемость,
· высокая избирательность,
· активность при доступных температурах и давлениях.
Механические требования
· прочность,
· малое гидравлическое сопротивление,
· однородность,
· оптимальная пористая структура.
referatwork.ru