|
|
|
|
 Far Far |
 WinNavigator WinNavigator |
 Frigate Frigate |
 Norton
Commander Norton
Commander |
 WinNC WinNC |
 Dos
Navigator Dos
Navigator |
 Servant
Salamander Servant
Salamander |
 Turbo
Browser Turbo
Browser |
|
|
 Winamp,
Skins, Plugins Winamp,
Skins, Plugins |
 Необходимые
Утилиты Необходимые
Утилиты |
 Текстовые
редакторы Текстовые
редакторы |
 Юмор Юмор |
|
|
|
File managers and best utilites |
Возбудители атипичных микобактериозов. Реферат микобактериозы
Реферат На тему: «Возбудители атипичных микобактериозов»
Размещено на http://www.allbest.ru/
Министерство Здравоохранения Республики Казахстан
АО «Медицинский Университет Астана»
Кафедра: микробиологии и вирусологии им. Ш. И. Сарбасовой
Выполнила: Мендигалиева С.Н.
Группа 246 ОМ
Проверила: Акимбекова Г.М.
Астана 2012
Введение
В последнее время клиницисты все чаще говорят о случаях нерасшифрованных хронических заболеваний, напоминающих по течению туберкулез, но не поддающихся лечению противотуберкулезными препаратами. Терапия антибиотиками и химиопрепаратами ранее неизлечимых или трудно излечимых болезней повлекла за собой выявление и описание новых, ранее неизвестных или редко встречавшихся нозологических форм. К их числу следует отнести кандидоз, нокардиоз и микобактериоз, которые часто являются следствием бесконтрольной антибиотико- и химиотерапии. В процессе лечения антибиотики широкого спектра действия, подавляя жизнедеятельность возбудителей, не щадят и чувствительные к лекарствам микробы нормальной микрофлоры человека. Остающиеся при этом или попадающие извне устойчивые к медикаментам микроорганизмы (к ним относятся дрожжеподобные грибы рода Кандида, сапрофитные и потенциально патогенные микобактерии, нокардии и др.) не испытывая на себе сдерживающего влияния антагонистов (из числа представителей нормальной микрофлоры человека), приживаются и накапливаются в организме. Если последний ослаблен предыдущим острым или хроническим заболеванием, то эти микроорганизмы могут вызвать тяжелый процесс, который при неправильной или запоздалой диагностике может принять неблагоприятное течение и привести к смерти.
Атипические микобактериозы
Атипические микобактериозы представляют собой заболевания, по клинике и рентгенологическим признакам близкие к туберкулезу. Их возбудителями являются кислотоустойчивые микобактерии, которые по культуральным, биохимическим свойствам и вирулентности отличаются от микобактерии туберкулеза.
Они обладают естественной лекарственной устойчивостью ко многим противотуберкулезным препаратам широкого спектра действия. В отличие от возбудителя туберкулеза они патогенны для белых мышей и крыс и не патогенны для морской свинки и кролика.
Изучение биологических свойств этих микобактерии выявило, что они представляют большую группу, состоящую из многих видов, которую объединили под общим названием «атипичные» микобактерии. Для человека атипичные микобактерии потенциально патогенны.
Пока еще не существует единого мнения об их происхождении. Установленное генетическое родство некоторых атипичных микобактерии с возбудителями туберкулеза позволяет рассматривать их как форму изменчивости микобактерии туберкулеза.
При этом одним из главных факторов, обусловливающих появление атипичных микобактерии, считается противотуберкулезная терапия.
Так, у детей и подростков при проведении антибактериальной терапии одновременно со значительным снижением высеваемости микобактерии отмечают повышение частоты обнаружения пигментных форм.
Обоснованно также и другое мнение, что атипичные микобактерии являются широко распространенными в природе самостоятельными видами, обладающими потенциальной патогенностью для человека и некоторых животных. Попадая извне в организм человека, они находят там особенно благоприятные условия для размножения при проведении антибактериальной терапии вследствие их устойчивости ко многим лекарственным препаратам.
Возбудители
В состав рода Mycobacterium семейства Mycobacteriaceae отдела Firmicutes включены неподвижные аэробные грамположительные палочковидные бактерии. Иногда они образуют нитевидные структуры, напоминающие мицелий грибов. Это и послужило основанием для их названия [греч. mykes, гриб и лат. bacterium, бактерия].
Для микобактерий характерно высокое содержание липидов, фосфатидов и восков в клеточных стенках (до 60%), что определяет их щёлоче-, спирто- и кисдотоустойчивость (признак особенно выражен у паразитических видов микобактерий).
Поэтому микобактерии плохо воспринимают анилиновые красители и обычные способы окрашивания. Для окраски применяют интенсивные методы, обычно Циля-Нильсена. Растут медленно или очень медленно; сапрофитические виды растут несколько быстрее. Некоторые виды образуют каротиноидные недиффундирующие в среду пигменты.
studfiles.net
Микобактериозы — реферат
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РЕСПУБЛИКИ БЕЛАРУСЬ
БЕЛОРУССКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ
Кафедра фтизиопульмонологии
Реферат на тему:
Микобактериозы
Подготовила студентка лечебного факультета 434 группы Лазовик Юлия
2013
Атипические микобактериозы представляют собой заболевания, по клинике и рентгенологическим признакам близкие к туберкулезу. Их возбудителями являются кислотоустойчивые микобактерии, которые по культуральным, биохимическим свойствам и вирулентности отличаются от микобактерии туберкулеза.
Они обладают естественной лекарственной устойчивостью ко многим противотуберкулезным препаратам широкого спектра действия. В отличие от возбудителя туберкулеза они патогенны для белых мышей и крыс и не патогенны для морской свинки и кролика.
Изучение биологических свойств этих микобактерии выявило, что они представляют большую группу, состоящую из многих видов, которую объединили под общим названием «атипичные» микобактерии. Для человека атипичные микобактерии потенциально патогенны.
Пока еще не существует единого мнения об их происхождении. Установленное генетическое родство некоторых атипичных микобактерии с возбудителями туберкулеза позволяет рассматривать их как форму изменчивости микобактерии туберкулеза.
При этом одним из главных факторов, обусловливающих появление атипичных микобактерии, считается противотуберкулезная терапия.
Так, у детей и подростков при проведении антибактериальной терапии одновременно со значительным снижением высеваемости микобактерии отмечают повышение частоты обнаружения пигментных форм.
Обоснованно также и другое мнение, что атипичные микобактерии являются широко распространенными в природе самостоятельными видами, обладающими потенциальной патогенностью для человека и некоторых животных. Попадая извне в организм человека, они находят там особенно благоприятные условия для размножения при проведении антибактериальной терапии вследствие их устойчивости ко многим лекарственным препаратам.
Возбудители
В состав рода Mycobacterium семейства Mycobacteriaceae отдела Firmicutes включены неподвижные аэробные грамположительные палочковидные бактерии. Иногда они образуют нитевидные структуры, напоминающие мицелий грибов. Это и послужило основанием для их названия [греч. mykes, гриб и лат. bacterium, бактерия].
Для микобактерий характерно высокое содержание липидов, фосфатидов и восков в клеточных стенках (до 60%), что определяет их щёлоче-, спирто- и кисдотоустойчивость (признак особенно выражен у паразитических видов микобактерий).
Поэтому микобактерии плохо воспринимают анилиновые красители и обычные способы окрашивания. Для окраски применяют интенсивные методы, обычно Циля-Нильсена. Растут медленно или очень медленно; сапрофитические виды растут несколько быстрее. Некоторые виды образуют каротиноидные недиффундирующие в среду пигменты.
Классификация микобактерий по патогенности:
При классификации микобактерий учитывают патогенность для человека, способность к пигментообразованию, скорость роста и способность синтезировать никотиновую кислоту (ниацин).
• По патогенности выделяют собственно патогенные (вызывающие конкретные заболевания), потенциально патогенные и сапрофитические микобактерии. Патогенными для человека свойствами обладают М. tuberculosis, M. leprae, M. bovis. Прочие виды, вызывающие поражения у человека, известны как атипичные микобактерии.
• По скорости роста выделяют быстрорастущие (дают видимый рост на . 4-7-е сутки), медленнорастущие (рост наблюдают через 7-10 и более дней) и не растущие на искусственных средах (М. leprae) виды микобактерий.
• По способности образовывать пигменты выделяют фотохромогенные (образуют пигмент на свету), скотохромогенные (образуют пигмент в темноте) и нефотохромогенные (не образуют пигмента) виды микобактерий.
Возбудителей микобактериозов называют атипичными микобактериями:
- -они не имеют корд-фактор,
- -каталазо–термостабильны
- -невирулентны для лабораторных животных
- -некоторые растут быстро на простых питательных средах,
- -часто устойчивы к противотуберкулёзным препаратам
M. canzasi | вызывают поражения лёгких |
М. ulcerans | язвы на конечностях |
M. avium | поражения лёгких, могут вызывать диарею часто даёт осложнения при СПИДе |
M. fortuitum | вызывает поражения кожи, может присоединяться к постоперационным инфекциям, вызывать сепсис |
Экология и распространение
В окружающей среде существует много атипичных потенциально патогенных микобактерий. Часть из них выделяется от людей и животных при различных заболеваниях легких, кожи, лимфатических узлов, других тканей и органов. Они получили общее название микобактериозы. Роль условно-патогенных микобактерий в инфекционной патологии человека растет с каждым годом. В эту группу заболеваний не входят туберкулез и проказа, хотя некоторые из них имеют сходный ход. Существующие методы лечения туберкулеза и микобактериозов разные, в связи с чем микробиологическая идентификация возбудителей приобретает особое значение. По классификации Раньйона атипичные микобактерии делятся на 4 группы: фотохромогенни, скотохромогенни, нефотохромогенни и быстрорастущие. К фотохромогенних микобактерий принадлежат Mycobacterium kanzasi, М. marinum, М ulcerans, М simiae. Все они кислотоустойчивые, образуют желто-оранжевый пигмент на свету, вызывают туберкулезоподобные заболевания легких, лимфадениты, поражения кожи и подкожной клетчатки. М ulcerans, например, вызывает язву Бурул .Скотохромогенные микобактерии (М scrofulaceum, М aquae, М flavescens др.). образуют желто-оранжевый пигмент в темноте, вызывают шейные лимфадениты у детей, реже патологические процессы в легких. Нефотохромогенные вида - М avium, М. intracellular - имеют очень слабую пигментацию колоний, или они вовсе не окрашены, вызывают туберкулезоподобные заболевания легких, кожи, почек, костей и суставов, опасны для больных с иммунодефицитами, особенно при ВИЧ-инфекции. Они вызывают туберкулез у птиц и редко у человека (М avium).В группу быстрорастущих микобактерий отнесены M.fortuitum, М. friedmanii, М. malmoense, М. smegmatis, М. phlei. Они причастны к возникновению абсцессов после инъекций у наркоманов, воспаления вокруг вживленных объектов (например, протезов сердечных клапанов). Поражение легких и лимфадениты у детей вызывает М. malmoense. Практическое значение в плане дифференциации различных видов микобактерий имеет М. smegmatis, особенно при лабораторной диагностике заболеваний мочеполовой системы.
Клинические проявления
Наиболее часто встречается микобактериоз легких, которым заболевают главным образом пожилые люди. Описаны отдельные случаи микобактериоза легких у лиц более молодого возраста и даже у подростков.
Второе место по частоте занимают поражения лимфатических узлов. В противоположность легочному микобактериозу лимфаденит, вызываемый потенциально патогенными микобактериями, наблюдается преимущественно у детей. В литературе описаны также заболевания мочеполовой системы, костей и суставов, мозговой оболочки и кожи той же этиологии.
Как показали многие исследователи, заболевания, причиной которых являются потенциально патогенные микобактерии, по клинической картине и течению весьма сходны с заболеваниями, вызываемыми микобактериями туберкулеза. Возможны образование каверн, кровотечения и кровохарканье. Микобактериоз характеризуется хроническим течением и часто сопровождается эмфиземой. Однако наряду с хроническими, продолжающимися годами процессами наблюдаются острые тяжелые заболевания, нередко завершающиеся смертью. Основной причиной смерти, по мнению некоторых исследователей, является легочное сердце.
Симптомы М весьма разнообразны и неспецифичны. Большинство пациентов предъявляют жалобы на длительный или периодически возникающий кашель, чаще сухой, иногда с мокротой. Больных беспокоят слабость, недомогание, умеренная одышка, иногда эпизоды кровохарканья, боли в грудной клетке, субфебрилитет, потеря массы тела. Бразильские исследователи у всех пациентов с диагностированным по критериям ATS М наблюдали кашель, интоксикационные жалобы были у 74% больных [24].
Рентгенологические изменения при М полиморфны. Условно выделяют два варианта М легких [5, 8, 37] — с наличием полостей распада с фиброзными стенками и с преимущественно очаговыми изменениями, визуализирующимися при КТ высокого разрешения, преимущественно в средних и нижних отделах легких, часто сочетающимися с бронхоэктазами.
Для выделения и идентификации НТМБ рекомендован [5] сбор диагностического материала в стерильные герметичные одноразовые контейнеры с исключением потенциальных источников загрязнения, особенно водопроводной воды, и фиксаторов.
По клинической картине микобактериоз можно разделить на три группы:
1) собственно микобактериоз, т. е. заболевание, вызванное одним из видов потенциально патогенных микобактерии;
2) смешанные формы (туберкулез + микобактериоз), при которых в выделениях больного обнаруживаются 2 возбудителя, чаще всего М. tuberculosis и М. avium;
3) последовательное развитие заболеваний, когда на фоне затихшего туберкулезного процесса возникает новое заболевание — микобактериоз.
Диагностика
Рис. 1. Рентгенологические проявления микобактериозов легких, вызванных различными возбудителями:
а, б – обзорная рентгенограмма и компьютерная томограмма органов грудной клетки больной Д., 69 лет.
Микобактериоз, вызванный МАС: рассеянные сливающиеся полиморфные очаги различной величины и интенсивности; в нижней доле правого легкого несколько полостей с неравномерно утолщенными стенками; средостение смещено влево средостения за счет выраженных пневмосклеротических и фиброзных изменений; интерстициальные и перибронхиальные уплотнения с наличием бронхоэктазов и участков буллезной эмфиземы; плевральные спайки.
в, г – обзорная рентгенограмма и планарная томограмма больной М., 24 лет.
Микобактериоз, вызванный МАС: легочный рисунок несколько усилен с обеих сторон, в С1-2 правого легкого участок инфильтрации легочной ткани, состоящий из слившихся полиморфных очагов неоднородной структуры.
д, е – обзорная рентгенограмма и компьютерная томограмма органов грудной клетки больной П., 32 лет.
Микобактериоз, вызванный M.kansassii: верхняя доля правого легкого практически разрушена, представлена системой полостей, самая крупная занимает С2 и часть С1, имеет неравномерно утолщенные стенки, внутри полости секвестры; в С6 на фоне деформированного легочного рисунка и полиморфных очагов несколько полостей; очаги засева в нижних отделах справа и в С3 и язычковых сегментах слева, некоторые очаги с распадом; правый корень смещен кверху, средостение смещено вправо.
ж, з — обзорная рентгенограмма и планарная томограмма больного Н., 57 лет.
Микобактериоз, вызванный M.xenopi: в верхней доле левого легкого на фоне грубых фиброзных изменений — многочисленные разнокалиберные полости с толстыми, неровными стенками, четкими внутренними очертаниями; множественные мелкие и средних размеров плотные очаги в остальных отделах слева и в верхней доле справа; корни легких деформированы, просветы крупных бронхов муфтообразно утолщены, уплотнены, просветы сегментарных – расширены по типу бронхоэктазов без содержимого; средостение значительно смещено влево.
При вызванных МАС М рентгенологические проявления были наиболее разнообразны. Чаще всего (6 из 9 больных) наблюдали более или менее распространенную очаговую диссеминацию в легочной ткани (у 3 чел. — двустороннюю) в сочетании с деформацией легочного рисунка и наличием (у 2 чел.) часто описываемых при МАС-инфекции «мультифокальных бронхоэктазов» (рис. 1 а, б). У 3 больных изменения в легочной ткани были представлены участками инфильтрации и фокусами в легочной ткани, неоднородной структуры (трактуемой как деструктивные изменения), весьма сходными с изменениями при инфильтративном туберкулезе легких (рис. 1 в, г).
Критерии диагностики микобактериозов по An Official ATS/IDSA Statement: Diagnosis, Treatment and Prevention of Nontuberculous Mycobacterial Diseases Am J Respir Crit Care Med. Vol 175. Рp. 367-416, 2007 [5]
Клинические критерии |
|
Микробиологические критерии |
или
или
|
referat911.ru
Микобактериозы — реферат
Для диагностики легочного М предпочтителен трехкратный сбор мокроты в разные дни. При невозможности получения мокроты рекомендовано исследование бронхиального смыва. В связи с различной чувствительностью штаммов НТМБ к противомикробным препаратам идентификация НТМБ на уровне вида и исследование их лекарственной чувствительности приобретает клиническую значимость [48]. При невозможности диагностики М микробиологическими и рентгенологическими методами показана бронхоскопия с биопсией легочной ткани, диагностическая торакотомия, эксцизионная биопсия лимфоузлов с гистологическим исследованием биоптата. Диагноз устанавливают при наличии НТМБ в пораженной ткани с характерным гранулематозным воспалением при условии исключения туберкулеза или других М.
Материалом для исследования служит мокрота, содержимое язв и других поражений кожи, пунктаты лимфатических узлов, промывные воды бронхов, моча и др.. Лабораторные исследования проводятся по тем же принципам и методам, что и при туберкулезе. После первичной микроскопии материал сеют на среды Левенштейна-Иенсена, Финна и обязательно на среду с салицилатом натрия. Перед посевом патологический материал обрабатывают 15-20 мин 2-5% раствором серной кислоты или 10% раствором фосфата натрия в течение 18-20 ч при 37 ° С. Атипичные микобактерии более чувствительны к такой обработки, чем палочки туберкулеза. Если обрабатывать мокроты малахитовым зеленым или генциановый фиолетовым - выделения возбудителей микобактериозов увеличивается в 3-4 раза.Для идентификации микобактерий предложено много тестов. Однако в бактериологических лабораториях практических медицинских учреждений использовать их просто невозможно. Зачастую для установления вида возбудителя учитывают цвет колоний, скорость роста субкультур, рост при различных температурах и особенно в среде с салицилатом натрия, определения каталазы, синтеза ниацина и др.. Практически все виды микобактерий дают рост на среде с салицилатом натрия, в то время как возбудители туберкулеза на нем не растут. Ниацин синтезирует лишь М. tuberculosis, а возбудители микобактериозов не образуют никотиновой кислоты.Разработаны методы идентификации микобактерий в реакциях преципитации и фаголизису. Серологические реакции для диагностики микобактериозов, особенно такие как РСК, РИФ, РНГА, можно будет использовать при условии изготовления специфических тест-систем. Большие возможности для определения возбудителей этих заболеваний открывает внедрение полимеразной цепной реакции.
Профилактика и лечение
Лечение М сложное и достаточно длительное. В схеме лечения могут быть использованы традиционные противотуберкулезные препараты (ПТП), хотя спектр ограничен устойчивостью к ним НТМБ, побочными эффектами, имеющейся сопутствующей патологией [8, 49]. В последнее время внимание привлекли вопросы немалой стоимости лечения М [50]. Применяют при М легких и оперативное лечение, в основном резекционные вмешательства [5, 8, 29], причем в последние годы аргументы в пользу хирургических методов звучат все чаще, особенно как элемента комплексного лечения [51, 52, 53].
Используемые в настоящее время фторхинолоны (офлоксацин, левофлоксацин, ципрофлоксацин, спарфлоксацин) in vitro активно действуют на МБ, но их активность существенно варьирует in vivo в зависимости от химического строения и физико-химических свойств препарата и нередко не обеспечивает клиническую эффективность. Kawahara [54] установил in vitro высокую эффективность фторхинолонов в отношении НТМБ. По данным Т.Ф. Оттен [55], наиболее эффективным препаратом в отношении НТМБ является левофлоксацин. После разового приема 500 мг его максимальная концентрация (6,2 мкг/мл) в сыворотке крови достигается в течение часа. В рандомизированном исследовании Британского торакального общества сочетание рифампицина и этамбутола при лечении МАС в 41% случаев позволило добиться положительного результата (при использовании изониазида — 16%) [56]. Прием кларитромицина в сочетании с рифампицином и этамбутолом был почти в два раза эффективнее сочетания ципрофлоксацина, рифампицина и этамбутола (23%) [56]. M. kansasii in vitro ингибируются сочетанием кларитромицина и моксифлоксацина [57].
Для этиотропного лечения M. abscessus рекомендуют ежедневный прием карбопенемов (имипенем), цефалоспоринов (цефокситин) и аминогликозидов (амикацин) в течение 2-4 месяцев [57]. На M. abscessusin vitro активно воздействуют макролиды, но фермент эритромицин-метилаза уменьшает его эффективность [58]. Достаточно активны в отношении M. abscessus линезолид и тигециклин, но высокая токсичность не позволяет использовать их достаточно широко [59]. Выделенные штаммы M. chelonaeобычно чувствительны к аминогликозидам (тобрамицин), макролидам, оксазолидинону (линезолид) и карбопенемам (имипенем) [60, 61]. Считается, что M. fortuitum обладает in vitro более широким спектром чувствительности, чем M. abscessus или M. chelonae.
Заключение
Микобактериоз обычно развивается только в ослабленном организме, ранее поврежденном каким-либо неблагоприятным воздействием. Так, большую роль в развитии микобактериоза у людей играет запыление атмосферы. Это заболевание чаще встречается у лиц, профессии которых связаны с работой в помещениях с повышенным содержанием пыли (шахтеры, литейщики, углекопы). Среди рабочих этих специальностей наблюдаются пневмокониоз, силикоз и другие заболевания, ослабляющие легочную ткань. Именно при таких условиях легко развиваются заболевания, вызванные менее вирулентными, но потенциально патогенными микобактериями. Развитию микобактериоза могут способствовать саркоидоз и эмфизема. Ослабление всего организма, а также лечение кортикостероидными препаратами также могут быть косвенной причиной возникновения микобактериоза.
referat911.ru
1.4.3.3. Возбудители микобактериозов.
Многие виды микобактерий могут вызывать у человека оппортунистические заболевания или микобактериозы. Проблема микобактериозов существенно обострилась в связи с глобальным распространением ВИЧ-инфекции. При подавлении клеточного иммунитета микобактерии становятся одними из ведущих оппортунистических патогенов.
Возбудители широко распространены в окружающей среде, обнаруживаются в воде и почве. Они выделяются из организма людей, теплокровных и холоднокровных животных.
Наиболее часто заболевания вызывает близкородственная группа микобактерий, которых относят к комплексу M. avium (M. avium complex или MAC).
Самостоятельные виды микобактериозов связаны с инфекцией M. kansasii, M. ulcerans, M. scrofulaceum, М. chelonae, М. fortuitum.
Комплекс M. avium включает несколько подвидов. Среди них – одноименный подвид M. avium subsp. avium, а также подвиды M. hominissius, M. silvaticum, M. paratuberculosis. К ним примыкает генетически близкий вид M. intracellulare.
M. avium – это возбудитель туберкулеза птиц, однако он может поражать и людей. Инфекция обычно передается воздушно-капельным путем, реже алиментарно.
У больных ВИЧ-инфекцией в стадии СПИДа бактерия вызывает генерализованное поражение с вовлечением респираторного и желудочно-кишечного тракта. Тяжелые микобактериозы отмечаются у 25-30% пациентов с ВИЧ-инфекцией при длительном течении заболевания.
Также M. avium может быть причиной шейного лимфаденита у детей и легочной патологии у взрослых.
Патогенных для человека M. avium предложено отнести к подвиду M. hominissius.
Подвид М. paratuberculosis вызывает гипертрофический энтерит крупного рогатого скота. Предполагается его участие в развитии болезни Крона у человека.
Подвид М. sylvaticum является причиной туберкулеза у лесных голубей.
Вид M. intracellulare был впервые выделен от больного человека. В дальнейшем он был обнаружен у животных, а также на объектах окружающей среды, где бактерии образуют биопленки. У людей он способен вызывать тяжелые заболевания легких, причем может поражать лиц без иммунодефицита.
Другие микобактерии также могут являться причиной легочных поражений. Среди них обнаруживают M. kansasii, М. simiae, M. scrofulaceum. Помимо легочных инфекций, вид M. scrofulaceum часто вызывает шейный лимфаденит у детей.
М. ulcerans является возбудителем язвы Бурули – поражения кожи, подкожной клетчатки с переходом на костную ткань, что сопровождается некрозом и изъязвлением. Болезнь обнаруживается у жителей тропической Африки, Австралии, Латинской Америки. Возбудитель выделяет липидный токсин – миколактон, который способствует развитию заболевания.
Из быстрорастущих видов к патогенным для человека относятся М. fortuitum и М. chelonae. Они могут вызывать раневые инфекции, постинъекционные абсцессы, язвы роговицы, легочные поражения.
Лабораторная диагностика микобактериозов включает микроскопию клинического материала с окраской бактерий по Цилю-Нильсену с последующим их выделением в чистой культуре.
Наиболее современными являются генетические методы идентификации возбудителей микобактериозов.
Для лечения инфекций, вызванных комплексом M. avium, назначают макролидные антибиотики и рифабутин, так как возбудители устойчивы к противотуберкулезным препаратам первого ряда.
Для местных микобактериальных процессов (лимфадениты, язвы) наряду с антибиотикотерапией используют хирургическое лечение.
14.4. Патогенные актиномицеты
Первое описание актиномикоза у людей в 1845 г. было сделано В. Лангенбеком, в чистой культуре возбудитель был выделен в 1887 г. К. Гарцем и в 1888 г. М. Афанасьевым.
Классификация
Данные бактерии относятся к порядку Actinomycetales, семейству Actinomycetaceae, роду Actinomyces. Род включает более 30 видов, среди них A. israelii, A. gerencseriae, A. naeslundii, A. viscosus, A. bovis и мн. др.
По морфологической организации актиномицеты сходны с грибами (название «actinomyces» происходит от двух слов: actis – луч и myces – гриб), однако генетический аппарат у них представлен нуклеоидом.
Морфология
Актиномицеты могут быть представлены прямыми или изогнутыми палочками, часто образуют нити. Имеют ветвистый несептированный субстратный или воздушный мицелий со спорами. Неподвижны, размножаются спорами, почкованием, фрагментацией. Некоторые актиномицеты могут образовывать полисахаридную капсулу вокруг нитей мицелия.
Грамположительны, есть варианты кислотоустойчивые и кислоточувствительные, В поражённых тканях они образуют друзы (переплетающийся мицелий).
Культуральные свойства
Среди актиномицетов встречаются факультативные и строгие анаэробы, последние чаще являются патогенными. Для своего роста актиномицеты нуждаются в СО2. Оптимальная температура роста 35-370С. Рост медленный, от 7 до 14 дней. Могут диссоциировать на R- и S-формы, давать гладкие и паукообразные колонии.
Хорошо растут на кровяном, сывороточном агаре, среде Сабуро. На кровяном агаре многие виды дают гемолиз, на других плотных средах молодые колонии плоские, легко снимающиеся с агара, зрелые культуры могут быть бугристыми, крошковидными, они более плотно связаны со средой.
Актиномицеты часто имеют пигменты различного цвета (красного, фиолетового, зеленого).
Биохимические свойства
Биохимические свойства вариабельны и отличаются у разных видов. Актиномицеты обладают сахаролитической и протеолитической активностью. Наиболее вирулентные возбудители относятся к строгим анаэробам.
Антигенная структура
Имеют видовой антиген клеточной стенки. По антигенной структуре актиномицеты разделены на 5 серогрупп (А, В, D, Е, F).
Распространение и экология
Актиномицеты входят в состав нормальной анаэробной микрофлоры ротовой полости, желудочно-кишечного тракта, влагалища, много их в строме зубного камня, криптах миндалин, слюнных железах, в конкрементах (камнях) желчевыводящих и мочевых путей. Они естественным путём выделяются в окружающую среду, где могут размножаться при температуре от 3-70С до 400С и сохраняться длительное время. В природе они встречаются во всех географических широтах.
Данные бактерии играют важную роль в экологии почвы, вызывая деградацию растительных остатков, лигнина, хитина. Среди актиномицетов есть штаммы, которые продуцируют антибиотики, бактериоцины, витамины.
Резистентность
Актиномицеты – это резистентные микроорганизмы, они малочувствительны к высушиванию, замораживанию и оттаиванию. Антисептики действуют на них в высоких концентрациях, как и на споровые культуры.
Характеристика заболеваний
Актиномицеты, как представители нормальной микрофлоры, в целом отличаются невысокой вирулентностью.
Однако многие из них могут стимулировать воспалительные процессы различной локализации, в первую очередь, в ротовой полости и челюстно-лицевой области. В большинстве случаев – это неспецифические смешанные инфекции, обусловленные разными видами возбудителей.
В развитии болезней периодонта участвуют A. israelii, A. gerencseriae, A. naeslundii, A. viscosus, A. odontolyticus.
В отдельных случаях актиномицеты могут вызывать урогенитальные инфекции, особенно у женщин, применяющих внутриматочные контрацептивы. Возможны инфекции органов брюшной полости после оперативных вмешательств или травм.
Специфическая инфекция или актиномикоз – это хроническое гранулематозное гнойное поражение различных систем и органов, которое характеризуется инфильтрацией тканей с последующим нагноением и возможным образованием свищей.
Основными возбудителями актиномикоза человека являются A. israelii, реже A. naeslundii, A. viscosus, A. meyeri.
Заболевание может развиваться в результате экзогенного и эндогенного инфицирования, часто в результате аутоинфекции на фоне иммунодефицитов, травм, гнойно-воспалительных поражений.
Источник инфекции – инфицированные люди или животные.
Пути передачи – воздушно-капельный, контактный, реже алиментарный.
Входные ворота – кожа и слизистые. Развитие инфекции связано с нарушением целостности покровных тканей.
Возбудитель распространяется гематогенно и лимфогенно. В тканях актиномицеты образуют друзы, вокруг них скапливаются лейкоциты, формируется грануляционная ткань, в которой много плазматических, эпителиоидных клеток и фибробластов. В центре друз происходит некроз клеток, распад тканей. Могут присоединяться вторичные инфекции за счет гноеродных кокков. При метастазировании актиномицетов в головной мозг или средостение заболевание часто заканчивается летально (рис. 16).
В зависимости от локализации различают несколько клинических форм заболевания: шейно-лицевую, торакальную, абдоминальную и т.д.
Течение заболевания утяжеляется иммунодефицитами, аутоиммунными реакциями и ГЧЗТ.
Иммунитет
Иммунитет при актиномикозе не формируется. Антитела не выполняют защитной функции.
Лабораторная диагностика
Материал для исследования: гной из свищей, мокрота, трупный материал и др.
Бактериоскопический метод. Готовят препарат «раздавленная капля», эмульгируя материал в 10-20%. Можно готовить мазки и окрашивать их по Романовскому-Гимзе. Обнаруживаются друзы или нити тонкого несептированного неветвящегося мицелия.
Бактериологический метод. Материал засевают на кровяной, сывороточный агары, среду Сабуро или сердечно-мозговой бульон. Посевы инкубируют 1-2 недели в аэробных и анаэробных условиях. Идентификацию проводят с учётом культуральных, биохимических и антигенных свойств.
Аллергический метод. Определяют ГЧЗТ в кожной пробе с актинолизатом.
Серологический метод. В парных сыворотках выявляют нарастание титра антител в ИФА, РСК, РПГА.
Лечение
Возбудители сохраняют чувствительность к пенициллину, можно использовать доксициклин или сульфаниламиды. Длительность приёма лекарственных средств составляет не менее 4-6 недель. Также применяют хирургические методы – иссечение пораженных тканей.
Профилактика заболевания только неспецифическая.
14.5. Листерии
В 1924 г. Э. Мюррей из крови лабораторных животных выделил новый вид грамположительных палочек, которые были названы Bacterium monocytogenes. В 1929 г. А. Нифельдт выделил аналогичного возбудителя от человека с ангиной и высоким моноцитозом. В 1940 г. по предложению Дж. Пири род возбудителя был назван Listeria, а заболевание получило название «листериоз».
Классификация
Возбудители относятся к семейству Listeriaceae, роду Listeria. Род включает 6 видов, среди них L. monocytogenes, L. ivanovii, L. murrayi и др. Типовым видом является L. monocytogenes, представители которого выделяются от человека и животных и могут вызывать у них заболевания.
Морфология
Листерии представляют собой мелкие грамположительные палочки или коккобактерии. Они не имеют спор, капсулы, являются перитрихами (образуют 1-5 жгутиков). Подвижность максимальна при 20-28оС. В мазках могут располагаться беспорядочно, под углом друг к другу, цепочками или параллельными рядами.
Культуральные свойства
Возбудители культивируются при 35-37оС на кровяном, шоколадном агаре, триптиказо-соевом бульоне и агаре, тиогликолевой среде. Могут расти и при более низких температурах. Инкубация длится 5-7 дней с ежеденевным контролем роста.
На кровяном агаре образуют мелкие (до 1 мм) полупрозрачные колонии, которые дают узкие зоны β-гемолиза. При росте на большинстве сред колонии напоминают капли росы.
Для улучшения условий выделения применяют селективные среды с антисептиками и антибиотиками (акрифлавином, полимиксином, налидиксовой кислотой.)
Бактерии могут диссоциировать на S- и R-формы. S-формы – это мелкие, круглые, слабовыпуклые, полупрозрачные колонии; R-формы – шероховатые, грубозернистые колонии с неровными краями.
На жидких средах листерии дают равномерное помутнение с последующим образованием осадка.
Биохимические свойства
Относятся к факультативным анаэробам. Возбудители каталазоположительны.
Выражена сахаролитическая активность. Разлагают до кислоты глюкозу, мальтозу, медленно ферментируют сахарозу, глицерин и лактозу. Не разлагают маннит и крахмал.
Не образуют индола и сероводорода, не восстанавливают нитраты в нитриты.
Антигенная структура
Листерии имеют соматический, термостабильный О-антиген и жгутиковый термолабильный Н-антиген. Известно 13 различных сероваров.
Факторы патогенности
Микробные адгезины и тейхоевые кислоты ответственны за адсорбцию возбудителя на клетках. Ведущим адгезином является белок интерналин.
Основным токсином листерий является гемолизин или О-листериолизин. Он повреждает мембраны клеток (порообразующий токсин) и обеспечивает выход листерий из фагосом при фагоцитозе. Сходным действием обладают ферменты фосфолипазы.
Поверхностный белок ActA вызывает полимеризацию актина в пораженных клетках, что обусловливает внутриклеточную подвижность листерий и их межклеточное распространение.
О-листериолизин, фосфолипазы и белок ActA кодируются генами хромосомного острова патогенности листерий.
Микробные сидерофоры обеспечивают возбудителей ионами железа.
Гликолипидный аналог эндотоксина стимулирует воспаление.
Резистентность
Возбудители обладают значительной резистентностью. Они длительное время сохраняются в почве и сточных водах, способны размножаться в фекалиях и органических растительных остатках. В сравнении с другими бесспоровыми бактериями листерии устойчивы к нагреванию, высушиванию, замораживанию.
Патогенез и характеристика заболевания
Листериоз – это зоонозное заболевания, которое сопровождается поражением иммунной и нервной системы с вовлечением внутренних органов и последующей септицемией.
Листериоз – болезнь с природной очаговостью. Резервуаром возбудителя в природе являются многие виды грызунов.
Источниками инфекции могут быть многие домашние и дикие животные, птицы (всего более 50 видов).
Пути передачи заболевания – человек заражается чаще всего алиментарным путём через загрязнённую возбудителем воду и пищевые продукты, реже – воздушно-капельным и контактным путями при разделывании мяса, обработке шкур и даже транссмиссивным через клещей и других кровососущих членистоногих.
Возможен вертикальный путь заражения от больной матери, риск заражения плода при беременности увеличивается более чем в 10 раз.
Инфицирующая доза у чувствительных лиц невелика (менее 1000 микроорганизмов).
Инкубационный период может длиться от нескольких дней до 2-3 недель.
Бактерии попадают в организм человека через воздухоносные пути, желудочно-кишечный тракт, слизистые зева, глаз, через поврежденную кожу.
Листериоз – это внутриклеточная инфекция. Микробные адгезины обеспечивают плотное прикрепление возбудителя к эпителию. Мембранными рецепторами для интерналина листерий являются клеточные молекулы-кадгерины. Связывание интерналина приводит к захвату и фагоцитозу листерий эпителиальными клетками, макрофагами и моноцитами, нейтрофилами.
После попадания листерий внутрь клеток они разрушают мембрану фагосомы при помощи О-листериолизина и выходят в цитоплазму фагоцитов. Это предохраняет бактерии от переваривания.
При 37оС в клетках организма человека бактерии теряют подвижность. Однако листериозный белок ActA полимеризует внутриклеточный актин, вызывая образование актиновых филаментов. Филаменты прикрепляются к полюсу микробной клетки. Образуется «актиновая комета» (или «пропеллер»), которая обеспечивает внутриклеточную подвижность листерий.
Пораженные клетки эпителия образуют мембранные выросты или филоподы, через которые листерии заражают соседние клетки.
В результате инфицирования макрофагов, моноцитов, нейтрофилов бактерии распространяются в организме, проникают в кровь, лимфу. Могут поражать миндалины, печень, селезёнку, легкие, надпочечники, центральную нервную систему.
Клинические проявления заболевания очень разнообразны. Развивается лихорадка. Локальная форма листериоза протекает по типу гастроэнтерита.
Чаще встречается ангино-септическая форма, реже нервная, глазо-железистая. Отмечаются пневмонии, менингиты.
Листериоз у беременных часто ведет к гибели плода, спонтанным абортам и невынашиванию. У новорожденных возникает септико-гранулематозная форма болезни или листериозный менингит.
Прогноз заболевания обычно благоприятный, однако при развернутой клинической картине болезни летальность остается весьма высокой – 25-30%. При листериозной септицемии летальность превышает 50%, при менигите – более 70%.
Иммунитет
Иммунитет носит клеточный характер, в меньшей степени – гуморальный. Считается, что большинство взрослого населения имеет сенсибилизированные лимфоциты к возбудителю.
После заболевания формируется долгоживущий клон клеток памяти, это обеспечивает стойкий иммунитет.
Лабораторная диагностика
Материал зависит от стадии и формы заболевания. Исследуют слизь из зева, пунктат увеличенных лимфоузлов, кровь, ликвор, у новорожденных – пуповинную кровь. При гибели плода исследуют секционный материал.
Предварительный диагноз некоторых форм листериоза может быть установлен при бактериоскопии амниотической жидкости или ликвора с окраской по Граму.
Бактериологический метод. Исследуемый материал засевают на глюкозо-печёночный или глюкозо-глицериновый бульон. Культивируют при 370С до трёх недель. Суточные колонии, имеющие зоны гемолиза, изучают под микроскопом. Затем пересевают на глюкозо-кровяной агар или другие плотные среды.
Выделенную культуру идентифицируют по морфологическим, культуральным, тинкториальным, биохимическим и антигенным свойствам в реакции агглютинации. Возможно использование систем автоматизированной биохимической идентификации возбудителей.
Таблица
Основные характеристики, используемые для дифференциации L.monocytogenes от других видов листерий
| Признак | L.monocytogenes | L.ivanovii | L.seeligeri | L.innocua | L.welshimeri | L.grayi |
| Ферментация маннита Ферментация ксилозы Ферментация рамнозы | - - + | - + - | - + - | - - +/- | - + +/- | + - +/- |
| Бета-гемолиз | + | + | + | - | - | - |
| САМР-тест - усиление гемолиза около штриха: Rhodococcus equi Staphylococcus aureus | -/+ + | + + | - + | - - | - - | -/+ - |
| Гидролиз лецитина без угля Гидролиз лецитина с углем | - + | + + | - - | - - | - - | - - |
| Патогенность для человека | Высокая | Низкая | Отсуствует | |||
Серологический метод используют со второй недели заболевания в динамике. Ставят РСК, реакцию агглютинации, ИФА или непрямую РИФ.
Экспресс-диагностика. Для выявления антигена в исследуемом материале используют РИФ. Можно использовать полимеразную цепную реакцию (ПЦР) для определения нуклеиновых кислот возбудителя.
Реже применяют биологическую пробу на белых мышах. После гибели мышей делают протокольные посевы из внутренних органов трупа, выделяют и идентифицируют культуру.
Лечение
Возбудитель устойчив к цефалоспоринам, умеренно устойчив к фторхинолонам. Лечение проводится бензилпенициллином или амоксициллином, возможна комбинация с макролидами. При аллергии на β-лактамы применяют ко-тримоксазол, доксициклин.
Профилактика только неспецифическая. Она сводится к комплексу санитарно-ветеринарных мероприятий, проводимых в животноводческих хозяйствах, на бойнях. В очагах проводят дератизацию, уничтожение бродячих кошек и собак. В неблагоприятных по листериозу районах молочные продукты подлежат обязательной термической обработке.
studfiles.net
Реферат: "Возбудители атипичных микобактериозов"
Выдержка из работы
Министерство Здравоохранения Республики Казахстан
АО «Медицинский Университет Астана»
Кафедра: микробиологии и вирусологии им. Ш. И. Сарбасовой
Реферат
На тему: «Возбудители атипичных микобактериозов»
Выполнила: Мендигалиева С. Н.
Группа 246 ОМ
Проверила: Акимбекова Г. М.
Астана 2012
Введение
В последнее время клиницисты все чаще говорят о случаях нерасшифрованных хронических заболеваний, напоминающих по течению туберкулез, но не поддающихся лечению противотуберкулезными препаратами. Терапия антибиотиками и химиопрепаратами ранее неизлечимых или трудно излечимых болезней повлекла за собой выявление и описание новых, ранее неизвестных или редко встречавшихся нозологических форм. К их числу следует отнести кандидоз, нокардиоз и микобактериоз, которые часто являются следствием бесконтрольной антибиотико- и химиотерапии. В процессе лечения антибиотики широкого спектра действия, подавляя жизнедеятельность возбудителей, не щадят и чувствительные к лекарствам микробы нормальной микрофлоры человека. Остающиеся при этом или попадающие извне устойчивые к медикаментам микроорганизмы (к ним относятся дрожжеподобные грибы рода Кандида, сапрофитные и потенциально патогенные микобактерии, нокардии и др.) не испытывая на себе сдерживающего влияния антагонистов (из числа представителей нормальной микрофлоры человека), приживаются и накапливаются в организме. Если последний ослаблен предыдущим острым или хроническим заболеванием, то эти микроорганизмы могут вызвать тяжелый процесс, который при неправильной или запоздалой диагностике может принять неблагоприятное течение и привести к смерти.
Атипические микобактериозы
Атипические микобактериозы представляют собой заболевания, по клинике и рентгенологическим признакам близкие к туберкулезу. Их возбудителями являются кислотоустойчивые микобактерии, которые по культуральным, биохимическим свойствам и вирулентности отличаются от микобактерии туберкулеза.
Они обладают естественной лекарственной устойчивостью ко многим противотуберкулезным препаратам широкого спектра действия. В отличие от возбудителя туберкулеза они патогенны для белых мышей и крыс и не патогенны для морской свинки и кролика.
Изучение биологических свойств этих микобактерии выявило, что они представляют большую группу, состоящую из многих видов, которую объединили под общим названием «атипичные» микобактерии. Для человека атипичные микобактерии потенциально патогенны.
Пока еще не существует единого мнения об их происхождении. Установленное генетическое родство некоторых атипичных микобактерии с возбудителями туберкулеза позволяет рассматривать их как форму изменчивости микобактерии туберкулеза.
При этом одним из главных факторов, обусловливающих появление атипичных микобактерии, считается противотуберкулезная терапия.
Так, у детей и подростков при проведении антибактериальной терапии одновременно со значительным снижением высеваемости микобактерии отмечают повышение частоты обнаружения пигментных форм.
Обоснованно также и другое мнение, что атипичные микобактерии являются широко распространенными в природе самостоятельными видами, обладающими потенциальной патогенностью для человека и некоторых животных. Попадая извне в организм человека, они находят там особенно благоприятные условия для размножения при проведении антибактериальной терапии вследствие их устойчивости ко многим лекарственным препаратам.
Возбудители
В состав рода Mycobacterium семейства Mycobacteriaceae отдела Firmicutes включены неподвижные аэробные грамположительные палочковидные бактерии. Иногда они образуют нитевидные структуры, напоминающие мицелий грибов. Это и послужило основанием для их названия [греч. mykes, гриб и лат. bacterium, бактерия].
Для микобактерий характерно высокое содержание липидов, фосфатидов и восков в клеточных стенках (до 60%), что определяет их щёлоче-, спирто- и кисдотоустойчивость (признак особенно выражен у паразитических видов микобактерий).
Поэтому микобактерии плохо воспринимают анилиновые красители и обычные способы окрашивания. Для окраски применяют интенсивные методы, обычно Циля-Нильсена. Растут медленно или очень медленно; сапрофитические виды растут несколько быстрее. Некоторые виды образуют каротиноидные недиффундирующие в среду пигменты.
Классификация микобактерий по патогенности:
При классификации микобактерий учитывают патогенность для человека, способность к пигментообразованию, скорость роста и способность синтезировать никотиновую кислоту (ниацин).
* По патогенности выделяют собственно патогенные (вызывающие конкретные заболевания), потенциально патогенные и сапрофитические микобактерии. Патогенными для человека свойствами обладают М. tuberculosis, M. leprae, M. bovis. Прочие виды, вызывающие поражения у человека, известны как атипичные микобактерии.
* По скорости роста выделяют быстрорастущие (дают видимый рост на. 4−7-е сутки), медленнорастущие (рост наблюдают через 7−10 и более дней) и не растущие на искусственных средах (М. leprae) виды микобактерий.
* По способности образовывать пигменты выделяют фотохромогенные (образуют пигмент на свету), скотохромогенные (образуют пигмент в темноте) и нефотохромогенные (не образуют пигмента) виды микобактерий.
Возбудителей микобактериозов называются атипичными микобактериями:
ь -они не имеют корд-фактор,
ь -каталазо-термостабильны
ь -невирулентны для лабораторных животных
ь -некоторые растут быстро на простых питательных средах,
ь -часто устойчивы к противотуберкулёзным препаратам
M. canzasi | вызывают поражения лёгких | |
М. ulcerans | язвы на конечностях | |
M. avium | поражения лёгких, могут вызывать диарею часто даёт осложнения при СПИДе | |
M. fortuitum | вызывает поражения кожи, может присоединяться к постоперационным инфекциям, вызывать сепсис | |
Экология и распространение
возбудитель атипичный микобактериоз
В окружающей среде существует много атипичных потенциально патогенных микобактерий. Часть из них выделяется от людей и животных при различных заболеваниях легких, кожи, лимфатических узлов, других тканей и органов. Они получили общее название микобактериозы. Роль условно-патогенных микобактерий в инфекционной патологии человека растет с каждым годом. В эту группу заболеваний не входят туберкулез и проказа, хотя некоторые из них имеют сходный ход. Существующие методы лечения туберкулеза и микобактериозов разные, в связи с чем микробиологическая идентификация возбудителей приобретает особое значение. По классификации Раньйона атипичные микобактерии делятся на 4 группы: фотохромогенни, скотохромогенни, нефотохромогенни и быстрорастущие. К фотохромогенних микобактерий принадлежат Mycobacterium kansasii, М. marinum, М ulcerans, М simiae, М. szulgaL Все они кислотостойкие, образуют желто-оранжевый пигмент на свету, вызывают туберкульозоподибни заболевания легких, лимфадениты, поражения кожи и подкожной клетчатки. М ulcerans, например, вызывает язву Бурул. Скотохромогенни микобактерии (М scrofulaceum, М aquae, М flavescensTb др.). Образуют желто-оранжевый пигмент в темноте, вызывают шейные лимфадениты у детей, реже патологические процессы в легких. Нефотохромогенни вида — М avium, М. intracellular, М хепори — имеют очень слабую пигментацию колоний, или они вовсе не окрашены, вызывают туберкульозоподибни заболевания легких, кожи, почек, костей и суставов, опасны для больных с иммунодефицитами, особенно при ВИЧ-инфекции. Они вызывают туберкулез у птиц и редко у человека (М avium).В группу быстрорастущих микобактерий отнесены M. fortuitum, М. friedmanii, М. malmoense, М. smegmatis, М. phlei. Они причастны к возникновению абсцессов после инъекций у наркоманов, воспаления вокруг вживленных объектов (например, протезов сердечных клапанов). Поражение легких и лимфадениты у детей вызывает М. malmoense. Практическое значение в плане дифференциации различных видов микобактерий имеет М. smegmatis, особенно при лабораторной диагностике заболеваний мочеполовой системы.
Клинические проявления
Наиболее часто встречается микобактериоз легких, которым заболевают главным образом пожилые люди. Описаны отдельные случаи микобактериоза легких у лиц более молодого возраста и даже у подростков.
Второе место по частоте занимают поражения лимфатических узлов. В противоположность легочному микобактериозу лимфаденит, вызываемый потенциально патогенными микобактериями, наблюдается преимущественно у детей. В литературе описаны также заболевания мочеполовой системы, костей и суставов, мозговой оболочки и кожи той же этиологии.
Как показали многие исследователи, заболевания, причиной которых являются потенциально патогенные микобактерии, по клинической картине и течению весьма сходны с заболеваниями, вызываемыми микобактериями туберкулеза. Возможны образование каверн, кровотечения и кровохарканье. Микобактериоз характеризуется хроническим течением и часто сопровождается эмфиземой. Однако наряду с хроническими, продолжающимися годами процессами наблюдаются острые тяжелые заболевания, нередко завершающиеся смертью. Основной причиной смерти, по мнению некоторых исследователей, является легочное сердце.
По клинической картине микобактериоз можно разделить на три группы:
1) собственно микобактериоз, т. е. заболевание, вызванное одним из видов потенциально патогенных микобактерии;
2) смешанные формы (туберкулез + микобактериоз), при которых в выделениях больного обнаруживаются 2 возбудителя, чаще всего М. tuberculosis и М. avium;
3) последовательное развитие заболеваний, когда на фоне затихшего туберкулезного процесса возникает новое заболевание -- микобактериоз.
Микробиологическая диагностика
Материалом для исследования служит мокрота, содержимое язв и других поражений кожи, пунктаты лимфатических узлов, промывные воды бронхов, моча и др. Лабораторные исследования проводятся по тем же принципам и методам, что и при туберкулезе. После первичной микроскопии материал сеют на среды Левенштейна-Иенсена. Финна и обязательно на среду с салицилатом натрия. Перед посевом патологический материал обрабатывают 15−20 мин 2−5% раствором серной кислоты или 10% раствором фосфата натрия в течение 18−20 ч при 37 ° С. Атипичные микобактерии более чувствительны к такой обработки, чем палочки туберкулеза. Если обрабатывать мокроты малахитовым зеленым или генциановый фиолетовым — выделения возбудителей микобактериозов увеличивается в 3−4 раза. Для идентификации микобактерий предложено много тестов. Однако в бактериологических лабораториях практических медицинских учреждений использовать их просто невозможно. Зачастую для установления вида возбудителя учитывают цвет колоний, скорость роста субкультур, рост при различных температурах и особенно в среде с салицилатом натрия, определения каталазы, синтеза ниацина и др. Практически все виды микобактерий дают рост на среде с салицилатом натрия, в то время как возбудители туберкулеза на нем не растут. Ниацин синтезирует лишь М. tuberculosis, а возбудители микобактериозов не образуют никотиновой кислоты. Разработаны методы идентификации микобактерий в реакциях преципитации и фаголизису. Серологические реакции для диагностики микобактериозов, особенно такие как РСК, РИФ, РНГА, можно будет использовать при условии изготовления специфических тест-систем. Большие возможности для определения возбудителей этих заболеваний открывает внедрение полимеразной цепной реакции.
Профилактика и лечение
Несмотря на то, что микобактериоз вызывается микробами со слабой вирулентностью для человека, и эти заболевания не передаются от человека к человеку, они требуют большого внимания, так как специфической противотуберкулезной терапии они не поддаются (благодаря наличию у возбудителей широкого спектра лекарственной устойчивости). Интенсивная противотуберкулезная терапия без учета лекарственной устойчивости возбудителей таким больным только вредит.
Большинство возбудителей микобактериоза устойчиво к тубазиду, стрептомицину и ПАСК. Некоторая часть возбудителей обладает чувствительностью к циклосерину, рифампицину и зтионамиду. Лечение больных микобактериозом чрезвычайно трудно; нередко при ограниченном процессе приходится прибегать к хирургическому лечению на фоне общеукрепляющей терапии.
Многочисленные виды микобактерий живут в окружающей нас природе, являются возбудителями заболеваний птиц, теплокровных и холоднокровных животных. Некоторые из этих микобактерий потенциально патогенны для человека. Из литературы известно, что контакт с больной птицей и домашним скотом, использование сырого молока и других продуктов питания от больных животных могут способствовать микобактериозу.
Только раннее выявление микобактериоза может привести к его успешному лечению. К сожалению, до настоящего времени эти заболевания нередко остаются нераспознанными и больных лечат по поводу самой различной ошибочно предполагаемой патологии. Число больных микобактериозом продолжает постоянно увеличиваться, и не случайно его относят к болезням будущего.
Заключение
Микобактериоз обычно развивается только в ослабленном организме, ранее поврежденном каким-либо неблагоприятным воздействием. Так, большую роль в развитии микобактериоза у людей играет запыление атмосферы. Это заболевание чаще встречается у лиц, профессии которых связаны с работой в помещениях с повышенным содержанием пыли (шахтеры, литейщики, углекопы). Среди рабочих этих специальностей наблюдаются пневмокониоз, силикоз и другие заболевания, ослабляющие легочную ткань. Именно при таких условиях легко развиваются заболевания, вызванные менее вирулентными, но потенциально патогенными микобактериями. Развитию микобактериоза могут способствовать саркоидоз и эмфизема. Ослабление всего организма, а также лечение кортикостероидными препаратами также могут быть косвенной причиной возникновения микобактериоза.
Показать Свернутьreferat.bookap.info
Реферат Микобактерии
Реферат на тему:
План:
- Введение
- 1 Биологическое описание
- 1.1 Пигментация
- 2 Патогенные виды
- 3 Представители рода микобактерий
- 3.1 Медленно растущие
- 3.1.1 Микобактерии туберкулёзного комплекса (MTBC)
- 3.1.2 Микобактерии avium-комплекса (MAC)
- 3.1.3 Gordonae-ветвь
- 3.1.4 Kansasii-ветвь
- 3.1.5 Нехромогенные/terrae-ветвь
- 3.1.6 Mycolactone-producing mycobacteria
- 3.1.7 Simiae-ветвь
- 3.1.8 Некатегоризированные
- 3.2 Со средним временем роста
- 3.3 Быстро растущие
- 3.3.1 Сhelonae-ветвь
- 3.3.2 Fortuitum-ветвь
- 3.3.3 Parafortuitum-ветвь
- 3.3.4 Vaccae-ветвь
- 3.3.5 CF-ветвь
- 3.3.6 Некатегоризированные
- 3.4 Некатегоризированные
ЛитератураПримечания - 3.1 Медленно растущие
Введение
Микобакте́рии (Mycobacteriaceae) — семейство актиномицетов. Единственный род — Mycobacterium. Некоторые представители рода Mycobacterium (напр. M. tuberculosis, M. leprae) патогенны для млекопитающих[1] (см. туберкулёз, микобактериоз, лепра).
Латинский префикс «myco-» означает как гриб, так и воск; в данном случае понятие отражает «воскоподобные» компоненты, составляющие часть клеточной стенки микобактериальных клеток.
1. Биологическое описание
Микобактерии аэробны и неподвижны (исключая вид Mycobacterium marinum, который демонстрирует подвижность вне макрофагов), и характеризуются кислото- и спиртоустойчивостью.[1] Микобактерии не содержат спор и капсул, и их принято считать грам-положительными бактериями. Согласно недавнему исследованию была показана возможность спорообразования у представителей Mycobacterium marinum и, возможно, у M.bovis [2]. Однако, данная работа была признана спорной [3]. Микобактерии не являются грам-положительными бактериями с эмпирической точки зрения (то есть большая часть видов не прокрашивается кристаллвиолетом достаточно хорошо), но они классифицируются, как кислотоустойчивые грам-положительные бактерии, в связи с отсутствием у них внешней клеточной мембраны. Все виды рода Mycobacterium характеризуются особой клеточной стенкой, более тонкой, гидрофобной, с наличием в ее составе восков, и богатой миколовыми кислотами/миколатами.
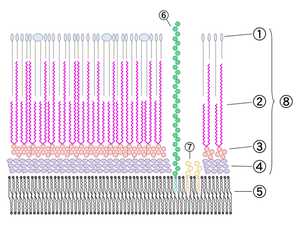
клеточная стенка микобактерии: 1-внешние липиды, 2-миколовые кислоты, 3-полисахариды (арабиногалактан), 4-пептидогликан, 5-билипидный слой, 6-липоарабиноманнан (LAM), 7-маннозиды фосфатидилинозита, 8-клеточная стенка
Клеточная стенка, помимо гидрофобных миколатов, в значительной степени состоит из сложных полисахаридов, некоторые из которых имеют для жизнедеятельности клетки особое значение. Терминальные фрагменты липоарабиноманнана, прежде всего его маннозные радикалы, неспецифически подавляют активацию Т-лимфоцитов и лейкоцитов периферической крови животных, что приводит к нарушению иммунного ответа на микобактерии.[4]. В ходе эволюции микобактерии выработали различные механизмы преодоления или инактивации неблагоприятных факторов внешней среды. Во-первых, это особая клеточная стенка. Во-вторых, это обширные метаболические возможности. Они способны инактивировать многие клеточные токсины и вещества (различные перекиси, альдегиды и другие), разрушающие клеточную оболочку. В-третьих, это морфологическая пластичность, заключающаяся в трансформации микобактерий (образование L-форм, дормантных клеток). По своей устойчивости, после спорообразующих бактерий, они занимают лидирующее место в царстве прокариот. Клетки сохраняют свою жизнеспособность в сухом состоянии до 3 лет. При нагревании некоторые виды микобактерий могут выдерживать температуру существенно выше 80 °С. Микобактерии туберкулёза устойчивы к органическим и неорганическим кислотам, щёлочам, многим окислителям, а также к ряду антисептических и дегидратирующих веществ, оказывающих губительное действие на другие патогенные микроорганизмы. Микобактерии проявляют устойчивость к воздействию спиртов и ацетона. Отмечено, что средства на основе четвертичного аммония не проявляют антимикобактериальной активности. В определённых условиях концентрации радикалов хлора и кислорода до 0,5 % также не оказывают губительного действия на микобактерии.
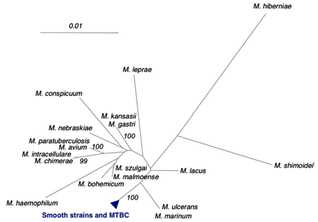
Филогенетическая позиция туберкулёзной палочки в пределах рода. Голубой треугольник свидетельствует о наличии последовательностей, идентичных или отличающихся в пределах одного нуклеотида. Последовательности ДНК рода Mycobacterium очень близки к аналогичным от микобактерий туберкулёза, которые были получены из базы данных BIBI (http://pbil.univ-lyon.fr/bibi/) и сопоставлены с результатами, полученными на 17 гладких и MTBC штаммов. Некорневые бифуркации дерева основаны на 1’325 соответствие нуклеотидной позиции гена 16S рРНК. Шкала дает попарные расстояния после коррекции Джукс-Кантора. Bootstrap support values higher than 90 % are indicated at the nodes.
Микобактерии туберкулёза нечувствительны к рассеянному солнечному свету и могут более года существовать во внешней среде без потери жизнеспособности. Коротковолновое ультрафиолетовое изучение оказывает универсальное бактерицидное действие на все микроорганизмы. Однако в реальных условиях, когда микобактерии туберкулёза находятся во взвешенном состоянии в виде клеточных агломератов с пылевыми частицами, их устойчивость к ультрафиолетовому излучению возрастает.[4]
Уникальность и ключевая роль миколовых кислот в структурной организации и физиологии микобактерий делают их отличной мишенью для этиотропной терапии.[5]
Размножаются делением клеток. Широко распространены в почве. Сапрофитные формы участвуют в минерализации органических остатков, некоторые окисляют парафины и другие углеводороды. Могут использоваться для борьбы с загрязнением биосферы нефтью.[6].
1.1. Пигментация
Согласно классификации Раньона нетуберкулёзных микобактерий на основе культуральных различий от 1959 г., по продукции пигмента колониями выделяют 4 группы микобактерий:
Фотохромогенные (Группа I) микобактерии, не пигментированные при выращивании в темноте, но приобретающие ярко-жёлтую или жёлто-оранжевую пигментацию после выдерживания или реинкубации на свету.- Ex: M. kansasii, M. marinum, M. simiae, M. asiaticum.
- Ex: M. scrofulaceum, M. gordonae, M. xenopi, M. szulgai.
- Ex: M. tuberculosis, M. avium, M.intra-cellulare, M. bovis, M. ulcerans
- Ex: M. chelonae
- Ex: M. phlei, M. smegmatis, M. fortuitum
2. Патогенные виды
Патогенные виды вызывают болезни человека (туберкулёз, лепру, микобактериозы) и животных. Всего известно 74 вида таких микобактерий. Они широко распространены в почве, воде и среди людей.
Туберкулёз у человека вызывают Mycobacterium tuberculosistypus (человеческий вид), Mycobacterium bovis (бычий вид) и Mycobacterium africanum (промежуточный вид). Эти виды способны проникать, жить и размножаться внутри человека.
Лепру (проказу) вызывает вид Mycobacterium leprae.
3. Представители рода микобактерий
В старой системе, микобактерии классифицировались, в зависимости от их свойств и скорости роста на питательных средах. Однако более новая номенклатура базируется на кладистике.
3.1. Медленно растущие
3.1.1. Микобактерии туберкулёзного комплекса (MTBC)
- Mycobacterium tuberculosis complex (MTBC) представители комплекса патогенны для человека и животных, и вызывают заболевание туберкулёз. Комплекс включает: M. tuberculosis, наиболее опасен для человека, как возбудитель туберкулёза M. bovis M. bovis BCG M. africanum M. canetti M. caprae M. microti M. pinnipedii
3.1.2. Микобактерии avium-комплекса (MAC)
- Mycobacterium avium complex (MAC), виды, составляющие данный комплекс патогенны для человека и животных, и чаще вызывают диссеминивованные процессы внелегочной локализации, и являлись ранее одной из основных причин смерти больных СПИДом. Комплекс включает: M. avium M. avium paratuberculosis M. avium silvaticum M. avium «hominissuis» M. colombiense
3.1.3. Gordonae-ветвь
3.1.4. Kansasii-ветвь
3.1.5. Нехромогенные/terrae-ветвь
- M. hiberniae
- M. nonchromogenicum
- M. terrae
- M. triviale
3.1.6. Mycolactone-producing mycobacteria
- M. ulcerans
- M. pseudoshottsii
- M. shottsii
3.1.7. Simiae-ветвь
- M. triplex
- M. genavense
- M. florentinum
- M. lentiflavum
- M. palustre
- M. kubicae
- M. parascrofulaceum
- M. heidelbergense
- M. interjectum
- M. simiae
3.1.8. Некатегоризированные
- M. branderi
- M. cookii
- M. celatum
- M. bohemicum
- M. haemophilum
- M. malmoense
- M. szulgai
- M. leprae, которая вызывает лепру
- M. lepraemurium
- M. lepromatosis, другая (менее распространенная) причина лепры
- M. africanum
- M. botniense
- M. chimaera
- M. conspicuum
- M. doricum
- M. farcinogenes
- M. heckeshornense
- M. intracellulare
- M. lacus
- M. marinum
- M. monacense
- M. montefiorense
- M. murale
- M. nebraskense
- M. saskatchewanense
- M. scrofulaceum
- M. shimoidei
- M. tusciae
- M. xenopi
3.2. Со средним временем роста
3.3. Быстро растущие
3.3.1. Сhelonae-ветвь
- M. abscessus
- M. chelonae
- M. bolletii
3.3.2. Fortuitum-ветвь
- M. fortuitum
- M. fortuitum subsp. acetamidolyticum
- M. boenickei
- M. peregrinum
- M. porcinum
- M. senegalense
- M. septicum
- M. neworleansense
- M. houstonense
- M. mucogenicum
- M. mageritense
- M. brisbanense
- M. cosmeticum
3.3.3. Parafortuitum-ветвь
- M. parafortuitum
- M. austroafricanum
- M. diernhoferi
- M. hodleri
- M. neoaurum
- M. frederiksbergense
3.3.4. Vaccae-ветвь
3.3.5. CF-ветвь
3.3.6. Некатегоризированные
- M. confluentis
- M. flavescens
- M. madagascariense
- M. phlei
- M. smegmatis
- M. thermoresistibile
- M. gadium
- M. komossense
- M. obuense
- M. sphagni
- M. agri
- M. aichiense
- M. alvei
- M. arupense
- M. brumae
- M. canariasense
- M. chubuense
- M. conceptionense
- M. duvalii
- M. elephantis
- M. gilvum
- M. hassiacum
- M. holsaticum
- M. immunogenum
- M. massiliense
- M. moriokaense
- M. psychrotolerans
- M. pyrenivorans
- M. vanbaalenii
- M. pulveris
3.4. Некатегоризированные
- M. arosiense
- M. aubagnense
- M. caprae
- M. chlorophenolicum
- M. fluoroanthenivorans
- M. kumamotonense
- M. novocastrense
- M. parmense
- M. phocaicum
- M. poriferae
- M. rhodesiae
- M. seoulense
- M. tokaiense
Литература
- Биологический энциклопедический словарь. М., Советская энциклопедия, 1989
- Перельман М. И., Корякин В. А., Богадельникова И. В. Фтизиатрия. ОАО Издательство «Медицина», 2004
Примечания
- ↑ 12Sherris Medical Microbiology. — 4th. — McGraw Hill, 2004. — ISBN 0-8385-8529-9
- Ghosh, Jaydip, Pontus Larsson, Bhupender Singh, B M Fredrik Pettersson, Nurul M Islam, Sailendra Nath Sarkar, Santanu Dasgupta, y Leif A Kirsebom. 2009. Sporulation in mycobacteria. Proceedings of the National Academy of Sciences of the United States of America 106, no. 26 (Junio 30): 10781-10786. http://www.ncbi.nlm.nih.gov/pubmed/19541637 - www.ncbi.nlm.nih.gov/pubmed/19541637
- Traag BA, Driks A, Stragier P, Bitter W, Broussard G, Hatfull G, Chu F, Adams KN, Ramakrishnan L, Losick R.2010. Do mycobacteria produce endospores? Proc Natl Acad Sci U S A. 2010 Jan 12;107(2):878-81.
- ↑ 12М. И. Перельман Национальное руководство. Фтизиатрия. — М.: ГЭОТАР-Медиа, 2007. — С. 75-91. — ISBN 978-5-9704-0490-4
- Mycobacterial Cell Wall Arabinogalactan // Bacterial Polysaccharides: Current Innovations and Future Trends. — Caister Academic Press, 2009. — ISBN 978-1-904455-45-5
- Ермоленко З.М., Холоденко В.П., Короткин Л.М. Штамм Mycobacterium flavescens ВКПМ В-6000, используемый для очистки воды и почвы от нефти и нефтепродуктов. - ru-patent.info/20/50-54/2053296.html = патент №2053296: Штамм Mycobacterium flavescens ВКПМ В-6000, используемый для очистки воды и почвы от нефти и нефтепродуктов. / Государственный научно-исследовательский институт прикладной микробиологии. — 1992.
wreferat.baza-referat.ru
Реферат: "Возбудители атипичных микобактериозов"
Выдержка из работы
Министерство Здравоохранения Республики Казахстан
АО «Медицинский Университет Астана»
Кафедра: микробиологии и вирусологии им. Ш. И. Сарбасовой
Реферат
На тему: «Возбудители атипичных микобактериозов»
Выполнила: Мендигалиева С. Н.
Группа 246 ОМ
Проверила: Акимбекова Г. М.
Астана 2012
Введение
В последнее время клиницисты все чаще говорят о случаях нерасшифрованных хронических заболеваний, напоминающих по течению туберкулез, но не поддающихся лечению противотуберкулезными препаратами. Терапия антибиотиками и химиопрепаратами ранее неизлечимых или трудно излечимых болезней повлекла за собой выявление и описание новых, ранее неизвестных или редко встречавшихся нозологических форм. К их числу следует отнести кандидоз, нокардиоз и микобактериоз, которые часто являются следствием бесконтрольной антибиотико- и химиотерапии. В процессе лечения антибиотики широкого спектра действия, подавляя жизнедеятельность возбудителей, не щадят и чувствительные к лекарствам микробы нормальной микрофлоры человека. Остающиеся при этом или попадающие извне устойчивые к медикаментам микроорганизмы (к ним относятся дрожжеподобные грибы рода Кандида, сапрофитные и потенциально патогенные микобактерии, нокардии и др.) не испытывая на себе сдерживающего влияния антагонистов (из числа представителей нормальной микрофлоры человека), приживаются и накапливаются в организме. Если последний ослаблен предыдущим острым или хроническим заболеванием, то эти микроорганизмы могут вызвать тяжелый процесс, который при неправильной или запоздалой диагностике может принять неблагоприятное течение и привести к смерти.
Атипические микобактериозы
Атипические микобактериозы представляют собой заболевания, по клинике и рентгенологическим признакам близкие к туберкулезу. Их возбудителями являются кислотоустойчивые микобактерии, которые по культуральным, биохимическим свойствам и вирулентности отличаются от микобактерии туберкулеза.
Они обладают естественной лекарственной устойчивостью ко многим противотуберкулезным препаратам широкого спектра действия. В отличие от возбудителя туберкулеза они патогенны для белых мышей и крыс и не патогенны для морской свинки и кролика.
Изучение биологических свойств этих микобактерии выявило, что они представляют большую группу, состоящую из многих видов, которую объединили под общим названием «атипичные» микобактерии. Для человека атипичные микобактерии потенциально патогенны.
Пока еще не существует единого мнения об их происхождении. Установленное генетическое родство некоторых атипичных микобактерии с возбудителями туберкулеза позволяет рассматривать их как форму изменчивости микобактерии туберкулеза.
При этом одним из главных факторов, обусловливающих появление атипичных микобактерии, считается противотуберкулезная терапия.
Так, у детей и подростков при проведении антибактериальной терапии одновременно со значительным снижением высеваемости микобактерии отмечают повышение частоты обнаружения пигментных форм.
Обоснованно также и другое мнение, что атипичные микобактерии являются широко распространенными в природе самостоятельными видами, обладающими потенциальной патогенностью для человека и некоторых животных. Попадая извне в организм человека, они находят там особенно благоприятные условия для размножения при проведении антибактериальной терапии вследствие их устойчивости ко многим лекарственным препаратам.
Возбудители
В состав рода Mycobacterium семейства Mycobacteriaceae отдела Firmicutes включены неподвижные аэробные грамположительные палочковидные бактерии. Иногда они образуют нитевидные структуры, напоминающие мицелий грибов. Это и послужило основанием для их названия [греч. mykes, гриб и лат. bacterium, бактерия].
Для микобактерий характерно высокое содержание липидов, фосфатидов и восков в клеточных стенках (до 60%), что определяет их щёлоче-, спирто- и кисдотоустойчивость (признак особенно выражен у паразитических видов микобактерий).
Поэтому микобактерии плохо воспринимают анилиновые красители и обычные способы окрашивания. Для окраски применяют интенсивные методы, обычно Циля-Нильсена. Растут медленно или очень медленно; сапрофитические виды растут несколько быстрее. Некоторые виды образуют каротиноидные недиффундирующие в среду пигменты.
Классификация микобактерий по патогенности:
При классификации микобактерий учитывают патогенность для человека, способность к пигментообразованию, скорость роста и способность синтезировать никотиновую кислоту (ниацин).
* По патогенности выделяют собственно патогенные (вызывающие конкретные заболевания), потенциально патогенные и сапрофитические микобактерии. Патогенными для человека свойствами обладают М. tuberculosis, M. leprae, M. bovis. Прочие виды, вызывающие поражения у человека, известны как атипичные микобактерии.
* По скорости роста выделяют быстрорастущие (дают видимый рост на. 4−7-е сутки), медленнорастущие (рост наблюдают через 7−10 и более дней) и не растущие на искусственных средах (М. leprae) виды микобактерий.
* По способности образовывать пигменты выделяют фотохромогенные (образуют пигмент на свету), скотохромогенные (образуют пигмент в темноте) и нефотохромогенные (не образуют пигмента) виды микобактерий.
Возбудителей микобактериозов называются атипичными микобактериями:
ь -они не имеют корд-фактор,
ь -каталазо-термостабильны
ь -невирулентны для лабораторных животных
ь -некоторые растут быстро на простых питательных средах,
ь -часто устойчивы к противотуберкулёзным препаратам
M. canzasi | вызывают поражения лёгких | |
М. ulcerans | язвы на конечностях | |
M. avium | поражения лёгких, могут вызывать диарею часто даёт осложнения при СПИДе | |
M. fortuitum | вызывает поражения кожи, может присоединяться к постоперационным инфекциям, вызывать сепсис | |
Экология и распространение
возбудитель атипичный микобактериоз
В окружающей среде существует много атипичных потенциально патогенных микобактерий. Часть из них выделяется от людей и животных при различных заболеваниях легких, кожи, лимфатических узлов, других тканей и органов. Они получили общее название микобактериозы. Роль условно-патогенных микобактерий в инфекционной патологии человека растет с каждым годом. В эту группу заболеваний не входят туберкулез и проказа, хотя некоторые из них имеют сходный ход. Существующие методы лечения туберкулеза и микобактериозов разные, в связи с чем микробиологическая идентификация возбудителей приобретает особое значение. По классификации Раньйона атипичные микобактерии делятся на 4 группы: фотохромогенни, скотохромогенни, нефотохромогенни и быстрорастущие. К фотохромогенних микобактерий принадлежат Mycobacterium kansasii, М. marinum, М ulcerans, М simiae, М. szulgaL Все они кислотостойкие, образуют желто-оранжевый пигмент на свету, вызывают туберкульозоподибни заболевания легких, лимфадениты, поражения кожи и подкожной клетчатки. М ulcerans, например, вызывает язву Бурул. Скотохромогенни микобактерии (М scrofulaceum, М aquae, М flavescensTb др.). Образуют желто-оранжевый пигмент в темноте, вызывают шейные лимфадениты у детей, реже патологические процессы в легких. Нефотохромогенни вида — М avium, М. intracellular, М хепори — имеют очень слабую пигментацию колоний, или они вовсе не окрашены, вызывают туберкульозоподибни заболевания легких, кожи, почек, костей и суставов, опасны для больных с иммунодефицитами, особенно при ВИЧ-инфекции. Они вызывают туберкулез у птиц и редко у человека (М avium).В группу быстрорастущих микобактерий отнесены M. fortuitum, М. friedmanii, М. malmoense, М. smegmatis, М. phlei. Они причастны к возникновению абсцессов после инъекций у наркоманов, воспаления вокруг вживленных объектов (например, протезов сердечных клапанов). Поражение легких и лимфадениты у детей вызывает М. malmoense. Практическое значение в плане дифференциации различных видов микобактерий имеет М. smegmatis, особенно при лабораторной диагностике заболеваний мочеполовой системы.
Клинические проявления
Наиболее часто встречается микобактериоз легких, которым заболевают главным образом пожилые люди. Описаны отдельные случаи микобактериоза легких у лиц более молодого возраста и даже у подростков.
Второе место по частоте занимают поражения лимфатических узлов. В противоположность легочному микобактериозу лимфаденит, вызываемый потенциально патогенными микобактериями, наблюдается преимущественно у детей. В литературе описаны также заболевания мочеполовой системы, костей и суставов, мозговой оболочки и кожи той же этиологии.
Как показали многие исследователи, заболевания, причиной которых являются потенциально патогенные микобактерии, по клинической картине и течению весьма сходны с заболеваниями, вызываемыми микобактериями туберкулеза. Возможны образование каверн, кровотечения и кровохарканье. Микобактериоз характеризуется хроническим течением и часто сопровождается эмфиземой. Однако наряду с хроническими, продолжающимися годами процессами наблюдаются острые тяжелые заболевания, нередко завершающиеся смертью. Основной причиной смерти, по мнению некоторых исследователей, является легочное сердце.
По клинической картине микобактериоз можно разделить на три группы:
1) собственно микобактериоз, т. е. заболевание, вызванное одним из видов потенциально патогенных микобактерии;
2) смешанные формы (туберкулез + микобактериоз), при которых в выделениях больного обнаруживаются 2 возбудителя, чаще всего М. tuberculosis и М. avium;
3) последовательное развитие заболеваний, когда на фоне затихшего туберкулезного процесса возникает новое заболевание -- микобактериоз.
Микробиологическая диагностика
Материалом для исследования служит мокрота, содержимое язв и других поражений кожи, пунктаты лимфатических узлов, промывные воды бронхов, моча и др. Лабораторные исследования проводятся по тем же принципам и методам, что и при туберкулезе. После первичной микроскопии материал сеют на среды Левенштейна-Иенсена. Финна и обязательно на среду с салицилатом натрия. Перед посевом патологический материал обрабатывают 15−20 мин 2−5% раствором серной кислоты или 10% раствором фосфата натрия в течение 18−20 ч при 37 ° С. Атипичные микобактерии более чувствительны к такой обработки, чем палочки туберкулеза. Если обрабатывать мокроты малахитовым зеленым или генциановый фиолетовым — выделения возбудителей микобактериозов увеличивается в 3−4 раза. Для идентификации микобактерий предложено много тестов. Однако в бактериологических лабораториях практических медицинских учреждений использовать их просто невозможно. Зачастую для установления вида возбудителя учитывают цвет колоний, скорость роста субкультур, рост при различных температурах и особенно в среде с салицилатом натрия, определения каталазы, синтеза ниацина и др. Практически все виды микобактерий дают рост на среде с салицилатом натрия, в то время как возбудители туберкулеза на нем не растут. Ниацин синтезирует лишь М. tuberculosis, а возбудители микобактериозов не образуют никотиновой кислоты. Разработаны методы идентификации микобактерий в реакциях преципитации и фаголизису. Серологические реакции для диагностики микобактериозов, особенно такие как РСК, РИФ, РНГА, можно будет использовать при условии изготовления специфических тест-систем. Большие возможности для определения возбудителей этих заболеваний открывает внедрение полимеразной цепной реакции.
Профилактика и лечение
Несмотря на то, что микобактериоз вызывается микробами со слабой вирулентностью для человека, и эти заболевания не передаются от человека к человеку, они требуют большого внимания, так как специфической противотуберкулезной терапии они не поддаются (благодаря наличию у возбудителей широкого спектра лекарственной устойчивости). Интенсивная противотуберкулезная терапия без учета лекарственной устойчивости возбудителей таким больным только вредит.
Большинство возбудителей микобактериоза устойчиво к тубазиду, стрептомицину и ПАСК. Некоторая часть возбудителей обладает чувствительностью к циклосерину, рифампицину и зтионамиду. Лечение больных микобактериозом чрезвычайно трудно; нередко при ограниченном процессе приходится прибегать к хирургическому лечению на фоне общеукрепляющей терапии.
Многочисленные виды микобактерий живут в окружающей нас природе, являются возбудителями заболеваний птиц, теплокровных и холоднокровных животных. Некоторые из этих микобактерий потенциально патогенны для человека. Из литературы известно, что контакт с больной птицей и домашним скотом, использование сырого молока и других продуктов питания от больных животных могут способствовать микобактериозу.
Только раннее выявление микобактериоза может привести к его успешному лечению. К сожалению, до настоящего времени эти заболевания нередко остаются нераспознанными и больных лечат по поводу самой различной ошибочно предполагаемой патологии. Число больных микобактериозом продолжает постоянно увеличиваться, и не случайно его относят к болезням будущего.
Заключение
Микобактериоз обычно развивается только в ослабленном организме, ранее поврежденном каким-либо неблагоприятным воздействием. Так, большую роль в развитии микобактериоза у людей играет запыление атмосферы. Это заболевание чаще встречается у лиц, профессии которых связаны с работой в помещениях с повышенным содержанием пыли (шахтеры, литейщики, углекопы). Среди рабочих этих специальностей наблюдаются пневмокониоз, силикоз и другие заболевания, ослабляющие легочную ткань. Именно при таких условиях легко развиваются заболевания, вызванные менее вирулентными, но потенциально патогенными микобактериями. Развитию микобактериоза могут способствовать саркоидоз и эмфизема. Ослабление всего организма, а также лечение кортикостероидными препаратами также могут быть косвенной причиной возникновения микобактериоза.
Показать Свернутьr.bookap.info
|
|
..:::Счетчики:::.. |
|
|
|
|
|
|
|
|