|
|
|
|
 Far Far |
 WinNavigator WinNavigator |
 Frigate Frigate |
 Norton
Commander Norton
Commander |
 WinNC WinNC |
 Dos
Navigator Dos
Navigator |
 Servant
Salamander Servant
Salamander |
 Turbo
Browser Turbo
Browser |
|
|
 Winamp,
Skins, Plugins Winamp,
Skins, Plugins |
 Необходимые
Утилиты Необходимые
Утилиты |
 Текстовые
редакторы Текстовые
редакторы |
 Юмор Юмор |
|
|
|
File managers and best utilites |
Реферат: Аутоаллергические (аутоиммунные) реакции. Аутоаллергия реферат
Введение в понятие «аутоаллергические болезни».
ФГОУ ВПО «Московская государственная академия ветеринарной медицины и биотехнологии им. К. И. Скрябина»
Кафедра патологической физиологии
Реферат на тему: «Аутоаллергия»
Москва 2007 год
Содержание:
1. Введение.
2. Актуальность проблемы.
3. Аутоаллергия.
4. Патогенетическая роль аутоантител.
5. Воспроизведение аутоаллергических процессов в эксперименте.
6. Аутоаллергические болезни:
а) Этиология.
б) Патогенез.
в) Патологическая анатомия аутоаллергических (аутоиммунных) процессов и болезней.
г) Классификация.
д) Диагностика.
е) Прогноз.
ж) Принципы лечения.
з) Профилактика.
7. Красная волчанка.
8. Гломерулонефрит.
9. Заключение.
10. Список литературы.
Аутоаллергические болезни (греч. autos сам + аллергия; синоним: аутоиммунные, аутоагрессивные болезни) - группа заболеваний, основным механизмом развития которых является реакция аутоантител и сенсибилизированных лимфоцитов с собственными тканями. Практически все клетки и ткани человека при определенных условиях могут быть объектом повреждающего действия лимфоцитов и аутоантител; поэтому клинические симптомы аутоаллергических болезней чрезвычайно разнообразны и могут проявляться как органными, так и системными поражениями.
Возникновение учения об аутоаллергии как причине болезней связано с именем И. И. Мечникова. В 1900- 1901 годах И. И. Мечников и его ученики экспериментально доказали возможность продукции антител к белкам собственных клеток организма.
В 1904 году Донат и Ландштейнер обнаружили в сыворотке крови больных пароксизмальной холодовой гемоглобинурией антитела, специфически направленные против собственных эритроцитов. В 1908 году Видаль, Абрами, Брюле выявили аутогемолизины у больных приобретенной гемолитической анемией. С. С. Головин в 1904 году высказал предположение об аутоиммунном патогенезе симпатической офтальмии. Особенно широкое распространение учение об аутоаллергии получило начиная с 40-50-х годов 20 в. При многих заболеваниях установлены аутоаллергические механизмы патогенеза. Следует, однако, строго разграничивать аутоаллеогические болезни, где эти механизмы считаются ведущими, и аутоаллергические синдромы, осложняющие болезни другого генеза. Типичными примерами последних являются постинфарктный синдром, симптоматическая аутоиммунная анемия при лимфолейкозе, острая дистрофия печени при инфекционном гепатите, аутоаллергические синдромы при ожогах и лучевой болезни.
Актуальность проблемы.
Аллергию называют «болезнью цивилизации». Аллергические заболевания с каждым годом привлекают все более пристальное внимание врачей разных специальностей. Несмотря на то, что аллергические болезни известны человеку более двух с половиной тысяч лет, в современном мире проблемы, связанные с вопросами диагностики, терапии и профилактики аллергопатологий остаются весьма актуальными. За последние же десятилетия проблема аллергии приняла масштаб глобальной медико- социальной проблемы. Аллергия- это состояние патологически повышенной реакции организма на какие- либо вещества чужеродной природы, в основе которой лежат иммунологические механизмы. Патологические состояния, характеризующиеся образованием антител и специфически реагирующих лимфоцитов, развиваются в ответ на контакт с соответствующим аллергеном (или аллергенами), который рассматривается как этиологический фактор (или факторы ) болезни. Эндоаллергенами (аутоаллергенами) являются измененные под воздействием различных факторов (вирусы, бактерии и др. агенты) компоненты клеток тканей организма человека (тиреоглобулин щитовидной железы, миелин мышечных волокон, хрусталик глаза и др.), которые в норме изолированы от систем, продуцирующих антитела и сенсибилизированные лимфоциты. В условиях патологического процесса происходит нарушение физиологической изоляции, что способствует образованию эндо (ауто)аллергенов и развитию аллергической реакции.
В последнее время под действием экологических факторов, факторов питания, в частности- использование всевозможных пестицидов для выращивания продуктов питания, вызываются сбои иммунной системы, которые влекут за собой развитие аутоаллергий. Под этими сбоями организм начинает действовать на собственные клетки и ткани, что является достаточным бедствием, поскольку в настоящее время в мире полно болезней, и помимо них еще и сам организм разрушает свои структуры, поэтому очень важно вовремя, направленно и качественно производить лечение организмов, страдающих аутоаллергическими болезнями и аутоаллергиями.
studfiles.net
Аутоаллергия
Аутоаллергия (греч. autos- сам + аллергия) - различные состояния измененной реактивности организма, вызванные повторными реакциями сенсибилизированных лимфоцитов и аутоантител с собственными тканями.
Возможность аутоаллергизации или аутосенсибилизации, т. е. сенсибилизации по отношению к собственным тканям организма, была продемонстрирована И. И. Мечниковым с сотрудниками в начале 20 в. Однако эти работы не привлекли к себе в то время должного внимания. В иммунологии долгие годы господствовало положение Эрлиха (P. Ehrlich) о невозможности выработки антител по отношению к собственным тканям в результате страха самоотравления (horror autotoxicus). Только последние 25—30 лет проблема аутоаллергии вновь привлекла к себе внимание исследователей. Был выявлен ряд реакций и заболеваний, в основе которых лежит аутоаллергический механизм.
Состояние аутоаллергии может развиться в организме в результате действия ряда механизмов. Чаще всего оно начинается с образования эндоаллергенов. А. Д. Адо (1960 год) предложил классификацию аутоаллергенов, которая отражает основные механизмы их образования в организме (схема).
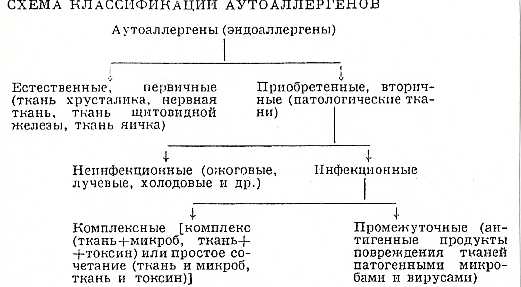
Естественные, или первичные, аутоаллергены- компоненты ряда неизмененных тканей (хрусталика, щитовидной железы и др.), по отношению к которым в организме отсутствует иммунологическая толерантность. При нарушении физиологической изоляции этих тканей иммунокомпетентные клетки продуцируют против них аутоантитела. Первичные аутоаллергены обладают слабыми аллергенными свойствами. Аутоантитела вырабатываются обычно в невысоких титрах, хотя и обладают выраженной специфичностью.
Механизм образования антител к первичным аутоаллергенам не до конца ясен. Иммунологическая толерантность организма к собственным белкам обусловлена наличием в иммунокомпетентных клетках особых веществ- репрессоров, угнетающих активность того участка генома, который связан с синтезом антител против собственных тканей. Исключение составляют ткани, относящиеся к естественным аутоаллергенам. Предполагают, что по отношению к ним действие репрессоров иммунокомпетентных клеток выпадает. По другой гипотезе, первичные аутоаллергены в процессе эмбрионального развития не имеют контакта с иммунокомпетентными клетками и поэтому в дальнейшем воспринимаются последними как чужеродные. По- видимому, нет иммунологической толерантности и в отношении антигенов, удаленных от циркуляции, а также некоторых внутриклеточных антигенов. Эти антигены под влиянием травмы или действия ферментов микробного и вирусного происхождения могут «обнажаться», попадать в кровоток и вызывать образование аутоантител.
Приобретенные, или вторичные аутоаллергены (неинфекционные и инфекционные) имеют большее значение в патологии. Неинфекционные аллергены могут образовываться при повреждении тканей физическими и химическими факторами, при гипоксии и пр. (например, в сердечной мышце при нарушениях ее кровоснабжения, в тканях при термических ожогах, повреждениях химическими веществами и прочих воздействиях). Образование аутоаллергенов может происходить также под влиянием некоторых лекарственных препаратов (антибиотики, сульфаниламиды, амидопирин и др.), после соединения с которыми белки организма приобретают аллергенные свойства. Поврежденная различными факторами ткань становится как бы чужеродной для организма и приобретает свойства аллергена. Часто повреждение, под влиянием которого образуются вторичные аутоаллергены, не ведет к полной деструкции ткани. Поэтому вырабатывающиеся аутоантитела обладают специфичностью и нередко органотропностью. Если повреждающее воздействие вызывает полную денатурацию белковых структур, то образующиеся антитела не реагируют с нормальными клетками и тканями.
Инфекционные аутоаллергены делятся на комплексные и промежуточные. Первые представляют собой комплекс (ткань + микроб, ткань + токсин) или простое сочетание (ткань и микроб, ткань и токсин) тканевого и инфекционного компонентов. Антитела, вырабатывающиеся на действие комплексного аутоаллергена, способны вступать в реакцию не только с ним, но и реагировать в отдельности как с тканью, так и с микробом, входящими в его состав. Промежуточные аутоаллергены (вирусиндуцированные антигены) были открыты А. Д. Адо и А. Х. Канчуриным (1960 год) при изучении иммунологических реакций, вызываемых некоторыми нейровирусами (например, фиксированным вирусом бешенства). По своим антигенным свойствам вирусиндуцированные антигены отличаются от свойств клетки и вируса. Антитела против данных антигенов реагируют лишь с ними, но не взаимодействуют ни с клеткой, ни с вирусом, взятыми в отдельности.
Аутоаллергические реакции, как показано исследованиями Каплана (M. H. Kaplan, 1958- 1964), И. М. Лямперт (1962- 1967) и др., могут возникнуть в результате действия так называемых общих или перекрестно реагирующих антигенов некоторых микробов и тканей организма (- гемолитический А- стрептококк- 5-й серотип и некоторые элементы ткани сердца; -гемолитический А-стрептококк- 12-й серотип и ткань почек; клебсиелла и ткань легких и др.). По- видимому, перекрестно реагирующие антигены микробов и тканей весьма широко распространены. При попадании в организм микробов, содержащих перекрестно реагирующие антигенные субстанции, против последних образуются антитела, которые взаимодействуют с элементами соответствующих тканей и вызывают их повреждение.
К развитию в организме аутоаллергических реакций могут привести нарушения в системах, продуцирующих антитела и сенсибилизированные лимфоциты, и в контролирующих эти системы механизмах. При этом может возникнуть продукция антител и сенсибилизированных лимфоцитов к компонентам собственных тканей, по отношению к которым в норме имеется иммунологическая толерантность. Бернет, Маккей и другие сторонники этой точки зрения считают, что аутоаллергические реакции развиваются тогда, когда в условиях патологии образуются так называемые запретные клоны клеток, участвующих в иммунологических реакциях против различных компонентов тканей (клонально- селекционная теория). Продукция аутоантител в значительной степени зависит от чувствительности иммунологического аппарата. Если эта чувствительность высокая, то образуется много антител даже при слабом антигенном раздражении. При низкой чувствительности иммунологического аппарата, напротив, антитела не продуцируются и при существенных антигенных воздействиях.
Образовавшийся аутоаллерген активируется, контактируя с макрофагами. В дальнейшем возможны два пути его воздействия. Во- первых, он может действовать на лимфоидную клетку, стимулируя ее пролиферацию и образование сенсибилизированных лимфоцитов. Образование сенсибилизированных лимфоцитов играет очень важную роль в патогенезе аутоаллергических реакций. Другой путь состоит во влиянии аутоаллергена на лимфоидную ткань таким образом, что она превращается в пиронинофильные клетки (плазмобласты, плазмоциты), вырабатывающие аутоантитела.
По местонахождению в организме различают фиксированные в тканях и свободно циркулирующие аутоантитела. Для определения аутоантител используют те же методики, что и для определения аллергических антител: реакцию связывания комплемента, прямую и непрямую реакции иммунофлюоресценции, реакцию преципитации в геле, реакцию пассивной гемагглютинации, реакцию потребления антиглобулина и др. При постановке иммунологических реакций иногда используют антигены, приготовленные не из собственных тканей обследуемого человека или животного, а из тканей других людей или других животных того же вида. При этом выявляются не истинные аутоантитела, а гомо- или изоантитела.
В патогенезе аутоаллергических реакций важное значение придается лимфоидным элементам. Пассивная передача некоторых экспериментальных аутоаллергических процессов (например, экспериментального аллергического энцефаломиелита) удается в основном при введении животным- реципиентам живых сенсибилизированных лимфоидных клеток, которые оказывают цитотоксическое действие на здоровые ткани. По- видимому, развитие аутоаллергических процессов обусловлено как возникновением повышенной чувствительности клеточного типа, так и выработкой аутоантител.
studfiles.net
Реферат - Аутоаллергические (аутоиммунные) реакции.
Аутоаллергия (аутоиммунитет) представляет собой иммунную реакцию гуморального или клеточного типа, направленную против собственных антигенов организма. Так как реакции протекают с разрушением собственных тканей, эти реакции называются также аутоагрессивными.
Этиология и патогенез аутоиммунитета.
Аутоиммунитет можно определить как патологическая иммунная реакция, направленная против антигенов собственного организма. В этих реакциях антигены называются аутоантигенами, антитела — аутоантителами, иммунная реакция — аутоиммунной.
Основными причинами аутоиммунитета являются собственные антигены, которые входят в состав структур организма.
Аутоантигены могут быть специфическими для данного биологического вида, для определённого индивидуума (изоантигены), для определенного органа (органоспецифические) или для определённых клеточных органелл (ДНК, митохондриальные белки).
К органоспецифическим антигенам, которые чаще вызывают аутоаллергию, относятся тиреоглобулин (соответствующая аутоиммунная болезнь называется тиреоидитом Хашимото), микросомы и антигены тиреоцитов (первичная микседема), рецепторы для тиреотропина на мембранах тиреоцитов (тиреотоксикоз), внутренний антианемический фактор Кастла (пернициозная анемия), цитоплазматические антигены клеток надпочечников (Аддисонова болезнь), цитоплазматические антигены клеток секретирующих стероиды (ранняя менопауза), антигены сперматозоидов (мужская стерильность), цитоплазматические антигены β-клеток поджелудочной железы (инсулинзависимый диабет I типа), мембранные рецепторы для инсулина (инсулиннезависимый диабет II типа), β-адренорецепторы (аллергическиие реакции немедленного типа), ацетилхолиновые рецепторы поперечно-полосатых мышц (миастения), миелин (диссеминированный склероз), базальные мембраны почечных клубочков (синдром Гудпасчера), отросчатые клетки кожи (пемфигоид), антигены глаза (симпатический офтальмит), эритроциты (гемолитическая анемия), тромбоциты (тромбоцитопеническая пурпура), зернистые лейкоциты (гранулоцитопения), антигены слизистой кишечника (язвенный колит), иммуноглобулины А (ревматоидный артрит), дезоксирибонуклеиновая кислота (системная красная волчанка). Хотя и внушительный, этот список далеко не полный, так как количество заболеваний с установленным аутоиммунным патогенезом постоянно растет.
В основе патогенеза аутоиммунных реакций лежат механизмы, характерные и для физиологических реакций – иммунологические реакции гуморального либо клеточного типа, ассоциированные с повреждениями сируктур и воспалительными явлениями, характерные для аллергических реакций. Так же, как и обычные аллергические, аутоиммунные реакции протекают по типу немедленных реакций (цитотоксические II типа, реакции посредством иммунных комплексов III типа, аутостимулирующие реакции V типа) или по типу замедленных клеточных реакций IV типа с участием сенсибилизированных лимфоцитов. Ключевым моментом патогенеза ауоталлергии является потеря физиологической толерантности к собственным антигенам ("self"), вследствие чего они становятся для иммунной системы чужеродными ("non self"). Против антигенов, ставших чужеродными, организм предпринимает иммунологическую атаку, направленную на удаление этого псевдо-«non self» антигена. Таким образом, происходит аутоагрессия с патологическими, иногда фатальными эффектами для организма.
Точный механизм аутоиммунитета в настоящее время еще неизвестен. Более того, возможно, что аутоиммунные заболевания могут иметь много патогенетических механизмов, некоторые из которых перечислены ниже.
Отсутствие иммунологической толерантности к некоторым нормальным органоспецифическим антигенам. Так, антигены некоторых органов онтогенетически развиваются изолираванно от иммунной системы (в органах, обладающих мощными гистогематическими барьерами – глаз, мозг, яички, яичники и другие). По этой причине клоны лимфоцитов, ответственные за их узнавание, не селектируются и не уничтожаются организмом в антенатальном периоде развития, поэтому к этим антигенам иммунная система не вырабатывает физиологической толерантности. Из-за этого изолированные антигены остаются для иммунной системы организма как будто чужими, «non self». Столько времени, сколько барьеры остаются непроницаемыми, контакт иммунной системы с этими антигенами невозможен, так как в системную циркуляцию антигены не попадают, равно как и иммунокомпетентные клетки, которые могут их выявить, не проникают в орган. По этой причине и иммунная (аллергическая) реакция не развивается. В случае травматического повреждения этих органов, органоспецифические антигены переходят барьер и попадают во внутреннюю среду организма, где обнаруживаются соответствующим клоном лимфоцитов как чужие, и против них развиваются иммунные (аллергические) реакции — аллергический офтальмит, энцефалит, орхит и др. Таким образом, эти реакции по своей сущности кажутся абсолютно физиологическими, хотя и с патологическими последствиями. Согласно этой гипотезе аутоаллергические заболевания представляются болезнями барьеров органов, а не иммунной системы, которая функционирует физиологически.
Появления мутантных клонов лимфоцитов. Вследствие спонтанных или индуцированных мутаций могут вновь появиться запрещённые клоны лимфоцитов, которые синтезируют и фиксируют на мембране рецепторы для собственных антигенов (эти клоны в онтогенезе были элиминированы). Таким образом, согласно этой гипотезе, аутоиммунитет является болезнью иммунной системы.
Аутоиммунитет как иммунодефицитное состояние. Вследствие генетических дефектов появляются гены иммунной гипореактивности. Эти мутантные гены у гетерозиготных лиц не проявляются, а у гомозиготов происходит экспрессия гипореактивности к любому микробному антигену. В случаях, когда микроорганизмы повреждают органы, обладающие гистогематическими барьерами, изолированные, секвестрированные органоспецифические антигены, к которым отсутствует физиологическая иммунологическая толерантность, высвобождаются, что вызывает аутоаллергические реакции путём вышеописанного механизма. Следовательно, в этой концепции патогенез аутоиммунных реакций представляется двояко: иммунодефицит создаёт условие для микробного поражения барьеров и высвобождения изолированных антигенов.
Иммунодефицит Т-супрессоров. Физиологическая толерантность к собственным антигенам обеспечивается и функцией лимфоцитов Т-супрессоров, которые ингибируют бласттрансформацию, пролиферацию В-лимфоцитов, их трансформацию в плазмоциты и, далее, синтез и продукцию антител к собственным антигенам. В отсутствии или при уменьшении популяции Т-супрессоров становится возможной иммунологическая реакция к собственным антигенам. Этот механизм лежит, возможно, в основе системной красной волчанки, ревматоидного артрита, диссеминированного склероза.
Нарушение процесса опознавания аутоантигенов. Собственные антигены опознаются рецепторами иммунокомпетентных клеток, контролируемые главным комплексом гистосовместимости (МНС). МНС представляет идиотипы или антиидиотипы иммуноглобулинов. Выработка антител к этим клеточным рецепторам и взаимодействие с ними приводит к нарушению опознования self-а и делает возможным развитие аутоиммунных реакций.
Перекрёстная реакция антигенов. Некоторые микробные антигены схожи по структуре с антигенными детерминантами макроорганизма («антигенная мимикрия»). В этих случаях проникшие микроорганизмы индуцируют выработку антител, которые могут взаимодействовать как с микробными антигенами, так и перекрёстно с собственными антигенами хозяина, что приводит к повреждению собственных тканей.
Изменение структуры аутоантигенов. Под действием ионизирующего излучения, высокой температуры, микробов, вирусов происходит денатурация собственных антигенов, к которым организм в онтогенезе выработал толерантность. В результате собственные антигены приобретают новые свойства, что вызывает иммунологическую реакцию организма. Пока остаётся неясным, почему антитела, выработанные против изменённого антигена, взаимодействуют и с неизмененными, интактными антигенами, вызывая тканевые аутоалергические повреждения, которые продолжаются даже после выведения из организма денатурированного антигена.
Представленные здесь гипотетичные механизмы не исключают друг друга и, вероятно, все они могут быть присутствовать в различных комбинациях в патогенезе аутоаллергических заболеваний, так как существенной их чертой является снятие иммунологической толерантности.
Хотя все аутоиммунные реакции имеют схожий патогенез, они обладают и некоторыми особенностями.
Тиреоидит Хашимото обусловлен выработкой антител против тиреоглобулина из состава тиреоцитов, а иммунологическая реакция активирует комплемент, который и вызывает воспаление и повреждение щитовидной железы.
Пернициозная анемия (В-12-дефицитная) основывается на локальном синтезе антител против внутреннего антианемического фактора, который секретируется слизистой желудка в желудочный сок и способствует защите и абсорбции витамина В12 (внешнего антианемического фактора). Освобождение и секреция в состав желудочного сока специфических антител инактивирует внутренний фактор, что вызывает мальабсорбцию и дефицит витамина В12 — таким образом, возникает мегалобластическая аутоиммунная анемия (анемия Аддисон-Бирмер).
Повреждение гемато-тестикулярного барьера приводит к выходу в системную циркуляцию спермальных антигенов, что обусловливает синтез антиспермальных антител, которые агглютинируют и иммобилизуют сперматозоиды, делая их неспособными к оплодотворению.
При болезни Гудпасчер (Goudpascher) (гломерулонефрит, ассоциированный с легочными кровотечениями) на базальной мембране почечного клубочка откладываются иммуноглобулины G и фрагмент С3 комплемента, что вызывает гломерулонефрит.
При миастении (мышечной слабости) происходит синтез аутоантител против рецепторов ацетилхолина на постсинаптической мембране скелетных мышц. Аутоиммунное повреждение рецепторов делает постсинаптическую мембрану ареактивной к ацетилхолину и, в результате, возникает мышечный парез, затруднение произвольных движений.
К аутоиммунным заболеванием III типа с иммунными комплексами относится системная красная волчанка (СКВ), которая имеет в основе патогенеза выработку антител к собственным нуклеопротеидам (ДНК, РНК). Так как нуклеопротеиды не обладают органной специфичностью, антитела взаимодействуют с ДНК и РНК всех органов. По этой причин поражение носит системный, генерализованный характер. Из-за того, что нуклеопротеиды хорошо растворимы, а комплемент частично истощается, комплекс антиген-антитело не может фагоцитироваться и долгое время циркулирует в крови, пропитывая субэндотелиальные пространства, поражая базальную мембрану капилляров кожи, сердца, почечных клубочков и других органов.
К клеточным аутоиммунным заболеваниям IV типа относится также тиреоидит, орхит, энцефалит и другие, в течение которых в повреждённом органе накапливаются моноциты, гистиоциты, лимфоциты, эпителиоидные клетки, другие эффекторные клетки, вызывающие прямой цитотоксический эффект, цитолиз посредством лимфокинов и лизосомальных ферментов.
www.ronl.ru
Аутоаллергия
синоним: эндоаллергия, аутоагрессия, аутоиммунитет)
патологический процесс, в основе которого лежит развитие иммунных реакций на антигены собственных тканей организма. Полагают, что в организме имеются (а не появляются, как считали ранее) аутоантитела к любым тканевым антигенам. Они участвуют в создании иммунологической толерантности и не приводят к повреждению тканей. Поэтому нельзя водить понятие «аутоаллергия» только к появлению аутоантител. Очевидно, имеют значение их количество и виды, угнетение макрофагального звена и фазы иммунного ответа, возраст, генотип и др.
В развитии А. различают механизм, связанный с образованием аутоаллергенов в организме, и механизм, обусловленный повреждением иммунной системы. В первом случае белки, клетки тканей приобретают чужеродные антигенные детерминанты и становятся т.о. аутоаллергенами (аутоантигенами, эндоаллергенами) или аутоаллергены освобождаются из клеток, где они находились в изолированном состоянии. При этом нормально функционирующая иммунная система реагирует на появление аутоаллергенов образованием аутоантител и (или) сенсибилизированных лимфоцитов, которые и вызывают повреждение. Эффекторными путями такого повреждения, согласно классификации Джелла и Кумбса (P.O. Cell, R.R.A. Coombs), являются 4 типа механизмов (см. Аллергия). Известны следующие возможности появления аутоаллергенов: нарушение изоляции естественных аутоаллергенов, конформационные изменения структуры белковых молекул или их деградация, образование комплексных аутоаллергенов и перекрестно реагирующих (общих) антигенов. Естественные (секвестрированные) аутоаллергены содержатся в клетках щитовидной железы, сетчатки глаза, в леммоцитах (шванновских клетках) и др. Они вступают в контакт с иммунокомпетентными клетками лишь при нарушении целостности клеток (травма, воспаление и др.). Конформационные изменения структуры белковых молекул или их деградация с появлением скрытых или образованием новых антигенных детерминант возникают под влиянием химических или физико-химических воздействий. Такие изменения с образованием аутоаллергенов происходят при ожогах, некрозах, воспалении, действии лизосомальных и микробных ферментов. Комплексные аутоаллергены образуются в случаях, когда химическое вещество (чаще всего лекарственный препарат) в качестве гаптена соединяется с белками тканей. Аналогичный эффект может вызывать вирус, если его антигены оказываются на поверхности клеток. Аутоаллергенами могут быть перекрестно реагирующие (общие) антигены многих микроорганизмов. Микроорганизмы, приспосабливаясь к существованию в макроорганизме, приобретают такие же антигенные детерминанты, которые имеются в тканях макроорганизма, что помогает им избежать действия иммунных механизмов хозяина. Однако в конечном счете этот иммунный механизм срабатывает, и образуются антитела к таким антигенным детерминантам, которые связываются с ними независимо от носителя детерминант — на микробе или клетках тканей. Такой механизм лежит в основе развития ревматизма, некоторых форм язвенного колита, бронхиальной астмы.
Вторая группа механизмов А. включает случаи, когда повреждена сама иммунная система, а антигены тканей не изменены. К этой группе относятся как соматическая мутация лимфоидных клеток с появлением так называемого запретного клона, для которого антигены хозяина (аутоантигены) становятся чужеродными, так и иммунодефицитные состояния, проявляющиеся в двух вариантах. Первый вариант связан с гомозиготностыо по гену низкого иммунного ответа на данный антиген. Его суть заключается в том, что сила ответа иммунной системы на каждый конкретный антиген генетически детерминирована. При низкой силе иммунного ответа иммунная реакция на антиген оказывается несовершенной. Если организм никогда не встретится с этим антигеном или встретится, но антиген относится к группе неинфекционных, то иммунного конфликта может и не быть. Но если этот антиген является составной частью возбудителя инфекционной болезни и этот возбудитель попадет в организм, то может развиться ситуация, когда организм не сможет создать защиту против такой инфекции. Возбудитель будет персистировать в организме и вызывать повреждение клеток тканей с освобождением из них изолированных аутоаллергенов и образованием аутоантител. Этот механизм предположительно имеет значение в развитии хронического рожистого воспаления, хронической герпетической инфекции. Второй вариант обусловлен развитием иммунодефицита по Т-супрессорам, что ведет к растормаживанию В-звена иммунных механизмов с усилением продукции различных аутоантител. Такой механизм выявлен при системной красной волчанке, ревматоидном артрите и других аутоиммунных (аутоаллергических) заболеваниях, а также при старении.
Аутоаллергия может быть связана с неспецифической поликлональной стимуляцией Т-хелперов и В-лимфоцитов. Под влиянием бактериальных липополисахаридов, различных митогенов, стимулирующих В-лимфоциты, усиливается образование различных аутоантител и (или) сенсибилизированных лимфоцитов. К развитию А. может привести нарушение идиотип-антиидиотипического взаимодействия. Вариабельный участок любого антитела имеет структуру, являющуюся отражением структуры антигена, вызвавшего образование этого антитела. Она получила название идиотипа и является для данного организма чужеродной. В связи с этим на нее идет образование анти-антитела, названного антиидиотипическим. Его особенность заключается в том, что конфигурация специфического участка аналогична таковой антигена, в связи с чем на антиидиотипическое антитело образуется анти-антиидиотипическое и т.д., и иммунная реакция постепенно затухает. Таков обычный процесс в регуляции иммунного ответа, однако у определенной группы людей этот баланс нарушается, и тогда появляется возможность развития аутоаллергии. А. возникает при некоторых вирусных инфекциях, возбудители которых проникают в клетки после соединения с гормональными рецепторами. В этом случае образующиеся антиидиотипические антитела приобретают конфигурацию вирусного антигена, посредством которой связываются с гормональными рецепторами клетки, становясь антирецепторными аутоантителами. Результатом такого взаимодействия является блокада гормонального рецептора либо его повреждение или возбуждение. Очевидно, по такому механизму развиваются некоторые виды сахарного диабета, гипогонадизма, гипопаратиреоза.
Выше перечислены отдельные механизмы развития А. Однако в естественно развивающемся аутоаллергическом процессе обычно принимают участие несколько таких механизмов. Так, например, возбудитель инфекции, вызывая повреждение клеток, может освобождать секвестрированные аутоаллергены, одновременно приводить к конформационным изменениям белковых молекул, образовывать комплексные антигены, оказывать поликлональную стимуляцию Т- или В-лимфоцитов и др.
См. также Аутоиммунные болезни.
Библиогр.: Адо А.Д. Общая аллергология, М., 1978; Механизмы иммунопатологии, под ред. С. Коена и др., пер. с англ., М., 1983; Николаев А.И. Аспекты частной аутоиммунопатологии, Ташкент, 1978; Петров P. В. Старение и аутоиммунные болезни, Иммунология. № 4, с. 88, 1984.
mirznanii.com
Аутоаллергия виды, симптомы, лечение, профилактика
Термином аутоаллергия обозначается извращенная, патологическая реакция иммунной системы к собственным клеткам и тканям.
Подобное нарушение становится причиной развития ряда тяжелых заболеваний, требующих точной диагностики и эффективного лечения.
Содержание:
- Общее понятие об аутоаллергии;
- Виды аутоаллергий;
- Симптомы заболевания;
- Лечение;
- Профилактика аутоаллергий.
Общее понятие об аутоаллергии
Организм каждого человека устроен так, что от рождения в нем заложена иммунологическая толерантность – физиологическое состояние, при котором иммунная система не реагирует извращенным образом на клетки и белки собственных тканей.

Под влиянием некоторых патологических изменений на ткани организма начинают вырабатываться аутоантитела и сенсибилизированные лимфоциты, которые и становятся причиной развития аутоаллергии.
Развитие патологии происходит двумя путями:
- Функционирование иммунной системы не нарушено, но появляется аутоаллерген, вызывающий патологическую реакцию иммунитета. Причиной образования аутоаллергенов на собственные ткани становится воздействие некоторых лекарственных форм, вирусов, микробов. При этом выделяются вещества, к которым у человека нет иммунологической толерантности – аутоаллергены сетчатки глаз, тканей щитовидной железы, белок миелина. Подобные вещества считаются естественными, но до повреждения органов они скрыты от иммунной системы и потому не вызывают никаких изменений в организме.
- Нарушается работа иммунной системы, при этом она теряет способность разделять белки на свои и чужеродные, и принимает их за аутоаллергены.
Истинные аутоаллергические болезни необходимо отличать от заболеваний, имеющих в своем развитии аутоаллергический компонент.
К ним относят те воспалительные и инфекционные болезни, при которых аутоаллергия присоединяется уже после их развития, то есть является, по сути, осложнением.
Читайте по теме: Что такое аллергия.
Признаки аутоаллергии выявляются при ожогах, некрозах, после сильных травм.
Аутоиммунные заболевания подразделяются на:
- органоспецифические;
- органонеспецифические.
В первом случае в патологический процесс вовлекается один вид ткани или орган, во втором случае аутоиммунные процессы затрагивает целую группу систем и органов.
Вернуться к содержанию ^
Виды аутоаллергий
Патогенез и этиология аутоаллергических болезней изучены в настоящее время не до конца, в связи с этим и нет точной классификации этого вида патологии.
Медиками используется классификация В. И. Иоффе, разработанная еще в 1963 году.
Согласно этой классификации, разделение на виды основано на механизмах аллергического процесса и по характеру аутоантигеннов.
Первая группа.
Это истинные аутоалергии, вызванные выходом физиологических антигенов, к которым у иммунной системы нет толерантности.
Происходящие при этом тканевые изменения можно описать как аллергические реакции с замедленным развитием.
К этой группе болезней относят:
- Аутоаллергический тиреоидит Хасимото;
- Симпатическую офтальмию;
- Энцефаломиелит;
- Рассеянный склероз;
- Идиоматическую аддисонову болезнь;
- Полиневрит некоторых видов.
Тиреоидит Хасимото.
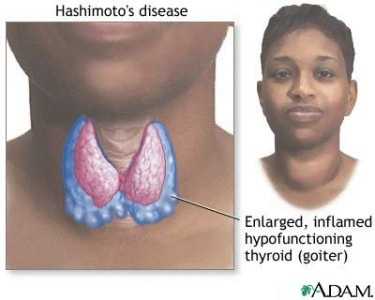
Врачи-аллергологи рекомендуют АЛЛЕРГОНИКС, как эффективное средство от аллергии. Средство содержит натуральные компоненты, живые клетки растений, восстанавливает обменные процессы в организме. Препарат проходил клинические тесты 8 лет. ВСЕ ПОДРОБНОСТИ ЗДЕСЬ.
Вторая группа.
Представлена аутоаллергиями, не обладающими органной специфичностью.
Патогенез болезни связан с изменениями, затрагивающими гомеостатический контроль иммунологических механизмов.
Самые частые заболевания этого вида:
- Гемолитическая анемия;
- Тромбоцитопеническая пурпура;
- Коллагенозы – заболевания с системным поражением волокон соединительной ткани. Это ревматоидный полиартрит, системная красная волчанка, ревматизм, склеродермия, узелковый периартрит, висцеральный эритематоз.

Третья группа.
Это заболевания, обусловленные повреждающим действием внешних причин – лекарств, вакцин, бактерий, вирусов.
При этом образуются комплексные и повреждающие аутоаллергены.
В эту группу аутоаллергий включены:
- Гломерулонефрит;
- Агранулоцитоз;
- Вакцинальный энцефаломиелит.
Вернуться к содержанию ^
Симптомы
Аутоаллергии не могут проявляться единой клинической картиной. Симптомы заболеваний напрямую зависят от того, какой орган, система или ткань повреждена.
Практически все аутоиммунные заболевания протекают тяжело, их первоначальное лечение часто требует госпитализации в стационар.
Аутоаллергический тиреоидит Хасимото.
Чаще всего заболевание развивается постепенно. Клиника патологии зависит от того какой формы тиреоидит формируется – атрофический или гипертрофический.
- При атрофической форме заболевания возникают такие симптомы как слабость, сонливость, снижается трудоспособность. У больного отмечается сухость кожи, выпадение волос, охриплость голоса, снижение слуха.
- При гипертрофической форме вначале развивается увеличение щитовидной железы. Сдавление гортанного нерва при этом приводит к изменению тембра голоса, больные также отмечают дискомфортные ощущения при проглатывании комка пищи. Гипертрофическая форма может протекать в виде гипотериоза, тиреотоксикоза с соответствующей симптоматикой.
Ревматизм.
Ревматизм чаще всего возникает после перенесенной стрептококковой инфекции – фарингита, ангины.
Начало болезни острое с температурой, лихорадочным синдромом, вялостью. В большинстве случаев возникает воспаление суставов, сопровождающееся болью.
Поражение сердечно сосудистой системы приводит к болям в области сердца, одышке, быстрой утомляемости.
Ревматизм может привести к поражениям почек, органов пищеварения, легких.
Гломерулонефрит.
Аутоиммунный гломерулонефрит это воспаление в почках, в первую очередь захватывающее клубочковые капилляры.
Заболевание протекает тяжело и подразделяется на несколько форм.
К общим симптомам гломерулонефрита можно отнести:
- Отечность. Отеки преимущественно появляются на глазах, особенно это заметно в утренние часы. Не исключено, что отечность будет затрагивать и нижние конечности. Скопление жидкости может быть весьма значительным, за счет чего вес болеющего человека быстро возрастает на несколько килограммов.
- Резкое уменьшение количества мочи – олигурия.
- Боль в области почек со стороны поясницы.
- Повышение АД определяется при гломерулонефрите у взрослых людей, для детей этот признак не характерен.
- Вялость, слабость, апатию, сонливость, возможно повышение температуры до 39 градусов.
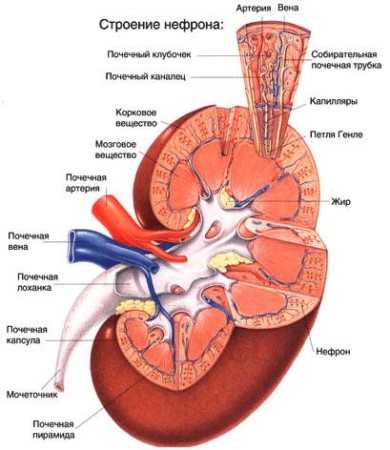
Хронический гломерулонефрит не проявляется выраженной симптоматикой, но отсутствие лечения в эту фазу болезни может стать причиной развивающейся почечной недостаточности.
Читайте по теме: Аллергия на глазах, как лечить заболевание.
Системная красная волчанка.
При системной красной волчанке в патологический процесс вовлекаются кровь, почки, кожный покров, сердце, головной и спиной мозг, легкие.
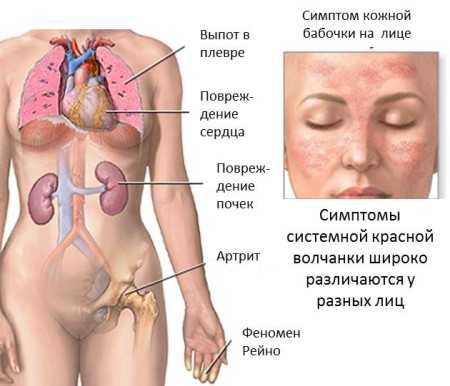
Симптомы волчанки многообразны и часто напоминают признаки других заболеваний.
К наиболее частым признакам заболевания относят:
- Выраженную слабость и быструю утомляемость;
- Скованность и отечность суставов, боли в них;
- Покраснение на лице, напоминающее крылья бабочки в расправленном виде. Этот признак выявляется у большинства больных красной волчанкой;
- Феномен Рейно, проявляющийся нарушением кровотока в пальцах;
- Боли в голове и груди;
- Поражения кожи, течение которых ухудшается под влиянием воздействия солнечных лучей;
- Потеря памяти;
- Спутанность сознания.
По подобным признакам выставить себе правильно диагноз практически невозможно.
Обязательно обратиться к врачу за консультацией необходимо, если появилась сыпь, повысилась температура тела, фиксируются боли в суставах, быстрая утомляемость.
Аутоаллергии проявляются множеством самых разных по своим проявлениям симптомов.
Некоторые виды аутоиммунных болезней долгое время текут скрыто, другие сразу проявляются выраженной клинической картиной.
Точно определить вид патологии может только врач после осмотра и диагностических процедур.
Вернуться к содержанию ^
Лечение
Схема лечения подбирается в зависимости от вида и стадии патологии, подразделяется оно на симптоматическое и патогенетическое.
Симптоматическое лечение направлено на уменьшение проявлений болезни, на купирование болей и на улучшение функционирование органа.
Патогенетическое лечение при аутоаллергиях в основном состоит из использования иммунодепрессантов, практически всегда с этой целью прибегают к использованию кортикостероидов.
Гормональные средства не только подавляют продукцию антител, но и снимают воспаление и замещают недостающие собственные кортикостероиды.
При аутоаллергиях обязательно необходимо заняться санацией хронических очагов инфекции и усилением защитных сил организма.
Вернуться к содержанию ^
Профилактика аутоаллергий
Так как аутоаллергии изучены не до конца, то и действенных профилактических мер по недопущению развития подобной патологии в медицине не разработано.
Профилактическое значение имеет сведение к минимуму воздействия на организм антигенных провокаторов, таких как вакцины, переливания крови, лекарственная терапия.
Особенно к использованию этих методов лечения нужно подходить с осторожностью в периоды повышенной реактивности иммунной системы, то есть после перенесенных респираторных и инфекционных заболеваний.
К профилактическим мерам можно отнести постоянную санацию очагов инфекции, лечение хронических заболеваний, предупреждение сильных переохлаждений.
Аутоаллергии это еще недостаточно исследованная группа заболеваний, но вероятность их появления у любого человека велика.
В связи с этим любое длительное ухудшение самочувствия, нарушение работы внутренних органов, температура, общее недомогание должны быть поводом обращения в медицинское учреждение.
Вернуться к содержанию ^
ОЦЕНКА СТАТЬИ:
Загрузка...ПОДЕЛИТЬСЯ С ДРУЗЬЯМИ:
allergiik.ru
Лекция - Аутоаллергические (аутоиммунные) реакции.
Аутоаллергия (аутоиммунитет) представляет собой иммунную реакцию гуморального или клеточного типа, направленную против собственных антигенов организма. Так как реакции протекают с разрушением собственных тканей, эти реакции называются также аутоагрессивными.
Этиология и патогенез аутоиммунитета.
Аутоиммунитет можно определить как патологическая иммунная реакция, направленная против антигенов собственного организма. В этих реакциях антигены называются аутоантигенами, антитела — аутоантителами, иммунная реакция — аутоиммунной.
Основными причинами аутоиммунитета являются собственные антигены, которые входят в состав структур организма.
Аутоантигены могут быть специфическими для данного биологического вида, для определённого индивидуума (изоантигены), для определенного органа (органоспецифические) или для определённых клеточных органелл (ДНК, митохондриальные белки).
К органоспецифическим антигенам, которые чаще вызывают аутоаллергию, относятся тиреоглобулин (соответствующая аутоиммунная болезнь называется тиреоидитом Хашимото), микросомы и антигены тиреоцитов (первичная микседема), рецепторы для тиреотропина на мембранах тиреоцитов (тиреотоксикоз), внутренний антианемический фактор Кастла (пернициозная анемия), цитоплазматические антигены клеток надпочечников (Аддисонова болезнь), цитоплазматические антигены клеток секретирующих стероиды (ранняя менопауза), антигены сперматозоидов (мужская стерильность), цитоплазматические антигены β-клеток поджелудочной железы (инсулинзависимый диабет I типа), мембранные рецепторы для инсулина (инсулиннезависимый диабет II типа), β-адренорецепторы (аллергическиие реакции немедленного типа), ацетилхолиновые рецепторы поперечно-полосатых мышц (миастения), миелин (диссеминированный склероз), базальные мембраны почечных клубочков (синдром Гудпасчера), отросчатые клетки кожи (пемфигоид), антигены глаза (симпатический офтальмит), эритроциты (гемолитическая анемия), тромбоциты (тромбоцитопеническая пурпура), зернистые лейкоциты (гранулоцитопения), антигены слизистой кишечника (язвенный колит), иммуноглобулины А (ревматоидный артрит), дезоксирибонуклеиновая кислота (системная красная волчанка). Хотя и внушительный, этот список далеко не полный, так как количество заболеваний с установленным аутоиммунным патогенезом постоянно растет.
В основе патогенеза аутоиммунных реакций лежат механизмы, характерные и для физиологических реакций – иммунологические реакции гуморального либо клеточного типа, ассоциированные с повреждениями сируктур и воспалительными явлениями, характерные для аллергических реакций. Так же, как и обычные аллергические, аутоиммунные реакции протекают по типу немедленных реакций (цитотоксические II типа, реакции посредством иммунных комплексов III типа, аутостимулирующие реакции V типа) или по типу замедленных клеточных реакций IV типа с участием сенсибилизированных лимфоцитов. Ключевым моментом патогенеза ауоталлергии является потеря физиологической толерантности к собственным антигенам ("self"), вследствие чего они становятся для иммунной системы чужеродными ("non self"). Против антигенов, ставших чужеродными, организм предпринимает иммунологическую атаку, направленную на удаление этого псевдо-«non self» антигена. Таким образом, происходит аутоагрессия с патологическими, иногда фатальными эффектами для организма.
Точный механизм аутоиммунитета в настоящее время еще неизвестен. Более того, возможно, что аутоиммунные заболевания могут иметь много патогенетических механизмов, некоторые из которых перечислены ниже.
Отсутствие иммунологической толерантности к некоторым нормальным органоспецифическим антигенам. Так, антигены некоторых органов онтогенетически развиваются изолираванно от иммунной системы (в органах, обладающих мощными гистогематическими барьерами – глаз, мозг, яички, яичники и другие). По этой причине клоны лимфоцитов, ответственные за их узнавание, не селектируются и не уничтожаются организмом в антенатальном периоде развития, поэтому к этим антигенам иммунная система не вырабатывает физиологической толерантности. Из-за этого изолированные антигены остаются для иммунной системы организма как будто чужими, «non self». Столько времени, сколько барьеры остаются непроницаемыми, контакт иммунной системы с этими антигенами невозможен, так как в системную циркуляцию антигены не попадают, равно как и иммунокомпетентные клетки, которые могут их выявить, не проникают в орган. По этой причине и иммунная (аллергическая) реакция не развивается. В случае травматического повреждения этих органов, органоспецифические антигены переходят барьер и попадают во внутреннюю среду организма, где обнаруживаются соответствующим клоном лимфоцитов как чужие, и против них развиваются иммунные (аллергические) реакции — аллергический офтальмит, энцефалит, орхит и др. Таким образом, эти реакции по своей сущности кажутся абсолютно физиологическими, хотя и с патологическими последствиями. Согласно этой гипотезе аутоаллергические заболевания представляются болезнями барьеров органов, а не иммунной системы, которая функционирует физиологически.
Появления мутантных клонов лимфоцитов. Вследствие спонтанных или индуцированных мутаций могут вновь появиться запрещённые клоны лимфоцитов, которые синтезируют и фиксируют на мембране рецепторы для собственных антигенов (эти клоны в онтогенезе были элиминированы). Таким образом, согласно этой гипотезе, аутоиммунитет является болезнью иммунной системы.
Аутоиммунитет как иммунодефицитное состояние. Вследствие генетических дефектов появляются гены иммунной гипореактивности. Эти мутантные гены у гетерозиготных лиц не проявляются, а у гомозиготов происходит экспрессия гипореактивности к любому микробному антигену. В случаях, когда микроорганизмы повреждают органы, обладающие гистогематическими барьерами, изолированные, секвестрированные органоспецифические антигены, к которым отсутствует физиологическая иммунологическая толерантность, высвобождаются, что вызывает аутоаллергические реакции путём вышеописанного механизма. Следовательно, в этой концепции патогенез аутоиммунных реакций представляется двояко: иммунодефицит создаёт условие для микробного поражения барьеров и высвобождения изолированных антигенов.
Иммунодефицит Т-супрессоров. Физиологическая толерантность к собственным антигенам обеспечивается и функцией лимфоцитов Т-супрессоров, которые ингибируют бласттрансформацию, пролиферацию В-лимфоцитов, их трансформацию в плазмоциты и, далее, синтез и продукцию антител к собственным антигенам. В отсутствии или при уменьшении популяции Т-супрессоров становится возможной иммунологическая реакция к собственным антигенам. Этот механизм лежит, возможно, в основе системной красной волчанки, ревматоидного артрита, диссеминированного склероза.
Нарушение процесса опознавания аутоантигенов. Собственные антигены опознаются рецепторами иммунокомпетентных клеток, контролируемые главным комплексом гистосовместимости (МНС). МНС представляет идиотипы или антиидиотипы иммуноглобулинов. Выработка антител к этим клеточным рецепторам и взаимодействие с ними приводит к нарушению опознования self-а и делает возможным развитие аутоиммунных реакций.
Перекрёстная реакция антигенов. Некоторые микробные антигены схожи по структуре с антигенными детерминантами макроорганизма («антигенная мимикрия»). В этих случаях проникшие микроорганизмы индуцируют выработку антител, которые могут взаимодействовать как с микробными антигенами, так и перекрёстно с собственными антигенами хозяина, что приводит к повреждению собственных тканей.
Изменение структуры аутоантигенов. Под действием ионизирующего излучения, высокой температуры, микробов, вирусов происходит денатурация собственных антигенов, к которым организм в онтогенезе выработал толерантность. В результате собственные антигены приобретают новые свойства, что вызывает иммунологическую реакцию организма. Пока остаётся неясным, почему антитела, выработанные против изменённого антигена, взаимодействуют и с неизмененными, интактными антигенами, вызывая тканевые аутоалергические повреждения, которые продолжаются даже после выведения из организма денатурированного антигена.
Представленные здесь гипотетичные механизмы не исключают друг друга и, вероятно, все они могут быть присутствовать в различных комбинациях в патогенезе аутоаллергических заболеваний, так как существенной их чертой является снятие иммунологической толерантности.
Хотя все аутоиммунные реакции имеют схожий патогенез, они обладают и некоторыми особенностями.
Тиреоидит Хашимото обусловлен выработкой антител против тиреоглобулина из состава тиреоцитов, а иммунологическая реакция активирует комплемент, который и вызывает воспаление и повреждение щитовидной железы.
Пернициозная анемия (В-12-дефицитная) основывается на локальном синтезе антител против внутреннего антианемического фактора, который секретируется слизистой желудка в желудочный сок и способствует защите и абсорбции витамина В12 (внешнего антианемического фактора). Освобождение и секреция в состав желудочного сока специфических антител инактивирует внутренний фактор, что вызывает мальабсорбцию и дефицит витамина В12 — таким образом, возникает мегалобластическая аутоиммунная анемия (анемия Аддисон-Бирмер).
Повреждение гемато-тестикулярного барьера приводит к выходу в системную циркуляцию спермальных антигенов, что обусловливает синтез антиспермальных антител, которые агглютинируют и иммобилизуют сперматозоиды, делая их неспособными к оплодотворению.
При болезни Гудпасчер (Goudpascher) (гломерулонефрит, ассоциированный с легочными кровотечениями) на базальной мембране почечного клубочка откладываются иммуноглобулины G и фрагмент С3 комплемента, что вызывает гломерулонефрит.
При миастении (мышечной слабости) происходит синтез аутоантител против рецепторов ацетилхолина на постсинаптической мембране скелетных мышц. Аутоиммунное повреждение рецепторов делает постсинаптическую мембрану ареактивной к ацетилхолину и, в результате, возникает мышечный парез, затруднение произвольных движений.
К аутоиммунным заболеванием III типа с иммунными комплексами относится системная красная волчанка (СКВ), которая имеет в основе патогенеза выработку антител к собственным нуклеопротеидам (ДНК, РНК). Так как нуклеопротеиды не обладают органной специфичностью, антитела взаимодействуют с ДНК и РНК всех органов. По этой причин поражение носит системный, генерализованный характер. Из-за того, что нуклеопротеиды хорошо растворимы, а комплемент частично истощается, комплекс антиген-антитело не может фагоцитироваться и долгое время циркулирует в крови, пропитывая субэндотелиальные пространства, поражая базальную мембрану капилляров кожи, сердца, почечных клубочков и других органов.
К клеточным аутоиммунным заболеваниям IV типа относится также тиреоидит, орхит, энцефалит и другие, в течение которых в повреждённом органе накапливаются моноциты, гистиоциты, лимфоциты, эпителиоидные клетки, другие эффекторные клетки, вызывающие прямой цитотоксический эффект, цитолиз посредством лимфокинов и лизосомальных ферментов.
www.ronl.ru
Аутоаллергия
К аллергическим реакциям замедленного типа относится большая группа реакций и заболеваний, возникающих в результате повреждения клеток и тканей аутоаллергенами, т. е. аллергенами, возникшими в самом организме. Это состояние называется аутоаллергией и характеризует способность организма реагировать на свои собственные белки.
Обычно в организме имеется приспособление, с помощью которого иммунологические механизмы отличают собственные белки от чужеродных. В норме в организме к собственным белкам и компонентам тела имеется толерантность (устойчивость), т. е. против собственных белков не образуются антитела и сенсибилизированные лимфоциты, поэтому собственные ткани и не повреждаются. Предполагают, что торможение иммунного ответа на собственные аутоантигены реализуют Т-лимфоциты-супрессоры. Наследственный дефект в работе Т-супрессоров и приводит к тому, что сенсибилизированные лимфоциты повреждают ткани собственного хозяина, т. е. возникает аутоаллергическая реакция. Если эти процессы становятся достаточно выраженными, то аутоаллергическая реакция переходит в аутоаллергическую болезнь.
В связи с тем, что ткани повреждаются собственными иммунными механизмами, аутоаллергию еще называют аутоагрессией, а аутоаллергические болезни — аутоиммунными болезнями. Иногда и то и другое называют иммунопатологией. Однако последний термин неудачен и пользоваться им как синонимом аутоаллергии не следует, ибо иммунопатология — это очень широкое понятие и в него, кроме аутоаллергии, еще входят:
иммунодефицитные болезни, т. е. заболевания, связанные или с выпадением способности образовывать какие-либо иммуноглобулины и связанные с этими иммуноглобулинами антитела, или с выпадением способности образовывать сенсибилизированные лимфоциты;
иммунопролиферативные болезни, т. е. заболевания, связанные с избыточным образованием какого-либо класса иммуноглобулинов.
логических состояниях приобретают аллергенные, чужеродные для организма их носителя свойства и становятся аутоаллергенами. Они обнаружены при ожоговой и лучевой болезни, при дистрофии и некрозах. Во всех этих случаях с белками происходят изменения, которые делают их чужеродными для организма.
Аутоаллергены могут образоваться в результате соединения попавших в организм лекарств, химических веществ с белками тканей. При этом вступившее в комплекс с белком чужеродное вещество обычно играет роль гаптена.
Комплексные аутоаллергены образуются в организме в результате соединения попавших в организм бактериальных токсинов и других продуктов инфекционного происхождения с белками тканей. Такие комплексные аутоаллергены могут, например, образовываться при соединении некоторых компонентов стрептококка с белками соединительной ткани миокарда, при взаимодействии вирусов с клетками тканей.
Во всех этих случаях суть аутоаллергической перестройки заключается в том, что в организме появляются необычные белки, которые воспринимаются иммунокомпетентными клетками как «не свои», чужеродные и поэтому стимулируют их к выработке антител и образованию сенсибилизированных Т-лимфоцитов.
Гипотеза Бернета объясняет формирование аутоантител дерепрессией в геноме некоторых иммунокомпетентных клеток, способных вырабатывать антитела к собственным тканям. В результате появляется «запретный клон» клеток, несущих на своей поверхности антитела, комплементарные к антигенам собственных неповрежденных клеток.
3. Белки некоторых тканей могут оказаться аутоаллергенами вследствие наличия у них общих антигенов с определенными бактериями. В процессе приспособления к существованию в макроорганизме у многих микробов появились антигены, общие с антигенами хозяина. Это тормозило включение иммунологических механизмов защиты против такой микрофлоры, так как по отношению к своим антигенам в организме существует иммунологическая толерантность и такие микробные антигены принимались как «свои». Однако в силу каких-то различий в строении общих антигенов происходило включение иммунологических механизмов защиты против микрофлоры, что одновременно вело и к повреждению собственных тканей. Предполагается участие подобного механизма в развитии ревматизма в связи с наличием общих антигенов у некоторых штаммов стрептококка группы А и тканей сердца; язвенного колита в связи с общими антигенами в слизистой оболочке кишки и некоторыми штаммами кишечной палочки.
В сыворотке крови больных инфекционно-аллергической формой бронхиальной астмы найдены антитела, реагирующие как с антигенами микрофлоры бронхов (нейссерия, клебсиелла), так и с тканями легких.
studfiles.net
|
|
..:::Счетчики:::.. |
|
|
|
|
|
|
|
|