Контрольная работа по химии на тему «Алканы» (10 класс)
Контрольная работа
Введение в органическую химию. Алканы.
Вариант 1.
1.Из предложенного перечня выберите названия органических веществ: а) метан; б) крахмал; в) серная кислота; г) глюкоза
2.Из предложенного перечня укажите («+» или «-») правильность утверждения:
а) чем больше молярная масса алкана, тем выше его температура кипения и плавления;
б) длина связи у алканов ровна 0, 155 нм
в) метан – это бесцветный газ, легче воздуха, не имеющих запаха.
г) валентность атома углерода в органических соединениях всегда равна V.
3. Какие из перечисленных молекулярных формул относятся к алканам: а) СН4; б) С 2Н6; в) С3Н6
4. Из предложенного перечня выберите названия алкана, которые при н.у. являются жидкостями:
5. Составьте структурную формулу 2- метил – 3 хлоргексана
Составьте структурную формулу 2- метил – 3 хлоргексана
6. Приведите названия по систематической номенклатуре 2 изомеров (на ваш выбор) с молекулярной формулой С6Н14. Назовите вещества.
7. Массовая доля водорода в ряду пропан, бутан:
а) увеличивается
б) уменьшается.
Свой ответ подтвердите расчетами.
8. В каком уравнении сумма коэффициентов больше:
А) пропан +О2=
Б) бутан +О2=
9. Составьте уравнения предложенных реакций, назовите продукты и укажите к какому типу относятся :
А) метан+О2 =
Б) Этан + 2 Сl2 =
В) СН3СООNa+ NaOH(ТВ)=
10. Установите формулу алкана, в котором массовая доля углерода равна 84%.
Контрольная работа
Введение в органическую химию. Алканы.
Вариант 2.
1.Из предложенного перечня выберите названия органических веществ природного происхождения : а) нефть; б) полиэтилен; в) природный газ; г) бензин
2. Из предложенного перечня укажите («+» или «-») правильность утверждения:
Из предложенного перечня укажите («+» или «-») правильность утверждения:
а) изомеры имеют одинаковый качественный и количественный состав;
б) длина связи у алканов ровна 0, 155 нм
в) пропан является газом.
г) валентность атома кислорода в органических соединениях всегда равна двум.
3. Из предложенного перечня выберите названия алкана, которые при н.у. являются газами:
5. Составьте структурную формулу 3- метил – 3 хлоргептана
6. Приведите названия по систематической номенклатуре 2 изомеров (на ваш выбор) с молекулярной формулой С7Н16. Назовите вещества.
7. Массовая доля водорода в ряду пентан, бутан: а) увеличивается; б) уменьшается.
Свой ответ подтвердите расчетами.
8. В каком уравнении сумма коэффициентов больше:
А) пентан +О2= Б) бутан +О2=
9. Составьте уравнения предложенных реакций, назовите продукты и укажите к какому типу относятся :
А) Этан+О2 =
Б) Метан + 2 Сl2 =
В) СН3СООNa+ NaOH(ТВ)=
10. Установите формулу алкана, в котором массовая доля углерода равна 82,76%.
Установите формулу алкана, в котором массовая доля углерода равна 82,76%.
Контрольная работа по теме «Алканы» (10 класс)
Контрольная работа №1 по теме «Аканы и циклоалканы».
Вариант 1.
1. Для вещества, имеющего строение
СН3 — СН — СН — СН3
| |
СН3 СН3
составьте формулы одного гомолога и двух изомеров. Дайте всем веществам названия по
систематической номенклатуре.
2. Напишите уравнения реакций: а) полного сгорания пентана в атмосфере кислорода;
б) изомеризации 2,2-диметилпропана; в) двух стадий хлорирования 1,1,1-трихлорэтана. Дайте названия продуктам реакции по систематической номенклатуре.
3. Установите молекулярную формулу органического вещества, если массовые доли углерода и водорода в нём соответственно равны 83,3% и 16,7%, а относительная плотность его паров по водороду равна 36.
4. Осуществите превращение, назовите вещества А, Б, В, Г по систематической номенклатуре:
AlCl3Cl2/ hn KOH/спирт
Пентан ——— А ——— Б —————- В
2 Na
Г
5.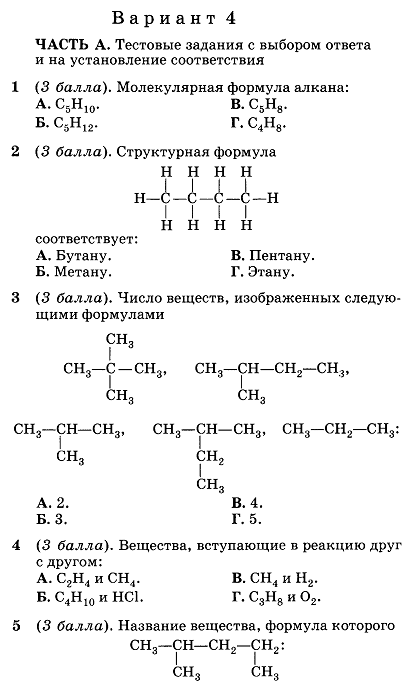 Смесь этана и пропана общим объёмом 6,72дм3(н.у.) сожгли в избытке кислорода, а затем обработали избытком известковой воды. Выпал осадок массой 80г. Найдите объёмы газов в исходной смеси .
Смесь этана и пропана общим объёмом 6,72дм3(н.у.) сожгли в избытке кислорода, а затем обработали избытком известковой воды. Выпал осадок массой 80г. Найдите объёмы газов в исходной смеси .
———————————————————————————————————————
Контрольная работа №1 по теме «Алканы и циклоалканы».
Вариант 2.
1. Для вещества, имеющего строение
CH3
|
СН3 —- С —- СН
|
CH3
Составьте формулы одного гомолога и двух изомеров. Дайте всем веществам названия по систематической номенклатуре.
2.Составьте уравнения реакций: а) полного сгорания этана; б) изомеризации
2-метилгептана; в) двух стадий бромирования пропана. Дайте названия продуктам реакции по систематической номенклатуре.
3. Установите молекулярную формулу органического вещества, содержащего 85,7% углерода и 14,3% водорода, если плотность его паров по воздуху равна 2,9.
4. Осуществите превращение, назовите вещества А, Б, В, Г по систематической номенклатуре:
AlCl3 Br2/ hn KOH/спирт
Бутан ——— А ————- Б ————— В
2 Na
Г
5. Определите объём кислорода, затраченного на сжигание 33,6дм3(н.у.) смеси метана и этана, если плотность смеси по водороду равна 10,335.
Тестовое задание по теме «Алканы и циклоалканы»
А1.Выберите неверное утверждение о химических и физических свойствах алканов:
1) метан, этан, пропан, бутан – газы при комнатной температуре;
2) при обычных температурах алканы малоактивны;
3) при высоких температурах вступают в реакции замещения и окисления;
4) характерны реакции присоединения.
А2. С увеличением молекулярной массы предельных углеводородов с неразветвлённой цепью их температуры плавления и кипения:
1) не изменяются; 2) увеличиваются; 3) уменьшаются;
4) температуры кипения увеличиваются, а температуры плавления уменьшаются.
А3. Какое из указанных соединений является изомером 2,3 – диметилбутана:
1) 2,4-диметилпентан; 2) 2-метилбутан;
3) 2,2-диметилпентан; 4) 2,2-диметилбутан.
А4. Относительная молекулярная масса алкана равна 114. Укажите число атомов углерода в алкане:
1) 8; 2) 6; 3) 10; 4) 12.
А5. Выберите название вещества, которое получается при нагревании 2-бромбутана с избытком металлического натрия:
1) 2,3-диметилгексан; 2) 3,4-диэтилбутан;
3) 3,4-диметилгексан; 4) 3-метил 4- этилпентан.
А6. Какое газообразное вещество образуется при сплавлении натрий-гидроксида и натрий-ацетата:
1) С2Н6; 2) С2Н4; 3) СН4; 4) СО2.
А7. Какое утверждение не применимо для реакции бромирования этана:
1) радикальная; 2) окислительно-восстановительная;
3) замещения; 4) присоединения.
А8. Реакции хлорирования алканов проводятся:
1) в присутствии катализатора – AlCl3;
3) в присутствии катализатора – платины;
4) путём продувания газообразного алкана через водный раствор галогена.
А9. В отличие от пропана бутан вступает в реакцию:
1) горения; 2) хлорирования при освещении УФ-светом;
3) разложения на простые вещества при сильном нагревании в вакууме;
4) изомеризации.
А10. Какой продукт образуется из 1,6 – дихлоргептана при взаимодействии с металлическим натрием:
1) циклогексан; 2) циклогептан;
3) метилциклогексан; 4) 1,4-диметилциклогексан.
А11. В какие реакции вступает циклопропан:
1) каталитического гидрирования;
2) присоединения галогеноводородов;
3) с бромной водой; 4) с раствором KMnO4
А12. Укажите правильные утверждения:
1) в гомологическом ряду алканов массовая доля углерода в молекуле увеличивается;
2) в гомологическом ряду циклоалканов массовая доля углерода в молекуле увеличивается;
3) алканы и циклоалканы встречаются в приподе;
4) алканы и циклоалканы являются насыщенными углеводородами.
А13. В результате каких реакций может быть получен этан:
1) сплавление C2H5COONa со щёлочью;
2) крекинг бутана;
3) взаимодействие бромметана с натрием;
4) взаимодействие бромэтана с цинком.
А14. Охарактеризуйте химическое строение молекул алканов и циклоалканов:
1) все атомы находятся в состоянии sp3— гибридизации;
2) все алканы и циклоалканы могут существовать в виде нескольких пространственных изомеров;
3) при гомолитическом разрушении молекул образуются свободные радикалы;
4) число возможных изомеров циклоалканов выше, чем в ряду алканов.
А15. Какие углеводороды имеют плотность паров 3,21г/л(н.у.):
1) н-пентан; 2) н-гексан; 3) 2-метилбутан; 4) 2-метилпропан.
А16. Укажите формулу галогенпроизводного этана, не имеющего изомеров:
1) C2H4Cl2; 2) C2H3Cl3; 3) C2H2Cl4; 4) C2HCl5.
А17. При действии спиртовым раствором щёлочи на 1-хлорпропан образуется продукт, в молекуле которого общее число атомов всех элементов равно:
1) 9; 2) 11; 3) 14; 4) 17.
А18. На полное сгорание 0,2моль алкана пошло 107л воздуха. Установите формулу алкана, объёмная доля кислорода в воздухе равна 20,94%:
Установите формулу алкана, объёмная доля кислорода в воздухе равна 20,94%:
1) СН4; 2) С3Н8; 3) С
А19. Углекислый газ, полученный при сжигании 3,2л метана, поглощается 38,2мл 32%-го раствора гидроксида калия плотностью 1,31г/мл. Установите массу образовавшейся соли:
1) 19,7г K2CO3; 2) 18,4 г K2CO3; 3) 12,6г KHCO3; 4) 8,9г KHCO3
А20. Найдите массу образовавшегося этана при взаимодействии этена с порцией водорода, содержащей 4,21 1024 молекул, если в реакцию вступило только 70% водорода:
1) 12,5г; 2) 4,67г; 3) 14,8г; 4)13,7г.
Контрольный срез по химии для 9-го класса
1. Из данного перечня веществ выпишите отдельно формулы оснований и солей; дайте названия всем веществам:
CO2; H2SO4; KOH; Cu(OH)2; K2SiO3; P2O5; Na2SO4; Fe(NO3)3; Al(OH)3; HCl; HBr; Zn(OH)2; AlPO4; FeO; H2SO3.
2. Укажите положение в периодической системе, число протонов, электронов и нейтронов в атомах химических элементов с порядковыми номерами: 15, 25, 50.
3. У какого из элементов каждой пары ярче выражены металлические свойства? Ответ поясните.
а) Na и Mg; б) Na и Rb.
Ba —— BaO —— Ba(OH)2 —— BaCl2 —— Ba(NO3)2 —— BaSO4
5. Образец фосфора содержит два изотопа — 31Р и 33Р. Средняя относительная атомная масса фосфора в образце равна 31,2. Определите мольную долю 33Р в образце.
——————————————————————————————————————
Контрольный срез по химии для 9-го класса
1. Из данного перечня веществ выпишите отдельно формулы оснований и солей, дайте названия всем веществам:
CO2; H2SO4; KOH; Cu(OH)2; K2SiO3; P2O5; Na2SO4; Fe(NO3)3; AL(OH)3; HCl; HBr; Zn(OH)2; AlPO4; FeO; H2SO3
2. Укажите положение в периодической системе, число протонов, электронов и нейтронов в атомах химических элементов с порядковыми номерами: 15, 25, 50.
Укажите положение в периодической системе, число протонов, электронов и нейтронов в атомах химических элементов с порядковыми номерами: 15, 25, 50.
3. У какого из элементов каждой пары ярче выражены металлические свойства? Ответ поясните.
а) Na и Mg; б) Na и Rb.
4. Составьте уравнения реакций, с помощью которых можно осуществить следующее превращение:
Ba —— BaO —— Ba(OH)2 —— BaCl2 —— Ba(NO3)2 —— BaSO4
5. Образец фосфора содержит два изотопа — 31Р и 33Р. Средняя относительная атомная масса фосфора в образце равна 31,2. Определите мольную долю 33Р в образце.
Контрольная работа по теме Алканы
Контрольная работа по теме «Алканы»
1 вариант
1. Общая формула гомологического ряда алканов:
Сnh3n 2. Cnh3n+2 3. Cnh3n-2 4. Cnh3n-6
2. Изомерами являются:
1) бутан и пентан
2) 2-метилбутан и 2,2-диметилпропан
3) 1,3-диметилпентан и 2-метилпентан
4) 3,3-диметилпентан и 2,2-диметилбутан
3. Верны ли следующие суждения о физических свойствах алканов?
Верны ли следующие суждения о физических свойствах алканов?
А. С увеличением относительной молекулярной массы у алканов увеличиваются температуры плавления и кипения.
Б. Метан имеет характерный запах.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
4. В уравнении реакции горения пентана коэффициент перед формулой кислорода равен:
1) 2
2) 4
3) 6
4) 8
5. Синтез-газ образуется в результате реакции между:
1) метаном и кислородом
2) метаном и хлором
3) метаном и водой
4) хлорметаном и водой
6. При полном сгорании циклического углеводорода образовался оксид углерода (IV) массой 3,52 г и вода массой 1,44 г. Относительная плотность этого углеводорода по воздуху равна 1,448. Найдите молекулярную формулу углеводорода.
7. Составьте формулы следующих веществ:
1) 2- бром-1- фторпропан;
2) 2,3-диметилпентан;
3) 2,2,4,4-тетраметилоктан
8. Массовая доля водорода в алкане равна 15,625%. Какова молекулярная формула данного алкана?
Массовая доля водорода в алкане равна 15,625%. Какова молекулярная формула данного алкана?
9. 1-хлорпропан → гексан → пропан → 2-хлорпропан → 2,3-диметилбутан
Контрольная работа по теме «Алканы»
2 вариант
1. Молекулярная формула циклобутана
1) СH4
2) C3H6
3) C4H10
4) C4H8
2. Гомологи – это:
1.Гексан и гексаналь. 2. Гексан и гексен. 3. Бутан и пентан. 4.Бутан и пентил.
3. Пропан:
1) не имеет гомологов с меньшим числом атомов углерода
2) является жидкостью
3) является газом при комнатной температуре
4) имеет меньшую относительную молекулярную массу, чем воздух
5) не имеет изомеров
6) растворяется в воде
4. При взаимодействии 1 моль метана с 3 моль хлора образуется:
1) 1 моль трихлорметана
2) 1 моль трихлорметана и 3 моль хлороводорода
3) 1 моль трихлорметана и 2 моль хлороводорода
4) 3 моль трихлорметана и 3 моль хлороводорода
5. Метан реагируют
Метан реагируют
1) с раствором KMnO4
2) с водородом
3) с кислородом
4) с бромной водой
6. При полном сгорании углеводорода образовался оксид углерода (IV) массой 0,88 г и вода массой 0,54 г. Относительная плотность этого углеводорода по водороду равна 15. Найдите молекулярную формулу углеводорода.
7. Составьте формулы следующих веществ:
1) 2,4,6-трихлорнонан;
2) изобутан;
3) 2,2-диметилпентан.
8. Массовые доли углерода и водорода в углеводороде равны соответственно 83,33% и 16,67%. Определите состав данного углеводорода.
9. Метан → ацетилен → этан → пропан → 1-хлорпропан
Контрольная работа по теме «Алканы»
3 вариант
1. Изомером гептана является:
1) 2,3-диметилгептан;
2) 2,3-диметилбутан;
3) 2,3-диметилпентан;
4) 2,3-диметилгексан.
2. Гомологами являются вещества, названия которых:
1) 2-метилпентан и 2-метилбутан
2) 2-метилпропан и бутан
3) 2,2-диметилбутан и 2-метилпентан
4) бутан и циклобутан
3.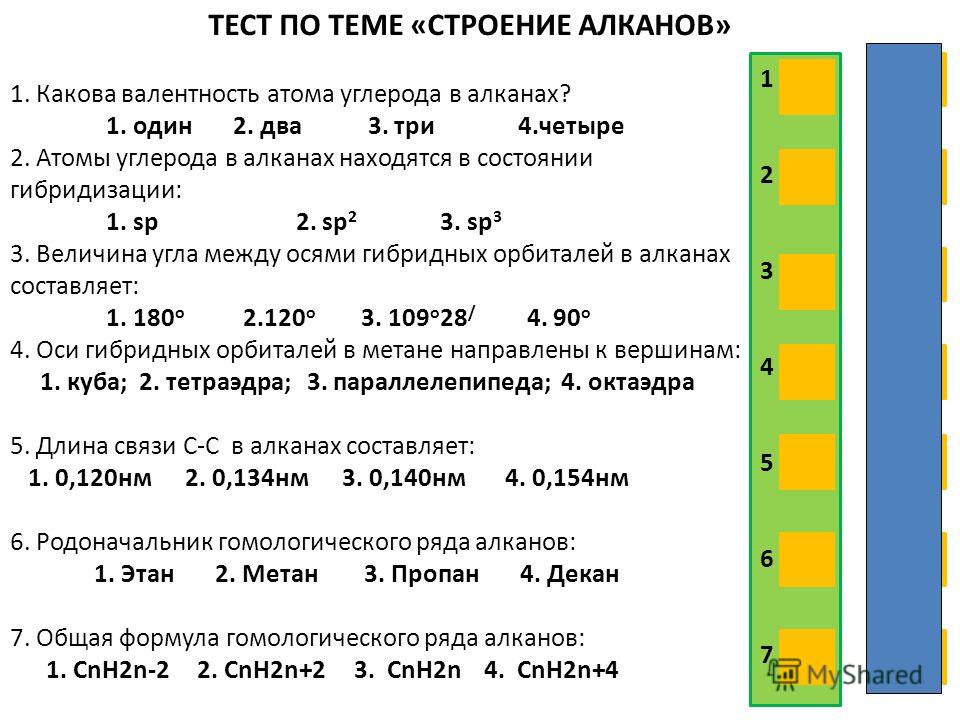 Верны ли следующие суждения о физических свойствах алканов?
Верны ли следующие суждения о физических свойствах алканов?
А. Все алканы -газообразные или жидкие вещества.
Б. Алканы хорошо растворяются в воде.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
4. При разложении метана не образуется:
1) водород
2) этилен
3) ацетилен
4) сажа
5. Пропан реагируют
1) с водой
2) с раствором KMnO4
3) с водородом
4) с хлором
6. У становите молекулярную формулу дибромалкана, содержащего 85,11 % брома.
7. Составьте формулы следующих веществ:
а) 1,2-дихлорэтан;
б) 3-метилгептан;
в) 2,4,6-триметилдекан
8. Найдите молекулярную формулу углеводорода, имеющего плотность 1,97 г/л, если при сгорании 4,4 г его в кислороде образуется 6,72 л СО2 и 7,2 г Н2О.
9. Бутан →этан →хлорэтан → бутан → изобутан
| ||||||||||||||||||||||
2 | 3 | 4 | 5 | |
Г | Г | А | Г | В |
6 | 7 | 8 | 9 | 10 |
В | Г | А | Б | А |
11 | 12 | 13 | 14 | 15 |
Б | А | Б | Б | А |
16 | 17 | 18 | 19 | 20 |
Г | Б | Б | В | Г |
Проверочная работа по теме «Номенклатура алканов»
Проверочная работа по теме: НОМЕНКЛАТУРА АЛКАНОВ
Вариант 1
1. Напишите структурную формулу и назовите по международной наменклатуре триметилэтилметан.
2. Напишите структурную формулу и назовите по рациональной наменклатуре 2,3-диметилпентан.
3. Назовите по рациональной номенклатуре
СН3
|
Н3С―С―СН3
|
СН3
4. Назовите по международной номенклатуре
СН3 СН2―СН3
| |
СН3―С ― СН―СН―СН3
| |
СН3 СН―СН3
|
СН3
5. Найдите наиболее длинную цепь углеродных атомов, выпишите ее в горизонтальный ряд и назовите парафин по международной номенклатуре
СН3―СН ― СН―СН2―СН―СН3
| | |
СН3 СН3 СН3
6. Какой углеводород получится при действии металлического натрия на бромэтан. Напишите уравнение реакции, назовите углеводород по международной номенклатуре.
Какой углеводород получится при действии металлического натрия на бромэтан. Напишите уравнение реакции, назовите углеводород по международной номенклатуре.
Проверочная работа по теме: НОМЕНКЛАТУРА АЛКАНОВ
Вариант 2
1. Напишите структурную формулу и назовите по международной наменклатуре диметилдиэтилметан.
2. Напишите структурную формулу и назовите по рациональной наменклатуре 3-метил-3-этилпентан.
3. Назовите по рациональной номенклатуре
СН2―СН3
|
Н3С―С ― СН―СН3
| |
Н3С СН3
4. Назовите по международной номенклатуре
СН3
|
Н3С―СН СН3
| |
СН3―СН2―С―СН2―С―СН3
| |
Н3С―СН2 СН2―СН3
5.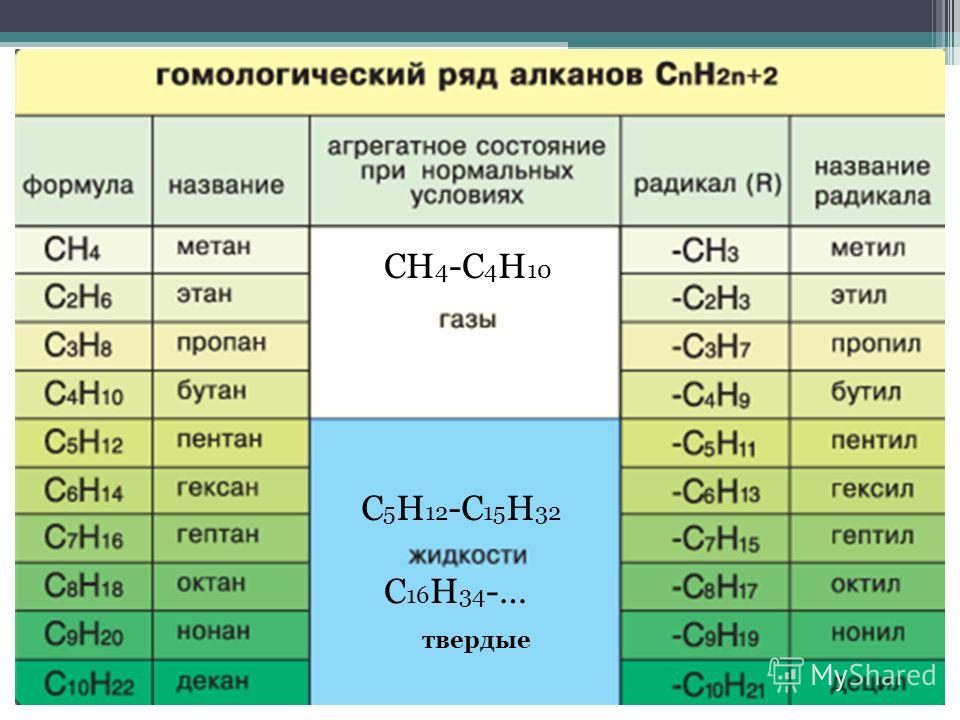 Найдите наиболее длинную цепь углеродных атомов, выпишите ее в горизонтальный ряд и назовите парафин по международной номенклатуре
Найдите наиболее длинную цепь углеродных атомов, выпишите ее в горизонтальный ряд и назовите парафин по международной номенклатуре
С2Н5
|
С2Н5―С―С2Н5
|
С2Н5
6. Какой углеводород получится при действии металлического натрия на 1-бромпропан. Напишите уравнение реакции, назовите углеводород по международной номенклатуре.
Проверочная работа по теме: НОМЕНКЛАТУРА АЛКАНОВ
Вариант 3
1. Напишите структурную формулу и назовите по международной наменклатуре метилдиэтилизопропилметан.
2. Напишите структурную формулу и назовите по рациональной наменклатуре 2,3,4-триметил-3-изопропилметан.
3. Назовите по рациональной номенклатуре
Н3С―СН―СН3
|
СН2―СН3
4. Назовите по международной номенклатуре
Назовите по международной номенклатуре
СН3
|
Н3С СН2 СН2―СН2―СН3
| | |
СН3―С―С―СН2―С―СН2―СН3
| | |
Н3С СН2 СН―СН3
| |
СН3 СН3
5. Найдите наиболее длинную цепь углеродных атомов, выпишите ее в горизонтальный ряд и назовите парафин по международной номенклатуре
С2Н5
|
СН3―СН―С ― СН2
| | |
СН3 С2Н5 С2Н5
6. Какой углеводород получится при действии металлического натрия на 2-хлорпропан. Напишите уравнение реакции, назовите углеводород по международной номенклатуре.
Какой углеводород получится при действии металлического натрия на 2-хлорпропан. Напишите уравнение реакции, назовите углеводород по международной номенклатуре.
Проверочная работа по теме: НОМЕНКЛАТУРА АЛКАНОВ
Вариант 4
1. Напишите структурную формулу и назовите по международной наменклатуре диметилдиизопропилметан.
2. Напишите структурную формулу и назовите по рациональной наменклатуре 2,2,4,4-тетраметилпентан.
3. Назовите по рациональной номенклатуре
СН3
|
СН3―СН―СН―СН―СН3
| |
СН3 СН2―СН3
4. Назовите по международной номенклатуре
СН3
|
Н3С―СН2 СН3 СН2―СН2 СН3
| | | |
СН3―СН―СН―С―СН2―СН2―С―СН3
| |
Н3С―СН2―СН2 СН3
5. Найдите наиболее длинную цепь углеродных атомов, выпишите ее в горизонтальный ряд и назовите парафин по международной номенклатуре
Найдите наиболее длинную цепь углеродных атомов, выпишите ее в горизонтальный ряд и назовите парафин по международной номенклатуре
С3Н7
|
СН3―С―СН3
|
СН3
6. Какой углеводород получится при действии металлического натрия на 1-хлор-2-метилпропан. Напишите уравнение реакции, назовите углеводород по международной номенклатуре.
Клавиатуры: Komplete Kontrol S49 / S61
Общее количество подключений
Интеграция с любой установкой с возможностью подключения по USB и питанием от шины; MIDI вход / выход; два назначаемых педальных входа; и гнездо для замка Kensington.
Восемь сенсорных ручек
Точная настройка всех ваших звуков — предварительно сопоставленные с наиболее полезными параметрами каждого инструмента и эффекта KOMPLETE и Native Kontrol Standard (NKS).
Регулировка высоты тона и модуляции
Эргономичные прорезиненные колеса высоты тона и модуляции, а также назначаемая сенсорная интеллектуальная полоса для расширенных творческих возможностей.
Световод
Просматривайте звуки, зоны клавиш, переключатели, шкалы и многое другое с первого взгляда с помощью индикаторов RGB над каждой клавишей.
Клавиатура Fatar
KOMPLETE KONTROL оснащен лучшими в отрасли клавишными панелями от Fatar — доступны с 49 или 61 полу-взвешенными клавишами с послекасанием.
Цветные дисплеи с высоким разрешением
При просмотре звуков, настройке параметров или создании эскизов эти цветные дисплеи с высоким разрешением позволяют сосредоточиться на творчестве, а не на компьютере.
Энкодер, 4 направления
Просматривайте звуки и управляйте проектами быстро и интуитивно.
Управление транспортом DAW
Получите прямой доступ к транспортным функциям в Logic Pro X, Ableton Live, Cubase, Nuendo и GarageBand.
MASCHINE control
Получите доступ в одно касание к своим сценам, узорам и многому другому в MASCHINE.
Как назвать органический соединения с использованием правил IUPAC
|
ВВЕДЕНИЕ В АЛКАНЫ И ЦИКЛОАЛКАНЫ Это вводная страница об алканах, таких как метан, этан, пропан, бутан и других.В нем рассматриваются их формулы и изомерия, их физические свойства и введение в их химическую реакционную способность. Что такое алканы и циклоалканы? Алканы Формулы Алканы — это простейшее семейство углеводородов — соединения, содержащие только углерод и водород. Они содержат только углерод-водородные связи и одинарные углерод-углеродные связи. Первые шесть:
Вы можете вычислить формулу любого из них, используя: C n H 2n + 2 Изомерия Все алканы с 4 или более атомами углерода в них обнаруживают структурную изомерию .Это означает, что для каждой молекулярной формулы вы можете нарисовать две или несколько различных структурных формул. Например, C 4 H 10 может быть любой из этих двух разных молекул: Они называются соответственно бутан и 2-метилпропан . | ||||||||||||
Примечание: Если вы не уверены в названиях органических соединений, различных способах рисования органических соединений или структурной изомерии, то вам действительно следует перейти по этим ссылкам, прежде чем продолжить. Вы должны прочитать всю страницу о рисовании органических молекул, но нет необходимости читать две другие, кроме того, где они говорят об алканах. Используйте кнопку НАЗАД в браузере, чтобы вернуться на эту страницу. | ||||||||||||
Циклоалканы Циклоалканы снова содержат только углерод-водородные связи и одинарные углерод-углеродные связи, но на этот раз атомы углерода объединены в кольцо. Самый мелкий циклоалкан — это циклопропан. Если вы посчитаете атомы углерода и водорода, вы увидите, что они больше не соответствуют общей формуле C n H 2n + 2 . Соединив атомы углерода в кольцо, вы должны были потерять два атома водорода. Вам он вряд ли когда-нибудь понадобится, но общая формула циклоалкана — C n H 2n . Не думайте, что все это плоские молекулы. Все циклоалканы, начиная с циклопентана и выше, существуют в виде «сморщенных колец». Циклогексан, например, имеет кольцевую структуру, которая выглядит следующим образом: Это известно как «стул» циклогексана — из-за его формы, которая отдаленно напоминает стул. | ||||||||||||
Примечание: Эта молекула постоянно меняется: атом слева, который в данный момент направлен вниз, переворачивается вверх, а атом справа — вниз. Во время процесса образуется другая (немного менее стабильная) форма циклогексана, известная как форма «лодочки».В таком расположении оба эти атома направлены вверх или вниз одновременно. | ||||||||||||
Физические свойства Точки кипения Факты Все указанные температуры кипения относятся к изомерам с «прямой цепью», которых больше одного. Обратите внимание, что первые четыре алкана являются газами при комнатной температуре. Твердые вещества не начинают появляться примерно до C 17 H 36 . Вы не можете быть более точными, потому что каждый изомер имеет разную температуру плавления и кипения. К тому времени, как вы получите 17 атомов углерода в алкане, будет невероятное количество изомеров! Циклоалканы имеют температуры кипения примерно на 10-20 K выше, чем соответствующие алканы с прямой цепью. Пояснения Между углеродом и водородом не так много разницы в электроотрицательности, поэтому полярность связи практически отсутствует.Сами молекулы также имеют очень небольшую полярность. Полностью симметричная молекула, такая как метан, совершенно неполярна. | ||||||||||||
Примечание: Если вы не уверены в электроотрицательности и полярности, вам действительно следует перейти по этой ссылке, прежде чем продолжить. Используйте кнопку НАЗАД в браузере, чтобы вернуться на эту страницу. | ||||||||||||
Это означает, что единственными притяжениями между одной молекулой и ее соседями будут дисперсионные силы Ван-дер-Ваальса.Они будут очень маленькими для такой молекулы, как метан, но будут увеличиваться по мере того, как молекулы становятся больше. Вот почему температуры кипения алканов увеличиваются с увеличением размера молекулы. | ||||||||||||
Примечание: Если вы не уверены в силах Ван-дер-Ваальса, вам следует перейти по этой ссылке, прежде чем продолжить. Используйте кнопку НАЗАД в браузере, чтобы вернуться на эту страницу. | ||||||||||||
Если есть изомеры, чем более разветвлена цепь, тем ниже температура кипения.Силы дисперсии Ван-дер-Ваальса меньше для более коротких молекул и действуют только на очень коротких расстояниях между одной молекулой и ее соседями. Коротким молекулам жира (с большим количеством разветвлений) сложнее лежать так близко друг к другу, как длинным тонким. Например, точки кипения трех изомеров C 5 H 12 составляют:
Немного более высокие температуры кипения циклоалканов, по-видимому, связаны с тем, что молекулы могут сближаться, поскольку кольцевая структура делает их более аккуратными и менее «извилистыми»! Растворимость Факты Нижеследующее в равной степени применимо к алканам и циклоалканам. Алканы практически не растворяются в воде, но растворяются в органических растворителях.Жидкие алканы являются хорошими растворителями для многих других ковалентных соединений. Пояснения Растворимость в воде Когда молекулярное вещество растворяется в воде, у вас должно быть
| ||||||||||||
Примечание: Если вы не уверены в водородных связях, вам следует перейти по этой ссылке, прежде чем продолжить. Используйте кнопку НАЗАД в браузере, чтобы вернуться на эту страницу. | ||||||||||||
Разрушение любого из этих аттракционов требует затрат энергии, хотя количество энергии, необходимое для разрушения дисперсионных сил Ван-дер-Ваальса в чем-то вроде метана, довольно незначительно.Однако это не относится к водородным связям в воде. В качестве упрощения, вещество будет растворяться, если при создании новых связей между веществом и водой выделяется достаточно энергии, чтобы восполнить то, что используется для разрушения первоначального притяжения. Единственное новое притяжение между молекулами алкана и воды — Ван-дер-Ваальс. Они не выделяют достаточно энергии, чтобы компенсировать то, что вам нужно для разрыва водородных связей в воде.Алкан не растворяется. | ||||||||||||
Примечание: Причина, по которой это упрощение, заключается в том, что вы также должны учитывать изменения энтропии, когда что-то растворяется. Если вы еще не знаете об энтропии, не беспокойтесь об этом! | ||||||||||||
Растворимость в органических растворителях В большинстве органических растворителей главными силами притяжения между молекулами растворителя являются ван-дер-ваальсовы силы — либо дисперсионные силы, либо диполь-дипольные притяжения. Это означает, что когда алкан растворяется в органическом растворителе, вы нарушаете силы Ван-дер-Ваальса и заменяете их новыми силами Ван-дер-Ваальса. Эти два процесса более или менее энергетически нейтрализуют друг друга, поэтому нет никаких препятствий для растворимости. Химическая реакционная способность Алканы Алканы содержат сильные одинарные углерод-углеродные связи и сильные углерод-водородные связи. Связи углерод-водород лишь очень слабо полярны, и поэтому в молекулах нет никаких частиц, несущих сколько-нибудь значительный положительный или отрицательный заряд, к которому могли бы быть привлечены другие объекты. Например, вы обнаружите (или, возможно, уже знаете), что многие органические реакции начинаются из-за того, что ион или полярная молекула притягивается к части органической молекулы, которая несет некоторый положительный или отрицательный заряд. Этого не происходит с алканами, потому что молекулы алканов не имеют разделения зарядов. В результате алканы имеют довольно ограниченный набор реакций. Можно
Все эти реакции описаны на отдельных страницах, если вы перейдете в меню алканов (см. Ниже). Циклоалканы Циклоалканы очень похожи на алканы по реакционной способности, за исключением очень маленьких, особенно циклопропана. Циклопропан гораздо более реактивен, чем можно было ожидать. Причина в валентных углах в кольце. Обычно, когда углерод образует четыре одинарные связи, валентные углы составляют около 109.5 °. В циклопропане они равны 60 °. При таком близком расположении электронных пар возникает сильное отталкивание между связующими парами, соединяющими атомы углерода. Это облегчает разрыв связей. Эффект этого исследуется на странице о реакциях этих соединений с галогенами, к которой вы можете получить доступ из меню алканов ниже.
В меню алканов.. . К меню прочих органических соединений. . . В главное меню. . . © Джим Кларк 2003 (изменено в июле 2015 г.) | ||||||||||||
PPT — Глава 2: Алканы и циклоалканы Презентация PowerPoint, скачать бесплатно
Глава 2: Алканы и циклоалканы
Структура алканов
9115 Органические соединения
9115 Номенклатура 9115
Алкильные группы
Нумерация родительской углеродной цепи Корневое название — это название самой длинной непрерывной углеродной цепи (родительской углеродной цепи). Группы, присоединенные к основной цепи, называются заместителями.Насыщенные заместители, содержащие только углерод и водород, называются алкильными группами. Назначается заменой -ана алкана на -ил
Основная цепь пронумерована так, чтобы первый заместитель , встречающийся в цепи, получил наименьший возможный номер. В этом случае каждый заместитель располагается по номеру углерода, к которому он присоединен. Когда две или более идентичных группы присоединены к основной цепи, используются префиксы, такие как ди-три-, тетра-.
Если есть две непрерывные цепи одинаковой длины, выберите с наибольшим количеством ответвлений.
Если есть ветви, равноотстоящие от каждого конца самой длинной цепочки, начните нумерацию ближайшей к третьей ветви.
Если нет третьей ветви, начните нумерацию с ближайшего заместителя , имя которого имеет буквенный приоритет;
Укажите название IUPAC для показанного соединения?
Дайте название IUPAC следующим соединениям:
Clicker Question Какое правильное название IUPAC для указанного ниже соединения? • 4-метилпентан • 2-метилпентан • Метилбутан • Диметилбутан
Алкильные и галогенные заместители
Существуют четыре различных бутильных группы:
. Буква R используется в качестве общего символа. алкильная группа. RH алкан RX X = F, Cl, Br, I (галоген) Алкилгалогенид Названные: F- (фтор-), Cl- (хлор-), Br- (бром-) I- (йод-)
Напишите формулу 2,2,4-триметилпентана
Щелчок Вопрос Студент назвал углеводород как 2-этилпентан и получил неправильную оценку. Каким должно быть правильное название соединения по ИЮПАК?
Назовите следующие соединения по системе IUPAC: Ch4CHFCh3Ch4 Напишите структуру 3,3-диметилоктана
Назовите следующие соединения по системе IUPAC: Ch4CHFCh3Ch4 Напишите структуру 3,3-диметилметилового эфира
Физические свойства алканов и несвязывающие межмолекулярные взаимодействия Молекулы воды полярны и обладают особым притяжением, называемым водородными связями.Алканы нерастворимы в воде, потому что они неполярны (все CC и CH почти чисто ковалентны)
Ван-дер-Ваальсовы притяжения Точки кипения алканов повышаются по мере увеличения длины цепи и падают по мере того, как цепи становятся разветвленными. и более почти сферической формы
Влияние молекулярных форм на аттракционы Ван-дер-Ваальса
Конформации алканов
Вопрос-кликер? Наиболее стабильная конформация пропана: • Затменная • Плоская • Лодка • Смещенная • Стул
Циклоалкановая номенклатура и конформация
Один заместитель всегда находится у атома углерода кольца с номером 1, остальные атомы углерода — это затем пронумерованы последовательно таким образом, чтобы дать другим заместителям наименьшие возможные номера.С другими заместителями один с наивысшим алфавитным приоритетом расположен на атоме углерода 1.
QR-коды Или перейдите на http://bit.ly/14tF1qx Лаборатория молекулярного моделирования: принесите все iPad в лабораторию на этой неделе Прочтите и Практика перед лабораторной работой, если у вас уже есть iPad на этой неделе Ссылка на инструкции iSpartan доступна на веб-сайте лаборатории, или вы можете использовать считыватели QR-кодов со своих смартфонов или iPad
iSpartan Basics Video Tutorial Или перейдите по ссылке http: / /немного.ly / WFr8jz
Дайте названия IUPAC для следующих соединений:
Циклопропан
Циклоалканы с более чем тремя атомами углерода неполярны и имеют «сморщенные» конформации.
Кликер Вопрос? Какова молекулярная формула циклоалкана с шестью атомами углерода? • C6h24 • C6h22 • C6h20 • C6h26 • C6H7
Кликер Вопрос? Валентный угол нормального тетраэдрического sp3-гибридизированного углерода равен 109.5 °. Каков приблизительный валентный угол C – C – C циклобутана? • 109,50 • 1200 • 600 • 1800 • 900
Конформация кресла циклогексана
Более крупные заместители в циклогексане (такие как метильная группа) стабильны в экваториальных положениях, чтобы избежать осевого сжатия.
Конформация Лодочка
Молекула глюкозы (шестичленное кольцо в конформации кресло .
Цис-транс-изомерия циклоалканов
Реакции алканов Одинарные углерод-углеродные связи Неполярные, поэтому относительно инертны и часто используются в качестве растворителей. Реагирует с кислородом и галогенами.
Подождите …
Пожалуйста, включите куки и перезагрузите страницу.
Это автоматический процесс. Ваш браузер в ближайшее время перенаправит вас на запрошенный контент.
Подождите до 5 секунд…
+ ((! + [] + (!! []) + !! [] + !! [] + !! [] + !! [] + !! [] + !! [] + []) + (! + [] + (!! []) + !! []) + (! + [] + (!! []) + !! [] + !! [] + !! [] + !! [ ] + !! [] + !! []) + (! + [] — (!! [])) + (! + [] + (!! []) + !! [] + !! []) + (+ !! []) + (! + [] + (!! []) + !! [] + !! [] + !! [] + !! []) + (! + [] + ( !! []) + !! [] + !! []) + (+ !! [])) / + ((! + [] + (!! []) — [] + []) + (! + [] + (!! []) + !! [] + !! [] + !! []) + (! + [] + (!! []) + !! [] + !! [] + !! []) + (+ !! []) + (+ !! []) + (! + [] + (!! []) + !! [] + !! []) + (! + [ ] + (!! []) + !! [] + !! [] + !! [] + !! []) + (! + [] — (!! [])) + (! + [] + (!! []) + !! [] + !! [] + !! [] + !! []))
+ ((! + [] + (!! []) + !! [] + !! [] + !! [] + !! [] + !! [] + []) + (! + [] + (!! []) + !! [] + !! [] + !! [ ] + !! [] + !! [] + !! [] + !! []) + (! + [] + (!! []) + !! [] + !! [] + !! [] + !! [] + !! []) + (! + [] — (!! [])) + (! + [] — (!! [])) + (! + [] + (!! [ ]) + !! []) + (! + [] + (!! []) + !! [] + !! []) + (! + [] + (!! []) + !! [] ) + (! + [] + (!! []) + !! [] + !! [] + !! [] + !! [] + !! [])) / + ((! + [] + (!! []) + !! [] + !! [] + !! [] + !! [] + !! [] + !! [] + !! [] + []) + (+ !! []) + (! + [] + (!! []) + !! [] + !! [] + !! []) + (+ !! []) + (! + [] + (!! []) + !! [] + !! [] + !! [] + !! [] + !! [] + !! [] + !! []) + (! + [] + (!! [ ]) + !! []) + (! + [] + (!! []) + !! []) + (! + [] + (!! []) + !! []) + (! + [] + (!! []) + !! [] + !! [] + !! [] + !! [] + !! [] + !! []))
+ ((! + [] + (!! []) + !! [] + !! [] + !! [ ] + !! [] + !! [] + !! [] + []) + (! + [] + (!! []) + !! []) + (! + [] + (!! [ ]) + !! [] + !! [] + !! [] + !! [] + !! [] + !! []) + (! + [] — (!! [])) + (! + [] + (!! []) + !! [] + !! []) + (+ !! []) + (! + [] + (!! []) + !! [] + !! [] + !! [] + !! []) + (! + [] + (!! []) + !! [] + !! []) + (! + [] + (!! []) + !! [] + !! [] + !! [] + !! [] + !! [])) / + ((! + [] + (!! []) + !! [] + !! [] + !! [] + !! [] + !! [] + !! [] + !! [] + []) + (! + [] + (!! []) — []) + ( ! + [] + (!! []) + !! [] + !! []) + (! + [] + (!! []) + !! [] + !! [] + !! [] + !! []) + (! + [] + (!! []) + !! [] + !! [] + !! []) + (! + [] + (!! []) +! ! []) + (! + [] + (!! []) — []) + (+ !! []) + (! + [] + (!! []) + !! [] + !! []))
+ ((! + [] + (!! []) + !! [] + !! [] + !! [] + !! [] + !! [] + []) + (! + [] + (!! []) + !! [] + !! [] + !! [] + !! [] + !! [] + !! [] + !! []) + ( ! + [] + (!! []) + !! [] + !! [] + !! [] + !! [] + !! []) + (! + [] — (!! []) ) + (! + [] — (!! [])) + (! + [] + (!! []) + !! []) + (! + [] + (!! []) + !! [] + !! []) + (! + [] + (!! []) + !! []) + (! + [] + (!! []) + !! [] + !! [] + !! [] + !! [] + !! [])) / + ((! + [] + (!! []) + !! [] + !! [] + !! [] + !! [] + !! [] + !! [] + !! [] + []) + (! + [] + (!! []) + !! [] + !! [] + !! []) + (! + [] — (!! [])) + (+ !! []) + (! + [] + (!! []) + !! [] + !! [] + !! [] ) + (+ !! []) + (! + [] + (!! []) + !! [] + !! [] + !! [] + !! [] + !! []) + ( ! + [] + (!! []) + !! [] + !! [] + !! [] + !! [] + !! [] + !! [] + !! []) + (! + [] + (!! []) + !! [] + !! [] + !! [] + !! [] + !! [] + !! [] + !! []))
+ ((! + [] + (!! []) + !! [] + !! [] + !! [] + !! [] + !! [] + !! [] + []) + (! + [] + (!! []) + !! []) + (! + [] + (!! []) + !! [] + !! [ ] + !! [] + !! [] + !! [] + !! []) + (! + [] — (!! [])) + (! + [] + (!! []) + !! [] + !! []) + (+ !! []) + (! + [] + (!! []) + !! [] + !! [] + !! [] + !! [ ]) + (! + [] + (!! []) + !! [] + !! []) + (+ !! [])) / + ((! + [] + (!! []) + !! [] + !! [] + !! [] + !! [] + !! [] + !! [] + []) + (! + [] + (!! []) + !! []) + (! + [] + (!! []) + !! [] + !! [] + !! [] + !! [] + !! [] + !! []) + (! + [] + (!! []) + !! [] + !! []) + (! + [] + (!! []) + !! [] + !! [] + !! [] + !! [] + !! [] + !! []) + (! + [] + (!! []) + !! [] + !! [] + !! [] + !! [] +! ! [] + !! []) + (! + [] — (!! [])) + (! + [] + (!! []) — []) + (! + [] + (!! []) + !! [] + !! [] + !! [] + !! [] + !! []))
+ ((! + [] + (!! []) + !! [ ] + !! [] + !! [] + !! [] + !! [] + !! [] + []) + (! + [] + (!! []) + !! []) + (! + [] + (!! []) + !! [] + !! [] + !! [] + !! [] + !! [] + !! []) + (! + [] — (!! [])) + (! + [] + (!! []) + !! [] + !! []) + (+ !! []) + (! + [] + (!! [ ]) + !! [] + !! [] + !! [] + !! []) + (! + [] + (!! []) + !! [] + !! []) + (+ !! [])) / + ((! + [] + (!! []) + !! [] + !! [] + !! [] + []) + (! + [] + (!! []) + !! [] + !! [] + !! []) + (! + [] + (!! []) + !! [] + !! [] + !! [] + !! []) + (+ !! []) + (! + [] + (!! []) + !! []) + (! + [] + (!! []) + !! [] +! ! []) + (! + [] + (!! []) + !! []) + (+ !! []) + (! + [] + (!! []) + !! [] + !! [] + !! [] + !! []))
90 004 + ((! + [] + (!! []) + !! [] + !! [] + !! [] + !! [] + !! [] + !! [] + []) + (! + [] + (!! []) + !! []) + (! + [] + (!! []) + !! [] + !! [] + !! [] + !! [ ] + !! [] + !! []) + (! + [] — (!! [])) + (! + [] + (!! []) + !! [] + !! []) + (+ !! []) + (! + [] + (!! []) + !! [] + !! [] + !! [] + !! []) + (! + [] + ( !! []) + !! [] + !! []) + (! + [] + (!! []) + !! [] + !! [] + !! [] + !! [] + !! [])) / + ((! + [] + (!! []) — [] + []) + (! + [] + (!! []) + !! [] + !! [ ] + !! [] + !! [] + !! [] + !! []) + (! + [] + (!! []) + !! []) + (! + [] + (! ! []) + !! [] + !! [] + !! [] + !! [] + !! []) + (! + [] + (!! []) + !! [] +! ! [] + !! [] + !! [] + !! [] + !! []) + (! + [] + (!! []) + !! [] + !! [] + !! [] + !! [] + !! []) + (! + [] + (!! []) + !! [] + !! [] + !! [] + !! []) + (! + [] + (!! []) + !! [] + !! [] + !! []) + (! + [] + (!! []) — []) »+ ((! + [] + (!! []) + !! [] + !! [] + !! [] + !! [] + !! [] + !! [] + []) + (! + [] + (!! []) + !! [] + !! [] + !! []) + (! + [] + (!! []) + !! [] + !! [] + !! [ ] + !! [] + !! [] + !! []) + (! + [] + (!! []) + !! [] + !! [] + !! []) + (! + [] + (!! []) + !! [] + !! [] + !! [] + !! [] + !! [] + !! [] + !! []) + (! + [ ] + (!! []) + !! [] + !! [] + !! [] + !! [] + !! [] + !! [] + !! []) + (! + [] + (!! []) + !! [] + !! [] + !! []) + (! + [] — (!! [])) + (! + [] + (!! []) + !! [])) / + ((! + [] + (!! []) + !! [] + !! [] + !! [] + !! [] + []) + (! + [] + (!! []) — []) + (! + [] + (!! []) + !! [] + !! [] + !! [] + !! []) + (! + [] + (!! []) + !! [] + !! []) + (! + [] + (!! []) + !! [] + !! [] + !! [] + !! [] + !! []) + (! + [] + (!! []) — []) + (! + [] + ( !! []) + !! [] + !! [] + !! [] + !! [] + !! [] + !! [] + !! []) + (! + [] + (! ! []) + !! [] + !! [] + !! [] + !! []) + (! + [] + (!! []) + !! [] + !! [] +! ! [] + !! []))
+ ((! + [] + (!! []) + !! [] + !! [] + !! [] + !! [] + !! [ ] + !! [] + !! [] + []) + (! + [] + (!! []) + !! [] + !! []) + (+ !! []) + (! + [] — (!! [])) + (! + [] + (!! []) + !! [] + !! [] + !! [] + !! [] + !! [] + !! []) + (! + [] + (!! []) + !! []) + (! + [] + (!! []) + !! [] + !! [] + !! [] + !! [] + !! [] + !! [] + !! []) + (! + [] + (!! []) + !! [] + !! [] + !! [ ] + !! [] + !! [] + !! []) + (+ !! [])) / + ((! + [] + (!! []) + !! [] + []) + (! + [] + (!! []) + !! [] + !! [] + !! [] + !! [] + !! []) + (! + [] — (!! [ ])) + (! + [] + (!! []) + !! [] + !! [] + !! [] + !! [] + !! []) + (! + [] + ( !! []) + !! [] + !! []) + (! + [] + (!! []) + !! []) + (! + [] + (!! []) +! ! [] + !! [] + !! [] + !! [] + !! [] + !! [] + !! []) + (! + [] — (!! [])) + ( ! + [] + (!! []) + !! [] + !! []))
+ ((! + [] + (!! []) + !! [] + !! [] + !! [] + !! [] + !! [] + !! [] + []) + (+ !! []) + (! + [] + (!! []) + !! [] + !! [] + !! [] + !! [] + !! []) + (! + [] + (!! []) + !! [] + !! [] + !! []) + (! + [] — (!! [])) + (! + [] + (!! []) + !! [] + !! []) + (! + [] + (!! []) — []) + (! + [] + (!! []) + !! [] + !! [] + !! []) + (! + [] + (!! []) + !! [ ])) / + ((! + [] + (!! []) + !! [] + !! [] + !! [] + !! [] + !! [] + []) + (! + [] + (!! []) + !! [] + !! [] + !! []) + (! + [] + (!! []) + !! [] + !! [] + !! [] + !! [] + !! [] + !! []) + (! + [] + (!! []) + !! [] + !! [] + !! [] + !! [] + !! []) + (! + [] + (!! []) + !! [ ] + !! []) + (! + [] + (!! []) — []) + (! + [] + (!! []) + !! [] + !! [] + !! []) + (! + [] + (!! []) + !! [] + !! [] + !! [] + !! []) + (! + [] + (!! []) + !! [] + !! [] + !! [] + !! [] + !! [] + !! []))
+ ((! + [] + (!! []) +! ! [] + !! [] + !! [] + !! [] + !! [] + !! [] + !! [] + []) + (! + [] + (!! []) + !! [
Материалы для учащихся 10-го КЛАССА 1–4 квартал LM
Мы все еще загружаем материалы для учащихся GRADE 10.По запросу, вот ссылки на файлы. Остальные файлы скоро будут загружены. Пожалуйста, проверяйте этот раздел время от времени.
Мы подготовили материалы для учащихся GRADE 10. Просто перейдите по ссылкам того, что вам нужно, чтобы попасть на страницу загрузки.
Материалы для учащихся 10-го КЛАССА (LM)
ARALING PANLIPUNAN Учебные материалы / Учебные материалы
Mga Isyung Pangkapaligiran at Pang-ekonomiya
ENGLISH Материалы для учащихся / Учебные материалы
FILIPINO Учебные материалы / Учебные материалы
Estratehiya sa Pag-aaral
Таласалита
Пагсасалита
Pag-unawa sa Binasa
МАТЕМАТИКА Материалы для учащихся / Учебные материалы
Паттерны и алгебра
- DLM 2 — Блок 7 Последовательности и серии
- Модуль EASE 1 Полиномиальные функции
- Модуль EASE 1 Поиск закономерностей в последовательностях, арифметических, геометрических и других аспектах
- Модуль EASE 2 Поиск закономерностей в последовательностях, арифметических, геометрических и других аспектах
- Модуль EASE 3 Поиск закономерностей в последовательностях, арифметических, геометрических и других аспектах
- Модуль EASE 4 Поиск закономерностей в последовательностях, арифметических, геометрических и других параметрах
- Модуль EASE 5 Поиск закономерностей в последовательностях, арифметических, геометрических и других параметрах
- Модуль EASE 6 Поиск закономерностей в последовательностях, арифметических, геометрических и других аспектах
- Последовательность арифметических действий для аккредитации и эквивалентности NFE
- Учебный материал для аккредитации и эквивалентности NFE Геометрическая последовательность
- Учебный материал по аккредитации и эквивалентности NFE, изучающий полиномы
MAPEH Учебные материалы / Учебные материалы
Материалы для учащихся SCIENCE / Учебные материалы
Живые существа и окружающая их среда
Учебные материалы / Учебные материалы TLE
Эти учебные материалы были совместно разработаны и проверены преподавателями государственных и частных школ, колледжей и / или университетов.

 7 Kb)
7 Kb) 0/0
0/0 Связи в молекуле алканов:
Связи в молекуле алканов: пропан; б). бутан; в). метан; г). водород?
пропан; б). бутан; в). метан; г). водород? Формулы только алканов записаны в ряду:
Формулы только алканов записаны в ряду:  СО и Н2 ?
СО и Н2 ? 11; б). 15; в). 23; г). 25?
11; б). 15; в). 23; г). 25?
 В общем, базовая часть названия отражает
номер атомов углерода в том, что вы назначили
родительская цепочка . Суффикс в названии отражает
тип (ы) функциональной группы (ей), присутствующей на (или внутри)
родительская цепочка. Другие группы, которые присоединены к родительской цепочке
называются заместителями .
В общем, базовая часть названия отражает
номер атомов углерода в том, что вы назначили
родительская цепочка . Суффикс в названии отражает
тип (ы) функциональной группы (ей), присутствующей на (или внутри)
родительская цепочка. Другие группы, которые присоединены к родительской цепочке
называются заместителями . Они показаны ниже.
Они показаны ниже.

 Гало-
заместитель считается одного ранга с алкильным заместителем в
нумерация родительской цепочки. Галогены представлены как
следует:
Гало-
заместитель считается одного ранга с алкильным заместителем в
нумерация родительской цепочки. Галогены представлены как
следует: ). Тройные связи называются аналогичным образом с использованием суффикса -yne .
Положение множественной связи (ей) в родительской цепи является (являются)
обозначается размещением числа (ей) первого углерода кратного
облигации непосредственно перед базовым названием.
). Тройные связи называются аналогичным образом с использованием суффикса -yne .
Положение множественной связи (ей) в родительской цепи является (являются)
обозначается размещением числа (ей) первого углерода кратного
облигации непосредственно перед базовым названием. При выборе нумерации двойные связи
учитывая самые низкие числа.
При выборе нумерации двойные связи
учитывая самые низкие числа. Если есть два
или несколько цепочек, конкурирующих за выбор в качестве родительской цепочки
(цепочка с наибольшим количеством связей), выбор идет к
(1) цепочка с наибольшим числом атомов углерода,
(2) количество атомов углерода равно, цепь, содержащая
максимальное количество двойных связей.
Если есть два
или несколько цепочек, конкурирующих за выбор в качестве родительской цепочки
(цепочка с наибольшим количеством связей), выбор идет к
(1) цепочка с наибольшим числом атомов углерода,
(2) количество атомов углерода равно, цепь, содержащая
максимальное количество двойных связей.