|
|
|
|
 Far Far |
 WinNavigator WinNavigator |
 Frigate Frigate |
 Norton
Commander Norton
Commander |
 WinNC WinNC |
 Dos
Navigator Dos
Navigator |
 Servant
Salamander Servant
Salamander |
 Turbo
Browser Turbo
Browser |
|
|
 Winamp,
Skins, Plugins Winamp,
Skins, Plugins |
 Необходимые
Утилиты Необходимые
Утилиты |
 Текстовые
редакторы Текстовые
редакторы |
 Юмор Юмор |
|
|
|
File managers and best utilites |
Реферат: Паранеопластические синдромы. Синдром свита реферат
Синдром Свита - Клиническая дерматология и венерология - 2013-03
Синдром Свита (синонимы — острый фебрильный нейтрофильный дерматоз, острый лихорадочный дерматоз; МКБ-Х 10.L98.2) — редкое заболевание из группы нейтрофильных дерматозов, характеризующееся рецидивирующим течением, болезненными ярко-красными папулами и воспалительными бляшками, сосцевидными возвышениями, лихорадкой, артралгией и нейтрофильным лейкоцитозом. Болеют чаще женщины в возрасте 30—60 лет. Синдром Свита также наблюдается в молодом возрасте и у детей [1, 2]. Самые юные пациенты — братья, у которых дерматоз развился на 10-й и 15-й день жизни [3].
Это заболевание имеет три клинические формы: классическую, или идиопатическую, ассоциированную с онкологическими заболеваниями и лекарственную (табл. 1) [2, 3].
Классический вариант синдрома Свита может ассоциироваться с инфекцией верхних дыхательных путей или желудочно-кишечного тракта, а также с беременностью [2—4]. При синдроме Свита, ассоциированном с онкологическим заболеванием крови, преобладания женщин не наблюдается, что чаще связано с острым миелогенным лейкозом. Среди сóлидных опухолей часто встречается рак молочной железы и желудочно-кишечного тракта [5]. Лекарственный вариант синдрома Свита чаще развивается после приема гранулоцитарного колониестимулирующего фактора [6, 7]. Однако есть данные о возникновении синдрома Свита при употреблении других лекарственных средств, таких как миноциклин, гидралазин, фуросемид [1].
На патогенез синдрома Свита влияют многие факторы. Предполагается, что в основе заболевания лежит септический процесс, сопровождающийся лихорадкой и периферическим лейкоцитозом. Этиологическим фактором может являться бактериальная инфекция, поскольку у большинства пациентов с классической формой синдрома Свита за 1—3 нед до развития кожных проявлений наблюдаются инфекция верхних дыхательных путей или ангина, которые протекают с лихорадкой. Другим аргументом в пользу бактериальной инфекции является улучшение состояния пациентов с синдромом Свита, развившемся на фоне иерсиниоза при приеме системных антибиотиков [2—4].
Синдром Свита может развиться при реакции гиперчувствительности к бактериальным, вирусным или опухолевым антигенам. На это указывают гистопатологические изменения и течение заболевания. Данная гипотеза подтверждается быстрым уменьшением выраженности симптомов и разрешением кожных очагов в ответ на кортикостероиды [3, 8].
Прямую или косвенную роль в развитии симптомов и очагов могут играть цитокины. Потенциальными цитокинами, участвующими в патогенезе синдрома Свита, считаются гранулоцитарно-макрофагально колониестимулирующий фактор, интерфероны, интерлейкин-1, -3, -6 и -8 [2, 3].
Кожные высыпания обычно сопровождаются высокой лихорадкой и лейкоцитозом. Лихорадка может не только предшествовать поражению кожи, но и возникать одновременно с высыпаниями и сохраняться в течение всего периода существования дерматоза. К другим признакам синдрома Свита относятся артралгия, головная боль и миалгия [1—3].
Высыпания располагаются чаще всего на лице, шее, руках и ногах; кожа туловища поражается реже. Кожные очаги при синдроме Свита возникают в форме болезненных, красных или лилово-красных папул или узлов. Высыпания могут появляться в виде единичного очага или множественных поражений и часто располагаются асимметрично. Выраженный отек очагов приводит к тому, что они выглядят прозрачными и напоминают везикулы; это состояние описывается как иллюзия везикуляции. На более поздних стадиях в центре этих образований начинается разрешение, которое приводит к картине кольцевидных или дугообразных очагов. Очаги могут быть буллезными, подвергаться изъязвлению у пациентов с синдромом Свита, развившимся на фоне онкологического заболевания. Высыпания увеличиваются в течение дней и недель, а затем могут сливаться и образовывать бляшки неправильной формы с четкими границами. Очаги разрешаются спонтанно или после лечения, не оставляя рубцов. Примерно у 1/3—2/3 пациентов возможны рецидивы заболевания, при этом сыпь обычно возникает на том же самом месте [2, 3]. С дерматозом ассоциируется патергия кожи, которая проявляется, когда очаги синдрома Свита развиваются на месте повреждения кожных покровов. К таким местам относятся участки проведения процедур, например биопсий, венозных пункций [2, 3]. Сюда же относят места укусов насекомых и кошачьих царапин [2, 3], зоны проведения лучевой терапии [2].
Синдром Свита может развиваться как пустулезный дерматоз [2—4]. Очаги появляются в форме крошечных пустул, расположенных поверх папул, или же в форме пустул на эритематозном фоне [2].
Кожные очаги при подкожном синдроме Свита обычно имеют вид эритематозных болезненных узлов на конечностях [2, 8]. Они часто имитируют узловатую эритему, для установления точного диагноза необходимо патогистологическое исследование.
К внекожным проявлениям при синдроме Свита относят поражение костей, центральной нервной системы, органов зрения и слуха, почек, кишечника, печени, сердца, легких, полости рта, мышц и селезенки [2—4]. Имеются данные о связи дерматоза и стерильного остеомиелита у детей. Частота поражения глаз при классическом синдроме Свита вариабельна, а при ассоциированной с онкологическим заболеванием форме дерматоза, так же как и при лекарственной, глаза поражаются редко. В свою очередь поражение слизистой оболочки полости рта в виде язв чаще наблюдается у пациентов с синдромом Свита, ассоциированным с гематологическими заболеваниями, и редко у больных классической формой синдрома [2—5].
Диагностические критерии синдрома Свита представлены в табл. 2 [9].
Для постановки диагноза необходимо наличие двух главных и двух дополнительных критериев.
Диагностика синдрома Свита в практике дерматолога сопряжена со значительными трудностями. За пациентами наблюдают по поводу других заболеваний кожи (многоформной эритемы, токсикодермии, узловатой эритемы, панникулита и др.).
Приводим наше наблюдение.
Больная М., 49 лет, обратилась в районный КВК с жалобами на повышение температуры до 39 °С, озноб, недомогание, головную боль, высыпания.
За 1 мес до появления высыпаний перенесла острую респираторную вирусную инфекцию. Госпитализирована в хирургическое отделение центральной районной больницы, где получала следующее лечение: цефазолин по 1,0 мл внутримышечно 2 раза в сутки в течение 2 дней; с 3-х суток — преднизолон, 30 мг внутривенно капельно; цефтриаксон внутривенно 3 раза в день. Температура снизилась через 1 сут до субфебрильной.
С диагнозом многоформная экссудативная эритема направлена в Гомельский областной клинический кожно-венерологический диспансер (ГОККВД), в условиях стационара получала преднизолон (90 мг/сут), юнидокс солютаб 100 мг (по 1 таблетке 2 раза в сутки), раствор дипроспана (1,0 мл внутримышечно на 6-е сутки стационарного лечения). На 3-и сутки лечения преднизолоном высыпания стали регрессировать. На 8-е сутки больная выписана с улучшением.
Через 3 сут пациентка отметила новые высыпания на тех же местах, болезненные при надавливании. Повторно поступила в ГОККВД. Назначено лечение: преднизолон 90 мг внутримышечно утром, преднизолон по 5 мг 4 таблетки в обед, следующие 2 сут — преднизолон 60 мг внутримышечно утром, затем последующие 2 сут — преднизолон 30 мг внутримышечно утром; магния сульфат, клемастин, калия оротат. Наружно применяли мазь синафлан. На 2—3-и сутки лечения высыпания стали регрессировать. На 16-е сутки больная выписана из стационара (доза преднизолона — на 20 мг).
Через несколько дней отметила обострение процесса (появление болезненных при пальпации высыпаний практически на тех же местах, боли в голеностопных суставах). Проконсультирована по телефону врачом-дерматологом КВК. Назначен преднизолон (40 мг/сут со снижением дозы и полной отменой в течение 2 мес). На 2-е сутки после приема 40 мг преднизолона высыпания стали регрессировать, болезненность в голеностопных суставах прошла. В процессе лечения при приеме 20 мг преднизолона пациентка отметила новое обострение.
При осмотре: патологические изменения кожи носят распространенный характер. Элементы сыпи склонны к группировке, в некоторых регионах расположены асимметрично. На коже лица, преимущественно лба, век правого глаза, височной области (рис. 1), Рисунок 1. Асимметричные высыпания на коже лица. груди, верхней части спины (рис. 2 и рис. 3),
Рисунок 1. Асимметричные высыпания на коже лица. груди, верхней части спины (рис. 2 и рис. 3), Рисунок 2. Высыпания на коже спины в виде псевдовезикул.
Рисунок 2. Высыпания на коже спины в виде псевдовезикул. Рисунок 3. При пальпации высыпания плотные, болезненные. кистей (рис. 4),
Рисунок 3. При пальпации высыпания плотные, болезненные. кистей (рис. 4), Рисунок 4. На коже указательного пальца правой кисти — плотная и болезненная бляшка красного цвета, возникшая после микротравмы (феномен патергии). правой голени определяются папулы, бляшки красного и красно-синюшного цвета, «сочные» на вид, некоторые — псевдовезикулярные (напоминают везикулу или пузырь), в том числе с корочкой в центральной части, болезненные и плотные при пальпации.
Рисунок 4. На коже указательного пальца правой кисти — плотная и болезненная бляшка красного цвета, возникшая после микротравмы (феномен патергии). правой голени определяются папулы, бляшки красного и красно-синюшного цвета, «сочные» на вид, некоторые — псевдовезикулярные (напоминают везикулу или пузырь), в том числе с корочкой в центральной части, болезненные и плотные при пальпации.
На основании анамнеза, жалоб, клинических проявлений предположительно был выставлен диагноз синдрома Свита. Для его уточнения с согласия больной под местной анестезией из очага поражения на плече произведена биопсия кожи.
Результаты патогистологического исследования(рис. 5—9). Рисунок 5. Обзорная фотография пораженного участка кожи.
Рисунок 5. Обзорная фотография пораженного участка кожи. Рисунок 6. Эпидермис интактен. Густоклеточная полиморфноядерная инфильтрация дермы.
Рисунок 6. Эпидермис интактен. Густоклеточная полиморфноядерная инфильтрация дермы. Рисунок 7. Формирование субэпидермальных пузырей с выходом в них нейтрофилов.
Рисунок 7. Формирование субэпидермальных пузырей с выходом в них нейтрофилов. Рисунок 8. Диффузная лейкоклазия (ядерная пыль в виде мелких гиперхромных фрагментов неправильной формы) среди клеточного инфильтрата.
Рисунок 8. Диффузная лейкоклазия (ядерная пыль в виде мелких гиперхромных фрагментов неправильной формы) среди клеточного инфильтрата. Рисунок 9. Выраженная полиморфноядерная инфильтрация, локализующаяся преимущественно в сосочковом слое дермы. Эпидермис в воспалительный процесс не вовлечен. Слабовыраженный акантоз, очаговая вакуолизация клеток шиповатого слоя. Определяются очаговые мелкофокусные субэпидермальные пузыри с выходом нейтрофилов в их просвет. Дерма: сосочковый слой дермы разрыхлен, отечен; выраженная полиморфноклеточная инфильтрация как диффузно, так и периваскулярно; инфильтрат проникает в гиподерму. В клеточном составе инфильтрата — одинаковое количество лейкоцитов и лимфоцитов, меньше мононуклеаров. Диффузно по инфильтрату наблюдается лейкоклазия. Заключение: гистологическая картина соответствует синдрому Свита.
Рисунок 9. Выраженная полиморфноядерная инфильтрация, локализующаяся преимущественно в сосочковом слое дермы. Эпидермис в воспалительный процесс не вовлечен. Слабовыраженный акантоз, очаговая вакуолизация клеток шиповатого слоя. Определяются очаговые мелкофокусные субэпидермальные пузыри с выходом нейтрофилов в их просвет. Дерма: сосочковый слой дермы разрыхлен, отечен; выраженная полиморфноклеточная инфильтрация как диффузно, так и периваскулярно; инфильтрат проникает в гиподерму. В клеточном составе инфильтрата — одинаковое количество лейкоцитов и лимфоцитов, меньше мононуклеаров. Диффузно по инфильтрату наблюдается лейкоклазия. Заключение: гистологическая картина соответствует синдрому Свита.
Результаты лабораторных исследований. Общий анализ крови: эритроциты — 4,08×1012 г/л, гемоглобин — 132 г/л, лейкоциты — 10×109 г/л, нейтрофилы: палочкоядерные — 15, сегментоядерные — 71; лимфоциты — 12, моноциты — 1, эозинофилы — 1, скорость оседания эритроцитов — 24 мм/ч. Таким образом, в анализе мочи отклонений от нормы не выявлено. Биохимические показатели: глюкоза крови — 4,0 ммоль/л, белок общий — 66 г/л, билирубин общий — 7,6 мкмоль/л, аланинаминотрансфераза — 37 ЕД, аспартатаминотрансфераза — 29 ЕД, С-реактивный белок — отрицательный, серомукоид 0,23 г/л. Серологическое исследование на токсоплазмоз: IgM к токсоплазме гондии – не выявлен, IgG более 200 МЕ/мл. LE-клетки не обнаружены (3 раза). Антинуклеарные антитела не выявлены.
Проведены консультации терапевта, гематолога, гинеколога, маммолога, инфекциониста, проктолога, эндокринолога.
Рентгенография органов грудной клетки: органы грудной клетки без патологии. Фиброгастродуоденоскопия: гастрит хронический поверхностный, ремиссия. Колоноскопия: хронический поверхностный левосторонний колит. Ультразвуковое исследование (УЗИ) молочныхжелез: признаки диффузной мастопатии. УЗИ яичников: единичные кисты в яичниках. УЗИ щитовидной железы: многоузловой зоб.
Учитывая течение заболевания, пациентки рекомендовано 1 раз в 6 мес углубленное обследование для исключения онкологической патологии и системных заболеваний крови.
Системная терапия синдрома Свита приведена в табл. 3 [2].
Терапия кортикостероидами в настоящее время является основным методом лечения синдрома Свита [1, 2, 10]. Системные кортикостероиды позволяют уменьшить выраженность симптомов и способствуют разрешению очагов. Пациентам с резистентной формой заболевания может потребоваться ежедневная внутривенная пульс-терапия метилпреднизолоном. Местное или внутриочаговое применение кортикостероидов эффективно при лечении хорошо отграниченных очагов [11].
Системные препараты II линии применяются после лечения препаратами выбора I линии, которые не оказали эффекта.
У некоторых пациентов с синдромом Свита состояние улучшалось после приема системных антибиотиков. Это были пациенты с воспалительными заболеваниями кишечника (получали метронидазол) [2, 4, 10] и больные с сопутствующей иерсиниозной или хламидийной инфекцией [2, 10]. Кроме того, в отдельных случаях описано эффективное лечение синдрома Свита другими препаратами: интерфероном-α [2, 11], ацитретином [2, 10], инфликсимабом [2], пентоксифиллином [2, 11]. Симптомы и очаги у некоторых больных с классической формой заболевания разрешаются без лечения.
У пациентов с синдромом Свита на фоне онкологического заболевания успешное лечение рака иногда приводит к разрешению дерматоза [5]. Подобным же образом отмена провоцирующего лекарства у пациентов с лекарственным синдромом Свита обычно влечет за собой разрешение синдрома [12].
Синдром Свита может рецидивировать как после спонтанной ремиссии, так и после клинического разрешения, достигнутого в результате проведенной терапии. Рецидивы синдрома Свита чаще встречаются у онкологических пациентов. Повторное возникновение дерматоза может указывать на паранеопластический синдром.
www.mediasphera.ru
Синдром Свита - Клиническая дерматология и венерология - 2014-04
Большой интерес для дерматологов представляют редкие кожные заболевания. Одним из таких заболеваний является синдром Свита, или острый фибрильный нейтрофильный дерматоз.
Сидром Свита впервые описал британский дерматолог R. Sweet в 1964 г. Чаще болеют женщины в возрасте 30—60 лет. Проявляется заболевание высыпаниями на коже (редко — на слизистых оболочках), артралгией, лихорадкой и лейкоцитозом.
Этиология синдрома Свита неизвестна. В некоторых случаях заболевание обусловлено иерсиниозом [1]. Определенную роль отводят влиянию хронических инфекций, преимущественно органов дыхания (тонзиллит, бронхит, бронхопневмония), аутоиммунных заболеваний [2]. Был зарегистрирован синдром Свита в ассоциации с беременностью [3]. Связь с опухолью выявляют у 20% больных. Острый миелолейкоз — наиболее частая причина синдрома; реже он обусловлен другими миелопролиферативными и лимфопролиферативными заболеваниями. Синдром может на годы предшествовать выявлению опухоли [4]. Предполагают, что заболевание представляет собой реакцию гиперчувствительности к бактериальным или вирусным антигенам.
Клинические проявления. Заболевание начинается с продромальных явлений, таких как головная боль, артралгия, боль в горле, диарея, конъюнктивит, лихорадка до 38—39 оС. Спустя 1—2 нед на коже лица, шеи, верхних и нижних конечностей возникают единичные или множественные элементы, представленные папулами красного или фиолетового цвета с четкими границами, плотноватой консистенцией, сливающимися в бляшки неправильной формы. Элементы сыпи отличаются выраженной болезненностью при пальпации. Со временем бляшки разрешаются от центра, превращаясь в кольца или дуги, и увеличиваются по периферии. Из-за сильного отека кожи высыпания напоминают пузыри [1]. Элементы сыпи могут быть представлены также везикулами или пузырями с напряженной покрышкой и серозно-гнойным содержимым. После вскрытия пузырей образуются язвы, и тогда очаг поражения напоминает гангренозную пиодермию [1].
На коже нижних конечностей первичные морфологические элементы могут быть представлены в виде глубоких узлов с выраженной болезненностью при пальпации. Крайне редко патологический процесс на коже носит распространенный характер.
На фоне адекватной терапии через 5—7 дней элементы сыпи разрешаются. Заболевание может рецидивировать, при этом характерно появление высыпаний на тех же самых местах.
При лабораторных исследованиях выявляют изменения в клиническом анализе крови (повышение СОЭ, нейтрофильный лейкоцитоз). Характерно увеличение уровня щелочной фосфатазы в крови.
Патоморфологические изменения представлены значительным отеком сосочкового слоя дермы, массивной лейкоцитарной инфильтрацией всех слоев дермы, лейкоклазией вокруг сосудов дермы. Четкой картины васкулита обычно нет [5]. В подкожной жировой клетчатке также наблюдаются отек и нейтрофильная инфильтрация. В эпидермисе можно увидеть субкорнеальные пустулы.
Дифференциальный диагноз. Необходимо проводить дифференциальную диагностику с многоформной экссудативной эритемой, гангренозной пиодермией, глубокой красной волчанкой Капоши—Ирганга, узловатой эритемой, крапивницей.
Лечение включает, прежде всего, системные кортикостероидные препараты (преднизолон, дексаметазон), которые очень быстро купируют патологический процесс. Возможно назначение антибиотиков, йодида калия, нестероидных противовоспалительных средств, неспецифических десенсибилизирующих препаратов, антигистаминных средств, поливитаминов, адаптогенов, иммуноактивных средств. При тяжелом течении заболевания могут быть использованы цитостатики, неогемодез, реополиглюкин. Местно назначают 1—2% растворы анилиновых красителей [2], топические кортикостероидные препараты.
Приводим результаты нашего наблюдения.
Больная Д., 57 лет, обратилась в октябре 2012 г. в КВД Белгорода с жалобами на высыпания на кожных покровах, повышение температуры тела, головную боль, недомогание. Диагноз направившего учреждения: «Многоформная экссудативная эритема».
Анамнез заболевания. Считает себя больной с сентября 2012 г., когда впервые на коже груди, спины, предплечий появились высыпания, сопровождающиеся незначительным зудом. За 1 нед до высыпаний пациентку беспокоили боль в горле и суставах. Самостоятельно не лечилась. Из анамнеза стало известно, что пациентка страдает хроническим бронхитом около 15 лет, гипертонической болезнью — около 10 лет.
При поступлении в стационар общее состояние оценили как удовлетворительное. Внутренние органы и системы организма без выраженной патологии. Температура тела 37,8 оС.
Локальный статус. Патологический процесс носил распространенный характер. На коже спины, плеч, предплечий имелись множественные папулы ярко-красного цвета, плотноватой консистенции, сливающиеся в бляшки до 5—8 см в диаметре, с четкими границами, болезненные при пальпации (cм. рисунок, а, б).
 Некоторые элементы напоминали везикулы (см. рисунок, в).
Некоторые элементы напоминали везикулы (см. рисунок, в). Рисунок 1. Клинические проявления синдрома Свита у пациентки Д. Множественные папулы и бляшки на коже спины (а) с участками разрешения в центре на коже в области плеча (б) и элементами сыпи в виде везикул (в) в момент поступления и спустя 5 дней после начала лечения: пятна с четкими границами на месте разрешения папул и бляшек (г).
Рисунок 1. Клинические проявления синдрома Свита у пациентки Д. Множественные папулы и бляшки на коже спины (а) с участками разрешения в центре на коже в области плеча (б) и элементами сыпи в виде везикул (в) в момент поступления и спустя 5 дней после начала лечения: пятна с четкими границами на месте разрешения папул и бляшек (г).
Результаты лабораторного исследования. Клинический анализ крови: эритроциты — 4,93·1012/л, гемоглобин — 152 г/л, тромбоциты — 256·109/л, эозинофилы — 2%, палочкоядерные — 10%, сегментоядерные — 70%, лимфоциты — 12%, моноциты — 6%, СОЭ — 35 мм/ч.
Общий анализ мочи: удельный вес — 1020, белок, глюкоза не обнаружены, лейкоциты — 1—2 в поле зрения, эритроциты — 0—1 в поле зрения.
Биохимический анализ крови: билирубин — 20 мкмоль/л, холестерин — 6,5 ммоль/л, общий белок — 72 г/л, глюкоза — 4,6 ммоль/л, аланинаминотрансфераза — 61 Ед/л, аспартатаминотрансфераза — 46 Ед/л, щелочная фосфатаза — 387 Ед/л.
Результаты анализов на сифилис (реакция микропреципитации, иммуноферментный) — отрицательные. Антитела к ВИЧ, НВsАg, HcVАg отрицательные.
Электрокардиограмма: ритм синусовый правильный, отклонение электрической оси сердца влево, гипертрофия левого желудочка.
Гистологическое исследование не проводили.
Назначено лечение: преднизолон 25 мг в сутки, супрастин по 1 мл внутримышечно 10 инъекций, аспаркам по 500 мг 3 раза в день; местно — мазь преднизолон 2 раза в день.
Через 7 дней элементы сыпи почти разрешились: на их месте сохранились пятна бледно-розового цвета с четкими границами (см. рисунок, г). Рисунок 1. Клинические проявления синдрома Свита у пациентки Д. Множественные папулы и бляшки на коже спины (а) с участками разрешения в центре на коже в области плеча (б) и элементами сыпи в виде везикул (в) в момент поступления и спустя 5 дней после начала лечения: пятна с четкими границами на месте разрешения папул и бляшек (г). Свежих высыпаний не было. Температура тела нормализовалась. На 15-е сутки элементы сыпи разрешились полностью. Больная выписана с рекомендациями продолжить прием преднизолона в дозе 20 мг в сутки с последующим снижением ее по 2,5 мг в неделю до полной отмены; прием аспаркама по 500 мг 3 раза в день. Назначена консультация терапевта, ревматолога, онколога.
Рисунок 1. Клинические проявления синдрома Свита у пациентки Д. Множественные папулы и бляшки на коже спины (а) с участками разрешения в центре на коже в области плеча (б) и элементами сыпи в виде везикул (в) в момент поступления и спустя 5 дней после начала лечения: пятна с четкими границами на месте разрешения папул и бляшек (г). Свежих высыпаний не было. Температура тела нормализовалась. На 15-е сутки элементы сыпи разрешились полностью. Больная выписана с рекомендациями продолжить прием преднизолона в дозе 20 мг в сутки с последующим снижением ее по 2,5 мг в неделю до полной отмены; прием аспаркама по 500 мг 3 раза в день. Назначена консультация терапевта, ревматолога, онколога.
В приведенном нами клиническом случае диагноз синдрома Свита основывался на данных анамнеза заболевания, клинической картины дерматоза, результатов дерматоскопии и течения заболевания. Трудности диагностики связаны с редкой встречаемостью синдрома Свита. Правильно поставленный дерматологом диагноз способствует быстрой ремиссии кожного процесса, а также своевременному обращению пациента к врачам других специальностей (терапевту, инфекционисту, ревматологу, онкологу) для выявления серьезной соматической или онкологической патологии.
www.mediasphera.ru
Синдром Свита - причины, симптомы, диагностика и лечение
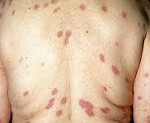
Синдром Свита – одна из форм нейтрофильного дерматоза, которая характеризуется островоспалительным рецидивирующим течением. Основными проявлениями данного заболевания являются бляшки розового или ярко-красного цвета, лихорадочное состояние, нейтрофилия, боли в суставах. Диагностика синдрома Свита производится на основании клинической картины, гистологического исследования кожи, лабораторных анализов (ОАК, биохимическое исследование, ИФА). В настоящий момент этиотропное лечение не разработано, применяется противовоспалительная терапия кортикостероидами и нестероидными противовоспалительными средствами.

Синдром Свита (острый фебрильный нейтрофильный дерматоз) является довольно редким острым дерматологическим заболеванием, которое имеет волнообразное течение. Первым эту патологию выявил и описал Р. Свит в 1964-м году, с тех пор данный дерматоз носит его имя. Распространенность патологии 1-9 случаев на 1 млн. населения. В основном синдром Свита поражает лиц старшего возраста (средний возраст– 56 лет), встречается преимущественно у женщин – половое распределение составляет 3:1. По другим данным, более 90% всех заболевших составляют лица женского пола, причем описан случай развития патологии во время беременности. Замечена взаимосвязь между возникновением синдрома Свита и целым рядом других патологий – гематологических, инфекционных и эндокринных. Также описаны случаи, когда развитие нейтрофильного дерматоза предшествовало появлению злокачественных опухолей.
Причины синдрома Свита
Этиология синдрома Свита на сегодняшний день точно неизвестна, имеются предположения об иммунологической реакции нетипичного вида, при которой не происходит классической активации системы комплемента. Стимуляция иммунной системы предположительно производится бактериальными, опухолевыми или вирусными антигенами, которые формируют накапливающиеся в тканях комплексы. После этого возможно развитие реакции сверхчувствительности по типу Артюса и прямое воздействие на воспалительные клетки с выделением значительного количества медиаторов. Гистохимическими исследованиями было выявлено, что в кожных бляшках при синдроме Свита наблюдается значительное (в десятки и сотни раз) повышение концентрации интерлейкина-6 и колониестимулирующего фактора гранулоцитов. Однако это может быть обусловлено острым воспалением, имеющим место при подобном поражении дермы.
В большинстве случаев синдром Свита возникает вскоре после перенесенной острой респираторной вирусной инфекции. Также в качестве провоцирующего дерматоз фактора могут выступать стрептококковые поражения, иерсиниоз, неспецифический язвенный колит, аутоиммунные заболевания (в частности, тиреоидит Хашимото, болезнь Крона). Примерно в 20% случаев синдром Свита является паранеопластической реакцией на наличие злокачественного гематологического заболевания (острого миелоидного лейкоза) или солидных опухолей молочной железы, ЖКТ, мочеполовых органов. В дерматологии довольно часто встречаются больные дерматозом такого типа, которые перенесли онкологические заболевания в прошлом.
Классификация синдрома Свита
В настоящее время изучено несколько форм синдрома Свита, которые различаются между собой факторами, провоцирующими развитие патологии.
- Классическая или идиопатическая форма – является наиболее распространенной (почти 80% больных), возникает вскоре после респираторного заболевания или на фоне аутоиммунных поражений, иерсиниоза, неспецифического язвенного колита.
- Синдром Свита, ассоциированный с паранеоплазией – более редкая форма (менее 20% от всех заболевших), наиболее часто возникает при миелобластном лейкозе и других злокачественных гематологических заболеваниях. Также может развиться по причине рака груди или опухоли желудочно-кишечного тракта. В некоторых случаях развитие дерматоза наступает через много лет после лечения и ремиссии онкологического заболевания.
- Синдром Свита, вызванный приемом некоторых лекарств – самый редкий тип заболевания, может возникать на фоне приема гранулоцитарного колониестимулирующего фактора. Имеются отдельные указания на появление дерматоза после приема фуросемида, миноциклина и гидралазина.
Симптомы синдрома Свита
Первым признаком синдрома Свита служит появление на поверхности кожи папул диаметром 2-8 миллиметров. Пятна ярко-красного цвета, располагаются на руках, груди, шее. Затем через 2-3 дня присоединяется значительное повышение температуры (до 40 градусов), лихорадка, боли в суставах. Продолжается образование папул, которые через 7-10 дней после появления первых симптомов синдрома Свита начинают сливаться в бляшки неправильной формы диаметром до 7-ми сантиметров. Кожный зуд в местах появления высыпаний на всем протяжении заболевания имеет среднюю интенсивность или не наблюдается совсем. В редких случаях множественные папулы возникают сразу на всей поверхности тела, что свидетельствует о генерализованной форме синдрома Свита.
Со временем, на фоне лечения или самопроизвольно, бляшки начинают разрешаться – снижается отечность кожи, уменьшается интенсивность окраски. Как правило, при синдроме Свита подобные процессы начинаются в центре бляшек, поэтому на некоторое время они принимают кольцевидную форму, а затем имеют вид дуг. После полного затухания воспалительных процессов на месте высыпаний часто остаются участки гиперпигментаций кожи, сохраняющиеся длительное время. Синдром Свита характеризуется рецидивирующим течением, поэтому возможно возобновление артралгии и лихорадки, новое появление папул и бляшек на тех же участках, которые были поражены ранее.
Диагностика синдрома Свита
Главными методами диагностики синдрома Свита являются дерматологический осмотр, общий и биохимический анализ крови, в некоторых случаях производят биопсию кожи в области поражения. При осмотре врачом-дерматологом выявляется диссеминированный характер высыпаний, однако их распределение, как правило, симметричное. Обнаруживается наличие папул и бляшек на разных этапах своего развития. Возможно наличие гиперпигментированных участков кожи, которые остались от прошлых атак синдрома Свита. При пальпации в строении бляшек выявляется более плотный валик по краям образования. Объективно также обнаруживается повышенная температура тела, больные жалуются на боли в суставах.
Общий анализ крови при синдроме Свита показывает выраженный нейтрофильный лейкоцитоз – общее количество лейкоцитов может достигать 10-12х109/л, из них доля нейтрофилов всех типов составляет 60-70%. Также нередко наблюдается повышенный уровень моноцитов, ускорение скорости оседания эритроцитов. Биохимический анализ выявляет незначительное повышение уровня печеночных ферментов (АСТ и АЛТ), иногда снижение общего белка. Кроме того, при наличии синдрома Свита имеет смысл провести исследование на уровень основных онкомаркеров, антител к иерсиниозу и стрептококковым инфекциям – в ряде случаев эти тесты могут быть положительными.
При гистологическом изучении тканей кожных бляшек, возникающих при синдроме Свита, наблюдается неизмененный эпидермис, отек дермы, расширение капилляров и нейтрофильная инфильтрация. Дифференциальную диагностику следует проводить с крапивницей, узловатой и многоформной экссудативной эритемой, иногда системной красной волчанкой.
Лечение, прогноз и профилактика синдрома Свита
Этиотропной терапии синдрома Свита на сегодняшний момент не существует, лечение производят противовоспалительными препаратами – глюкокортикоидами (преднизолон), нестероидными противовоспалительными средствами (индометацин). У ряда больных отмечена положительная реакция на использование дапсона (противомикробное средство) и йодида калия. Наружно также назначают глюкокортикостероиды – в форме крема или мази, длительность лечения составляет 5-10 дней.
Прогноз синдрома Свита благоприятный, высыпания при правильно проведенном лечении быстро исчезают, оставляя после себя лишь участки повышенной пигментации, артралгия не возвращается после выздоровления. Однако существует риск рецидива заболевания, на тех же или новых областях тела. Кроме того, развитие синдрома Свита является поводом для обращения к онкологу и проведения комплексного обследования из-за риска наличия злокачественной опухоли или гематологической онкопатологии.
www.krasotaimedicina.ru
Реферат: Паранеопластические синдромы
Паранеопластические синдромы
Паранеопластические синдромы - это синдромы, вызываемые новообразованиями, вдали от первичной опухоли и её метастазов.
Паранеопластические синдромы могут быть вследствие:1). Продукции опухолью различных веществ.2). Поглощения опухолью необходимых организму веществ.3). Развития противоопухолевого иммунного ответа, который становится чрезмерным и переходит в синдром.Опухоли могут выделять некоторые гормоны, некоторые факторы роста и цитокины (например, ИЛ-1 и ФНО), антитела (например при синдроме Ламбера-Итона).Много паранеопластических синдромов, особенно иммунной природы, не проходят после лечения опухоли. Паранеопластический синдром может быть первым проявлением опухоли и их знание лежит в основе ранней диагностики новообразований.При опухолях, которые секретируют белковые вещества, можно проводить контроль за лечением опухолью по их уровню.В некоторых случаях, когда опухоль некурабельна, можно снять паранеопластический синдром и его осложнения.
Виды паранеопластических синдромов:- эндокринопатии- гематологические- желудочно-кишечные- почечные- кожные- неврологические- прочие.
Эндокринопатии
Синдром эктопической продукции АКТГ
В 1928 году Браун впервые описал синдром эктопической продукции АКТГ у больного с мелко-клеточным раком лёгкого, у которого наблюдались гирсутизм, сахарный диабет, гипертензия и гиперплазия коры надпочечников. В 1965 году было описано 88 больных с синдромом Кушинга при раке. Недавно было установлено, что АКТГ выделяется не в чистом виде, а в виде предшественника - проопиомеланокортина , который кроме АКТГ содержит ещё и бета-эндорфин и альфа-меланоцитстимулирующий гормон. В отличие от болезни Кушинга (гиперкортицизм при аденоме гипофиза) при синдроме эктопической продукции АКТГ повышено отношение предшественников гормонов к уровню АКТГ. Этот синдром чаще развивается при мелкоклеточном раке лёгкого. Синдром Кушинга развивается у 3-7% больных с мелкоклеточным раком лёгкого. У многих больных, не смотря на то, что у них и выделяется повышенное количество предшественника АКТГ, синдром не развивается.
Клиника. Характерно ожирение, гирсутизм (у женщин оволосение по мужскому типу, из-за дегидроэпиандростерона), лунообразное лицо, пурпурные стрии, депрессия, аменорея, гипертензия, слабость, отёки (из-за альдостерона), сахарный диабет (ГКС повышают глюкозы в крови главным образов за счёт глюконеогенеза в печени). При определении у больного повышенной продукции кортизола необходимо проводить дифференциальную диагностику между болезнью Кушинга (встречается наиболее часто, в 55-82%), дисфункцией коры надпочечников (5-32%), синдромом эктопической продукции АКТГ (11-25%) и повышенной продукцией кортикотропин-рилизинг гормона (КТРГ) (1-2%). Для синдрома эктопической продукции АКТГ характерна миопатия со слабостью, гиперпигментация и гипокалиемия, которая может представлять опасность для больного. Болезнь Кушинга встречается чаще у женщин (3:1), в то время как синдром эктопической продукции АКТГ чаще у пожилых мужчин.
Диагностика. Первый шаг диагностической программы, это выяснение уровня патологии - разграничение первичных нарушений в коре надпочечников, аденомы гипофиза и синдрома эктопической продукции АКТГ. Используют различные диагностические тесты - наиболее распространённые из них, это определение уровня кортизола в суточной моче, низко- и высоко-дозный дексаметазоновый тест. У здоровых людей низкие дозы дексаметазона (2 мг) подавляют продукцию кортизола, при болезни Кушинга и синдроме эктопической продукции АКТГ - не изменяют. Результаты оценивают по уровню 17-кортикостероидов в моче.Кроме того, с помощью метода радиоанализа можно непосредственно измерить уровень АКТГ в крови. При первичных нарушениях в коре надпочечников уровень АКТГ низкий, в то время как при болезни Кушинга и АКТГ-зависимом синдроме Кушинга - повышен. Обычно при синдроме эктопической продукции АКТГ уровень его в плазме выше, чем при болезни Кушинга, но это не всегда так, особенно при медленно растущих опухолях (например, при бронхиальном карциноиде). По уровню АКТГ можно исключить первичные нарушения в коре надпочечников и дальше показан высокодозный (большой) дексаметазоновый тест. Высокие дозы (8 мг) дексаметазона подавляют продукцию кортизола при болезни Кушинга и не подавляют при синдроме эктопической продукции АКТГ и первичных нарушениях в коре надпочечников. Ложно-положительные результаты большого дексаметазонового теста могут быть получены при повышенном метаболизме дексаметазона (приём дифенилгидантоина, фенобарбитала, примидона, при тиреотоксикозе). Кроме того, при бронхиальном карциноиде продукция кортизола снижается в 40-50% случаев. Хотя дексаметазоновые тесты надёжны, они затруднительны в выполнении и их чувствительность и специфичность не совершенны. Есть ещё два тесте - тест с метирапоном и КТРГ-стимулирующий тест. Метирапон блокирует синтез кортизола из 11-дезоксикортизола в коре надпочечников, что у здоровых людей приводит к повышению уровня АКТГ. При болезни Кушинга уровень АКТГ повышается, тогда как при синдроме эктопической продукции АКТГ - нет. Идентично при втором тесте, введение КТРГ при болезни Кушинга повышает уровень АКТГ, при синдроме эктопической продукции - нет. Комбинация дексаметазоновых тестов и КТРГ-стимулирующего теста приводит к диагностической точности 98%. Также можно применяют другие, менее распротранённые тесты:- взятие крови из нижней каменистой вены и её сравнение с периферической кровью. Этот тест можно проводить с или без введения КТРГ. Однако он инвазивный и очень дорогой.- длительная инфузия дексаметазона в течение 7 часов (1мг/час) - чувствительность 100%, специфичность 90%, диагностическая точность 98%. - определение сывороточного хромогранина А, который является маркёром синдрома эктопической продукции АКТГ.
Лечение.
Синдром эктопической продукции часто встречается при опухолях лёгких. Так что это диктует выполнить рентгенологическое исследование лёгких. Ренигенография и КТ позволяют обнаружить опухоль лёгкого в 90% случаев и бронхиальный карциноид в 36% при рентгенонрафии и в 85% при КТ. Опухоли, продуцирующие АКТГ, обычно имеют рецепторы к октреотиду и поэтому для диагностики может использоваться сцинтиграфия с октреотидом. Кроме того, для терапии таких опухолей можно использовать радиоактивный октреотид или соматостатин.
Хирургическое лечение - метод выбора ранних стадий опухолей лёгких с синдромом Кушинга, что в последующем снимает симптомы. Некоторым больным можно провести двустороннюю адреналэктомию с последующей заместительной терапией ГКС и минералокортикоидами. Пациенты с тяжёлой мышечной слабостью и некотролируемой гипертензией - кандидаты на эту операцию.
При неоперабельных опухолях применяют ингибиторы кортизола - митотан, аминоглютетимид, метирапон и кетоконазол. Митотан - эффективен в снижении уровня кортизола, но он очень токсичен и медленно начинает действовать.Аминоглютетимид - используется в ограниченных ситуациях, потому что не всегда эффективен.Обычно используется метирапон, особенно в комбинации с аминоглютетимидом. Препаратом выбора является кетоконазол в дозе 400-1200 мг/день, у немногих может быть гипоадренализм. Также может применяться октреотид.
Синдром эктопической продукции АДГ
Впервые описан у двух пациентов с раком лёгкого, у которых наблюдалась гипонатриемия. В 1968 году был выделен аргинин-вазопрессин. С помощью радиоиммунного исследования удалось установить, что вазопрессин содержится в большинстве мелкоклеточных раках лёгкого, однако только у 3-15% развивается этот синдром. Вазопрессин связывается с рецепторами в собирательных трубочках и восходящем колене петли Генле. В результате этого реабсорбируется вода, а натрий идёт в дистальный отдел нефрона. Опухолевые клетки продолжают выделять АДГ, не смотря на сниженную осмолярность, приводя в конечном счёте к гипонатриемии.
Клиника и диагностика.
Главными симптомами синдрома эктопической продукции АДГ являются водная интоксикация и гипонатриемия, снижение осмолярности крови, повышение осмолярности мочи вследствие повышенного содержания в ней натрия. Всё это наблюдается при нормальном ОЦК (нет гиповолемии), при нормальной функции почек, надпочечников и щитовидной железы. У большинства пациентов нет никаких жалоб. Если они развиваются, то это связано с интоксикацией ЦНС - слабость, снижение аппетита, головная боль, снижение ментальной функции. При прогрессировании может быть делирий и судороги.
При обнаружении у больного раком гипонатриемии необходимо выяснять её причину. Первый шаг диагностической программы - это определение ОЦК. При синдроме эктопической продукции АДГ ОЦК в пределах нормы. При сердечной недостаточности, нефротическом синдроме, злокачественном асците и серьёзных заболеваниях печени гипонатриемия сочетается с гиперволемией. Гипонатриемия при нормальной ОЦК может быть при гипотиреозе, почечной патологии, болезни Аддисона, приёме некоторых лекарственных веществ.
При обнаружении гиперпродукции АДГ следует искать этому причину. Это может быть заболевания ЦНС, легочные заболевания, приём некоторых лекарственных веществ. Синдром эктопической продукции АДГ ставится путём исключения других причин. Однако для лечения выяснение причины повышенной продукции АДГ не имеет существенного значения. Среди новообразований гиперпродукция АДГ встречается при мелкоклеточном раке лёгкого (75%), немелкоклеточном раке лёгкого, опухолях головы и шеи. У многих людей гиперпродукция АДГ развивается после лечения мелкоклеточного рака лёгкого. Многие химиотерапевтические препараты (винкристин, винбластин, винорелбин, ифосфамид, циклофосфамид, циспластин) могут вызвать транзиторное повышение АДГ.
Лечение.
Обычно после химиотерапии мелкоклеточного рака лёгкого проходит и синдром. Также снижают ОЦК и используют различные фармакологические средства. При уровне Na меньше 130 ммоль/л ежедневно из организма выводят 500 мл жидкости. Если это мероприятие не повышает Na выше 130 ммоль/л, то назначают демеклоциклин (в дозе 600-1200 мг/сутки), который является антагонистом вазопрессина. Также применяют фрудрокортизон, мочевину и литий. В тяжёлых случаях (кома, судороги) можно применять гипертонические растворы с фуросемидом. Однако нельзя повышать Na слишком быстро, так как может быть центральный миелинолиз моста.
Гипокальцемия
Гипокальцемия обычно появляется в результате метастазов рака молочной железы, предстательной железы, рака лёгкого в кости либо если опухоль продуцирует кальцитонин. Хотя гипокальцемия встречается чаще, чем гиперкальциемия, она реже даёт симптомы. Лишь в тяжёлых случаях бывают судороги. Инфузия кальция начинают при положительных симптомах Хвостека и Труссо (карпальный спазм со сниженным кровотоком).
Опухолевая остеомаляция
Остеомаляция у взрослых может быть при мальабсорбции, почечном тубулярном ацидозе, хронической почечной недостаточности. Опухолевая остеомаляция характеризуется размягчением костей, гипофосфатемией, гиперфосфатурией, снижением уровня витамина Д. Обычно встречается в возрасте 30-40 лет. У пациентов наблюдается боль в костях, фосфатурия, почечная глюкозурия, гипофосфатемия, нормокальцемия, нормальная функция паратгормона, снижение 1,25-диоксивитамина Д3 и повышение щелочной фосфатазы. Предположительный механизм остеомаляции - это нарушение образования 1,25-диоксивитамина Д и секреция опухолевыми клетками фосфатурических веществ. Обычно встречается при доброкачественных мезенхимальных опухолях (гемангиомы, гемангиоперицитомы), реже - при раке предстательной железы и миеломной болезни. Лечение - удаление опухоли, применение больших доз витамина Д и фосфата.
Опухолевая продукция кальцитонина
Кальцитонин продуцируется С-клетками щитовидной железы. Кальцитонин предотвращает вымывание Са из костей и увеличивает экскрецию Са, натрия и фосфатов с мочой. Встречается при медуллярной карциноме щитовидной железы. По его уровню можно следить за течением заболевания. Также кальцитонин может выделяться при мелкоклеточном раке лёгкого, карциноиде, раке груди, желудочно-кишечного тракта.
Продукция гонадотропинов
Из гонадотропинов у человека синтезируются фолликулостимулирующий гормон, лютеинизирующий гормон и хорионический гонадотропин. ФСГ и ЛГ продуцируются гипофизом. ХГТ секретируется плацентой и в норме имеется только у беременных женщин. Из-за того, что уровень ФСГ и ЛГ варьирует в норме в широких пределах, для паранеопластических синдромов ценность представляет ХГТ. Основная проблема гиперпродукции гонадотропинов - это гинекомастия у мужчин. В таких ситуациях определяют уровень ХГТ, тщательно исследуют яички и делают рентгенографию грудной клетки. Основная причина повышения ХГТ - это герминогенные опухоли яичек и опухоли лёгких, но также ХГТ может выделяться при карциноме коры надпочечников, гепатоме, раке желудочно-кишечного тракта. Как и при всех герминогенных опухолях, эти пациенты чувствительны к химиотерапии.
Другие гормонпродуцируемые опухоли
Нетрофобластные негонадные опухоли могут выделять человеческий плацентарный лактоген. Это может проявляться повышением уровня эстрогена, ХГТ и гинекомастией. Человеческий плацентарный лактоген у небеременных женщин - это признак паранеопластического синдрома. Опухоли поджелудочной железы, бронхиальный карциноид могут выделять рилизинг гормон гормона роста, что приводит к акромегалии. Для лечения применяют аналоги соматостатина. Опухоли лёгкого, толстой кишки, груди, яичников, шейки матки, гипернефрома может выделять пролактин, что у женщин проводит к галакторее. Опухоли яичка могут выделять тироид-стимулирующий гормон и приводить к тиреотоксикозу.
Гипогликемия
Гипогликемия обычно встречается при инсулиномах, но может также встречаться при саркомах, мезотелиомах. Механизмы гипогликемии различны - выделение инсулиноподобных факторов роста 1 и 2, гиперметаболизм глюкозы, массивное прорастание опухоли в печень, выделение веществ, стимулирующих выработку инсулина, пролиферация рецепторов к инсулину и секреция инсулина самой опухолью. Лечение паранеопластической гипогликемии - инфузия глюкозы, подкожное или внутримышечное введение глюкагона или выскоих доз кортикостероидов.
Гематологические проявления рака
Эритроцитоз
Эритроцитоз чаще встречается при почечной карциноме из-за повышенной продукции эритропоэтина. К эритроцитозу также могут приводить кисты почек. При опухоле Вильмса и гемангиоме почки эритроцитоз встречается редко. Эритроцитоз также может быть при гепатоме, мозжечковой гемангиобластоме, феохромацитоме, опухолях коры надпочечников (также из-за повышенного образования эритропоэтина). Опухоли коры надпочечников и вырилизируюзие опухоли яичников могут выделять андрогены, что приводит к повышению количества эритроцитов. Действие эритропоэтина могут усиливать простагландины, так что опухоли с продукцией простагландинов также могут приводить к эритроцитозу. Следует проводить дифференциальную диагностику с эритроцитозом неопухолевого генеза. При истинной полицитемии (polycythemia vera) обычно наблюдается повышенное количество лейкоцитов, тромбоцитов и спленомегалия. Эритроцитоз может быть при гемоглобинопатиях, повышенном содержании карбоксигемоглобина.Опухолевый эритроцитоз обычно не требует лечения, однако если очень высокий гематокрит (55% для мужчин и 50% для женщин), проводят флеботомию. Уровень эритроцитов можно использовать для контроля за лечением опухоли.
Анемия
Самые распространённые виды анемий у раковых больных - это нормоцитарная нормохромная анемия, анемия вследствие метастазов в костный мозг и анемия вследствие химио- и радиотерапии. Нормохромная нормоцитарная анемия при опухолях характеризуется снижением уровня железа в крови, нормальным или повышенным содержанием уровня ферритина, нормальными запасами железа и низким уровнем эритропоэтина. Считается, что ИЛ-1, ФНО подавляеют действие эритропоэтина. Реже анемия вызывается аплазией эритроцитов, что встречается при тимоме, хроническом миелоцитарном лейкозе, других лейкозах и лимфомах. При опухолях В-лимфоцитов (хронический лимфоцитарный лейкоз, лимфомы) может наблюдаться аутоиммунная гемолитическая анемия. Она характеризуется положительным прямым антиглобулиновым тестом, ретикулоцитозом, снижением уровня гаптоглобина, повышением ЛДГ. ГКС менее эффективны при такой анемии, чем при других аутоиммунной природы. Реакция Кумбса может становиться отрицательной при лечении опухоли.При тромботической тромбоцитопенической пурпуре, врождённых сосудистых аномалиях, гемолитико-уремической синдроме, при раке желудочно-кишечного тракта, сердца, лёгких, предстательной железы, при химиотерапии митомицином С может быть микроангиопатическая гемолитическая анемия. Обычно сочетается с тромбоцитопенией. У пациентов также обычно наблюдается шистоцитоз и микросфероцитоз.
Гранулоцитоз
Гранулоцитоз с повышением количества лейкоцитов больше 15х10(9)/л часто встречается при болезни Ходжкина, лимфоме, раке желудка, лёгких, поджелудочной железы, меланоме. Механизм его - это образование опухолевыми клетками колониестимулирующего фактора гранулоцит-макрофагов, ИЛ-3, ИЛ-1 и др. Гранулоцитоз при опухолях характеризуется зрелыми нейтрофилами, что отличает его от хронического миелоцитарного лейкоза, где появляются незрелые клетки, базофилы, эозинофилы, снижается ЩФ в лейкоцитах, повышается витамин В12 и способность к его связыванию, имеется филадельфийская хромосома.
Гранулоцитопения
Гранулоцитопения может появляться в связи с химиотерапией, радиотерапией и прорастанием опухоли в костный мозг. Механизм его - опухоль продуцирует вещества, которые угнетают гранулопоэз. При болезни Ходжкина могут выделяться антитела против гранулоцитов. Лечение - применения колониестимулирующего фактора гранулоцитов, колониестимулирующего фактора гранулоцит-макрофагов.
Эозинофилия и базофилия
Эозинофилия обычно встречается при болезни Ходжкина. Опухолевые клетки продуцируют фактор, который селективно вызывает образование эозинофилов. Также эозинофилию объясняют выделением колониестимулирующего фактора гранулоцит-макрофагов, ИЛ-3, ИЛ-5. Высокая эозинофилия приводит к симптомам, подобным при синдроме Лёффлера, который характеризуется узелковыми инфильтратами в лёгких, кашлем и лихорадкой. Базофилия обычно встречается при хроническом миелогенном лейкозе и редко является клинически значимой.
Тромбоцитоз
Тромбоцитоз наблюдается при болезни Ходжкина, лимфомах, некотрых карциномах и лейкозах. Тромбоцитоз встречается при многих миелопролиферативных заболеваниях, включая истинную полицитемию и хронический миелогенный лейкоз, при воспалительных заболеваниях, кровотечениях, недостаточности железа, гемолитической анемии, после спленэктомии. Механизм его - это выработка опухолью тромбопоэтина. Тромбоцитоз при опухолях очень редко приводит к тромбозам и кровотечениям и лечения обычно не требуется.
Тромбоцитопения
Её причинами у раковых больных обычно являются химиотерапия, лучевая терапия, ДВС-синдром, инфильтрация опухоли в костный мозг. Встречается при хроническом лейкозе, лимфомах, болезни Ходжкина. У пациентов может проявляться кровотечениями, петехиями, пурпурой. Для лечения применяют преднизолон и/или спленэктомию. Тромбоцитопения также может быть при приёме гепарина, тиазидных диуретиков и других лекарственных веществ.
Тромбофлебит
Впервые связь тромбофлебита и опухоли была замечена Труссо и этот синдром носит его имя. Характерен мигрирующий характер тромбофлебита. Рецидивирующие тромбозы глубоких вен, устойчивость к варфарину, тромбозы в нетипичных местах должны усилить подозрение на рак. Особенно высок риск мигрирующего тромбофлебита при раке поджелудочной железы, но он также может быть при раке груди, яичников, простаты. У раковых больных повышены факторы свёртывания крови. Муцинозные аденокарциномы продуцируют сиаловую кислоту, которая активирует фактор Х и приводит к гиперкоагуляционному состоянию. При опухолевых тромбозах происходит ряд нарушений в системе свёртывания крови: повышение катаболизма фибриногена и тромбоцитов, снижение протеина С, S и антитромбина, прямое образование тромбина, тромбоцитоз. Лечение можно начинать с гепарина, хотя обычно это безуспешно. Лучше применять низкомолекулярные гепарины.
Коагулопатии и ДВС
Основные нарушения в системе свёртывания крови у раковых больных - это повышенный уровень фибрина, продуктов деградации фибриногена, тромбоцитоз, гиперфибриногенемия, ДВС с фибринолизом. Всё это может сопровождаться повышенным синтезом фактором свёртывания крови и тромбоцитов. ДВС с потреблением тромбоцитов и факторов свёртывания крови бывает редко, обычно при остром промиелоцитарном лейкозе или адренокарциноме. ДВС характеризуется нормальным протромбиновым временем, тромбоцитопенией, гипофибриногенемией. У 90% больных повышено количество тромбоцитов. Самый ценный тест для диагностики ДВС - это определение продуктов деградации фибрина. Главное в введении больных с ДВС - это определение факторов свёртывания крови и лечение ими. Применяют сочетание факторов свёртывания крови, тромбоциты с гепарином. Монотерапия гепарином противоречива и обычно используется при хроническом течении ДВС. Также применяют антиагреганты, ингибиторы и активаторы фибринолиза, но эффективность их не доказана. Противопоказана эпсилон-аминокапроновая кислота. Самое главное - лечение опухоли.
Небактериальный тромботический эндокардит
Небактериальный тромботический эндокардит может привести к тромботическим и геморрагическим осложнениям и может быть с или без ДВС. Он характеризуется стерильными тромбоцитарными осложнениями на левых клапанах сердца. Типичное проявление в мозг - появление локальной или диффузной неврологической симптоматики. Диффузная симптоматика - это конфузия, судороги, дезориентация. Диагностический тест - церебральная ангиография, что позволяет выявить множественные артериальные окклюзии. У многих выслушиваются сердечные шумы. ЭхоКГ выявляет вегетации размером больше 2 мм. Небактериальный тромботический эндокардит обычно встречается при аденокарциноме лёгких, лимфомах, лейкозах. Могут быть кровотечения в кожу, ЦНС, ЖКТ, верхние дыхательные пути, урогенитальный тракт и нижние дыхательные пути. Основное лечение - это лечение опухоли. Показано назначение антикоагулянтов.
Желудочно-кишечные проявления рака
Белок-теряющая энтеропатия
Белок-теряющая энтеропатия характеризуется чрезмерной потерей сывороточного белка в ЖКТ, что приводит к гипопротеинемии. Раньше считали, что гипопротеинемия является следствием нарушения синтеза белка. Однако сейчас доказано, что синтез белка нормальный или даже повышен, а снижается период полужизни белков в крови. Также было показано, что потеря белка через кишечник способствует гипопротеинемии, не являясь её единственной причиной.
В норме ЖКТ играет незначительную роль в катаболизме сывороточного белка. Только около 10% альбуминов и глобелинов теряется через ЖКТ. Считается, что при белок-теряющей энтеропатии происходит повышение проницаемости в слизистой для белка из-за нарушения клеточной структуры, эрозий, язв и нарушения оттока лимфы. Теоритически гипоальбуминемия может быть при любом раке ЖКТ. Также была описана гипоальбкминемия при СПИДе и саркоме Капоши. Вовлечение кишечника при лимфомах (включая макроглобулинемию Вальденстрема), болезни Ходжкина может такде привести в белок-теряющей энтеропатии.
В отличие от почечной потери белка, потеря белка при нарушениях ЖКТ не зависит от размера белка. При белок-теряющей энтеропатии теряются белки всех размеров - альбумины, иммуноглобулины, церулоплазмин - в отличие от нефортического синдрома. При гипопротеинемии различных причин большее снижение происходит тех белков, которые длительно циркулируют в крови (например, альбумины), чем коротко-живущих (например, ретинол-связывающий белок). Также при гипопротеинемии может снижаться железо, медь, кальций.
Клинические белок-теряющая энтеропатия проявляется гипопротеинемией. Она может сопровождаться отёками, но очень редко связана с тяжёлыми отёками и анасаркой. Не смотря на тот факт, что происходит снижение глобулинов и факторов свёртывания крови, присоединение оппортунистических инфекций и развитией коагулопатий наблюдается редко. У пациентов может быть диарея.
Диагностика белок-теряющей энтеропатии в общем не сложна. Необходимо исключить другие причины гипопротеинемии - мальнутриция, болезни печени. Раньше исследовали потерю белка с калом. Сейчас применяются новые методы исследования с использованием альфа1-антитрипсина, белка, который не расщепляется в ЖКТ. Следовательно, если они теряется, то он полностью экскретируется со стулом. Клиренс этого протеина используется для подтверждения диагноза белок-теряющей энтеропатии.
Лечение заключается в лечении первичной опухоли. При лимфатической обструкции показана диета с малым содержанием жира. Используются среднецепочечные ТАГ, которые не транспортируются по лимфатической системе. При таком лечение симптомы проходят у 50% больных.
Анорексия и кахекия у раковых больных
Синдром анорексии-кахексии у раковых больных - самый распространённый паранеопластический синдром, характеризующийся потерей аппетита, тошнотой и потерей веса. У 15% раковых больных потеря массы тела больше 10%. У пациентов с потерей больше 10% массы тела - низкая выживаемость из-за присоединения инфекции и из-за плохого заживления ран. Некоторое лечение рака может привести к нарушению обмена веществ, такие как послеоперационный илеус, эзофагит, стоматит.
Опухоли продуцируют вещества, которые изменяют восприятие пищи, особенно вкус и запах, приводя к недостатку удолетворения. В ЦНС изменяется уровень серотонина. Вследствие нарушения секреции желчи и панкреатического сока может быть мальдигестия и мальабсорбция. У пациентов с тошнотой может развиться отвращение к пищи, которое трудно поддаётся терапии.
У раковых больных в крови повышается уровень ИЛ1, ИЛ6, ФНО, гамма-интерферона, серотонина. Назначение этих цитокинов приводит к анорексии и кахексии, это доказывает их этиологическую роль. Физиологические изменения под влиянием этих цитокинов весьма многочисленны, через сложные механизмы они приводят к потере массы тела. У нормальных людей при голодании сначало истощаются жировые депо, у раковых же больных - и жировые депо, и белки скелетной мускулатуры.
В лечении используют парентеральное питание. Однако во многих исследованиях было показано, что полное парентеральное питание не улучшает прогноз больных из-за присоединения инфекции и механических осложнений. По возможности человека надо кормить через ЖКТ, что более дешевей и более физиологичней. Для определения базальных энергетических затрат используют формулу Гарриса-Бенедикта. На опухолевый процесс добавляется ещё 20-30%. При присоединение инфекции - добавляется ещё больше.
Используют также фармакологические препараты - стимуляторы аппетита, кортикостероиды, анаболические стероиды, антидепрессанты, анальгетики, антиэметики. ГКС коротким курсом улучшает аппетит и настроение, но их применение ограничено из-за мышечной слабости. Прогестероны - мегестрол и медроксипрогестерона ацетат - являются стимуляторами аппетитаю Назначение мегестрола ацетата (480 мг/день) - на 12 недель - увеличивает массу тела в среднем на 5,41 кг, но выживаемость не улучшает. При этом повышается риск тромбоэмболий. Используется также дронабиол, однако он более эффективен при анорексии при СПИДе. К несчастью терапия анорексии и кахексии у раковых больных малоэффективна.
Почечные проявления рака
Ятрогенные нефропатии, тубуло-интерстициальные, гломерулярные нарушения и нарушения водно-элекролитного баланса широко встречаются у раковых больных. Радиационные нефриты, токсичность ЛС (циспластин, антибиотики, анальгетики, радиоконтрастные препараты) приводят к различным формам почечной недостаточности. Инфильтраты при лейкозах, осаждение в канальцах различных веществ (белковая нефропатия, кальциевая, мочекислая нефропатия) приводит к тубуло-интерстициальным поражениям. Мембранная гломерулопатия, болезнь минимальных изменений, амилоидоз, коагулопатия потребления приводят к гломерулярным нарушениям. В конечном счёте гиперкальциемия, гипокальциемия, гипонатриемия приводят к нарушению водно-электролитного баланса.
Гломерулярные нарушения
Большинство мембранных нефропатий являются идиопатическими, но иногда они могут быть ассоциированы с раком, особенно у пожилых людей. В одном из исследовании из 101 человек с идиопатическим нефротическим синдромом, 11% было связано с раком, 8 % из которых - мембранозная нефропатия. Нефротический синдром характеризуется протеинурией, гипертензией и микроскопической гематурией. 60% с раком лёгкого, желудка и толстой кишки имеют мембранозную нефропатию. При раке прямой кишки, поджелудочной железы, яичника, предстательной железы, почек, кожи может быть гломерулонефрит. При иммунофлюоресцентном исследовании выявляют грунлярные свечения иммуноглобулинов и комплемента, при элекронной микроскопии - субэпительиальные отложения. Поражение клубочков при раке несёт иммунокомплексный механизм.
Нефротический синдром проходит после лечения опухоли. Для симптоматического лечения применяют петлевые диуретики, которые снимают периферические отёки. Тщательно следят за развитием тромбоэмболических осложнений, особенно тромбозом почечной вены.
Другие гломерулярные нарушения включают мембрано-пролиферативный гломерулонефрит и болезнь минимальных изменений. В большинстве случаев причиной болезни минимальных изменений является болезнь Ходжкина, очень редко - рак поджелудочной, мезотелиома. Имеется связь между активностью лимфомы и степенью протеинурии. При хроническом лимфоцитарном лейкозе может быть гломерусклероз, мембранозно-пролиферативный гломерулонефрит. В редких случаях может быть прогрессирующий гломерулонефрит.
Микроваскулярные поражения
Гемолитико-уремический синдром часто встречается после химиотерапии (митомицин С), но может быть и как паранеопластический синдром. В основном встречается при гигантских гемангиомах, раке простаты, желудка. Был описан вторичный, после пурпуры Шенляйна-Геноха, почечный васкулит у пациента с раком лёгкого, но он встречается очень редко. Более часто вторичный почечный васкулит встречается при криоглобулинемии, осложнении гепатоцеллюлярной карциномы и гепатита С.
Опухолевая инфильтрация
По данным вскрытий почки очень часто поражаются инфильтративными и пролиферативными процессами. У 40-60% больных с лейкозом имеются инфильтраты в почках. Неходжкинские лимфомы чаще поржают почки, чем болезнь Ходжкина. Имеется прочная связь между вовлечением в процесс почек и костного мозга. При лимфомах поражение узловое, при лейкозе - инфильтративное. Лечение опухоли приводит к разрешению изменений в почках.
Кожный паранеопластический синдром
С опухолями связан широкий спектр кожных проявлений. В большинстве случаев их причина остаётся неясной. Имеются кожные симптомы, которые специфичны для некоторых новообразований.
Пигментные нарушения и кератоз
Чёрный акантоз (acanthosis nigricans) характеризуется серо-коричневыми гиперпигментированными бляшками, которые чаще всего появляются на шее, в подмышечной области, на сгибательных поверхностях конечностей. Различают 4 группы - злокачественный, наследственный, эндокринный и идиопатический. Злокачественная форма характеризуется быстрым прогрессированием, сильным зудом. Встречается с одинкавой частотой у мужчин и женщин и обычно связан с аденокарциномой ЖКТ, раком желудка, лёгких, яичника. Патогенез остаётся неизвестным.
Пальмарное рубцевание (tripe palms) - характеризуется утолщением ладоней, вельветовой поверхностью и гиперпигментацией. Обычной сочетается с чёрным акантозом и встречается при раке лёгкого и желудка.
Меланоз - вызывается анормальным отложением меланина и характеризуется диффузной гиперпигментацией. Обычно локализуется на открытых частях тела. Гистологически обнаруживают гранулы меланина в меланоцитах и дерме. Меланоз может быть при опухолях, секретируемых АКТГ. Очень похож на гемохроматоз.
Симптом Лезера-Трелата - характеризуется появлением себорейного кератоза. Основная причина - это рак желудка. Также может быть при раке груди, при лимфомах.
Акрокератоз или симптом Базекса - характеризуется симметричным псориатоформным акральным гиперкератозом. Встречается при чешуйчато-клеточном раке пищевода, шеи и головы. Причина - продукцию перекрёстных АГ к опухоли и базальном мембране, синтез факторов роста (например, инсулиноподобный фактор роста-1).
Болезни Педжета характеризуется эритематозным кератозом вокруг ареолы, соска и связан с раком груди. Экстрамаммарная болезнь Педжета характеризуется эритематозным экссудативным дерматитом и локализуется в области промежности, гениталий. Гистологически болезнь Педжета характеризуется крупными бледными клетками в эпидермисе и плюс-тканью. В 50% случаев экстрамаммарная болезнь Педжета связана с каким-либо нововобразованием.
Нейтрофильный дерматоз
Синдром Свита характеризуется лихорадкой, нейтрофилией и появлением эритематозных болзненных бляжек, обычно на шее, верхних конечностях, лице. Морфологически в них обнаруживают дифференцированные нейтрофилы. Обычно встечается при остром миелобластном лейкозе. Этиология - предполагается гиперчувствительность. Для лечения используют ГКС.
Эритемы
Спиралевидная эритема - выглядит как дерево на спиле. Встречается при опухолях лёгких, груди, ЖКТ.При глюкагономе встречается некротизирующая мигрирующая эритема.
Эндокринные и метаболические поражения
Системный нодулярный панникулит (некроз подкожножировой клетчатки) - характеризуется появлением фиолетовых узелков. Встречается при опухолях поджелудочной железы. Может сопровождатся полиартралгией, лихорадкой, эозинофилией. Подобное поражение встречается при панкреатите вследствие высвобождения в сыворотку панкреатических ферментов (лидазы, амилазы, трипсина).
Синдром Кушинга характеризуется багровыми стриями, гиперпигментацией, телеангиэктазиями, атрофией кожи и лёгким гирсутизмом. Синдром Кушинга встречается при секреции АКТГ при мелкоклеточном раке лёгкого, раке ЩЖ, раке яичек и др.
Синдром Адисона - характеризуется генерализованной гиперпигментацией, особенно в области ран, местах давления и трения. Синдром встречается при недостаточности глюкокортикостероидов и опухолях надпочечников.
Буллёзные и уртикарные поражения
Параенеопластический пемфигоид чаще встречается при В-клеточных пролиферативных заболеваниях (лимфомах, хроническом лимфоцитарном лейкозе, болезни Кастлмана, тимоме, макроглобулинемии Вальденстрема). У пациентов развиваются блезненные буллёзные язвы. Часто вовлекаются внутренние органы, 30% умирает от дыхательной недостаточности. У пациентов с паранеопластическим пемфигоидом вырабатываются антитела к десмоглеину 1 и 3, что приводит к акантолизу. Течение болезни имеет прогрессирующий характер. Применяют кортикостероиды, циклоспорин и циклофосфамид.
При лимфомах встречается буллёзный пемфигоид.
При аденокарциномах толстой кишки, урогенитального тракта и лимфомах может встречаться синдром Муира-Торра, который характеризуется неоплазией сальных желез.
Смешанные поражения
Приобретённый ихтиоз характеризуется генерализованной сухостью, гиперкератозом ладоней и подошв. Обычно связан с болезнью Ходжкина, но может быть при лимфомах, множественной миеломе и других новообразованиях. Ихтиоз проходит после вылечивания рака.
Дерматомиозит характеризуется эритемой или телеангиэктазиями пальцев, верхней части грудной клетки, периорбитальной области. Частота рака у больных с дерматомиозитом варьирует от 10 до 50%, увеличиваясь с возрастом.
Пахидермопериостоз характеризуется утолщением кожи, губ, ушей, век, макроглоссией, повышенным потоотделением. Причина этого синдрома неизвестна, однако он часто встречается при бронхогенном карциноиде.
Гипертрихоз характеризуется появлением длинным жёстких волос в ушах, на лбу, возможны по всему телу. Встречается при опухолях лёгких, толстой кишки, мочевого пузыря и других.
При болезни Ходжкина, кожной Т-клеточной карциноме может быть зуд. Сильный зуд в ноздрях может быть у пациентов с опухолями мозга.
Отложение амилоида, что проявляется макроглоссией, поверхностными желтоватыми или розовыми жировыми узелками, могут быть при множественной миеломе, макроглобулинемии Вальденстрема.
Герпес-зостер - везикулёзное поражение по ходу дерматом. Наблюдается при иммуносупрессивных опухолях (болезни Ходжкина, лимфомах, лейкозах).
Врождённые заболевания
Болезнь Коудена (Cowden's disease) характеризуется множественными гамартомами. Наследуется по аутосомно-доминантному типу. Язык выглядит как "булыжная мостовая". Наблюдается пальмо-плантарный кератоз. Патогномичны множественные лицевые трихилеммомы. Чаще встречается у женщин. У таких людей повышен риск рака груди и щитовидной железы.
Синдром Гарденера (Gardener's syndrome) - наследуется по аутосомно-доминантному типу. Часто переходит в рак. Синдром включает множественные остеомы, фибромы, липомы, десмоидные опухоли, фибросаркомы, эпидермоидные кисты, лейомиомы. Характерным признаком является полипоз толстой кишки и прямой кишки. У половины больных после 30 лет развивается рак толстой кишки. Если не лечить, то пациенты доживают до 50 лет. Рекомендуется тотальная колонэктомия для предупреждения развития рака.
Синдром Петц-Егерса (Peutz-Jeghers syndrome) - наследуется по аутосомно-доминантному типу. Характеризуется гамартомными полипами ЖКТ, пигментацией лица, губ, слизистой оболочки рта. Риск развития рака составляет 2-3%. Из полипов могут образовываться карциномы. Рак развивается в более молодые годы.
Пальмарный и плантарный кератоз - наследуется аутосомно-доминантно и связан с развитией карциномы пищевода.
Нейрофиброматоз (болезнь Реклингхаузена) - характеризуется нейрофибромами и пятнами "кофе с молоком". Наследуется по аутосомно-доминантному типу. У таких больных иногда развивается феохромацитома.
Неврологические проявления рака
Теоритически под неврологическим паранеопластическим синдромом понимают любые нарушения ЦНС, не связанные с прорастанием в неё опухоли или с метастазами. Но обычно под ним понимают любые нарушения ЦНС. Неврологический паранеопластический синдром подразделяется по анатомическому принципу.
Частота. Нервно-мышечные нарушения (в основном в виде миопатии и периферической нейропатии) встречается довольно часто, в лёгких проявлениях почти у всех больных. Паранеопластический неврологический синдром встречается очень редко, у 1% раковых больных.
Патогенез. Причина и патогенез многих неврологических проявлений рака неизвестна. Различные симптомы объясняютяс различными механизмами. В 1888 году Оппенгейм предположил, что опухоли могут выделять нейротоксические вещества. Сейчас не известно паранеопластического синдрома с этим механизмом. Нервная система может вторично поражаться из-за выделяемых опухолью горомнов (АКТГ, паратгормон) и цитокинов (ФНО и ИЛ).
Паранеопластический синдром может быть вследствие оппортунистической инфекции. Прогрессирующий мультифокальный энцефалит в рамках паранеопластического синдрома вызывается JC-вирусом. У 12,5% пациентов в паранеопластическим неврологическим синдромом (включая паранеопластическую дегенерацию мозжечка и лимбический энцефалит) определяют 14-3-3 протеин в СМЖ, появляемый при болезни Кретцфельда-Якоба (Creutzfeldt-Jakob disease). Сейчас пока не ясно, какую роль играет протеин 14-3-3 в развитии паранеопластического синдрома и ведутся исследования.
Другой возможные механизм - это поглощение опухолевыми клетками биохимических веществ. Например, при больших метастатических карциноидных опухолях развивается энцефалопатия вследствие поглощения опухолью триптофана и ниацина. Однако больше неизвестно опухолей, которые бы приводили к этому синдрому через этот механизм. К тому же непонятно, как опухоли маленьких размеров могут поглотить много веществ, до такой степени, чтобы развилась их недостаточность.
Много синдромов возникает по Т-клеточному механизму. Исследование ЦНС пациентов с паранеопластическим синдромом показывает интенсивность воспалительного инфильтрата (включая Т-клетки). Большинство неврологических паранеопластических синдромом развивается по аутоиммунному механизму. Некоторые опухоли продуцирую антигены, которые в норме продуцируются только в ЦНС. Иммунная система реагирует на эти антигены и поражает нервную систему. Подострая мозжечковая дегенерация, оптический неврит, опсоклонус-миоклонус, подострая сенсорная нейропатия, миастения гравис, миастенический синдром Ламбера-Итона связаны с продукцией аутоантител. Хорошо описан синдром Ламбера-Итона, когда при миелоклеточном раке лёгкого вырабатываются аутоантитела против потенциал-зависимых кальциевых каналов.
Диагностика. Поскольку в большинстве случаев неврологический паранеопластический синдром развивается до того, когда становится известно, что у больного рак, диагностика очень трудна. Может быть два варианта:1). Известно, что у человека имеется рак, и тогда вопрос состоит в том, является ли неврологические симптомы проявлением метастаза или отдалёнными эффетками опухоли.2). Не известно, что у больного рак и надо решать вопрос, это связано с раком или нет. В первом случае в большинстве случаев неврологическая симптоматика обусловлена метастатическим поражением. Неврологические симптомы, которые могут вызвать трудности при постановке диагноза, это деменция, дисфункция мозжечка, слабость конечностей. Деменция - один из хорошо описанных отдалённых эффектов рака на НС. Однако, похожие симптомы могут быть у пациентов с множественными метастазами головного мозга, лептоменингеальным поражением, при нейродегенеративных нарушениях (болзень Альцгеймера), у пожилых пациентов с низкими резервами мозга и системными нарушениями метаболизма. Метастазы головного мозга обычно заметны на ЯМР и КТ. При болезни Альцгеймера - гидроцефалия на нейроснимках и нарушения в СМЖ. У пациентов с лимфомами следует учитывать инфекции ЦНС, такие как токосплазмоз, грибковый менингит, прогрессирующую мультифокальную лейкоэнцефалопатию.
При мозжечковой дисфункции сперва следует подумать о метастазе, а потом об отдалённых эффектах опухоли. Характеризуется билатеральным нарушением выполнения коленно-пяточной и пальце-носовой проб, дизартрией. Нистагма обычно нет. Также характерна деменция. Метастатическое поражение мозжечка характеризуется нарушением походки. Речь и верхние конечности в норме. Появляется односторонняя атаксия без тяжёлой дизартрии (гемисферальное поражение). МРТ и КТ уточняют диагноз.
Большие трудности в диагностике имеются у больных со слабостью конечностей, отсутствием рефлексов, с/без дисфункцией МП и кишечника. Врач может подозревать паранеопластическую периферическую нейропатию, но более вероятней - это вовлечение в процесс cauda equina лептоменингеальной опухолью. Диагноз устанавливается по исследованию СМЖ, КТ и ЯМР.
Многие неврологические паранеопластические синдром - такие как сенсомоторная периферическая нейропатия, деменция, острая поперечная миелопатия - случаются почти с такой же частотой, что и в обычной популяции. И обычно поиски опухоли у таких больных оказываются неплодотворными. Однако некоторые неврологические симптомы встречаются с очень большой частотой у раковых больных. Это дерматомиозит в среднем и пожилом возрасте, подострая мозжечковая дегенерация, подострая сенсорная нейропатия, подострая моторная нейропатия. У таких пациентов следует тщательно искать опухоль.
Аутоантитела.
У некоторых пациентов с неврологическим паранеопластическим синдромом определяют различные аутоантитела. Некоторые из них связаны с определённым синдромом (например, антитела к потенциал-зависимым Са-каналам при синдроме Ламбера-Итона), некоторые - с различными синдромами. Например, анти-Hu антитела обнаруживаются при паранеопластическом энцефалите, сенсорной нейропатии, мозжечковой дегенерации, опсоклонусе-миоклонусе. Обнаружение аутоантител анти-Yo с 90%-вероятностью доказывает на рак груди или гинекологический рак. Однако, аутоантитела не обязательны для паранеопластического синдрома. С другой стороны, присутствие аутоантител не всегда указывает на то, что имеется паранеопластический синдром.
Лечение.
Лечение неврологических паранеопластических синдромом в основном неэффективно. Исключение лишь составляет синдром Ламбера-Итона (при котором эффективен плазмаферез и 3,4-диаминопиридин) и опсоклонус-миоклонус, которые хорошо поддаётся терапии ГКС. Имеются заявления об успешном применении протеина А иммуноадсорбции. Также при синдроме Ламбера-Итона и опсоклонус-миоклонус эффективно лечение опухоли. Основная причина неэффективности лечения - это быстрое начало синдрома и обычно к тому времени, как поставят диагноз, происходят необратимые изменения. Иммуносупрессивная терапия у таких больных может приводить к опухолевому росту и увеличивает смертность.
Энцефаломиелит
Энцефаломиелит морфологически характеризуется воспалительной реакцией, периваскулярной лимфоцитарной инфильтрацией, накоплением лимфоцитов в мозге. Проявления могут быть самыми различными в зависимости от локализации поражения. Например, при вовлечении в процесс спинного мозга может быть поперечный миелит или моторная нейропатия, при поражении симпатической НС - ортостатическая гипертензия. Остаётся неизвестно, почему у разных людей поражаются различные отделы ЦНС. Лечения не разработано и нарушения приводят к тяжёлой слабости.
Мозжечковая дегенерация
Клинически характеризуется мозжечковыми симптомами - атаксией, дизартрией, дисфагией и патогенетически - поражением клеток Пуркинье мозежчка. Это самый распространённый неврологический паранеопластический синдром. Он встречается у 1% раковых больных. Обычно возникает при мелкоклеточном раке лёгкого, раке яичника, лимфомах (особенно ходжкинских), раке груди.
В большинстве случаев неврологическая симптоматика предшествует обнаружению опухоли в течение месяцев и лет. Начало обычно резкое, с симметричной атаксией рук и ног, прогрессирующее от нескольких недель до нескольких месяцев. Обычно имеется дизартрия и иногда нистагм. Серопозитивные пациенты "прогрессируют" быстрее. Обычно характерна лёгкая или средняя деменция. МРТ и КТ не определяют каких-либо нарушений, лишь на последних стадиях - лёгкую атрофию мозжечка. СМЖ может быть нормальна, но обычно в ней обнаруживают плеоцитоз и повышенный белок. В СМЖ часто повышается Ig G и присутствуют олигоклональные вещества.
С мозжечковой дегенерацией связано несколько аутоантител. Титр их выше в СМЖ, чем в крови, что указывет на их продукцию в ЦНС. Наиболее часто находят аутоантитела анти-Yo (поликлональные антитела класса Ig G к клеткам Пуркинье). Обычно их находят у женцин с сопутствующим раком груди, яичника, женских половых органов.
Другие пациенты не имеют аутоантитела анти-Yo, но имеют другие - антинейрональные нуклеарные аутоантитела типа 1 (анти-Hu) и анти-Ri антитела. Анти-Hu также связано с паранеопластическим энцефаломиелитом и сенсорной нейропатией. При болезни Ходжкина и некоторых других опухолях никаких специфических антител не обнаруживают.
В редких случаях возможна ремиссия, в основном у пациентов с болезнью Ходжкина и при отсутствии антител к клеткам Пуркинье.
Лимбический энцефалит
Паранеопластический лимбический энцефаломиелит - редкое осложнение рака яичка, мелкоклеточного рака лёгкого и некоторых других новообразований. Также может встречаться при отсутствии рака. Патоморфологически синдром характеризуется гибелью нейронов в amygdala, гипокампе и коре. Обычно имеется глиоз, инфильтрация кровеносных сосудов лимфоцитами, микроглиальные узелки. Клиника проявляется в подостром развитии расстройства личности и нарушении кратковременной памяти. Реже могут быть судороги, галлюцинации, дехориентация. У пациентов с лимбическим энцефалитом и тестикулярном раке находят аутоантитела анти-Та. Эффективного лечения нет. Было опубликовано, что лечение опухоли приводит к улучшению.
Паранеопластический опсоклонус-миоклонус
Опсоклонус - прерывистая нестабильность глазных яблок, характеризуется высокоамплитудным, автономным, хаотическим, содружественным движением глаз. Часто сочетается с местным миоклонусом и атаксией. Опсоклонус рассматривается в двух аспектах. У детей может быть опсоклонус вследствие вирусной инфекции, которая поражает мозг. Реже опсоклонус (с или без миоклонуса) развивается в рамках паранеопластического синдрома. У детей опсоклонус обычно появляется при нейробластоме и встречается у 2% детей с этой опухолью. Примерно 50% с опсоклонусом имеют нейробластому. Паранеопластический опсоклонус-миоклонус у детей отвечает на кортикостероидныю терапию. Однако в некоторых исследованиях остаточные неврологические явления наблюдадись в 69% случаев.
У взрослых опсоклонус-миоклонус встречается реже и реже ассоциирован с опухолью. Только у 20% имеется опухоль и в большинстве случаев это опухоль лёгких. Как при многих других неврологических паранеопластических синдромах, неврологическая симптоматика обычно предшествует диагностике рака. В СМЖ обычно находят лёгкий плеоцитоз и незначительное повышение белка. ЯМР и КТ как правило не показывают никаких изменений. Лечение малоэффективно. У некоторых больных находят анти-Hu и анти-Ri антитела.
Рак-ассоциированная ретинопатия
Дегенерация фоторецепторов в сетчатке - редкий паранеопластический синдром. В основном (90%) встречается при мелкоклеточном раке лёгкого. Но может быть при меланоме и других опухолях. Происходит дегенерация палочек, колбочек, ганглионарных клеток сетчатки. Также обычно обнаруживают лимфоцитарную инфильтрацию наружного слоя сетчатки. Клинически определяют фоточувствительность, скотомы, уменьшение диаметра артериол. Часто присутствует снижение цветного зрения, ночная слепота, снижение остроты зрения. СМЖ обычно в норме. В некоторых случаях неходят аутоантитела к клеткам сетчатки. Кортикостероиды иногда приводят к улучшению функций органа зрения.
Подострая сенсорная нейропатия
Подострая сенсорная нейропатия - редкий паранеопластический синдром, который характеризуется потерей чувствительности в конечностях. Чаще встречается без рака и обычно связан с первичным синдромом Съогрена. В большинстве случаев сенсорная нейропатия предшествует диагнозу рака, в 20% - развивается на фоне рака. В 90% слечаев встречается при мелкоклеточном раке лёгкого. Женщины болеют чаще мужчин.
Патоморфологические изменения находят в ганглиях задних корешков и гассериеновых ганглиях. Часто имеется лимфоцитарная инфильтрация ганглиев и вторичную потерю белого вещества задних столбов спинного мозга. Основные клинические симптомы - это онемелость, покалывание, боли в конечностях. Потеря чувствительности прогрессирует дни-недели и постепенно вовлекает все четыре конечности, потом подымается на туловище и голову. Теряются сухожильные глубокие рефлексы. Моторная функция обычно сохранена. Большинство пациентов не могут ходить. Лечение ГКС и плазмаферез неэффективны. Синдром иногда уменьшается спонтанно или после лечения опухоли.
Подострая моторная нейропатия
Подострая моторная нейропатия обычно связана с болезнью Ходжкина и другими лимфомами. Синдром характеризуется постепенным нарастанием мышечной слабости, без значительной потери чувствительности. Скорость нервного проведения нормальная. Электромиография показывает нарушение иннервации. В СМЖ обычно повышается уровень белка, плеоцитоза нет. Наблюдается патология клеток передних рогов спинного мозга, демиелинизация передних корешков и демиелинизация белого вещества спинного мозга. При болезни Ходжкина часто встречается специфическая моторная нейропатия - синдром Гийена-Барре. Эффективного лечения пока не найдено.
Сенсомоторная периферическая нейропатия
Смешанная моторная и сенсорная нейропатия очень часто встречается у раковых больных. В большинстве случаев она связана с нейротоксической химиотерапией, мальнутрицией и метаболическими нарушениями и не относится к паранеопластической. Описаны случаи сенсомоторной нейропатии при раке лёгкого. Нейропатия характеризуется нарушением чувствительности по типу "перчаток и носков". Бульбарные структуры обычно интактны. СМЖ - нормальная или с незначительно повышенным белком. Имеются обычно нарушение скорости проведения по нервному волокну и на электромиографии - признаки денервации. Гистологически выявляют дегенерацию аксонов и/или сегментарную демиелинизацию. Специфического лечения нет.
Миастенический синдром Ламбера-Итона
Синдром Ламбера-Итона характеризуется нарушением проведения импульса в нервно-мышечном соединении, что приводит к слабости мышц. Примерно у 40% пациентов с этим синдрмом отсутствует рак. Чаще болеют женщины. В 60% случаев развивается при раке лёгкого.
Синдром Ламбера-Итона развивается вследствие пражения потенциал-зависимых Са-каналов антителами. В результате этого нарушается вход Са в терминальную часть аксона и снижается высвобождения ацетилхолина. Синдром Ламбера-Итона экспериментально воспроизводится на животных путём введения Ig G больного человека.
Клинически характеризуется мышечной слабостью и усталостью. В отличии от классической myasthenia gravis, в процесс не вовлечена бульбарная мускулатура, хотя у 30% имеется дисфагия. Около половины пациентов имеют нарушение холинергической автономной системы (сухость во рту, импотенция).
В отличие от многих паранеопластических синдромов, синдром Ламбера-Итона хорошо поддаётся лечению плазмаферезом, в/в введением Ig, иммуносупрессивной терапией. Также используются средства, повышающие выделение трансмиттера (например, 3,4-диаминопиридин). Пиридостигмин удлиняет эффект 3,4-диаминопиридина, но в отдельности от неэффективен. Лечение опухоли также приводит к улучшению.
Дерматомиозит и полимиозит
Дерматомиозит и полимиозит - воспалительные миопатии, характеризующие подострым развитием мышечной слабости, с или без боли. При дерматомиозите имеется классическая гелиотропная сыпь на лице, локтях, коленях, в дополнение к мышечной слабости. В большинстве случаев эти состояния являются идиопатическими, и только в 10% связаны с опухолью. Чаще наблюдается при раке лёгкого и груди. Кроме мышечной слабости и поражения кожи, в крови повышается креатин-киназа. При биопсии мышц находят воспалительные инфильтраты, некрозы волокон, атрофию волокон. Стандартная терапия - иммунодепрессанты, в том числе ГКС. Синдром имеет непостоянное течение.
Смешанные синдромы
Эти синдромы встречаются очень редко. Stiff-person syndrome - очень редко встречается у женщин с раком груди. Характеризуется судорогами и окоченением мышц. В крови находят аутоантитела к антиамфифизину. У некоторых больных описана острая некротическая миопатия. При тимоме описана классическая myasthenia gravis.
Различные другие паранепластические синдромы
Гипертрофическая остеоартропатия
Гипертрофическая остеоартропатия была известна с древности. 25 столетий назад его описал Гиппократ как "барабанные палочки" и это синдром называют его именем - пальцами Гиппократа. В одно время этот синдром был назван легочной гипертрофической остеоартропатией, но вследствие того, что он встречается не только при заболеваниях лёгких, название упростили до гипертрофической остеоартропатии.
Периостоз характеризуется периостальной пролиферацией трубчатых костей, особенно большеберцовой и бедренной. Неполные формы ГОА характеризуются увеличением кончиков пальцев, изолированным периостозом, пахидермией, связанной с малыми проявлениями синдрома (синовиальные выпоты, себорея, фолликулит, гипергидроз, гипертрофическая гастропатия, акростеолиз). Некоторые исследователи для диагностики используют пробу с НПВС.
ГОА может быть первичной и вторичной. Вторичная в свою очередь бывает местной и генерализованной. Местная форма наблюдается у больных с гемиплегией, аневризмой, инфекционным артритом и открытым баталловым протоком. Генерализованная форма встречается чаще и встречается при шести группах заболеваниях:1). Болезни лёгких (самая частая причина) - мелкоклеточный рак лёгкого, метапластические поражения, цистический фиброз, легочной фиброз, хронические инфекции (абсцесс, бронхоэктатическая болезнь), артериовенозная фистула. 2). Болезни сердца - синие пороки сердца.3). Болезни печени - цирроз печени, печёночная карцинома.4). Болезни кишечника - болезнь Крона, неспецифический язвенный колит, опухоли кишечника.5). Болезни средостения - карцинома пищевода, тимома, ахалахия.6). Прочие причины - болезнь Грейвса, талассемия.
Барабанные палочки проходят после лечения опухоли, пересадке лёгких или печени. Эффективны НПВС. Хирургическое лечение и колхицин эффективны в меньшей степени. В многих случаях синдром терапии не поддаётся.
Лихорадка
Лихорадка встречается у многих пациентов с раком. Причины лихорадки чаще всего инфекции, опухоль, лекарственные причины, реакция продуктов крови и аутоиммунные заболевания. В 30% случаев причиной лихорадкой у раковых больных является непосредственно опухоль, в большинстве же случаев лихорадка обусловлена инфекцией. Основной дифференциальный признак - это уровень нейтрофилов. У лиц с нейтропенией большая вероятность инфекции, у лиц с нормальным количеством нейтрофилов - чаще всего другие причины. Лишь у 20% с лихорадкой и нормальным количеством нейтрофилов причиной лихорадки является инфекция.
При отсутствии инфекции считается, что опухоль продуцирует цитокины, которые и повышают температуру. Лихорадка чаще всего встречается при почечной карциноме (лихорадка встречается у половины больных с этой опухолью). У 1/3 больных с гепатомой развивается лихорадка. Лихорадка Пель-Эбштейна встречается при болезни Ходжкина и является важным прогностическим признаком. Также она может быть при неходжкинских лимфомах. Острый лейкоз, остеосаркома, миксома предсердия, феохромацитома, опухоли гипоталамуса редко связаны с развитием лихорадки.
В последние 20 лет хорошо описаны эндогенные пирогены. Главным из них является ИЛ 1. От выделяется при болезни Ходжкина. ИЛ 1 также увеличивает количество нейтрофилов и кортизола и связан с острой фазой ответа. ФНО также вызывает лихорадку, но действует на другие рецепторы, чем ИЛ 1. Также лихорадку вызывают ИЛ 6 и интерферрон.
Основная задача лечения лихорадки - это лечение инфекции. У пациентов с нейтропенией лихорадка сама по себе опасна для жизни. Если инфекция исключена, то основная терапия - это НПВС. Они уменьшают температуру путём ингибирования ЦОГ, уменьшения синтеза ПГЕ2. Некоторые исследователи используют пробу с НПВС для выяснения причины лихорадки. Если температура снижается после приёма напроксена и индометацина, то лихорадка скорей всего связана с опухолью. Также эффективны кортикостероиды, которые ингибируют ПГЕ2 и блокируют транскрипцию мРНК, кодирующую продукцию пирогенных цитокинов.
www.yurii.ru
Синдром Свита
Клиническая картина
Очаги при синдроме Свита высыпают остро и могут быть болезненными. Они имеют сливовый цвет и «сочный» вид (псевдовезикулярные).
Очаги могут возникнуть на любой поверхности кожи, но обычно появляются на голове, шее, ногах, руках, тыльных поверхностях кистей и пальцах рук.
Другие признаки
■ Системные симптомы включают лихорадку выше 38 С (50%), недомогание, артралгии или артрит (62%), поражение глаз (конъюнктивит, эписклерит, иридоциклит) (33%) и афты в полости рта (13%).
Редко имеется неитрофильныи инфильтрат в пределах верхних дыхательных путей, легких, печени, почек и мозга.
Лабораторная диагностика и биопсия цитарную формулу > 8000 клеток/мл с более чем 70% полиморфноядерных нуклеоцитов, повышенные СОЭ и уровень щелочной фосфатазы (40%).
■ Биопсия кожи показывает избыток нейтрофилов в дерме с выраженным субэпидермальным отеком без васкулита.
Дифференциальный диагноз
■ Многоформная эритема.
■ Узловатая эритема.
■ Побочные медикаментозные реакции. Крапивница.
Течение и прогноз
■ Синдром Свита у некоторых пациентов проходит самостоятельно.
■ Синдром Свита быстро реагируют на системные кортикостероиды. Типично лабораторные параметры корректируются в течение 72 ч, а кожные очаги очищаются в течение 3—9 дней.
■ У небольшого числа пациентов (15%) в течение нескольких лет бывают рецидивы.
Лечение
Системные кортикостероиды (преднизон 0,5—1,5 мг/кг/день) дают быстрое улучшение, их дозу постепенно снижают в течение 2—6 нед.
Миноциклин по 100 мг 2 раза в день или доксициклин («Юнидокс Солютаб») по 100 мг 2 раза в день могут быть эффективными средствами.
Прием внутрь иодида калия 15 мг/кг/день препятствует хемотаксису нейтрофилов и равен по эффективности системным кортикостероидам.
Другие средства: колхицин, дапсон, клофазимин, нестероидные противовоспалительные препараты и циклоспорин.
Острые, болезненные эритематозные бляшки, узлы, псевдовезикулы и, иногда, пузыри в форме колец или дуг появляются на конечностях. В случае распространенного заболевания иногда поражается туловище.
Очаги представлены болезненными эритематозными папулами и бляшками, также могут высыпать и псевдовезикулы или пустулы. Пустулы находятся внутри либо прилегают к очагу. Очаги имеют тенденцию множиться, но встречаются и изолированные. Бляшки обычно измеряются несколькими сантиметрами, но встречаются превышающие 20 см в диаметре.
Атипичныи синдром Свита (также известный как нейтрофильный дерматоз тыла кисти) — это недавно описанное заболевание. Характеризуется чрезвычайно болезненными, гноящимися сине-пурпурными узелками и бляшками, часто сопровождающимися изъязвлениями, локализующимися на тыльной поверхности кисти. Эффективны пероральные стероиды, неэффективны антибиотики.
medservices.info
Синдром Свита

Синдром Свита – одна из форм нейтрофильного дерматоза, которая характеризуется островоспалительным рецидивирующим течением. Основными проявлениями данного заболевания являются бляшки розового или ярко-красного цвета, лихорадочное состояние, нейтрофилия, боли в суставах. Диагностика синдрома Свита производится на основании клинической картины, гистологического исследования кожи, лабораторных анализов (ОАК, биохимическое исследование, ИФА). В настоящий момент этиотропное лечение не разработано, применяется противовоспалительная терапия кортикостероидами и нестероидными противовоспалительными средствами.
Синдром Свита

Синдром Свита (острый фебрильный нейтрофильный дерматоз) является довольно редким острым дерматологическим заболеванием, которое имеет волнообразное течение. Первым эту патологию выявил и описал Р. Свит в 1964-м году, с тех пор данный дерматоз носит его имя. Распространенность патологии 1-9 случаев на 1 млн. населения. В основном синдром Свита поражает лиц старшего возраста (средний возраст– 56 лет), встречается преимущественно у женщин – половое распределение составляет 3:1. По другим данным, более 90% всех заболевших составляют лица женского пола, причем описан случай развития патологии во время беременности. Замечена взаимосвязь между возникновением синдрома Свита и целым рядом других патологий – гематологических, инфекционных и эндокринных. Также описаны случаи, когда развитие нейтрофильного дерматоза предшествовало появлению злокачественных опухолей.
Причины синдрома Свита
Этиология синдрома Свита на сегодняшний день точно неизвестна, имеются предположения об иммунологической реакции нетипичного вида, при которой не происходит классической активации системы комплемента. Стимуляция иммунной системы предположительно производится бактериальными, опухолевыми или вирусными антигенами, которые формируют накапливающиеся в тканях комплексы. После этого возможно развитие реакции сверхчувствительности по типу Артюса и прямое воздействие на воспалительные клетки с выделением значительного количества медиаторов. Гистохимическими исследованиями было выявлено, что в кожных бляшках при синдроме Свита наблюдается значительное (в десятки и сотни раз) повышение концентрации интерлейкина-6 и колониестимулирующего фактора гранулоцитов. Однако это может быть обусловлено острым воспалением, имеющим место при подобном поражении дермы.
В большинстве случаев синдром Свита возникает вскоре после перенесенной острой респираторной вирусной инфекции. Также в качестве провоцирующего дерматоз фактора могут выступать стрептококковые поражения, иерсиниоз, неспецифический язвенный колит, аутоиммунные заболевания (в частности, тиреоидит Хашимото, болезнь Крона). Примерно в 20% случаев синдром Свита является паранеопластической реакцией на наличие злокачественного гематологического заболевания (острого миелоидного лейкоза) или солидных опухолей молочной железы, ЖКТ, мочеполовых органов. В дерматологии довольно часто встречаются больные дерматозом такого типа, которые перенесли онкологические заболевания в прошлом.
Классификация синдрома Свита
В настоящее время изучено несколько форм синдрома Свита, которые различаются между собой факторами, провоцирующими развитие патологии.
- Классическая или идиопатическая форма – является наиболее распространенной (почти 80% больных), возникает вскоре после респираторного заболевания или на фоне аутоиммунных поражений, иерсиниоза, неспецифического язвенного колита.
- Синдром Свита, ассоциированный с паранеоплазией – более редкая форма (менее 20% от всех заболевших), наиболее часто возникает при миелобластном лейкозе и других злокачественных гематологических заболеваниях. Также может развиться по причине рака груди или опухоли желудочно-кишечного тракта. В некоторых случаях развитие дерматоза наступает через много лет после лечения и ремиссии онкологического заболевания.
- Синдром Свита, вызванный приемом некоторых лекарств – самый редкий тип заболевания, может возникать на фоне приема гранулоцитарного колониестимулирующего фактора. Имеются отдельные указания на появление дерматоза после приема фуросемида, миноциклина и гидралазина.
Симптомы синдрома Свита
Первым признаком синдрома Свита служит появление на поверхности кожи папул диаметром 2-8 миллиметров. Пятна ярко-красного цвета, располагаются на руках, груди, шее. Затем через 2-3 дня присоединяется значительное повышение температуры (до 40 градусов), лихорадка, боли в суставах. Продолжается образование папул, которые через 7-10 дней после появления первых симптомов синдрома Свита начинают сливаться в бляшки неправильной формы диаметром до 7-ми сантиметров. Кожный зуд в местах появления высыпаний на всем протяжении заболевания имеет среднюю интенсивность или не наблюдается совсем. В редких случаях множественные папулы возникают сразу на всей поверхности тела, что свидетельствует о генерализованной форме синдрома Свита.
Со временем, на фоне лечения или самопроизвольно, бляшки начинают разрешаться – снижается отечность кожи, уменьшается интенсивность окраски. Как правило, при синдроме Свита подобные процессы начинаются в центре бляшек, поэтому на некоторое время они принимают кольцевидную форму, а затем имеют вид дуг. После полного затухания воспалительных процессов на месте высыпаний часто остаются участки гиперпигментаций кожи, сохраняющиеся длительное время. Синдром Свита характеризуется рецидивирующим течением, поэтому возможно возобновление артралгии и лихорадки, новое появление папул и бляшек на тех же участках, которые были поражены ранее.
Диагностика синдрома Свита
Главными методами диагностики синдрома Свита являются дерматологический осмотр, общий и биохимический анализ крови, в некоторых случаях производят биопсию кожи в области поражения. При осмотре врачом-дерматологом выявляется диссеминированный характер высыпаний, однако их распределение, как правило, симметричное. Обнаруживается наличие папул и бляшек на разных этапах своего развития. Возможно наличие гиперпигментированных участков кожи, которые остались от прошлых атак синдрома Свита. При пальпации в строении бляшек выявляется более плотный валик по краям образования. Объективно также обнаруживается повышенная температура тела, больные жалуются на боли в суставах.
Общий анализ крови при синдроме Свита показывает выраженный нейтрофильный лейкоцитоз – общее количество лейкоцитов может достигать 10-12х109/л, из них доля нейтрофилов всех типов составляет 60-70%. Также нередко наблюдается повышенный уровень моноцитов, ускорение скорости оседания эритроцитов. Биохимический анализ выявляет незначительное повышение уровня печеночных ферментов (АСТ и АЛТ), иногда снижение общего белка. Кроме того, при наличии синдрома Свита имеет смысл провести исследование на уровень основных онкомаркеров, антител к иерсиниозу и стрептококковым инфекциям – в ряде случаев эти тесты могут быть положительными.
При гистологическом изучении тканей кожных бляшек, возникающих при синдроме Свита, наблюдается неизмененный эпидермис, отек дермы, расширение капилляров и нейтрофильная инфильтрация. Дифференциальную диагностику следует проводить с крапивницей, узловатой и многоформной экссудативной эритемой, иногда системной красной волчанкой.
Лечение, прогноз и профилактика синдрома Свита
Этиотропной терапии синдрома Свита на сегодняшний момент не существует, лечение производят противовоспалительными препаратами – глюкокортикоидами (преднизолон), нестероидными противовоспалительными средствами (индометацин). У ряда больных отмечена положительная реакция на использование дапсона (противомикробное средство) и йодида калия. Наружно также назначают глюкокортикостероиды – в форме крема или мази, длительность лечения составляет 5-10 дней.
Прогноз синдрома Свита благоприятный, высыпания при правильно проведенном лечении быстро исчезают, оставляя после себя лишь участки повышенной пигментации, артралгия не возвращается после выздоровления. Однако существует риск рецидива заболевания, на тех же или новых областях тела. Кроме того, развитие синдрома Свита является поводом для обращения к онкологу и проведения комплексного обследования из-за риска наличия злокачественной опухоли или гематологической онкопатологии.
mymednews.ru
Синдром Свита - причины, симптомы, диагностика, лечение, фото
Синдром Свита – это достаточно редкое (или редко диагностируемое) заболевание, отнесенное к группе нейтрофильных дерматозов. Заболевание характеризуется волнообразным течением. Проявляется синдром Свита появлением папул или бляшек ярко-красного цвета, лихорадочным состоянием, болью в суставах, лейкоцитозом нейтрофильным.
Причины развития заболевания
 Женщины 30-50 лет болеют этим заболеванием чаще чем мужчины.
Женщины 30-50 лет болеют этим заболеванием чаще чем мужчины.Причины, вызывающие синдром Свита к настоящему времени выявить не удалось. Однако в большинстве случаев болезнь Свита развивается на фоне гематологических злокачественных патологий.
Синдром Свита, который не связан с онкологией, чаще всего, диагностируется у женщин возрастной группы 30-50 лет. Мужчины болеют примерно в три раза реже, причем, представители сильного пола заболевают в старшем возрасте – после 60.
Намного реже синдром Свита развивается на фоне заболеваний органов ЖКТ и дыхательной системы. Отмечены случаи, развития болезни Свита после введения медикаментов некоторых групп. Подобную реакцию могут дать антибиотики, препараты йода и брома.
Клиническая картина
За несколько недель до появления высыпаний, характерных для болезни Свита, у больного появляются общие симптомы, характерные для кишечной инфекции или гриппа. Больные жалуются на расстройства пищеварения, общую слабость, утомляемость, ломоту и боли в суставах и мышцах. Температура может подниматься до 40 градусов.
Затем появляются высыпания на коже. Локализуется сыпь при синдроме Свита на конечностях, шее, лице. Сыпь на туловище, как правило, отсутствует, однако, были описаны случаи, когда сыпь покрывала полностью все тело.
Высыпания при болезни Свита представляют собой папулы или узлы, цвет высыпаний – фиолетово-красный. Новообразования быстро разрастаются и сливаются в бляшки, которые могут достигать в диаметре 5 см и более. Бляшки имеют неправильную, нередко причудливую форму, границы четко выражены.
Кожа в местах высыпаний отечна, поэтому бляшки нередко выглядят, как пузыри, но они имеют плотную структуру. Такие высыпания называют псевдовезикулами. На пораженной коже можно заметить участки некроза, а также, корки и мокнущие эрозии.
Если у больного синдромом Свита выраженный лейкоцитоз, то сыпь проявляется настоящими пузырями, а не псевдовезикулами. При этой форме заболевания очаги поражения на коже выглядят, как гангренозная пиодермия. Высыпания достаточно болезненны при надавливании. Это могут быть и одиночные элементы, и множественные. Распределяются они беспорядочно.
 У больных синдромом Свита наблюдается лихорадочное состояние.
У больных синдромом Свита наблюдается лихорадочное состояние.У большинства людей, заболевших синдромом Свита, отмечаются нарушения общего состояния: лихорадочное состояние, боли в суставах, общее недомогание. У некоторых больных в процесс вовлекаются глаза, у них развивается конъюктивит или эписклерит.
Для болезни Свита характерен феномен патергии, заключается он в том, что новые высыпания появляются на месте микротравмы кожи, например, после инъекции.
Если больной не получает лечение, симптомы болезни Свита продолжают нарастать в течение нескольких недель, затем пораженная кожа постепенно заживает. Длительность периода болезни составляет 3-9 недель.
Синдром Свита склонен к рецидивированию, повторные случаи заболевания отмечаются у половины пациентов. При этом кожа поражается в тех же местах, что и при первом проявлении болезни.
Методы диагностики
Диагностика синдрома Свита, как правило, вызывает серьезные затруднения, так как оно встречается относительно нечасто и практикующим врачам практически не приходится с ним сталкиваться.
Диагноз ставится на основании изучении клинической картины и на проведении гистологических исследований биоптатов кожи, взятых с места поражения.
При проведении исследования можно отметить ярко выраженный отек верхних слоев дермы, наличие в ней инфильтрата из нейтрофилов.
Основные критерии диагностики:
- Внезапное возникновение характерной сыпи.
- Наличие дермального инфильтрата, состоящего из нейтрофильных гранулоцитов. При этом признаки лейкоцитокластического васкулита отсутствуют.
Дополнительными критериями являются:
- Лихорадочное состояние или перенесенное ранее инфекционное заболевание.
- Лейкоцитоз нейтрофильный.
- Артралгия (боли в суставах без деформации тканей), поражение глаз.
- Положительный результат при проведении патергической пробы (на месте укола образуются новые высыпания).
- Полное отсутствие улучшения при лечении антибиотиками и заметный эффект при применении кортикостероидов.
Чтобы больному был поставлен диагноз – синдром Свита, необходимо, чтобы у него присутствовали оба основных признака и любые два из списка дополнительных симптомов.
Больные при подозрении на синдром Свита должны быть направлены на консультацию к онкологу, поскольку это заболевание нередко является вторичным признаком онкологии.
Лечение
 Для лечения широко применяют преднизолон.
Для лечения широко применяют преднизолон.Успех в лечении болезни Свита во многом зависит от успеха лечения основного заболевания, которое стало причиной развития синдрома.
Для лечения синдрома Свита применяют кортикостероиды, как правило, Преднизолон. Препарат назначается в таблетках, использование инъекций исключено. Лечение продолжается не менее 3 недель.
При лихорадочном состоянии применяют жаропонижающие средства. При тяжелом течении синдрома Свита назначается Дапсон, Циклоспорин, Индометацин и йодид калия.
Местно для смазывания высыпаний применяют кремы или жировые взвеси (болтушки), содержащие кортикостероиды.
Лечение народными средствами
Для лечения синдрома Свита можно применять и средства, рекомендованные народной медициной.
Поскольку кожные проявления при болезни Свита образуют отеки, для устранения отечности рекомендуется использовать настои, приготовленные листа брусники, толокнянки, мелиссы, цветков боярышника и каштана. Настои можно готовить из любого из перечисленных растений или из их смеси. Для приготовления целебного настоя необходимо взять ложку травы или смеси из трав и стакан воды. Настаивать лекарственное средство лучше в термосе. Приготовленный настой процедить и выпить в течение дня.
Для того чтобы снизить интенсивность воспалительного процесса при болезни Свита, рекомендуется применять кору козьей ивы, лист березы, цветки таволги и бузины черной, корни лопуха и аира. Настои готовятся по описанной выше схеме.
Местно для снятия при синдроме Свита воспаления можно применять компрессы из сырой красной свеклы. Корнеплод нужно очистить и натереть на мелкой терке. Массу накладывают на марлю, прикладывают к пораженной коже, сверху накрывают пленкой и фиксирую эластичным или обычным бинтом. Аналогично можно приготовить компресс из листа алоэ.
Профилактика и прогноз
Профилактики заболевания болезнью Свита не существует, так как к настоящему времени не совсем ясны механизмы развития этого заболевания.
Прогноз при идиопатической форме болезни Свита (не связанной с основным заболеванием) благоприятный. Если болезнь Свита возникла на фоне онкологического или иного основного заболевания прогноз на выздоровления зависит от успешности лечения ассоциированной болезни. При отсутствии ремиссии основного заболевания будут наблюдаться рецидивы синдрома Свита.
dermalatlas.ru
|
|
..:::Счетчики:::.. |
|
|
|
|
|
|
|
|



