 0,25 мм. Сито с изменяющимся углом наклона приводится в колебательное движение от индивидуального привода с частотой вращения вала около 2700 об/мин.
0,25 мм. Сито с изменяющимся углом наклона приводится в колебательное движение от индивидуального привода с частотой вращения вала около 2700 об/мин.Роль белков в организме. Ферменты.
Роль белков в организме.
Функции белков в организме разнообразны. Они в значительной мере обусловлены сложностью и разнообразием форм и состава самих белков.
Белки - незаменимый строительный материал. Одной из важнейших функций белковых молекул является пластическая. Все клеточные мембраны содержат белок, роль которого здесь разнообразна. Количество белка в мембранах составляет более половины массы.
Многие белки обладают сократительной функцией. Это прежде всего белки актин и миозин, входящие в мышечные волокна высших организмов. Мышечные волокна - миофибриллы - представляют собой длинные тонкие нити, состоящие из параллельных более тонких мышечных нитей, окруженных внутриклеточной жидкостью. В ней растворены аденозинтрифосфорная кислота (АТФ), необходимая для осуществления сокращения, гликоген - питательное вещество, неорганические соли и многие другие вещества, в частности кальций.
Велика роль белков в транспорте веществ в организме. Имея различные функциональные группы и сложное строение макромолекулы, белки связывают и переносят с током крови многие соединения. Это прежде всего гемоглобин, переносящий кислород из легких к клеткам. В мышцах эту функцию берет на себя еще один транспортный белок - миоглобин.
Еще одна функция белка - запасная. К запасным белкам относят ферритин - железо, овальбумин - белок яйца, казеин - белок молока, зеин - белок семян кукурузы.
Регуляторную функцию выполняют белки-гормоны.
Гормоны - биологически активные вещества, которые оказывают влияние на обмен веществ. Многие гормоны являются белками, полипептидами или отдельными аминокислотами. Одним из наиболее известных белков-гормонов является инсулин. Этот простой белок состоит только из аминокислот. Функциональная роль инсулина многопланова. Он снижает содержание сахара в крови, способствует синтезу гликогена в печени и мышцах, увеличивает образование жиров из углеводов, влияет на обмен фосфора, обогащает клетки калием. Регуляторной функцией обладают белковые гормоны гипофиза - железы внутренней секреции, связанной с одним из отделов головного мозга. Он выделяет гормон роста, при отсутствии которого развивается карликовость. Этот гормон представляет собой белок с молекулярной массой от 27000 до 46000.
Одним из важных и интересных в химическом отношении гормонов является вазопрессин. Он подавляет мочеобразование и повышает кровяное давление. Вазопрессин - это октапептид циклического строения с боковой цепью:
Регуляторную функцию выполняют и белки, содержащиеся в щитовидной железе - тиреоглобулины, молекулярная масса которых около 600000. Эти белки содержат в своем составе йод. При недоразвитии железы нарушается обмен веществ.
Другая функция белков - защитная. На ее основе создана отрасль науки, названная иммунологией.
В последнее время в отдельную группу выделены белки с рецепторной функцией. Есть рецепторы звуковые, вкусовые, световые и др. рецепторы.
Следует упомянуть и о существовании белковых веществ, тормозящих действие ферментов. Такие белки обладают ингибиторными функциями. При взаимодействии с этими белками фермент образует комплекс и теряет свою активность полностью или частично. Многие белки - ингибиторы ферментов - выделены в чистом виде и хорошо изучены. Их молекулярные массы колеблются в широких пределах; часто они относятся к сложным белкам - гликопротеидам, вторым компонентом которых является углевод.
Если белки классифицировать только по их функциям, то такую систематизацию нельзя было бы считать завершенной, так как новые исследования дают много фактов, позволяющих выделять новые группы белков с новыми функциями. Среди них уникальные вещества - нейропептиды (ответственные за важнейшие жизненные процессы: сна, памяти, боли, чувства страха, тревоги).
Биологические катализаторы.
В основе всех жизненных процессов лежат тысячи химических реакций. Они идут в организме без применения высокой температуры и давления, т. е. в мягких условиях. Вещества, которые окисляются в клетках человека и животных, сгорают быстро и эффективно, обогащая организм энергией и строительным материалом. Но те же вещества могут годами храниться как в консервированном (изолированном от воздуха) виде, так и на воздухе в присутствие кислорода. Возможность быстрого переваривания продуктов в живом организме осуществляется благодаря присутствию в клетках особых биологических катализаторов - ферментов.
Ферменты - это специфические белки, входящие в состав всех клеток и тканей живых организмов играющие роль биологических катализаторов. О ферментах люди узнали давно. Еще в начале прошлого века в Петербурге К.С.Кирхгоф выяснил, что проросший ячмень способен превращать полисахарид крахмал в дисахарид мальтозу, а экстракт дрожжей расщеплял свекловичный сахар на моносахариды - глюкозу и фруктозу. Это были первые исследования в ферментологии. Хотя на практике применение ферментативных процессов было известно с незапамятных времен (сбраживание винограда, сыроварение и др.).
В разных изданиях применяются два понятия : "ферменты" и "энзимы". Эти названия идентичны. Они обозначают одно и тоже - биологические катализаторы. Первое слово переводится как "закваска", второе - "в дрожжах".
Долгое время не представляли, что же происходит в дрожжах, какая сила, присутствующая в них, заставляет вещества разрушаться и превра
www.studsell.com
Белки - азотистые соединения. В их состав входят углерод, водород, кислород, азот и сера, содержание которых в отдельных белках изменяется незначительно: С – 51-55%; Н – 6,5-6,7; О – 21,5-23,5; N – 15,0-18,6 и S – 0,3-2,5%.
Белковые вещества растительного и животного происхождения подразделяются на три группы:
1) белки, растворимые в воде или других жидкостях;
2) нерастворимые белки;
3) сложные белки – протеиды.
К группе растворимых относятся альбумины, глобулины, проламины, глютелины, протамины и гистоны.
Альбуминысодержат серу, растворимы в чистой воде, в солевых растворах, кислотах и щелочах. Содержатся в животном и растительном сырье.
Глобулиныв чистой воде не растворяются, хорошо растворимы в слабых растворах (5-15%) нейтральных солей. В растворах большей концентрации осаждаются. Встречаются больше всего в растительном мире ( в основном в семенах). Подобно альбуминам хорошо денатурируются при нагревании, механическом воздействии и т.п.
Проламины– растительные белки, растворимы в этиловом спирте концентрации 60-80%. В пшенице эта группа белка представлена глиадином, на долю которого приходится половина всего белка клейковины.
Глютелинытоже содержатся в семенах злаков, в зерне пшеницы представлены глютенином, участвующим вместе с глиадином в образовании клейковины. В воде, в растворах спирта и нейтральных солей нерастворимы; растворяются в слабых растворах кислот и щелочей.
Протамины и гистонывходят в состав белков клеточных ядер, что говорит об их важной роли в жизненных процессах. Встречаются в основном в белках животного происхождения, обладают выраженными щелочными свойствами, растворимы в воде, при нагревании не свёртываются.
К группе нерастворимых белков относятся белки животной природы. Они не растворяются ни в солевых растворах, ни в органических растворителях, растворяются при длительном нагревании в воде.
К этой группе относятсяколлаген(белок сухожилий) икератин(белок шерсти, копыт и рогов).
К протеидам, или сложным белкам, относятся фосфопротеиды, гликопротеиды, липопротеиды, нуклеопротеиды и др.
Фосфопротеиды– соединения белка с фосфорной кислотой, нерастворимы в воде, растворимы в щелочах. Эти белки представлены в молоке казеином, главным белком молока. Казеин осаждается в молоке слабыми растворами кислот.
Гликопротеиды– соединения белка и углеводов, встречаются в хрящевых тканях животных.
Нуклеопротеиды– белки, связанные с нуклеиновой кислотой. Это особо важная группа сложных белков, играющих первостепенную роль в жизнедеятельности организмов, в частности, в явлении наследственности. Содержатся в большом количестве в клеточных ядрах, а также в плазме клеток.
Хромопротеидысостоят из белка и красящего вещества небелковой природы. Их представителем является гемоглобин крови, выполняющий роль переносчика кислорода в организме.
Строение белков.
В химическом отношении белки являются аминокислотными полимерами. В настоящее время описано более 150 аминокислот, но только 22 из них являются составными частями белка. В белке пшеницы обнаружено всего 20 аминокислот. Аминокислоты (R-CH-COOH) являются своеобраз- Nh3
разными кирпичиками, из которых строится белковая молекула. Основной связью в молекулах белка является пептидная связь (-CO-NH-). Кроме пептидной в молекуле белка важную роль играют и дисульфидные связи (-S-S-).
В структуре белка различают 4 уровня организации:
первичная структура представлена последовательным соединением аминокислот в цепочку, в которой свободная аминная группа (-Nh3) одной аминокислоты соединена с карбоксильной группой (-COOH) другой аминокислоты, другая аминокислота таким же образом связана с третьей аминокислотой, третья - с четвёртой и т. д., до образования крупной молекулярной нити, называемой полипептидной цепочкой. В каждом белке аминокислоты в полипептидной цепочке чередуются в определённом порядке и постоянном составе;
вторичной структурой является спиралевидная структура полипептидной цепочки в пространстве. Скручивание её в спираль происходит под воздействием водородных связей (- H…O=) полярных групп соседних аминокислот;
третичная структура проявляется в компактной упаковке спиралевидной цепочки в пространстве. Наличие этой структуры подтверждено рентгеноструктурным анализом белков;
четвертичная структура представлена соединением в одну субъединицу нескольких полипептидных цепочек, сочленённых между собой нековалентными связями (водородными, гидрофобными и др.) и ориентированных определённым образом в пространстве в виде глобул или волокон, в зависимости от чего различают белки глобулярные и фибриллярные.
В создании вторичной, третичной и четвертичной структур участвуют водородные, ионные (солевые) и так называемые гидрофобные связи. Солевые связи возникают между щелочными (основными) и кислотными группами белка. Гидрофобное взаимодействие возникает между неполярными участками белковой молекулы.
Свойства белков.
Как сказано выше, белки являются сложными органическими азотистыми соединениями, состоящими из аминокислотных остатков, связанных между собой пептидными связями и образующих полипептидные цепочки, которые благодаря дисульфидным , водородным и ионным связям, а также гидрофобным взаимодействиям вполне определённым образом располагаются в пространстве и имеют при данных условиях для данного белка вполне определённую конформацию. Наиболее важными технологическими свойствами белков являются денатурация, набухание в воде (гидратация), способность образовывать пены и др.
Денатурация– это изменение пространственной ориентации белковой молекулы, не сопровождающееся разрывом ковалентных связей. Денатурация может вызываться повышением температуры, механическим и химическим воздействием, ультразвуком, ионизирующим облучением и другими факторами. Денатурация белков играет важную роль в технологических процессах, связанных с образованием структурных систем полуфабрикатов и готовых продуктов (хлеба, макаронных, кондитерских и других изделий).
Набуханиеобусловлено способностью белков, относящихся к гидрофильным веществам, поглощать воду и при определённых условиях образовывать растворы, называемые студнями. Набухший в воде белок пшеничной муки образует клейковину. Студни и клейковина обладают свойствами упругости и эластичности, пластичности и ползучести, т. е. свойствами твёрдого и жидкого тела.
Свойство набухания играет большую роль в технологии (набухание зерна при замочке, муки при замесе теста).
Пенообразование– способность белков образовывать эмульсии в системе жидкость – газ, называемые пенами. Белки как пенообразователи широко используются при изготовлении многих кондитерских изделий.
Белки представляют собой главный материал для построения тканей человеческого тела и являются незаменимой частью пищи. Биологическая ценность белков зависит от аминокислотного состава – наличия в них незаменимых аминокислот. Кроме того, специфические белки – ферменты – выполняют роль биологических катализаторов и в этом случае очень часто бывают связаны с витаминами и микроэлементами. Роль белков как источника энергии незначительна. Лишь 12-15% общего количества энергии организм получает от белковой части пищи.
Незаменимыми называются некоторые аминокислоты, не вырабатываемые самим организмом человека, а поступающие в него в готовом виде, т. е. с белками пищи. Незаменимых аминокислот восемь (таблица 1).
Таблица 1. Суточная потребность человека в аминокислотах (в г)
Аминокислоты (незаменимые) | Потребность, г | Аминокислоты | Потребность, г |
Триптофан | 1 | Гистидин1 | 1,5-2 |
Лейцин | 4-6 | Аргинин1 | 5-6 |
Изолейцин | 3-4 | Цистин | 2-3 |
Валин | 3-4 | Аланин | 3 |
Треонин | 2-3 | Серин | 3 |
Лизин | 3-5 | Глютаминовая кислота | 16 |
Метионин | 2-4 | Аспарагиновая кислота | 6 |
Фенилаланин | 2-4 | Пролин | 5 |
Глицин | 3 |
1Гистидин и аргинин тоже незаменимы применительно к рационам детского питания.
Белки в организме расщепляются до аминокислот, а из них затем синтезируются собственные белки. В молодом организме в связи с его ростом синтез белка протекает наиболее интенсивно. В организме взрослого человека процессы роста прекращаются, но, тем не менее, всё время происходит замена отживающих клеток новыми, построение которых невозможно без поступления белка извне. Белки нужны также для синтеза гормонов, нервных тканей и ферментов. Белки организма человека полностью обновляются примерно за 12 – 14 дней.
Энергоспособность белка составляет в расчёте на 1 г около 16,7 кДж.
Потребность в белках человека, не связанного с интенсивным физическим трудом, составляет 1,1-1,3 г белка в сутки на килограмм массы тела. Это значит, что человек массой 70 кг должен получать ежедневно 80-100 г белка.
Продукты, содержащие незаменимые аминокислоты, называются полноценными. При отсутствии в пище хотя бы одной незаменимой аминокислоты нарушается или становится невозможным синтез белков в организме, нарушается баланс азотистых веществ, что отрицательно сказывается на развитии и функциональной деятельности организма. Пища, содержащая все необходимые компоненты питания, называется сбалансированной по всем незаменимым факторам, в том числе и по аминокислотному составу. Отсутствие в ней незаменимых факторов приводит к прекращению роста и истощению организма, снижению его физиологической деятельности, иммунитета и в дальнейшем к гибели.
Таким образом, для рационального питания необходимо не только достаточное количество белка в рационе человека, но важен и его качественный, т. е. аминокислотный, состав. Белки животного происхождения (белки мяса, рыбы, яйца, молока и молочных продуктов) более полноценны, чем растительные. Поэтому до 60% белковой части рациона должны составлять белки животного происхождения.
2) Показатели качества, по которым оцениваются продукты питания. Классификация методик определения показателей качества пищевых продуктов.
Проблема качества в настоящее время имеет первостепенное значение. Изобилие продуктов питания для населения и сырья для промышленности в нашей стране будет достигнуто на основе изобилия высококачественной продукции животноводства и растениеводства. При этом следует учитывать, что высокое качество сырья одновременно означает прирост валового продукта, сокращение потерь при его хранении, увеличение выхода и повышение качества готовой продукции, снижение издержек производства.
Под качеством кулинарной продукции понимают совокупность потребительских свойств, обусловливающих её пригодность удовлетворять потребность людей в рациональном питании. Само понятие «качество» имеет не абсолютное, а относительное значение. В зависимости от назначения одни и те же продукты будут иметь различное качество.
Можно привести много примеров, когда один и тот же продукт является хорошим для удовлетворения данной потребности и совершенно непригоден для другого применения. Например, пшеничная мука с низким содержанием и плохим качеством белков, образующих клейковину, является хорошим сырьём для выработки печенья и очень плохим для выпечки хлеба; из ячменя с низким содержанием белка получают хорошее пиво, но такой ячмень даёт плохую перловую крупу.
Понятие «качество» применяют прежде всего при оценке товароведческих или товарно-потребительских достоинств продукта, а уже потом при определении способности этого продукта удовлетворять физиологические потребности организма человека. Совокупность показателей продукта (физических, химических, технологических, биологических и др.), определяющих его товарно-потребительские достоинства, характеризует уровень качества (экстра, высший, 1, 2 сорта и т.д.).
Совокупность тех же показателей продукта, определяющих его биологические достоинства, является мерой его полезности для человека. Нередко уровень качества продукта и его полезность вступают в противоречия.
Один и тот же продукт по своим торгово-товароведческим показателям может быть удостоен высшей аттестации, но с точки зрения удовлетворения биологической потребности человека он не может быть отнесён к продуктам, полезным для человека (например водка, табак и др.).
Высокая степень очистки или рафинации продукта часто находится в противоречии с его полезностью для человека. Продукты с высокой степенью очистки по праву относятся к изделиям экстра-класса, но в биологическом отношении эти продукты уступают по качеству продуктам этого вида с меньшей степенью рафинации. Например, в рафинированном растительном масле меньше биологически активных веществ, чем в сыром; столовой соли типа «экстра» отсутствуют соединения йода; хлеб из тёмных сортов муки содержит больше витаминов группы В и полезных минеральных солей, чем хлеб из светлых сортов муки; жирное мясо не полезнее постного и т. д. Следовательно, высший сорт продукта не всегда характеризуется наивысшим уровнем его биологической полезности.
Пищевая ценность продуктов характеризуется доброкачественностью, энергетической способностью, сенсорными и физиологическими свойствами. К наиболее существенным единичным показателям качества кулинарной продукции можно также отнести безвредность, высокие пищевые, вкусовые и товарные достоинства.
Доброкачественнымисчитаются такие продукты, которые не содержат веществ, вредных для организма человека ( ядовитые вещества, соли тяжёлых металлов, ядовитые алкалоиды, гликозиды, продукты распада органических веществ, токсины – яды, выделяемые некоторыми плесневыми грибами ), и посторонних примесей. В продуктах не должно быть патогенных микроорганизмов, плесневых грибов, вредителей, а также возбудителей инвазионных заболеваний.
Энергетическаяценностьопределяется путём умножения содержания в продукте жиров (в %) на число 37,7, белков на 16,7, углеводов на 15,7 и последующего суммирования результатов. Результаты получаем в джоулях на 100 г продукта.
Органолептическая(сенсорная)ценностьпродуктов характеризуется показателями, определяемыми органами чувств: внешний вид, консистенция, вкус и запах. Сенсорная ценность тесно связана с усвояемостью продуктов. Наиболее важным показателем является вкус. Высокими вкусовыми достоинствами обладают продукты, универсальные по химическому составу и содержащие ценные пищевые кислоты, и ароматические вещества.
Продукты, имеющие в своём составе разложившиеся органические вещества, обладают низкими вкусовыми свойствами.
Физиологическаяценностьпродуктов определяется наличием в них полезных элементов для осуществления процессов основного обмена веществ в организме. Понятие физиологической ценности отражает также влияние потребляемых продуктов на нервную, сердечно-сосудистую, пищеварительную и другие системы организма и на его сопротивляемость инфекционным заболеваниям. Кофеин в чае и кофе, теобромин в шоколаде, спирт в напитках, экстрактивные азотистые вещества возбуждающе действуют на нервную и сердечно-сосудистую систему. Иммунные тела в молоке и антимикробные вещества в мёде повышают устойчивость организма к инфекционным заболеваниям. Пищевые кислоты, особенно молочная в кисломолочных продуктах, подавляют гнилостные процессы в кишечнике. Пористая структура некоторых продуктов обусловливает равномерное наполнение желудка, улучшает работу органов пищеварения, стимулирует ощущение сытости.
Безвредностькулинарной продукции обеспечивают посредством строгого соблюдение санитарно-гигиенических требований, предъявляемых к производству кулинарной продукции, том числе к способам и режимам обработки продуктов, на всех стадиях технологического процесса.
Высокие пищевые достоинства кулинарной продукции в оптимальном варианте обусловливают соответствие её по составу формуле сбалансированного питания. Однако практически каждому виду кулинарной продукции присущи свои пищевые достоинства, как правило, отличные от формулы сбалансированного питания, что осложняет составление на её основе физиологически сбалансированного рациона питания.
Многие блюда и кулинарные изделия, составляющие основной ассортимент выпускаемой предприятиями общественного питания продукции, нуждаются в повышении пищевой ценности путём увеличения содержания в них витамина С, некоторых витаминов группы В, лучшей сбалансированности аминокислотного состава белков по их общему содержанию, а также количеству полиненасыщенных жирных кислот.
Высокиевкусовыедостоинствапищи – это те её показатели, которые мы воспринимаем органолептически, к которым мы привыкли и с которыми связаны наши представления о вкусной, хорошо приготовленной пище.
По привычным органолептическим восприятиям определяют кулинарную готовность пищи.
Пища всегда должна быть вкусной, и профессиональный уровень современного инженера-технолога общественного питания определяется не способностью изобретать блюда, а умением правильно вести технологический процесс обработки продуктов и приготовлять вкусные кушанья. «То полезно и питательно, что приятно и вкусно», - говорил И. П. Павлов.
Для удовлетворения индивидуальных вкусов потребителей на предприятиях общественного питания необходима также разнообразная продукция в ассортименте.
Желательность и удобство потребления кулинарной продукции определяют её высокиетоварныедостоинства. Для того чтобы продукция соответствовала этому показателю качества, например, капусту для фарша рубят, а не шинкуют соломкой, а копчёную колбасу нарезают тонкими ломтиками.
Важно, чтобы эти показатели качества продукции имели количественное выражение и установленный средний уровень, который должен выдерживаться в течение всего времени реализации продукции. Установленный уровень не только определяет качество продукции, но и является отправной точкой для совершенствования технологии её производства.
Кроме того, пищевые, вкусовые и товарные достоинства в общей оценке качества продукции должны иметь равное значение, т. е. нельзя говорить, что пища должна быть полезной и необязательно вкусной или наоборот. При совершенствовании технологии возможно улучшение одного или нескольких показателей качества конкретной продукции, но при этом остальные показатели должны соответствовать установленному уровню.
Необходимым условием для оценки качества кулинарной продукции или совершенствования её технологии является также воспроизводимость последней, т. е. формулировка рекомендуемых способов и режимов обработки должна быть такой, чтобы по данной технологии разные специалисты могли приготовить равноценную продукцию независимо от её количества.
Показатели качества продукции устанавливают различными методами: экспериментальным, расчётным, органолептическим, социологическим, экспертным, в принятом для них порядке.
Оценка уровня качества может производиться дифференциальным методом по единичным показателям качества, комплексным методом с использованием обобщающего показателя качества (например, энергоёмкость продукции) или смешанным методом. Следует помнить, что только при строгом соблюдении этих положений можно объективно оценить достоинства той или иной технологии и качество производимой на её основе продукции.
Химический состав пищевых продуктов является основным показателем ценности продуктов. Средней физиологической нормой соотношения между белками, жирами и углеводами является формула 1:1:4. Этой норме должен соответствовать суточный рацион пищи в целом, так как отдельно любой продукт по своему химическому составу этой норме не удовлетворяет.
Под физиологической, а точнее, биологической ценностью понимают сбалансированное содержание в продуктах усвояемых незаменимых аминокислот, витаминов, минеральных элементов и необходимых жирных кислот – линолевой, линоленовой и арахидоновой. В природе нет таких продуктов, которые содержали бы в нужном количестве все перечисленные здесь элементы пищи. По этим элементам должен быть сбалансирован весь суточный пищевой рацион.
На качество продуктов оказывают влияние разнообразные факторы внешней среды и производства. Наиболее важными из них являются: вид и качество сырья, способы и условия производства, упаковка, транспортирование и хранение. Качество сырья определяется его составом и технологическими свойствами с учётом целевого назначения. Например, зерно пшеницы может иметь различное назначение: получение муки хлебопекарной, кондитерской, макаронной.
Одним из основных показателей качества сырья является содержание в нём питательных веществ. Количество и качество их регламентировано соответствующими стандартами.
Производство продуктов связано с воздействием на сырьё различными технологическими примами, целью которых является повышение качества и усвояемости продуктов. Осуществление этой цели во многом зависит от опыта и мастерства персонала, технической оснащённости предприятия, технического уровня производства, его санитарно-гигиенического состояния и многих других факторов.
Режимы и условия хранения готовой продукции существенно влияют на её качество. В большинстве случаев при хранении решается комплексная задача – сохранение качества и количества продукта. В ряде случаев хранение продукции при определённых условиях и режимах является продолжением технологической обработки ( например, созревание сыра, вина, пива и т. п.), в результате которой качество продуктов существенно улучшается. Нарушение оптимальных условий и режимов хранения приводит к потере качества и количества продуктов.
3.Методы очистки пищевых масс (фильтрация, отстаивание, осаждение под действием центробежных сил, с помощью мембран). Физико-химические основы этих процессов.
Известны физические и физико-химические методы очистки.
Физические методы.
К физической очистке относится очистка свекловичного сока от пульпы – мелких кусочков свекловичной стружки. Обычно эта очистка производится путём фильтрации в специальных фильтрах ловушках. К этим методам относится так называемое рафинирование крахмала, заключающееся в выделении из крахмального молока механических примесей – мезги. Рафинирование производится на плоских сотрясательных ситах, представляющих собой каркас с натянутой на нём мелкой ситовой тканью. Сито имеет обычно уклон около 25 мм на 1 м и совершает 400- 600 продольных колебаний в минуту с амплитудой 7-10 мм.
При производстве растительных масел после шнековых прессов в масле содержится большое количество твёрдых суспензированных частиц, которые отделяются на вибрационных ситах. Сито состоит из металлической коробки, разделённой по длине на две камеры. В коробке установлено плетеное сито с размером отверстий 0,25 0,25 мм. Сито с изменяющимся углом наклона приводится в колебательное движение от индивидуального привода с частотой вращения вала около 2700 об/мин.
0,25 мм. Сито с изменяющимся углом наклона приводится в колебательное движение от индивидуального привода с частотой вращения вала около 2700 об/мин.
Масло поступает на вибрационное сито с температурой 60-70оС и, проходя через отверстия сит, направляется в сборники, а мезга удаляется на повторную переработку. Осадок обычно представляет собой смесь фосфатидов, слизей и белковых веществ.
К физическим способам очистки пищевых суспензий относятся также отстаивание, фильтрация и разделение при помощи центробежных сил.
Отстаивание.Осаждение под действием собственного веса твёрдых частиц, находящихся во взвешенном состоянии в жидкой среде, называют отстаиванием. Сущность отстаивания заключается в том, что неоднородная система, находящаяся в аппарате в состоянии покоя или движущейся с малой скоростью, разделяется в нём на составные части под действием веса. Осаждение частиц происходит по законам падения тел в среде, которая оказывает сопротивление их движению.
Скорость осаждения взвешенных частиц зависит от их плотности, степени дисперсности и физических свойств жидкости, в которой они осаждаются. В начальный момент частицы падают ускоренно, но через некоторый промежуток времени, когда сопротивление жидкой фазы уравновесит действие веса, они приобретают постоянную скорость осаждения ос.
ос.
Согласно закону Стокса постоянная скорость осаждения ( в м/с) может быть определена для ламинарной области по уравнению.
 =d2g(
=d2g( -
-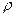 )/18
)/18 , (1)
, (1)
где d – приведенный диаметр частицы, м; g – ускорение свободного падения, м/с2; - плотность твёрдой частицы, кг/м3;
- плотность твёрдой частицы, кг/м3;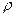 - плотность среды, кг/м3;
- плотность среды, кг/м3; - динамическая вязкость среды, Па.с.
- динамическая вязкость среды, Па.с.
Максимальный размер частиц, осаждение которых подчиняется закону Стокса, находят, подставив уравнение (1) вместо скорости осаждения её выражение через критерий Рейнольдса
 =
= Re/d
Re/d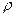 .
.
Приняв Re=2, т.е. предельное значение Re для ламинарной области, получим
dmax= g(
g(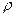 т-
т-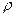 )
) 1,56
1,56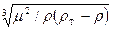 . (2)
. (2)
Формулы (1) и (2) справедливы для условий, когда частицы имеют шарообразную форму и область ламинарного осаждения соответствует Re<2. Для переходной области, где 2<Re<500 и Re>150000 применяются другие соотношения.
Обычно осаждение взвешенных частиц, находящихся в суспензии, осуществляется в отстойниках периодического и непрерывного действия. В большинстве случаев применяются многоярусные отстойники непрерывного действия с отводом осветлённой жидкой фазы и уплотнённого осадка из каждой секции.
При расчете отстойников определяются их производительность по осветлённой жидкости и необходимая площадь поверхности осаждения.
Производительность отстойника (в м3/с)
Vосв=Fh/ , (3)
, (3)
где F – площадь поверхности осаждения, м2; h – слой осветлённой жидкости, м; - время разделения суспензии на осветлённый слой жидкости и слой осадка, с.
- время разделения суспензии на осветлённый слой жидкости и слой осадка, с.
Так как =h/
=h/ , то
, то
Vосв=F . (4)
. (4)
Из уравнения (4) видно, что производительность отстойника не зависит от его высоты, она зависит только от скорости и площади поверхности осаждения. Поэтому при необходимости высокой производительности отстойников, требующих больших площадей поверхности осаждения, их делают многоярусными.
Фильтрование.Фильтрованием называют процесс разделения суспензий с использованием пористых перегородок, которые задерживают твёрдую фазу суспензии и пропускают её жидкую фазу. Этот процесс разделения суспензий называют фильтрованием с образованием осадка. В некоторых случаях твёрдые частицы проникают в поры фильтровальных перегородок и задерживаются в них, не образуя осадка. Такое фильтрование называется фильтрованием с закупориванием пор. Обычно в пищевой промышленности применяют фильтрование через слой осадка.
Движущей силой процесса фильтрации является перепад давлений над перегородкой (или слоем осадка и перегородкой) и под перегородкой. Перепад давлений создаётся при помощи вакуума, давления сжатого воздуха, подачи суспензии поршневым или центробежным насосом или гидростатического давления.
При разделении суспензий с небольшой концентрацией тонкодисперсной твёрдой фазы часто применяют вспомогательные фильтровальные вещества – диатомит, перлит, целлюлозу, асбест, активированный уголь и пр. Вспомогательные материалы представляют собой тонкодисперсные или тонковолокнистые вещества, наносятся тонким слоем на фильтровальную перегородку и, образуя своды над порами перегородки, препятствуют их забиванию. Если вспомогательные вещества образуют слой осадка на фильтрующей перегородке, то вначале фильтруют суспензию этого вещества, жидкой фазой которой являются вода или фильтрат суспензии. Вспомогательные вещества добавляют в количестве около 1% к массе фильтруемой суспензии.
В процессе фильтрования при постоянной разности давлений скорость фильтрации уменьшается, так как сопротивление слоя осадка возрастает с увеличением его толщины. Если перепад давлений при фильтровании увеличивается с возрастанием толщины осадка, то такой процесс называют фильтрованием с постоянной скоростью.
Получаемые при фильтровании осадки делят на сжимаемые, частицы которых с повышением давления деформируются, а размер пор капилляров уменьшается, и несжимаемые, размер и форма частиц которых не меняются с увеличением давления при фильтровании.
Так как в процессе фильтрования в большинстве случаев p=const, а сопротивление слоя осадка с течением времени изменяется, то скорость фильтрации
p=const, а сопротивление слоя осадка с течением времени изменяется, то скорость фильтрации
 =dV/Fd
=dV/Fd , (5)
, (5)
Где V – количество фильтрата, м3; F- площадь поверхности фильтрации, м2; - продолжительность фильтрования, с.
- продолжительность фильтрования, с.
Скорость фильтрации прямо пропорциональна перепаду давлений и обратно пропорциональна общему сопротивлению слоя осадка Rоси фильтрующей перегородки Rф, следовательно,
dV/Fd =
= p/ (Rос+ Rф). (6)
p/ (Rос+ Rф). (6)
где V – объём фильтрата, м3; p – разность давлений, Па; Rос– сопротивление слоя осадка, Па; Rф– сопротивление фильтрующей перегрузки, Па.
p – разность давлений, Па; Rос– сопротивление слоя осадка, Па; Rф– сопротивление фильтрующей перегрузки, Па.
Если в уравнение (6) ввести удельную производительность фильтра d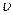 =dV/F (в м3/м2), сопротивление осадка с учётом вязкости жидкой фазы суспензии
=dV/F (в м3/м2), сопротивление осадка с учётом вязкости жидкой фазы суспензии (в Па.с) представить как произведение удельного сопротивления r (в 1/м2) на толщину слоя осадка, находящегося в 1 м3фильтруемой суспензии, то уравнение (6) представится в следующем виде:
(в Па.с) представить как произведение удельного сопротивления r (в 1/м2) на толщину слоя осадка, находящегося в 1 м3фильтруемой суспензии, то уравнение (6) представится в следующем виде:
d =(r
=(r x
x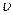 /
/ p + Rф/
p + Rф/ p) d
p) d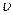 , (7)
, (7)
где x – толщина осадка, м.
Интегрируя это выражение в пределах от 0 до и от 0 до
и от 0 до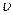 , найдём продолжительность фильтрации (в с)
, найдём продолжительность фильтрации (в с)
 =r
=r x
x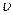 2/2
2/2 p+ Rф
p+ Rф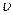 /
/ p=b
p=b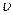 2+ Rф
2+ Rф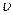 /
/ p, (8)
p, (8)
где b=r x/2
x/2 p.
p.
Удельный объём фильтрата (в м3/м2), прошедший через единицу площади поверхности фильтрующей перегородки за время , определяется из уравнения (8)
, определяется из уравнения (8)
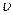 = - Rф/r
= - Rф/r x+
x+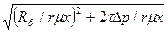 . (9)
. (9)
В промышленности для разделения суспензий применяются фильтры циклического действия: рамные фильтр-прессы, патронные фильтры, листовые фильтры – и фильтры непрерывного действия: барабанные вакуум фильтры и дисковые.
Осаждение под действием центробежной силы.Недостатком осаждения в отстойниках является их большие объёмы и значительное время осаждения. Отстойники малоэффективны при осаждении мелких частиц, имеющих размеры dэ<5 мкм, или когда их плотность близка к плотности среды. Значительно увеличивается эффективность процесса разделения суспензий с применением центробежных сил.
Поле действия центробежных сил создаётся вращательным движением потока разделяемой жидкости при тангенциальном её подводе в гидроциклоны или при направлении разделяемого потока во вращающийся корпус осадительных центрифуг.
Для определения эффективности осаждения в центробежных аппаратах необходимо сравнить величину центробежной силы с силой тяжести, действующей на частицу.
При вращательном движении суспензии в центробежных устройствах на частицу действует центробежная сила ( в Н)
Gц=m 2R, (10)
2R, (10)
где m – масса частицы, кг; - угловая скорость вращения частицы, с-1; R- радиус вращения частицы, м.
- угловая скорость вращения частицы, с-1; R- радиус вращения частицы, м.
Сила тяжести без учёта подъёмных сил составит
Gт=mg. (11)
Сравнивая уравнения (10) и (11), получим
Gц= Gт 2R/g, (12)
2R/g, (12)
т. е. центробежная сила больше сил тяжести в 2R/g раз.
2R/g раз.
Величину Ф= 2R/g называют фактором разделения. Чем больше фактор разделения, тем выше разделительная способность центробежных устройств.
2R/g называют фактором разделения. Чем больше фактор разделения, тем выше разделительная способность центробежных устройств.
При ламинарном режиме осаждения скорость осаждения (в м/с) определяется по уравнению Стокса с учётом фактора разделения
 =
= , (13)
, (13)
где d- размер частиц, м; g- ускорение свободного падения, м/с2;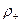 - плотность твёрдых частиц, кг/м3;
- плотность твёрдых частиц, кг/м3; - плотность среды, кг/м3;
- плотность среды, кг/м3; - вязкость среды, Па.с;
- вязкость среды, Па.с; - угловая скорость вращения, с-1; R- радиус вращения, м.
- угловая скорость вращения, с-1; R- радиус вращения, м.
Только в частном случае частица при центробежном разделении суспензии может находиться в ламинарном режиме. Обычно при центробежном разделении фактор разделения и скорость осаждения изменяются, так как они зависят от переменного радиуса R, изменяющегося с увеличением толщины осадка, а поэтому осаждения происходят по режимам: ламинарному, промежуточному и турбулентному.
Разделение растворов с помощью мембран.Весьма перспективным способом разделения пищевых растворов является процесс разделения под давлением через полупроницаемую перегородку (мембрану) – обратный осмос, или ультрафильтрация.
Ультрафильтрация предназначена для разделения низкоосмотических растворов и позволяет задерживать сравнительно крупные молекулы с молекулярной массой выше 500. Ультрафильтрация осуществляется при сравнительно низком давлении 0,05-1,0 МПа. Обратный осмос применяется для разделения растворов низкомолекулярных веществ, обладающих высоким осмотическим давлением, при этом рабочее давление составляет 5,0 - 10,0 МПа.
Разделение растворов мембранным методом происходит без фазовых превращений и при температуре окружающей среды.
Мембраны должны обладать высокой селективностью к извлекаемому веществу, высокой проницаемостью, достаточной механической прочностью, устойчивостью к воздействию агрессивных сред, постоянством параметров в процессе длительной эксплуатации.
Анизотропные мембраны представляют собой пластины толщиной 0,01-0,4 мкм. Наибольшее распространение получили ацетатцеллюлозные мембраны. Кроме этих мембран изготовляются мембраны на основе триацетатцеллюлозы, этилцеллюлозы, полиамидов, целлофана и др.
Мембраны получают путём облучения тонких полимерных плёнок потоком заряженных частиц – протонов или -частиц – с последующим химическим травлением. Ведутся исследования по изготовлению мембран с жёсткой структурой на основе металлов, пористого стекла, металлокерамики и т. п.
-частиц – с последующим химическим травлением. Ведутся исследования по изготовлению мембран с жёсткой структурой на основе металлов, пористого стекла, металлокерамики и т. п.
Особый интерес этот способ представляет для опреснения морской воды, разделения сахарных растворов, фруктовых соков, очистки продуктов микробиологических производств, сточных вод и т. д.
4. Хлебные злаки: краткая характеристика пшеницы, ржи, тритикале. Сколько и какие виды этих культур выращиваются в районе или области, где вы проживаете? Какова урожайность различных культур? В каких областях народного хозяйства используются?
Основные хлебные культуры - пшеницу, рожь, овес, кукурузу, рис, просо, сорго относят к семейству злаковых, классу однодольных растений. Различают две формы злаковых - яровые и озимые. Яровые растения высевают весной, за летние месяцы они проходят полный цикл развития и осенью дают урожай. Озимые растения сеют осенью, до наступления зимы они прорастают, а весной продолжают свой жизненный цикл и созревают несколько раньше, чем яровые. Озимую и яровую формы имеют пшеница, рожь, ячмень и тритикале. Все остальные злаки бывают только яровыми. Озимые сорта, как правило, дают более высокий урожай, однако их можно выращивать в районах с высоким снежным покровом и достаточно мягкими зимами.Пшеница– одна из важнейших зерновых культур. Это главная продовольственная культура для большинства населения земного шара. Ценность пшеницы заключается в том, что её белки способны образовывать клейковину, имеющую большое значение при производстве хлеба, макаронных изделий, манной крупы и других изделий. Пшеничная мука даёт хлеб лучшего качества, более вкусный и полнее усваиваемый, чем мука из зерна других культур (ржи, ячменя, овса, кукурузы). Пшеничное зерно и продукты его переработки имеют диетическое значение (хлебные изделия, приготовленные из целого зерна, с добавлением отрубей, клейковины и др.).Пшеница – культура однолетняя. В Беларуси возделывается пшеница озимая и яровая. Озимую пшеницу, как менее зимостойкую, по сравнению с яровой, высевают в более южных районах. На долю яровой пшеницы приходится 70-75% всей посевной площади под пшеницей, на долю озимой – 25-30%.Пшеница представлена большим разнообразием видов. В нашей стране наиболее распространены два вида – мягкая (около 90% всех посевов) и твёрдая пшеница. Твёрдая пшеница более требовательна к плодородию почвы, по урожайности она обычно уступает мягкой. Важно уметь различать зерно мягкой и твёрдой пшеницы по внешнему виду.Характеристика мягкой и твёрдой пшеницы по внешнему виду| Признаки | Зерно пшеницы | |
| мягкой | твёрдой | |
| Окраска | Красная разных оттенков и белая | Янтарная (за рубежом встречается краснозерная) |
| Форма зерна | Преимущественно овально-круглая | Удлинённая, в поперечном разрезе зерно угловатое |
| Стекловидность | В большинстве случаев зерно частично стекловидное, но имеются полностью стекловидные и мучнистые зёрна | Преобладают стекловидные зёрна (95-100%) |
| Форма зародыша | Округлая, более или менее вогнутая | Продолговатая, выпуклая |
| Бородка (хохолок) | Сильно развита, легко различима | Слабо развита, не вооружённым глазом не видна, различима лишь при увеличении в 5-6 раз |
| Отношение длины к ширине | 2:1 | 3/2:1 |
Ранние заморозки приостанавливают процессы синтеза в зерне при созревании. Хлебопекарное качество муки из такого зерна ухудшается. Хлеб получается с липким заминающимся мякишем, небольшого объёма, с плохо развитой пористостью, с солодовым или травянистым привкусом. Степень повреждения связана со стадией созревания зерна: на ранних стадиях созревания повреждение более глубокое, чем на более поздних. Зерно полной технической спелости заморозков не боится.
Прорастание зерна – начальный этап жизненного цикла растения. Для прорастания семени требуются повышенная влажность, тепло и воздух (кислород). Эти условия создаются при нарушении правил хранения. Главная особенность прорастания – распад в эндосперме и семядолях высокомолекулярных веществ до низкомолекулярных растворимых веществ при участии воды и под действием ферментов. Мука из проросшего зерна или из партии пшеницы, содержащей проросшие зёрна, даёт неудовлетворительный по качеству хлеб с липким, пониженной эластичности сладковатым мякишем, с характерной красновато-буроватой коркой. Подовый хлеб имеет повышенную расплываемость.
По стандарту пшеницу классифицируют по типам и подтипам. Типы пшеницы различают по видам, времени высева (яровая, озимая), цвету зерна и его стекловидности I – мягкая яровая краснозёрная; II – яровая твёрдая; III – мягкая яровая белозёрная; IV – мягкая озимая краснозёрная; V – мягкая озимая белозёрная; V – мягкая озимая белозёрная; VI – твёрдая озимая. Типы (кроме V и VI) разделяют на подтипы по оттенку типовой окраски зерна и его стекловидности. Например, I и IV типы имеют по четыре совпадающих по признакам подтипа: 1 – тёмно-красная с общей стекловидностью не менее 75%; 2 – красная, стекловидность не менее 60%; 3 – светло-красная, или жёлто-красная, стекловидность не менее 40%; 4 – преобладают жёлтые и желтобокие зёрна, придающие всей партии жёлтый оттенок, стекловидность менее 40%. Второй тип разделяют на два подтипа, третий тоже на два подтипа, пятый и шестой деления на подтипы не имеют.
Пшеницу, кроме типов, подразделяют на пять классов. Классы различают по типовому составу, состоянию (не греющаяся, в здоровом состоянии), запаху, цвету, стекловидности, натуре, количеству проросших зёрен. Важнейшими признаками классов служит содержание и качество клейковины, а для мягкой пшеницы, кроме того, число падения. Содержание клейковины колеблется по классам: по яровой пшенице: 1 класс – не менее 36%, 5 – не ограничивается; по озимой – 1 класс – не менее 28%, 5 – не ограничивается. Мягкая и твёрдая пшеница всех классов, кроме пятого, предназначена для использования в непродовольственных целях.
По стандарту (ГОСТ 9353) качество зерна пшеницы оценивают по следующим показателям: запах, цвет и обесцвеченность, влажность, содержание сорной и зерновой примесей, заражённость, типовой состав, число падения, натура, сте6кловидность, массовая доля и качество клейковины, содержание токсичных элементов.
Под урожай 2006 г. озимой пшеницей в республике было засеяно 240,2 тыс. га. Весной яровыми пересевалась третья часть посевов – 31,7% (76 тыс. га). Основные причины неоптимальный сортовой состав и использование нерайонированных сортов.
Рожь– вторая культура, мука из которой идёт на приготовление хлеба. Она относится к важнейшим хлебным культурам, особенно в районах с ограниченным возделыванием пшеницы. Ржаной хлеб отличается специфическим ароматом и вкусом. По вкусовым качествам, перевариваемости и усвояемости ржаной хлеб уступает только пшеничному. Ржаной хлеб по составу и свойствам гармонично дополняет хлебные изделия из пшеничной муки. Место ржаного хлеба в рационе большинства населения нашей страны закреплено вековыми традициями. Проросшее зерно ржи (красный ржаной солод) используют в качестве вкусовой добавки при производстве некоторых сортов ржаного хлеба из смеси пшеничной и ржаной муки.
Рожь почти исключительно озимая, яровую высевают в незначительных количествах. Эта культура менее требовательна к условиям произрастания, по сравнению с пшеницей, она вызревает в северных районах, где пшеница не растёт. Среднее содержание белка (12%) несколько меньше и с более узкими границами колебаний (10-17%), чем в зерне пшеницы. Вместе с тем наиболее дефицитных для злаковых культур незаменимых аминокислот лизина и треонина в ржаной муке примерно в 1,5 раза больше, чем в пшеничной. Белковые вещества обладают повышенной растворимостью в воде (около 30%). В условиях обычного тестоведения белки ржи не образуют клейковину.
Если при оценке хлебопекарного достоинства пшеничной муки решающую роль отводят белково-протеиназному комплексу, то для ржаной муки наибольшее значение приобретает углеводно-амилазный комплекс. В образовании вязких свойств ржаного теста большую роль играют набухание крахмала и гидратация слизей. Слизи представляют собой полисахариды, в большинстве случаев растворимые в воде. В зерне ржи их сравнительно много (от 2,5 до 7,4%). Слизи зерна ржи очень легко набухают в воде и образуют вязкие растворы.
Высокая активность амилолитических ферментов, расщепляющих крахмал, более низкая температура клейстеризации ржаного крахмала по сравнению с пшеничным, дополняют приведённые особенности поведения крахмала и слизей в процессах тестоведения, что в совокупности с названными выше составляет специфичность хлебопекарного достоинства ржаной муки.
Амилолитический комплекс состоит из двух ферментов: -амилазы, или сахарогенамилазы, и
-амилазы, или сахарогенамилазы, и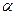 -амилазы, или декстриногенамилазы. Они существенно различаются между собой по характеру действия на крахмал.
-амилазы, или декстриногенамилазы. Они существенно различаются между собой по характеру действия на крахмал.
По стандарту качество зерна ржи оценивают по техническим требованиям, в которые входят: влажность, натура, сорная примесь ( в том числе испорченные зёрна), галька, вредная примесь (спорынья, семена вязеля разноцветного, гелиотропа опушенноплодного и др.), зёрна с розовой окраской, фузариозные зёрна, зерновая примесь, заражённость вредителями. Измеряют число падения и по его величине зерно ржи подразделяют на 4 класса: первый класс – более 200 с; второй – 200-141 с; третий – 140-80 с; четвёртый – менее 80 с. Рожь первых трёх классов предназначена для переработки в муку, четвёртого класса – для кормовых целей и для переработки в комбикорма. В районах, где не определяют число падения в зерновой примеси, указывают примесь проросших зёрен.
Тритикале– новая зерновая культура, представляющая собой новый ботанический род. Она получена в результате скрещивания двух разных ботанических родов – пшеницы и ржи. Тритикале привлекает к себе особое внимание в связи с тем, что по многим показателям (урожайности, содержанию белка и незаменимых аминокислот, пищевой и кормовой ценности и др.) она превосходит родителей, а по устойчивости к неблагоприятным почвенно-климатическим условиям и к наиболее опасным болезням превосходит пшеницу и не уступает ржи. По внешнему виду зерновка тритикале совмещает в себе признаки родителей. Она обычно более длинная, чем зерновка пшеницы (10-12 мм), и более широкая, чем зерновка ржи ( до 3 мм). Эндосперм имеет структуру, типичную для злаковых культур. Нередко в результате повышенной активности -амилазы, разрушающей крахмальные зёрна, созревшие зёрна получаются плохо выполненными, сморщенными. По натуре зерно тритикале уступает пшенице (пшеница 785-808 г/л, тритикале 730-754 г/л), но обычно превосходит рожь (550-712 г/л). Содержание белка в зерне тритикале на 1-1,5% выше, чем у пшеницы, и на 3-4% выше, чем у ржи. Содержание клейковины такое же, как у пшеничного зерна, или на 2-4% выше, но качество её из-за наследственности ржи ниже6 она слабая. В зерне тритикале повышенное содержание слизей. Хлебопекарное достоинство тритикалевой муки хуже, чем пшеничной: хлеб имеет меньший объём, уплотнённый, заминающийся мякиш, корка иногда покрыта трещинами.
-амилазы, разрушающей крахмальные зёрна, созревшие зёрна получаются плохо выполненными, сморщенными. По натуре зерно тритикале уступает пшенице (пшеница 785-808 г/л, тритикале 730-754 г/л), но обычно превосходит рожь (550-712 г/л). Содержание белка в зерне тритикале на 1-1,5% выше, чем у пшеницы, и на 3-4% выше, чем у ржи. Содержание клейковины такое же, как у пшеничного зерна, или на 2-4% выше, но качество её из-за наследственности ржи ниже6 она слабая. В зерне тритикале повышенное содержание слизей. Хлебопекарное достоинство тритикалевой муки хуже, чем пшеничной: хлеб имеет меньший объём, уплотнённый, заминающийся мякиш, корка иногда покрыта трещинами.
Тесто из тритикалевой муки по свойствам ближе к ржаному. Наилучший по качеству хлеб получается из смеси муки пшеничной (70-80%) и тритикалевой (20-30%). Зерно тритикале целесообразно перерабатывать в муку обойную 95%-ную и обдирную 87%-ную по традиционным схемам помола ржи. Хлеб из такой муки, выпеченной по схеме ржаного хлеба, приближается по качеству к аналогичным изделиям из ржи. За рубежом зерно тритикале широко используют для кормовых целей (зерно, сенаж, летний силос). Подчёркивается ценность зерна кормового назначения: оно содержит такое же или большее количество белка, чем зерно пшеницы, повышено содержание незаменимых аминокислот лизина и триптофана, не обладает токсичностью ржи (отсутствуют 5-алкилрезорцинолы). Известны сорта тритикале Амфидиплоид 206, АД 201,АД 209, АД 1 (кормовой). Корм на основе зерна тритикале обладает высокой усвояемостью.
В Беларуси планируется к 2010 г. посевные площади тритикале довести до 420 тыс. га.
По стандарту качество зерна тритикале оценивают по тем же показателям, что и зерно пшеницы.
Зерновые и зернобобовые культуры занимают 43,1% (2004) посевной площади. Среди зерновых культур преобладают озимая рожь и яровой ячмень (15,1%). При общем сокращении посевных площадей значительно выросли посевы озимой и яровой пшеницы, тритикале (29,3%). Сокращаются площади под озимой рожью. Наиболее урожайными в условиях Беларуси являются тритикале (30-40 ц/га), пшеница (25-27 ц/га). В 2004г валовой сбор зерна составил 7,02 млн. т, что в 1,1 раза больше, чем в наиболее урожайном за последние 20 лет 1990.
В 2006 г. в Борисовском районе намолочено 61120 тонн зерна, тем самым к намолоту 2005 г. обеспечена прибавка 4929 тонн. Урожайность составила 22,3 ц/га. В счёт поставок зерна для государственных нужд сдано 6975 тонн при плане 6800 тонн: госзаказ выполнен на 102,6%.
Особенно хорошую урожайность – свыше 50 центнеров с гектара – дали озимые культуры.
Список литературы:
18 мая 2007 г.
superbotanik.net
Роль белков в организме. Ферменты.
Роль белков в организме.
Функции белков в организме разнообразны. Они в значительной мере обусловлены сложностью и разнообразием форм и состава самих белков.
Белки - незаменимый строительный материал. Одной из важнейших функций белковых молекул является пластическая. Все клеточные мембраны содержат белок, роль которого здесь разнообразна. Количество белка в мембранах составляет более половины массы.
Многие белки обладают сократительной функцией. Это прежде всего белки актин и миозин, входящие в мышечные волокна высших организмов. Мышечные волокна - миофибриллы - представляют собой длинные тонкие нити, состоящие из параллельных более тонких мышечных нитей, окруженных внутриклеточной жидкостью. В ней растворены аденозинтрифосфорная кислота (АТФ), необходимая для осуществления сокращения, гликоген - питательное вещество, неорганические соли и многие другие вещества, в частности кальций.
Велика роль белков в транспорте веществ в организме. Имея различные функциональные группы и сложное строение макромолекулы, белки связывают и переносят с током крови многие соединения. Это прежде всего гемоглобин, переносящий кислород из легких к клеткам. В мышцах эту функцию берет на себя еще один транспортный белок - миоглобин.
Еще одна функция белка - запасная. К запасным белкам относят ферритин - железо, овальбумин - белок яйца, казеин - белок молока, зеин - белок семян кукурузы.
Регуляторную функцию выполняют белки-гормоны.
Гормоны - биологически активные вещества, которые оказывают влияние на обмен веществ. Многие гормоны являются белками, полипептидами или отдельными аминокислотами. Одним из наиболее известных белков-гормонов является инсулин. Этот простой белок состоит только из аминокислот. Функциональная роль инсулина многопланова. Он снижает содержание сахара в крови, способствует синтезу гликогена в печени и мышцах, увеличивает образование жиров из углеводов, влияет на обмен фосфора, обогащает клетки калием. Регуляторной функцией обладают белковые гормоны гипофиза - железы внутренней секреции, связанной с одним из отделов головного мозга. Он выделяет гормон роста, при отсутствии которого развивается карликовость. Этот гормон представляет собой белок с молекулярной массой от 27000 до 46000.
Одним из важных и интересных в химическом отношении гормонов является вазопрессин. Он подавляет мочеобразование и повышает кровяное давление. Вазопрессин - это октапептид циклического строения с боковой цепью:
Регуляторную функцию выполняют и белки, содержащиеся в щитовидной железе - тиреоглобулины, молекулярная масса которых около 600000. Эти белки содержат в своем составе йод. При недоразвитии железы нарушается обмен веществ.
Другая функция белков - защитная. На ее основе создана отрасль науки, названная иммунологией.
В последнее время в отдельную группу выделены белки с рецепторной функцией. Есть рецепторы звуковые, вкусовые, световые и др. рецепторы.
Следует упомянуть и о существовании белковых веществ, тормозящих действие ферментов. Такие белки обладают ингибиторными функциями. При взаимодействии с этими белками фермент образует комплекс и теряет свою активность полностью или частично. Многие белки - ингибиторы ферментов - выделены в чистом виде и хорошо изучены. Их молекулярные массы колеблются в широких пределах; часто они относятся к сложным белкам - гликопротеидам, вторым компонентом которых является углевод.
Если белки классифицировать только по их функциям, то такую систематизацию нельзя было бы считать завершенной, так как новые исследования дают много фактов, позволяющих выделять новые группы белков с новыми функциями. Среди них уникальные вещества - нейропептиды (ответственные за важнейшие жизненные процессы: сна, памяти, боли, чувства страха, тревоги).
Биологические катализаторы.
В основе всех жизненных процессов лежат тысячи химических реакций. Они идут в организме без применения высокой температуры и давления, т. е. в мягких условиях. Вещества, которые окисляются в клетках человека и животных, сгорают быстро и эффективно, обогащая организм энергией и строительным материалом. Но те же вещества могут годами храниться как в консервированном (изолированном от воздуха) виде, так и на воздухе в присутствие кислорода. Возможность быстрого переваривания продуктов в живом организме осуществляется благодаря присутствию в клетках особых биологических катализаторов - ферментов.
Ферменты - это специфические белки, входящие в состав всех клеток и тканей живых организмов играющие роль биологических катализаторов. О ферментах люди узнали давно. Еще в начале прошлого века в Петербурге К.С.Кирхгоф выяснил, что проросший ячмень способен превращать полисахарид крахмал в дисахарид мальтозу, а экстракт дрожжей расщеплял свекловичный сахар на моносахариды - глюкозу и фруктозу. Это были первые исследования в ферментологии. Хотя на практике применение ферментативных процессов было известно с незапамятных времен (сбраживание винограда, сыроварение и др.).
В разных изданиях применяются два понятия : "ферменты" и "энзимы". Эти названия идентичны. Они обозначают одно и тоже - биологические катализаторы. Первое слово переводится как "закваска", второе - "в дрожжах".
Долгое время не представляли, что же происходит в дрожжах, какая сила, присутствующая в них, заставляет вещества разрушаться и превращаться в более простые. Только после изобретения микроскопа было установлено, что дрожжи - это скопление большого количества микроорганизмов, которые используют сахар в качестве своего основного питательного вещества. Иными словами, каждая дрожжевая клетка "начинена" ферментами способными разлагать сахар. Но в то же время были известны и другие биологические катализаторы, не заключенные в живую клетку, а свободно "обитающие" вне ее. Например, они были найдены в составе желудочных соков, клеточных экстрактов. В связи с этим в прошлом различали два типа катализаторов: считалось, что собственно ферменты неотделимы от клетки и вне ее не могут функционировать, т.е. они "организованы". А "неорганизованные" катализаторы, которые могут работать вне клетки, называли энзимами. Такое противопоставление "живых" ферментов и "неживых" энзимов объяснялось влиянием виталистов, борьбой идеализма и материализма в естествознании. Точки зрения ученых разделились. Основоположник микробиологии Л. Пастер утверждал, что деятельность ферментов определяется жизнью клетки. Если клетку разрушить, то прекратиться и действие фермента. Химики во главе с Ю. Либихом развивали чисто химическую теорию брожения, доказывая, что активность ферментов не зависит от существования клетки.
В 1871 г. русский врач М.М. Манассеина разрушила дрожжевые клетки, растирая их речным песком. Клеточный сок, отделенный от остатков клеток, сохранял свою способность сбраживать сахар. Через четверть века немецкий ученый Э. Бухнер получил бесклеточный сок прессованием живых дрожжей под давлением до 5*10 Па. Этот сок, подобно живым дрожжам, сбраживал сахар с образованием спирта и оксида углерода (IV):
фермент
C6h32O6--->2C2H5OH + 2CO2
Работы А.Н. Лебедева по исследованию дрожжевых клеток и труды других ученых положили конец виталистическим представления в теории биологического катализа, а термины "фермент" и "энзим" стали применять как равнозначные.
В наши дни ферментология - это самостоятельная наука. Выделено и изучено около 2 тыс. ферментов.
Свойства ферментов.
Важнейшим свойством ферментов является преимущественное одной из нескольких теоретически возможных реакций. В зависимости от условий ферменты способны катализировать как прямую так и обратную реакцию. Это свойство ферментов имеет большое практическое значение.
Другое важнейшее свойство ферментов - термолабильность, т. е. высокая чувствительность к изменениям температуры. Так как ферменты являются белками, то для большинства из них температура свыше 70 C приводит к денатурации и потере активности. При увеличении температуры до 10 С реакция ускоряется в 2-3 раза, а при температурах близких к 0 С скорость ферментативных реакций замедляется до минимума.
Следующим важным свойством является то, что ферменты находятся в тканях и клетках в неактивной форме (проферменте). Классическими его примерами являются неактивные формы пепсина и трипсина. Существование неактивных форм ферментов имеет большое биологическое значение. Если бы пепсин вырабатывался сразу в активной форме, то пепсин "переваривал" стенку желудка, т. е. желудок "переваривал" сам себя.
Классификация ферментов.
На Международном биохимическом съезде было принято, что ферменты должны классифицироваться по типу реакции, катализируемой ими. В названии фермента обязательно присутствует название субстрата, т. е. того соединения, на которое воздействует данный фермент, и окончание -аза. (Аргиназа катализирует гидролиз аргинина и т.д.)
По этому принципу все ферменты были разделены на 6 признаков:
1.Оксидоредуктазы - ферменты, катализирующие окислительно-восстановительные реакции, например катализа:
2h4O2-->O2+2h4O
2.Трансферазы - ферменты, катализирующие перенос атомов или радикалов.
3.Гидролазы - ферменты, разрывающие внутримолекулярные связи путем присоединения молекул воды, например фосфатаза.
4.Лиазы - ферменты, отщепляющие от субстрата ту или иную группу без присоединения воды, негидролитическим путем.
Например, отщепление карбоксильной группы декарбоксилазой.
5.Изомеразы - ферменты, катализирующие превращение одного изомера в другой.
6.Синтетазы - ферменты, катализирующие реакции синтеза.
Ферментология - молодая и перспективная наука, отделившаяся от биологии и химии и обещающая много удивительных открытий тем, кто решит заняться ею всерьез.
topref.ru
. Ферменты.
Роль белков в организме.
Функции белков в организме разнообразны. Они в значительной мере обусловлены сложностью и разнообразием форм и состава самих белков.
Белки - незаменимый строительный материал. Одной из важнейших функций белковых молекул является пластическая. Все клеточные мембраны содержат белок, роль которого здесь разнообразна. Количество белка в мембранах составляет более половины массы.
Многие белки обладают сократительной функцией. Это прежде всего белки актин и миозин, входящие в мышечные волокна высших организмов. Мышечные волокна - миофибриллы - представляют собой длинные тонкие нити, состоящие из параллельных более тонких мышечных нитей, окруженных внутриклеточной жидкостью. В ней растворены аденозинтрифосфорная кислота (АТФ), необходимая для осуществления сокращения, гликоген - питательное вещество, неорганические соли и многие другие вещества, в частности кальций.
Велика роль белков в транспорте веществ в организме. Имея различные функциональные группы и сложное строение макромолекулы, белки связывают и переносят с током крови многие соединения. Это прежде всего гемоглобин, переносящий кислород из легких к клеткам. В мышцах эту функцию берет на себя еще один транспортный белок - миоглобин.
Еще одна функция белка - запасная. К запасным белкам относят ферритин - железо, овальбумин - белок яйца, казеин - белок молока, зеин - белок семян кукурузы.
Регуляторную функцию выполняют белки-гормоны.
Гормоны - биологически активные вещества, которые оказывают влияние на обмен веществ. Многие гормоны являются белками, полипептидами или отдельными аминокислотами. Одним из наиболее известных белков-гормонов является инсулин. Этот простой белок состоит только из аминокислот. Функциональная роль инсулина многопланова. Он снижает содержание сахара в крови, способствует синтезу гликогена в печени и мышцах, увеличивает образование жиров из углеводов, влияет на обмен фосфора, обогащает клетки калием. Регуляторной функцией обладают белковые гормоны гипофиза - железы внутренней секреции, связанной с одним из отделов головного мозга. Он выделяет гормон роста, при отсутствии которого развивается карликовость. Этот гормон представляет собой белок с молекулярной массой от 27000 до 46000.
Одним из важных и интересных в химическом отношении гормонов является вазопрессин. Он подавляет мочеобразование и повышает кровяное давление. Вазопрессин - это октапептид циклического строения с боковой цепью:
Регуляторную функцию выполняют и белки, содержащиеся в щитовидной железе - тиреоглобулины, молекулярная масса которых около 600000. Эти белки содержат в своем составе йод. При недоразвитии железы нарушается обмен веществ.
Другая функция белков - защитная. На ее основе создана отрасль науки, названная иммунологией.
В последнее время в отдельную группу выделены белки с рецепторной функцией. Есть рецепторы звуковые, вкусовые, световые и др. рецепторы.
Следует упомянуть и о существовании белковых веществ, тормозящих действие ферментов. Такие белки обладают ингибиторными функциями. При взаимодействии с этими белками фермент образует комплекс и теряет свою активность полностью или частично. Многие белки - ингибиторы ферментов - выделены в чистом виде и хорошо изучены. Их молекулярные массы колеблются в широких пределах; часто они относятся к сложным белкам - гликопротеидам, вторым компонентом которых является углевод.
Если белки классифицировать только по их функциям, то такую систематизацию нельзя было бы считать завершенной, так как новые исследования дают много фактов, позволяющих выделять новые группы белков с новыми функциями. Среди них уникальные вещества - нейропептиды (ответственные за важнейшие жизненные процессы: сна, памяти, боли, чувства страха, тревоги).
Биологические катализаторы.
В основе всех жизненных процессов лежат тысячи химических реакций. Они идут в организме без применения высокой температуры и давления, т. е. в мягких условиях. Вещества, которые окисляются в клетках человека и животных, сгорают быстро и эффективно, обогащая организм энергией и строительным материалом. Но те же вещества могут годами храниться как в консервированном (изолированном от воздуха) виде, так и на воздухе в присутствие кислорода. Возможность быстрого переваривания продуктов в живом организме осуществляется благодаря присутствию в клетках особых биологических катализаторов - ферментов.
Ферменты - это специфические белки, входящие в состав всех клеток и тканей живых организмов играющие роль биологических катализаторов. О ферментах люди узнали давно. Еще в начале прошлого века в Петербурге К.С.Кирхгоф выяснил, что проросший ячмень способен превращать полисахарид крахмал в дисахарид мальтозу, а экстракт дрожжей расщеплял свекловичный сахар на моносахариды - глюкозу и фруктозу. Это были первые исследования в ферментологии. Хотя на практике применение ферментативных процессов было известно с незапамятных времен (сбраживание винограда, сыроварение и др.).
В разных изданиях применяются два понятия : "ферменты" и "энзимы". Эти названия идентичны. Они обозначают одно и тоже - биологические катализаторы. Первое слово переводится как "закваска", второе - "в дрожжах".
Долгое время не представляли, что же происходит в дрожжах, какая сила, присутствующая в них, заставляет вещества разрушаться и превращаться в более простые. Только после изобретения микроскопа было установлено, что дрожжи - это скопление большого количества микроорганизмов, которые используют сахар в качестве своего основного питательного вещества. Иными словами, каждая дрожжевая клетка "начинена" ферментами способными разлагать сахар. Но в то же время были известны и другие биологические катализаторы, не заключенные в живую клетку, а свободно "обитающие" вне ее. Например, они были найдены в составе желудочных соков, клеточных экстрактов. В связи с этим в прошлом различали два типа катализаторов: считалось, что собственно ферменты неотделимы от клетки и вне ее не могут функционировать, т.е. они "организованы". А "неорганизованные" катализаторы, которые могут работать вне клетки, называли энзимами. Такое противопоставление "живых" ферментов и "неживых" энзимов объяснялось влиянием виталистов, борьбой идеализма и материализма в естествознании. Точки зрения ученых разделились. Основоположник микробиологии Л. Пастер утверждал, что деятельность ферментов определяется жизнью клетки. Если клетку разрушить, то прекратиться и действие фермента. Химики во главе с Ю. Либихом развивали чисто химическую теорию брожения, доказывая, что активность ферментов не зависит от существования клетки.
В 1871 г. русский врач М.М. Манассеина разрушила дрожжевые клетки, растирая их речным песком. Клеточный сок, отделенный от остатков клеток, сохранял свою способность сбраживать сахар. Через четверть века немецкий ученый Э. Бухнер получил бесклеточный сок прессованием живых дрожжей под давлением до 5*10 Па. Этот сок, подобно живым дрожжам, сбраживал сахар с образованием спирта и оксида углерода (IV):
фермент
C6h22O6--->2C2H5OH + 2CO2
Работы А.Н. Лебедева по исследованию дрожжевых клеток и труды других ученых положили конец виталистическим представления в теории биологического катализа, а термины "фермент" и "энзим" стали применять как равнозначные.
В наши дни ферментология - это самостоятельная наука. Выделено и изучено около 2 тыс. ферментов.
Свойства ферментов.
Важнейшим свойством ферментов является преимущественное одной из нескольких теоретически возможных реакций. В зависимости от условий ферменты способны катализировать как прямую так и обратную реакцию. Это свойство ферментов имеет большое практическое значение.
Другое важнейшее свойство ферментов - термолабильность, т. е. высокая чувствительность к изменениям температуры. Так как ферменты являются белками, то для большинства из них температура свыше 70 C приводит к денатурации и потере активности. При увеличении температуры до 10 С реакция ускоряется в 2-3 раза, а при температурах близких к 0 С скорость ферментативных реакций замедляется до минимума.
Следующим важным свойством является то, что ферменты находятся в тканях и клетках в неактивной форме (проферменте). Классическими его примерами являются неактивные формы пепсина и трипсина. Существование неактивных форм ферментов имеет большое биологическое значение. Если бы пепсин вырабатывался сразу в активной форме, то пепсин "переваривал" стенку желудка, т. е. желудок "переваривал" сам себя.
Классификация ферментов.
На Международном биохимическом съезде было принято, что ферменты должны классифицироваться по типу реакции, катализируемой ими. В названии фермента обязательно присутствует название субстрата, т. е. того соединения, на которое воздействует данный фермент, и окончание -аза. (Аргиназа катализирует гидролиз аргинина и т.д.)
По этому принципу все ферменты были разделены на 6 признаков:
1.Оксидоредуктазы - ферменты, катализирующие окислительно-восстановительные реакции, например катализа:
2h3O2-->O2+2h3O
2.Трансферазы - ферменты, катализирующие перенос атомов или радикалов.
3.Гидролазы - ферменты, разрывающие внутримолекулярные связи путем присоединения молекул воды, например фосфатаза.
4.Лиазы - ферменты, отщепляющие от субстрата ту или иную группу без присоединения воды, негидролитическим путем.
Например, отщепление карбоксильной группы декарбоксилазой.
5.Изомеразы - ферменты, катализирующие превращение одного изомера в другой.
6.Синтетазы - ферменты, катализирующие реакции синтеза.
Ферментология - молодая и перспективная наука, отделившаяся от биологии и химии и обещающая много удивительных открытий тем, кто решит заняться ею всерьез.
www.coolreferat.com