
Скачать (234 Kb)
Оглавление
1. Введение2. Классификация методов люминесценции 2.1 По способу возбуждения 2.2 По длительности 2.3 По механизму свечения3. Схемы Яблонского4. Заключение5. Список литературы
Все вещества при сильном нагревании начинают излучать электромагнитную энергию. Излучение нагретых веществ называют тепловым равновесным излучением. Однако некоторые вещества излучают электромагнитную энергию без нагревания – при комнатной температуре. Такое излучение называют люминесценцией, а люминесцентные вещества – люминофорами. В отличие от теплового, люминесценция является неравновесным излучением.
По В. Л. Левшину, люминесценция – это свечение атомов, молекул, ионов и других более сложных комплексов, возникающее в результате электронного перехода в этих частицах при их возвращении из возбужденного состояния в нормальное.
Метод молекулярной люминесцентной спектроскопии характеризуется высокой чувствительностью (порядок обнаружения 10-3 мг/мл), так как относится к силовым – выходной сигнал увеличивается с увеличением интенсивности источника излучения. В идеальных условиях удается достичь пределов обнаружения на уровне пикограммов в миллилитре.
В реферате приведена классификация методов люминесценции по способу возбуждения, механизму и длительности, описаны схемы Яблонского.
Из определения люминесценции следует, что для её возбуждения необходимо подводить энергию извне, так как она теряется при излучении. Поэтому виды люминесценции естественно классифицировать по внешнему источнику возбуждения энергии.
| Источник возбуждения | Вид люминесценции |
| Электромагнитное излучение видимой и ультрафиолетовой области спектра | фотолюминесценция |
| Поток электронов (катодные лучи) | Катодолюминесценция |
| Поток ионов щелочных металлов в вакууме | Ионолюминесценция |
| Рентгеновское излучение | Рентгенолюминесценция |
| Радиоактивное излучение | Радиолюминесценция |
| Тепловая энергия | Термолюминесценция (кандолюминесценция) |
| Ультразвук | Сонолюминесценция |
| Механическое воздействие | Триболюминесценция |
| Энергия химических реакций | Хемолюминесценция |
| Энергия биологических процессов | Биолюминесценция |
Наиболее часто в аналитической практике используют фотолюминесценцию и хемилюминесценцию.
Тип люминесценции зависит от того, какие переходы осуществляются в молекуле при поглощении ею квантов возбуждающего излучения.Молекулярная люминесценция по длительности и спектральному составу:
Испускание фотонов флуоресценции происходитпри переходе электрона с нулевого колебательного уровня состояния на любой колебательный уровень основного состояния. Флуоресценция является кратковременным излучением с длительностью 10-10-10-7 секунд и наблюдается при комнатной температуре. Энергия фотонов флуоресценции меньше энергии фотонов поглощения.
При определенных условиях (обычно при температуре -196 °С, в отсутствие парамагнитных молекул) для триплетных молекул оказывается возможнымзапрещенный переходс излучением фотонов фосфоресценции. Это излучение имеет значительно большую длительность 10-4-10-2 секунд. Энергия фотонов фосфоресценции меньше энергии фотонов кратковременной флуоресценции.
Помимо флуоресценции и фосфоресценции существует еще один вид люминесценции, который идентичен по спектральному составу флуоресценции, но характеризуется длительностью, свойственной фосфоресценции. Этот вид люминесценции называют замедленной флуоресценцией, поскольку перед излучением фотонов молекула некоторое время находится в триплетном состоянии.Этот тип молекулярной люминесценции наблюдается в весьма ограниченных диапазонах температур, вязкостей и концентраций растворов. По сравнению с флуоресценцией и фосфоресценцией ее интенсивность невелика и достигает максимальных значений при комнатной и более высоких температурах, заметно ослабевая с понижением температуры.

Рисунок 1. Схемы энергетических уровней и электронных переходов.
1 – основной уровень; 2, 3 – возбужденные уровни; 4 – метастабильный уровень; ↑ – поглощение; ↓ – люминесценция;  – безызлучательный переход.
– безызлучательный переход.
Поглощающими и излучающими центрами являются одни и те же частицы (атомы, ионы или молекулы). Этот вид свечения присущ в основном веществам в газообразном состоянии, органическим и неорганическим веществам в растворах и чистым органическим веществам.
Резонансная люминесценция характерна преимущественно для атомов, простейших молекул, находящихся в газообразном состоянии при низких давлениях, спонтанная — для паров и растворов сложных молекул, вынужденная — для сложных органических молекул, находящихся при низкой температуре или помещенных в вязкие или стеклообразные среды (полимерные пленки, сахарные леденцы).
Акты поглощения и излучения разделены не только во времени, но и пространственно. В процессе возбуждения происходит разделение частицы на две противоположно заряженные. Последовательность их рекомбинации сопровождается выделением энергии. Этот вид свечения является основным в свечении кристаллофосфоров – сложных кристаллических веществ с дефектной структурой.
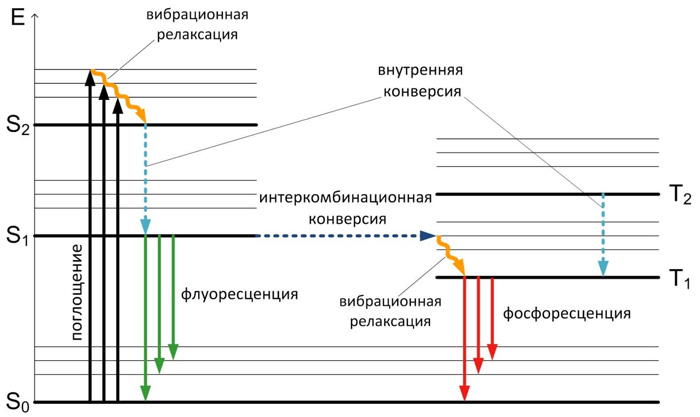
Поглощение и испускание света хорошо иллюстрирует диаграмма уровней энергии, предложенная Яблонским (Рисунок 2).
Рисунок 2. Диаграмма уровней энергии Яблонского
Основное, первое и второе электронные состояния обозначают S0, S1, и S2 соответственно.Каждый из этих уровней энергии может состоять из множества колебательных энергетических уровней, обозначаемых 0, 1, 2 и т. д. Влияние растворителя во внимание не принимается.
Переходы между различными электронными уровнями обозначены вертикальными линиями. Такое представление используется, чтобы наглядно показать мгновенную природу поглощения света. Этот процесс происходит примерно за 10-15 с, время, слишком короткое для заметного смещения ядер (принцип Франка-Кондона).
В возбуждённых состояниях молекулы находятся очень недолго (в синглетном состоянии обычно значительно меньше, чем в триплетном) и становятся очень реакционноспособными.
В соответствии с распределением Больцмана, при комнатной температуре большинство молекул находятся на самом нижнем колебательном уровне основного синглетного состояния S0. Именно такие молекулы преимущественно и будут поглощать излучение.
Из-за большой разности энергий между уровнями S0 и S1 по существу, ни у каких флуорофоров состояние S1 не может быть заселено термическим путем. Даже малое термически активированное заселение первого возбужденного колебательного состояния молекул можно зарегистрировать, используя различие спектров поглощения при разных температурах.
За поглощением света обычно следует несколько других процессов. Возбуждение флуорофора, как правило, происходит до некоторого высшего колебательного уровня состояний (S1 либо S2). 3а некоторыми редкими исключениями, для молекул в конденсированной фазе характерна быстрая релаксация на самый нижний колебательный уровень состояния S1. Этот процесс называется внутренней конверсией и происходит большей частью за 10-12 с. Поскольку типичные времена затухания флуоресценции близки к 10-8 с, внутренняя конверсия обычно полностью заканчивается до процесса испускания. Следовательно, испускание флуоресценции чаще всего осуществляется из термически равновесного возбужденного состояния.
Аналогично поглощению обратный переход электронов на самый нижний электронный уровень также приводит к колебательно возбужденному состоянию. Термическое равновесие достигается за время порядка 10-12 с. Интересным следствием из такого рассмотрения является то, что спектр поглощения молекулы отражает колебательную структуру возбужденных электронных состояний, а спектр испускания — колебательную структуру основного электронного состояния. В большинстве случаев электронное возбуждение не сильно изменяет расположение колебательных уровней энергии. В результате этого колебательные структуры, проявляющиеся в спектрах поглощения и испускания, сходны.
Молекулы в состоянии S1 могут также подвергаться конверсии в первое триплетное состояние Т1. Испускание из Т1 называемое фосфоресценцией, обычно сдвинуто в сторону больших длин волн (меньших энергий) по сравнению с флуоресценцией. Конверсия из S1 в Т1 называется интеркомбинационной конверсией. Переход из Т1 в основное состояние запрещен, в результате чего константа скорости такого испускания на несколько порядков меньше соответствующей константы для флуоресценции.
На испускание флуоресценции могут влиять и другие факторы, не показанные в явном на диаграмме Яблонского: влияние растворителей, релаксация растворителя, тушение, а также реакции, происходящие в возбужденных состояниях.
Люминесценция — один из видов излучения вещества, избыточного над тепловым излучением тела при данной температуре. Излучение наблюдается вследствие перехода электронно-возбужденных атомов, молекул, радикалов, ионов — так называемых центров люминесценции, в основное состояние. По длительности процесса излучения различают кратковременную люминесценцию, называемую флуоресценцией и медленную люминесценцию, называемую фосфоресценцией
В 1852 году Джордж Стокс установил, что длина волны фотолюминесценции больше длины волны возбуждающего света (правило Стокса). В 1864 году им предложено использование явления люминесценции для качественного анализа органических веществ. Широкое применение люминесцентные методы анализа получили в 30-е годы XX века благодаря работам Вавилова и его школы.
Процесс люминесценции может происходить в различных веществах, находящихся в разных агрегатных состояниях. Особенности излучения различных люминесцентных центров могут быть использованы в аналитических целях.
Для возбуждения люминесцентного центра могут быть использованы различные источники. Необходимым условием их эффективности является величина энергии излучения, которая должна быть достаточной для возбуждения электронного перехода в исследуемом веществе. Разные виды люминесценции находят применение в различных вариантах метода люминесцентного анализа.
Наиболее универсальный метод возбуждения люминесценции — фотовозбуждение исследуемого вещества. Он используется чаще всего как в атомных, так и в молекулярных методах анализа. При фотовозбуждении легко регулировать длину волны возбуждающего излучения, его интенсивность и поляризацию. При анализе многокомпонентной смеси возможно возбудить электронный переход, сопровождающийся люминесценцией только у одного из компонентов смеси. Таким образом, становится возможным проводить избирательный (селективный) анализ смеси веществ.
Наиболее широкое применение в аналитических целях имеет молекулярная фотолюминесценция для веществ, находящихся в растворе.
Извините, ничего не найдено.
studentoriy.ru
Общие сведения о люминесценции.
Люминесценция является одним из широко распространенных в природе видов излучения. Помимо люминесценции известны и другие свечения, которые, однако, существенно отличаются от нее, например, температурное излучение, свечения, наблюдаемые при быстром движении электрических зарядов (тормозное излучение, Свечение Вавилова Черенкова) и т. п.
Люминесценцией называют избыток излучения над температурным при условии, что избыточное излучение обладает конечной длительностью, превышающей период световых колебаний (~ 10-10 сек).
Это определение основано на противопоставлении люминесценции температурному излучению, свойства которого хорошо известны. Вместе с тем оно указывает на наличие у люминесценции конечной длительности послесвечения, превышающей период световых колебаний. Это условие позволяет отличать люминесценцию от отражения, рассеяния и излучения Вавилова-Черенкова, которые являются практически безынерционными.
Очень многие вещества обладают способностью люминесцировать. При этом они могут находиться в газообразном, жидком и твердом состояниях. Простейшими из них являются газы и пары различных элементов (О2, I2, Na2 и т. д.). Люминесцентными свойствами обладают соли некоторых веществ (редкоземельных элементов, ураниловых соединений), ароматические соединения (нафталин, бензол, антрацен, и производные и др.), растворы ряда красителей, а также многие другие вещества. Особый класс люминесцирующих соединений составляют так называемые кристаллофосфоры неорганические вещества (например. ZnS, CaS и др.), в кристаллическую решетку которых введены ионы тяжелых металлов (например, Ag, Cu, Mn и др.).
Для того чтобы вещество начало люминесцировать, к нему необходимо извне подвести определенное количество энергии. Тогда его частицы переходят в новое, более богатое энергией, возбужденное состояние, в котором они пребывают определенное время, после чего вновь возвращаются в невозбужденное состояние, отдавая при этом часть энергии возбуждения в виде квантов люминесценции.
Энергия возбуждения может быть подведена к веществу различными способами. В зависимости от метода возбуждения возникающее свечение получает различные названия. Так, при возбуждении свечения оптическими частотами оно носит название фотолюминесценции; свечение, возникающее под действием катодных лучей, называется катодолюминесценцией; при возбуждении веществ рентгеновыми лучами возникает рентгенолюминесценция; при облучении их лучами
радиоактивных элементов наблюдается радиолюминесценция; свечение, появляющееся при химических реакциях, получило название хемилюминесценции; свечение, возникающее под действием электрического поля, называется электролюминесценцией. Люминесценция может быть получена и с помощью других источников возбуждения.
Возникновение люминесценции и ряд ее свойств легко понять из схемы, изображенной на рис.1. Энергия молекулы складывается из электронной энергии, колебательной энергии ядер и энергии вращения. Все виды энергии квантованы, причем кванты энергии вращения гораздо меньше квантов электронной и колебательной энергии. На рис. 1 уровни 0" и 0 являются нижними колебательными энергетическими уровнями нормального I и воз-
бужденного II состояния молекулы. Состояние 0 отличается от 0" на квант электронной энергии, величина которого определяет расстояние по вертикали между уровнями 0" и 0. Каждому значению электронной энергии соответствует ряд возможных значений колебательной энергии молекулы. Если не учитывать энергию вращения, то возможные значения энергии молекулы для электронных состояний I и II характеризуются системой энергетических уровней 0" 4" и 0 4, положение последних определяется суммой электронной и колебательной энергии.
Распределение молекул по колебательным уровням как невозбужденного, так и возбужденного электронного состояния описывается
формулой Больцмана:
(1)
где N0 полное число всех молекул; Ni число молекул на уровне i; Еi значение колебательной энергии, соответствующее уровню i. Если при некоторой температуре Ei >> kT, то в соответствии с формулой (1) подавляющая часть молекул должна находиться на нулевом колебательном уровне. Для комнатной температуры это условие обычно выполняется, что позволяет считать, что в этом случае практически все молекулы находятся на нулевом уровне. Таким образом, по мере роста номера уровня число находящихся на нем молекул быстро убывает.
На рис. 1 поглощение световых квантов различной величины обозначено стрелками, идущими вверх, а излучение квантов люминесценции стрелками, направленными вниз. Длины стрелок пропорциональны величинам энергии поглощенных или излученных квантов h т. е. пропорциональны частотам соответствующих линий в спектрах поглощения или излучения. Из рис. 1 видно, что разности частот линий поглощения дают расстояния между колебательными уровнями верхнего электронного состояния; о строении нижнего электронного состояния можно судить по разностям частот линий излучения. Это открывает возможность анализа колебательных состояний молекул с помощью спектров люминесценции.
Оптические свойства люминесцирующих веществ описываются с помощью целого ряда характеристик. Сюда относятся сп
www.studsell.com
<span Arial",«sans-serif»">Общие сведения о люминесценции.
<span Arial",«sans-serif»">
<span Arial",«sans-serif»">Люминесценцияявляется одним из широко распространенных в природе видов излучения. Помимо люминесценцииизвестны и другие свечения, которые, однако, существенно отличаются от нее,например, температурное излучение, свечения, наблюдаемые при быстром движенииэлектрических зарядов (тормозное излучение, Свечение Вавилова — Черенкова) и т. п.
<span Arial",«sans-serif»">Люминесценциейназывают избыток излучения над температурным при условии, что избыточноеизлучение обладает конечной длительностью, превышающей период световых колебаний(~ 10-10 сек).
<span Arial",«sans-serif»">Этоопределение основано на противопоставлении люминесценции температурномуизлучению, свойства которого хорошо известны. Вместе с тем оно указывает наналичие у люминесценции конечной длительности послесвечения, превышающейпериод световых колебаний. Это условие позволяет отличать люминесценцию ототражения, рассеяния и излучения Вавилова-Черенкова, которые являются практическибезынерционными.
<span Arial",«sans-serif»">Очень многие веществаобладают способностью люминесцировать. При этом они могут находиться в газообразном,жидком и твердом состояниях. Простейшими из них являются газы и пары различныхэлементов (О2,
I2, Na2 и т. д.). Люминесцентнымисвойствами обладают соли некоторых веществ (редкоземельных элементов, ураниловыхсоединений), ароматические соединения (нафталин, бензол, антрацен, и производныеи др.), растворы ряда красителей, а также многие другие вещества. Особый класслюминесцирующих соединений составляют так называемые кристаллофосфоры — неорганические вещества (например. ZnS,CaS и др.), в кристаллическую решетку которых введены ионытяжелых металлов (например, Ag, Cu,Mn и др.).<span Arial",«sans-serif»">Для тогочтобы вещество начало люминесцировать, к нему необходимо извне подвестиопределенное количество энергии. Тогда его частицы переходят в новое, болеебогатое энергией, возбужденное состояние, в котором они пребывают определенное время, после чего вновь возвращаются в невозбужденное состояние, отдавая при этом часть энергии возбуждения в виде квантовлюминесценции.
<span Arial",«sans-serif»; color:black;letter-spacing:.05pt">Энергия возбуждения может быть подведена квеществу различ
ными способами. В зависимости от метода возбуждениявозникающее свечение получает различные названия. Так, при возбуждении свеченияоптическими частотами оно носит название фотолюминесценции; свечение, возникающее под действием катодных лучей,называется катодолюминесценцией; при возбуждении веществ рентгеновыми лучами возникает рентгенолюминесценция; при облучении ихлучами<span Arial",«sans-serif»; color:black;letter-spacing:-.05pt">
<span Arial",«sans-serif»;color:black; letter-spacing:-.05pt">радиоактив
ныхэлементов наблюдается радиолюминесценция;свечение, появляющеесяпри химических реакциях, получило название хемилюминесценции;свечение, возникающее под действием электрического поля,называется электролюминесценцией. Люминесценция может быть получена и с помощью других источников возбуждения.<span Arial",«sans-serif»; color:black;letter-spacing:-.15pt">Возникновение люминесценции и ряд еесвойств легко понять
из схемы, изображенной на рис.1. Энергия молекулы складывается из электронной энергии, колебательной энергии ядер и энергии вращения. Все виды энергии квантованы, причем кванты энергии вращения гораздо меньше квантов электронной и колебательной энергии. На рис. 1 уровни 0" и0' являются нижними колебательными энергетическими уровнями нормального I ивоз-<span Arial",«sans-serif»;color:black; letter-spacing:-.05pt">бужденного
II состояния молекулы. Состояние0' отличается от 0" на квант электронной энергии, величина которого определяет расстояние по вертикали междууровнями 0" и 0'. Каждомузначению электронной энергии соответствует ряд возможных значений колебательнойэнергии молекулы. Если не учитывать энергию вращения, то возможные значенияэнергии молекулы для электронных состояний I и IIхарактеризуются системой энергетических уровней 0" — 4" и 0'— 4', положение последних определяется суммой электронной и колебательной энергии.<span Arial",«sans-serif»; color:black">Распределение молекул по колебательным уровням как невозбужденного, так и возбужденного электронногосостояния описывается
<span Arial",«sans-serif»; color:black;letter-spacing:-.1pt">
<span Arial",«sans-serif»;color:black; letter-spacing:-.05pt">формулой Больцмана:
<span Arial",«sans-serif»;color:black; letter-spacing:-.05pt">
(1)<span Arial",«sans-serif»;mso-ansi-language: EN-US">
<span Arial",«sans-serif»;color:black; letter-spacing:-.05pt">где
N0 — полноечисло всех молекул; Ni — число молекул на уровне i; Еi — значениеколебательной энергии, соответствующее уровню i. Если при некоторой температуреEi >> kT, то в соответствии с формулой (1) подавляющая часть молекул должна находиться на нулевомколебательном уровне. Для комнатной температуры это условие обычновыполняется, что позволяет считать, что в этом случае практически все молекулынаходятся на нулевом уровне. Таким образом, по мере роста номера уровня числонаходящихся на нем молекул быстро убывает.<span Arial",«sans-serif»">На рис.1 поглощение световых квантов различной величины обозначено стрелками, идущимивверх, а излучение квантов люминесценции — стрелками, направленными вниз.Длины стрелок пропорциональны величинам энергии поглощенных или излученныхквантов
hnт. е. пропорциональны частотам соответствующих линий в спектрах поглощения илиизлучения. Из рис. 1 видно, что разности частот линий поглощения даютрасстояния между колебательными уровнями верхнего электронного состояния; остроении нижнего электронного состояния можно судить по разностям частот линий излучения. Это открывает возможностьанализа колебательных состояний молекул с помощью спектров люминесценции.<span Arial",«sans-serif»">Оптическиесвойства люминесцирующих веществ описываются с помощью целого рядахарактеристик. Сюда относятся спектры поглощения и люминесценции, поляризациясвечения (и поляризационные спектры), выход люминесценции, длительностьвозбужденного состояния молекул, закон затухания свечения и кривые термическоговысвечивания.
<span Arial",«sans-serif»">Спектры поглощения.
<span Arial",«sans-serif»">Спектромпоглощения вещества называется совокупность коэффициентов поглощения,характеризующих его поглощательную способность к лучам оптического диапазоначастот. Коэффициенты поглощения определяются из закона Ламберта—Бера.
<span Arial",«sans-serif»">Спектрыпоглощения люминесцирующих веществ крайне разнообразны. Одни из них имеют видочень узких полос (растворы солей редкоземельных элементов), другие — более широкихполос с четко выраженной колебательной структурой(растворы ураниловых солей), наконец, спектры поглощения многих веществ представляютсобой широкие размытые полосы, структуру которых не удается выяснить даже принизких температурах (растворы красителей).
<span Arial",«sans-serif»; color:black">Спектры поглощения могутсущественно меняться при изменении концентрации раствора, его кислотности или щелочности (величины его рН), природы растворителя, температуры и ряда других факторов.
<span Arial",«sans-serif»;color:black">Спектрылюминесценции.
<span Arial",«sans-serif»; color:black">Спектром люминесценции называется распределение излучаемойвеществом энергии по частотам или длинам волн. Подобно спектрам поглощения,интенсивность и форма спектров люминесценции у разных веществ могут бытьвесьма различными, и они могут существенно изменяться при вариации тех жепараметров (концентрации, величины
pH раствораи т. д.)<span Arial",«sans-serif»">Выход люминесценции.
<span Arial",«sans-serif»"> Выход люминесценции характеризуетэффективность трансформации возбуждающего света в свет люминесценции висследуемом веществе. Различают энергетический и квантовый выходы люминесценции.Энергетическим выходом люминесценцииназывают отношение излучаемой веществом энергии
Eл к поглощеннойэнергии возбуждения Еп:<span Arial",«sans-serif»"> <img src="/cache/referats/22395/image004.gif" v:shapes="_x0000_i1026"> (2)
<span Arial",«sans-serif»">Квантовымвыходом люминесценции называют отношение числа квантов люминесценции,излученных веществом
Nл к числу поглощенныхквантов возбуждающего света Nп:<span Arial",«sans-serif»"> <img src="/cache/referats/22395/image006.gif" v:shapes="_x0000_i1027"> (3)
<span Arial",«sans-serif»">Выходлюминесценции очень чувствителен к внешним воздействиям, которые во многихслучаях приводят к тушению свечения. Так, известно тушение люминесценциипосторонними примесями, возникающее при добавлении к раствору постороннихвеществ — тушителей. Тушителями могут служить
KI,анилин и другие вещества. В результате взаимодействия возбужденных молекуллюминесцентного вещества с молекулами тушителя возникает безизлучательный разменэнергии возбуждения. Безизлучательные переходы развиваются и при увеличениитемпературы раствора, обуславливая появление температурного тушения.<span Arial",«sans-serif»">Вбольшинстве случаев увеличение концентрации также приводит к тушению свечения.При этом концентрационное тушение обычно начинает проявляться лишь придостижении некоторой пороговой концентрации, величина которой характерна дляисследуемого вещества. В более разведенных растворах выход люминесценции независит от концентрации. Это обстоятельство может быть использовано в люминесцентноманализе при подборе оптимальных условий его проведения.
<span Arial",«sans-serif»">Концентрационноетушение имеет двоякую природу. С одной стороны, при увеличении концентрациимогут образовываться ассоциированные молекулы, не обладающие люминесцентнойспособностью, но поглощающие энергию возбуждения. С другой стороны, междувозбужденными и невозбужденными молекулами может осуществляться индукционныйперенос, или, как говорят, миграция энергии возбуждения. Такой перенос энергиивозбуждения прежде всего на нелюминесцентные ассоциаты приводит к развитиюконцентрационного тушения.
<span Arial",«sans-serif»">Известныи другие виды тушения (тушение растворителем, тушение электролитами, тушениепри диссоциации и ионизации молекул и т. д.). При проведении люминесцентногоанализа интенсивность свечения играет очень большую роль. Поэтому учет тушения,изменяющего интенсивность люминесценции и затрудняющего анализ, является крайневажным.
<span Arial",«sans-serif»">Закон затухания люминесценции.
<span Arial",«sans-serif»">Законзатухания свечения после прекращения возбуждения может быть различным у разныхвеществ, что часто позволяет по нему определять природу и кинетику свечения; вместе с тем он может служить ианалитической характеристикой. Закон затухания свечения растворов имолекулярных кристаллов обычно достаточно хорошо выражается экспоненциальной зависимостью
<span Arial",«sans-serif»">
<span Arial",«sans-serif»"> <img src="/cache/referats/22395/image008.gif" v:shapes="_x0000_i1028"> (4).
<span Arial",«sans-serif»"> где
I — интенсивностьсвечения в момент времени t; I0— интенсивность свечения вмомент прекращения возбуждения; t — средняядлительность возбужденного состояния (время, в течение которого интенсивностьсвечения уменьшается в е раз, т. е. в 2,7 раза). В других случаях затуханиесвечения может происходить по более сложному закону. Так, например, затуханиесвечения кристаллофосфоров хорошо описывается эмпирической формулой<span Arial",«sans-serif»"> <img src="/cache/referats/22395/image010.gif" v:shapes="_x0000_i1029"> (5)
<span Arial",«sans-serif»">где
A,b, a — постоянные, причемобычно a<span Arial",«sans-serif»">Длительность возбужденного состояния молекул.
<span Arial",«sans-serif»">Послепрекращения возбуждения свечение не исчезает мгновенно, а продолжается определенный промежуток времени.Длительность возбужденного состояния у разных соединений может существенноразличаться. Она характерна для каждого вещества и является его важнойоптической характеристикой. Так, для растворов обычно
t~10-8—10-9сек. Затухание свечения кристаллофосфоров протекает по сложным законам и можетпродолжаться секунды, минуты и даже часы.<span Arial",«sans-serif»">Такимобразом, у жидких растворов
t очень невелико и ихлюминесценция затухает практически мгновенно. Такие свечения часто называют флуоресценцией. При введении тех жевеществ в очень вязкие среды (в желатину, сахарные леденцы и т. д.), а такжепри замораживании растворов возникает длительное свечение, продолжающееся долисекунды и даже целые секунды. Свечение такого вида называют замедленной флуоресценцией, или фосфоресценцией. Известны два видазамедленной флуоресценции: при одном спектр свечения совпадает со спектромфлуоресценции (a-процесс), при второмнаблюдается резко отличный спектр свечения, сдвинутый в сторону длинных волн (b-процесс).<span Arial",«sans-serif»">Замедленнаяфлуоресценция обусловлена попаданием возбужденных молекул на энергетическиеуровни, непосредственный переход с которых в невозбужденное состояние неразрешен. Эти уровни называются метастабильными; молекула может их покинутьлишь под влиянием внешних воздействий (например, при нагревании). Возбужденныемолекулы пребывают на метастабильных уровнях значительное время, вызываяувеличение длительности послесвечения.
<span Arial",«sans-serif»">Присложном законе затухания (например, (5)) понятие средней длительности возбужденногосостояния
t уже неприменимо. В этом случае дляхарактеристики длительности послесвечения обычно принимают время, в течениекоторого интенсивность свечения исследуемого образца уменьшается в определенноечисло раз (в 100—1000 раз).<span Arial",«sans-serif»">Кривые термического высвечивания.
<span Arial",«sans-serif»">У многихвеществ (кристаллофосфоров, минералов, кварца и др.), предварительновозбужденных ультрафиолетовой, рентгеновской или радиоактивной радиацией, принагревании возникает свечение, получившее название термолюминесценции. Оно наблюдаетсяпри температурах, значительно меньших тех, при которых появляется видимоетемпературное излучение.
<span Arial",«sans-serif»">Термолюминесценцияимеет следующее происхождение. Под действием возбуждающей радиации электроныотрываются от ионов облучаемого вещества; часть их непосредственнорекомбинирует с ионизованными центрами, что приводит к возникновению кратковременногосвечения кристаллофосфоров; другая часть электронов задерживается вблизи местнарушения периодичности кристаллической решетки — на уровнях локализации. Освобождениеэлектронов с мест локализации происходит за счет тепловой энергии. Их последующаярекомбинация с ионизованными центрами вызывает длительное свечениекристаллофосфоров.
<span Arial",«sans-serif»">Уровнилокализации могут иметь различную энергетическую глубину, т. е. могут удерживатьэлектроны с различной силой. Мелкие уровни освобождаются уже при температурежидкого азота, глубокие — при +300, +400°С. При постепенном нагреваниипредварительно возбужденного фосфора последовательно освобождаются уровниразной глубины, и интенсивность термолюминесценции то увеличивается, тоуменьшается. Кривые, характеризующие зависимость яркости свечения фосфора оттемпературы, получили название кривых термического высвечивания. Они являютсяважной характеристикой кристаллофосфоров и могут быть использованы для аналитическихцелей.
<span Arial",«sans-serif»">
<span Arial",«sans-serif»">Основные закономерности свечения, используемые в люминесцентноманализе.
<span Arial",«sans-serif»">
<span Arial",«sans-serif»">Закон независимости спектра люминесценции от длины
<span Arial",«sans-serif»">волны возбуждающего света.
<span Arial",«sans-serif»">
При возбуждении свечения различнымидлинами волн молекулы вещества, поглощая кванты разной величины, попадают наразличные колебательные уровни возбужденного электронного состояния. Поэтомуможно ожидать, что спектр люминесценции будет зависеть от длины волнывозбуждающего света. Однако оказалось, что каждое вещество в конденсированномсостоянии имеет совершенно определенный спектр люминесценции, который нечувствителен к изменению длины волны возбуждающего света.<span Arial",«sans-serif»">Этообъясняется тем, что молекулы, перешедшие в результате возбуждения на различныеколебательные уровни возбужденного состояния (рис. 1), успевают за время, многоменьшее, чем средняя длительность возбужденного состояния
t,растратить часть колебательной энергии и образовать систему возбужденных молекул,обладающих равновесным распределением колебательной энергии, определяемым температурой.Из этих вполне определенных для данной температуры состояний и происходятпереходы молекул в невозбужденное состояние, сопровождающиеся излучением. Поэтомуна опыте всегда наблюдается один и гот же спектр люминесценции, не зависящий отдлины волны возбуждающего света.<span Arial",«sans-serif»">Независимостьспектра люминесценции от длины волны возбуждающего света позволяет на практикепользоваться для возбуждения широкими спектральными участками. При отсутствиивторичного поглощения оказывается возможным не обращать внимания на составвозбуждающего света, что очень сильно облегчает проведение анализа.
<span Arial",«sans-serif»">Закон Стокса—Ломмеля.
<span Arial",«sans-serif»">Стоксомбыло сформулировано правило, согласно которому свет люминесценции всегда имеетбольшую длину волны по сравнению со светом, применявшимся для возбуждения.Однако во многих случаях правило Стокса не выполняется. Спектры поглощения илюминесценции многих веществ частично накладываются друг на друга. Если длявозбуждения взять частоту (например,
n = 530·10-12сек-1), находящуюся в области наложения спектров, то согласноправилу Стокса должна появляться лишь та часть спектра люминесценции, котораярасположена по левую сторону от выбранной частоты. Однако в соответствии сзаконом независимости спектра люминесценции от возбуждающей длины волны вбольшинстве случаев наблюдается полный спектр люминесценции, имеющий целый рядчастот, превышающих частоту возбуждающего света (заштрихованная область). Такимобразом, правило Стокса нарушается. Часть спектра люминесценции, состоящая излучей с частотами, большими частоты возбуждающего света, называется антистоксовской. Ее возникновение можнообъяснить наличием у излучающих молекул помимо энергии возбуждения ещеопределенного запаса колебательной энергии. Сумма энергий возбуждающего и колебательногоквантов позволяет получать большие кванты люминесценции, обусловливающиепоявление антистоксовской части спектра. Ломмель уточнил правило Стокса,предложив для него следующую формулировку: спектр излучения в целом и егомаксимум всегда сдвинуты по сравнению со спектром поглощения и его максимумом всторону длинных волн. Закон Стокса—Ломмеля строго выполняется для очень широкогокруга веществ.<span Arial",«sans-serif»">Сдвигспектров люминесценции относительно спектров поглощения дает возможность болееили менее просто отфильтровывать рассеянную часть возбуждающего света,примешивающегося к люминесценции. Это обстоятельство широко используется впрактике люминесцентного анализа.
<span Arial",«sans-serif»">Закон Вавилова.
<span Arial",«sans-serif»">С. И.Вавиловым установлено, что энергетический выход люминесценции растет пропорциональнодлине волны возбуждающего света, затем в некотором спектральном интервале оностается постоянным, после чего в области наложения спектров поглощения илюминесценции начинает быстро падать. Падение энергетического выхода свеченияпроисходит в антистоксовской части спектра.
<span Arial",«sans-serif»">Легкопоказать, что пропорциональность энергетического выхода длине волнывозбуждающего света соответствует постоянству квантового выхода в той же спектральнойобласти, где в излучение всегда переходит одна и та же доля возбуждающих световых квантов. С. И. Вавилов дал своему закону формулировку, согласно которойлюминесценция может сохранять постоянный квантовый выход, если возбуждающаяволна преобразуется в среднем в более длинную, чем она сама. Наоборот, выход люминесценциирезко уменьшается при обратном преобразовании длинных волн в короткие. Закон Вавилова широкоиспользуется в люминесцентном анализе при подборе оптимальных условий проведенияопыта.
<span Arial",«sans-serif»">Правило зеркальной симметрии спектров поглощения и
<span Arial",«sans-serif»"> люминесценции.
<span Arial",«sans-serif»">Дляширокого круга веществ (растворов красителей, ряда ароматических и многихдругих соединений) выполняется установленное В. Л. Левшиным правило зеркальнойсимметрии спектров поглощения и излучения, согласно которому спектры поглощенияи люминесценции, изображенные в функции частот, оказываются зеркально-симметричнымиотносительно прямой, проходящей перпендикулярно оси частот через точкупересечения обоих спектров, т. е.
<span Arial",«sans-serif»"> <img src="/cache/referats/22395/image012.gif" v:shapes="_x0000_i1030"> (6)
<span Arial",«sans-serif»">или
<span Arial",«sans-serif»"> <img src="/cache/referats/22395/image014.gif" v:shapes="_x0000_i1031"> (7)
<span Arial",«sans-serif»">Здесь
nП—частота поглощаемого света; nЛ — симметричная частоталюминесценции; n0 — частота линиисимметрии. При этом по оси ординат для спектров поглощения откладываютсякоэффициенты поглощения a, а для спектровлюминесценции — квантовые интенсивности IКВ=I/n.<span Arial",«sans-serif»">Изуравнения (9) видно, что при наличии зеркальной симметрии
Dn=nП- nЛ, и nП связаны линейнойзависимостью. Если откладывать по оси абсцисс nП, а по оси ординат Dn, то при строгомвыполнении правила должна получиться прямая линия.<span Arial",«sans-serif»">Дляосуществления зеркальной симметрии необходимо выполнение двух условий —зеркальной симметрии частот и зеркальной симметрии интенсивностей поглощения илюминесценции в соответствующих частях спектра.
<span Arial",«sans-serif»">Дляосуществления симметрии частот необходимо, чтобы энергетические уровнивозбужденного и невозбужденного состояний были построены одинаково. Для наличиязеркальной симметрии интенсивностей необходимо, чтобы распределение молекул поэнергетическим уровням верхней и нижней систем было одинаковым и чтобывероятности соответствующих излучательных и поглощательных переходов были равны,или пропорциональны друг другу. Эти условия выполняются лишь у части молекул. Увеществ, следующих правилу зеркальной симметрии, можно по одному из спектров(люминесценции или поглощения) без измерений установить форму другого. Отступленияот правила зеркальной симметрии могут быть использованы для установления величиныотклонений от условий его выполнения.
<span Arial",«sans-serif»">Правилозеркальной симметрии оказывается весьма полезным при проведении люминесцентногоанализа, а также при расшифровке спектров и установлении энергетических уровнейисследуемых молекул.
<span Arial",«sans-serif»">
<span Arial",«sans-serif»">Виды люминесцентного анализа и характеристика его особенностей.
<span Arial",«sans-serif»">
<span Arial",«sans-serif»">Люминесцентным анализом
называетсяобнаружение и исследование различных объектов с помощью явлений люминесценции.Наиболее важной задачей люминесцентного анализа является определениехимического состава исследуемых веществ и установление процентного содержания вних отдельных компонентов. Анализ такого вида носит соответственно название качественного и количественного химическоголюминесцентного анализа.<span Arial",«sans-serif»">Качественныйхимический люминесцентный анализ основан на том, что люминесцентные свойстваявляются характерным признаком излучающего вещества, тесно связанным с его составом,общим состоянием и структурой его молекул.
<span Arial",«sans-serif»">Количественныйхимический люминесцентный анализ основан на использовании определеннойзависимости между интенсивностью люминесценции и концентрацией люминесцентноговещества. В большинстве случаев условия анализа подбираются так, чтобы осуществляласьпропорциональность между интенсивностью свечения и концентрацией вещества.Однако такая зависимость имеет место лишь в случаях, когда концентрацииневелики. При высоких концентрациях определяемого вещества для осуществленияанализа приходится тем или иным способом учитывать сложную зависимость интенсивностисвечения от концентрации.
<span Arial",«sans-serif»">Клюминесцентному анализу относится также изучение структуры и колебательныхчастот молекул по спектрам излучения, создающее фундамент для качественноголюминесцентного анализа.
<span Arial",«sans-serif»">Чистохимические задачи не исчерпывают возможностей люминесцентного анализа. С егопомощью можно обнаруживать и выявлять различные объекты и их детали, изучение которыхоказывается невозможным при обычных условиях наблюдения и освещения. Люминесцентныйанализ такого рода получил название люминесцентногоанализа обнаружения или сортовоголюминесцентного анализа.
<span Arial",«sans-serif»">Люминесцентныйанализ обладает рядом особенностей, которые отличают его от всех других видованализа. Люминесцентный анализ необычайно чувствителен. С его помощью можнообнаружить в пробе присутствие вещества с концентрацией ~10-10 – 10-11г/г. Это более чем на три порядка превосходит чувствительность эмиссионногоспектрального анализа, что позволяет работать с исчезающе малыми количествамиисследуемого вещества ~10-12 – 10-15 г. С помощью люминесцентного анализа можноисследовать очень небольшие объемы раствора, а также анализировать мельчайшиекрупинки порошков, в которых содержатся следы других люминесцирующих веществ.
<span Arial",«sans-serif»">Важным преимуществом люминесцентного анализа являются его простота и скорость, во много раз превосходящие скорость химическогоанализа.
<span Arial",«sans-serif»">В товремя как при химическом и эмиссионном спектральном анализе анализируемыевещества разлагаются, при люминесцентном анализе они, как правило, неподвергаются изменениям и их можно использовать в дальнейшей работе. Этопреимущество люминесцентного анализа особенно существенно при исследованиитрудно синтезируемых уникальных веществ, получаемых в ничтожных количествах. Вотдельных случаях возбуждения люминесценции коротковолновыми ультрафиолетовымилучами в веществе могут происходить фотохимические превращения. Однакосоответствующим подбором условий опыта эти трудности обычно могут быть обойдены.
<span Arial",«sans-serif»">Перечисленныесвойства люминесцентного анализа дают представление о его исключительныхвозможностях, в определенных отношениях значительно превосходящих возможностидругих видов анализа. Однако следует отметить, что необычайно высокая чувствительностьлюминесцентного анализа одновременно создает и серьезные трудности егопроведения, существенно ограничивая области его применения. Присутствие вобразце даже ничтожных количеств люминесцирующих примесей обусловливаетпоявление нового свечения, которое накладывается на люминесценцию основного вещества,искажая как спектральный состав, так и интенсивность его излучения. Поэтомузначительные успехи в применении люминесцентного анализа могли быть достигнутылишь на основе всестороннего развития учения о люминесценции в целом, послетого как были установлены общие законы свечения и накоплен большой материал олюминесцентных свойствах различных классов соединений.
<span Arial",«sans-serif»">Наиболеераспространенным и хорошо разработанным является люминесцентный анализ,основанный на возбуждении фотолюминесценции. При анализе кристаллических неорганическихвеществ (минералов, алмазов и др.) применяют катодное и рентгеновскоевозбуждения. В отдельных случаях в аналитических целях используют явленияхемилюминесценции и радиолюминесценции.
<span Arial",«sans-serif»">
<span Arial",«sans-serif»">
www.ronl.ru
Введение 3
1. Теоретические основы люминесцентного метода анализа 4
1.1 Классификация методов 4
1.2 Качественный и количественный анализ 7
1.3 Приборы для анализа 12
2. Люминесцентное определение количества растительных жиров в молочных продуктах 14
2.1 Люминесцентные методы контроля состава молока 17
2.2 Исследование молочных продуктов отечественных и зарубежных производителей 19
2.3 Люминесцентный анализ маргарина 24
Заключение 26
Список литературы 27
Содержание
Таким образом, приборы, реализующие люминесцентный метод определения состава молока, характеризуются высокой точностью, невозмущающим исследуемый образец действием, не требуют использования химреактивов и могут быть использованы в производственных условиях.
2.2 Исследование молочных продуктов отечественных и зарубежных производителей
Физико-химические методы исследования масел и жиров основаны на определении физических и химических констант (точка плавления, удельный вес, число Рейхерта — Мейсля, число омыления).
Эти методы трудоемки, длительны и требуют специальных реактивов. Для установления этих показателей необходимо наличие довольно большого количества жира, которое невозможно иногда получить, например, при исследовании гарниров и кремов.
Известно, что растительные жиры и молочные жиры обладают способностью люминесцировать под влиянием возбуждающих факторов, причем молочный жир и растительные жиры имеют различный цвет люминесценции [1].
Различаются так же и показатели преломления растительных жиров и молочного жира. Поэтому были проведены исследования по применению этих двух методов для определения соотношения фракций молочного и растительного жиров на примере модельных жировых композиций молочный жир — растительный жир и сухие растительные сливки — сухое обезжиренное молоко.
В качестве растительного компонента использовался растительный жир «Союз-71», который представляет собой смесь пальмового, кокосового и соевого растительных жиров.
Результаты исследования модельных композиций представлены в таблице 1 и на рисунке 5.
Из таблицы 1 и рисунка 5 следует, что при увеличении процентного содержания растительного жира в модельных композициях — растительный жир — молочный жир от
10. до 90%, показатель преломления увеличивался с 1,4604 до 1,4658; цвет люминесценции изменяется от желтого (молочный жир) до интенсивно-голубого (растительный жир).
Увеличение значения показателя преломления объясняется снижением содержания насыщенных низкомолекулярных кислот, входящих в состав молочного жира, и увеличением ненасыщенных жирных кислот, входящих в состав растительного жира, в модельных композициях.
Таблица
1. Исследование модельных композиций молочный жир — жир «Союз-71»
Состав образца Коэффициент преломления Цвет люминесценции Молочный жир 1,4604 Желтый
10. «Союз-71"+90% молочный жир 1,4606 Бледно-желтый
20. «Союз-71"+80%молочный жир 1,4614 Бледно-голубой
40. «Союз-71"+60%молочный жир 1,4624 Голубой
80. «Союз-71"+20%молочный жир 1,4638 Интенсивно-голубой
80. «Союз-71"+20%молочный жир 1,4648 Интенсивно-голубой
90. «Союз-71"+10%молочный жир 1,4658 Интенсивно-голубой Жир «Союз-71» 1,4664 Интенсивно-голубой
Рис.
5. Исследование модельных композиций «Молочный жир — жир «Союз 71»
Использование рефрактометрического метода позволит определить массовую долю молочного жира в составе жировых продуктов (например — спредов), которое регламентируется нормативной документацией. Для этого необходимо определить значение показателя преломления спреда, и по предварительно построенному градуировочному графику найти массовую долю молочного жира. Построение градуировочного графика необходимо проводить не реже двух раз в год в зимний и летний периоды, а также при поступлении новых видов растительных жиров на предприятие.
При исследовании методом люминесценции модельных композиций сухих молочных смесей, составленных из растительных сливок и сухого обезжиренного молока, цвет люминесценции так же менялся в зависимости от процентного содержания растительных сливок от желтого (10% растительных сливок) до интенсивно голубого (от
50. до 100% растительных сливок).
Исследованы несколько образцов сухих молочных продуктов методом люминесценции. Результаты представлены в таблице 6.
Таблица
6. Исследование молочных продуктов отечественных и зарубежных производителей
№ образца Наименование
продукта, страна
изготовитель Цвет люминесценции 1 Сухое цельное молоко (Россия, Новогрузский МКК) Желтый; свечение однородное 2 Сухое цельное молоко (Россия, р.п. Полтавка) Желтый; свечение однородное 3 «СОПЬЮ КРИМА» (Корея) Голубой; свечение неоднородное 4 «Виэль Люкс» (Россия) Голубой; свечение неоднородное 5 «Золотое молоко» (Корея), Голубой; свечение неоднородное 6 «NEW MILKY EXTRA» (Корея) Голубой; свечение однородное 7 Сливки сухие немолочные (Россия) Голубой; свечение однородное
6. желтое однородное свечение свидетельствует об отсутствии в образцах растительных жиров, неоднородное голубое свечение свидетельствует о комбинированном жировом составе, однородное голубое свечение свидетельствует о том, что жировая фаза данного образца представлена жирами растительного происхождения.
Проведено исследование образцов сливочного масла «Крестьянского», выработанного разными производителями Омской области и другими регионами, люминесцентным методом. Исследования показали, что в трех из семи образцов масла было обнаружено присутствие растительных жиров.
Маргарин — это высококачественный эмульсионный жировой продукт, на основе растительных масел и животных жиров в натуральном и переработанном виде с добавлением различных компонентов. Маргарин представляет собой высокодисперсную эмульсию жира и воды, что, наряду с высокой температурой плавления, определяет его высокую усвояемость — 94%. Биологическая ценность обусловливается содержанием полиненасыщенных жирных кислот, фосфатидов, витаминов [4].
Маргарин относится к числу скоропортящихся продуктов, поэтому при хранении и транспортировке, особенно в не-благоприятных условиях, его химический состав более или менее сильно изменяется. При повышенной температуре, доступе воздуха, солнечного света жировая основа маргарина портится, прогоркает. Изменение и порча маргарина может в этих условиях протекать по двум направлениям: за счет окисления с нарастанием перекисного числа и за счет гидролиза жира с нарастанием только кислотного числа. Может изменяться также твердость маргарина, что связано с рекристаллизацией жировой основы или тиксотропными превращениями.
Нежировая часть маргарина довольно легко поражается плесенями и другими микроорганизмами, что сопровождается порчей маргарина.
Устойчивость маргарина при хранении зависит от ряда факторов, в частности, от состава жировой смеси, характера и дисперсности эмульсии, режима ее охлаждения, пластической обработки, плотности упаковки.
Данные спектрального анализа позволили определить присутствие в составе маргарина молочного ненасыщенных жирных кислот.
Максимумы при
27. нм отвечают линоленовой кислоте. Эта кислота является жизненно необходимой для человеческого организма. Линоленовая кислота, самая активная из omega-6 кислот, превращается в простагландин Е
1. Это вещество усиливает иммунитет, снижает риск сердечно-сосудистых заболеваний, уменьшает воспалительные процессы, регулирует работу мозга и нервной системы, нормализует уровень инсулина, ускоряет обмен веществ и способствует похудению. Из рисунка 6 видно, что с течением времени её количество снижается, что связано с процессами окисления маргарина.
Рис.
6. Рис. 2. Электронные спектры поглощения маргарина молочного до (1) и после (2) 30 суток хранения
Спектральный анализ в видимой области спектра проводили для обнаружения каротиноидов, которые вводятся в состав маргарина согласно рецептуре. Каротиноиды имеют три четких максимума в области 440−490 см-1 [1].
Как видно из рисунка 6 каротиноиды присутствуют в исследуемых образцах маргарина, но их содержание уменьшается с увеличением сроков хранения, что понижает пищевую ценность маргарина.
В заключение следует отметить, что с момента открытия спонтанного сверхслабого свечения растений Л. Колли (1954) и тканей органов животных Б. Н. Тарусовым (1961) задачи практического применения люминесцентных методов претерпели значительные изменения. На начальных этапах использования сверхслабого свечения в биологии многих ученых привлекало спонтанное свечение различных биообъектов.
Соответственно, основным требованием к люминометрам была высокая чувствительность прибора. С развитием представлений о механизме биохемилюминесценции стало очевидным, что практически невозможно учесть или количественно оценить вклад всех факторов в спонтанное свечение. Наряду с этим накапливалась информация об индукторах люминесценции и количественной зависимости эмиссии света в хемилюминесцентных реакциях от концентрации реагирующих веществ. Наиболее изучена в настоящее время индуцированная люминесценция, электролюминесценция и др., с помощью которой стало возможным не только изучать, но и моделировать окислительно-восстановительные процессы, происходящие в биологических объектах, по изменению интенсивности свечения в процессе реакции.
Благодаря экспрессности, чувствительности, возможности автоматизации измерения и компьютерной обработке полученных результатов люминесцентные методы находят все более широкое применение для решения практических задач в биологии, медицине и пищевой промышленности.
Донченко Л.В. Безопасность пищевой продукции: Учебник. / Л.В. Донченко, В.Д. Надытка. — 2-е изд. — М.: Дели принт, 2005. — 348 с.
Нечаев А.П. Пищевая химия / А.П. Нечаев. — СПб.: ГИОРД, 2001. — 592 с.
Барашков Н.И. Люминесцентный анализ на службе здоровья / Н.И. Барашков. — М.: Наука, 1985. — 95 с.
Кириллов В.В. Современные спектральные методы анализа, используемые в пищевой промышленности / В.В. Кирилов. — СПб.: СПбГУНиПТ, 2006. — 99 с.
2
Рис. 1 Энергетическая модель люминесценции
г
д
а
б
в
г
Ен - основное (нормальное)
энергетическое состояние
Ев - возбуждённое
энергетическое состояние
2 подуровни
1 основного уровня
0
Ев 0 (Ев 1 (Ев 2
Рис. 2 Спектры поглощения (1)
и флюоресценции (2)
Рис. 3. Зависимость интенсивности флюоресценции от концентрации флюоресцирующего вещества
а)
б)
Рис. 4 Влияние длины волны возбуждающего излучения на выход (а) и интенсивность (б) флюоресценции.
1. Донченко Л.В. Безопасность пищевой продукции: Учебник. / Л.В. Донченко, В.Д. Надытка. — 2-е изд. — М.: Дели принт, 2005. — 348 с.
2. Нечаев А.П. Пищевая химия / А.П. Нечаев. — СПб.: ГИОРД, 2001. — 592 с.
3. Барашков Н.И. Люминесцентный анализ на службе здоровья / Н.И. Барашков. — М.: Наука, 1985. — 95 с.
4. Кириллов В.В. Современные спектральные методы анализа, используемые в пищевой промышленности / В.В. Кирилов. — СПб.: СПбГУНиПТ, 2006. — 99 с.
список литературы
referatbooks.ru
<span Arial",«sans-serif»">Общие сведения о люминесценции.
<span Arial",«sans-serif»">
<span Arial",«sans-serif»">Люминесценцияявляется одним из широко распространенных в природе видов излучения. Помимо люминесценцииизвестны и другие свечения, которые, однако, существенно отличаются от нее,например, температурное излучение, свечения, наблюдаемые при быстром движенииэлектрических зарядов (тормозное излучение, Свечение Вавилова — Черенкова) и т. п.
<span Arial",«sans-serif»">Люминесценциейназывают избыток излучения над температурным при условии, что избыточноеизлучение обладает конечной длительностью, превышающей период световых колебаний(~ 10-10 сек).
<span Arial",«sans-serif»">Этоопределение основано на противопоставлении люминесценции температурномуизлучению, свойства которого хорошо известны. Вместе с тем оно указывает наналичие у люминесценции конечной длительности послесвечения, превышающейпериод световых колебаний. Это условие позволяет отличать люминесценцию ототражения, рассеяния и излучения Вавилова-Черенкова, которые являются практическибезынерционными.
<span Arial",«sans-serif»">Очень многие веществаобладают способностью люминесцировать. При этом они могут находиться в газообразном,жидком и твердом состояниях. Простейшими из них являются газы и пары различныхэлементов (О2,
I2, Na2 и т. д.). Люминесцентнымисвойствами обладают соли некоторых веществ (редкоземельных элементов, ураниловыхсоединений), ароматические соединения (нафталин, бензол, антрацен, и производныеи др.), растворы ряда красителей, а также многие другие вещества. Особый класслюминесцирующих соединений составляют так называемые кристаллофосфоры — неорганические вещества (например. ZnS,CaS и др.), в кристаллическую решетку которых введены ионытяжелых металлов (например, Ag, Cu,Mn и др.).<span Arial",«sans-serif»">Для тогочтобы вещество начало люминесцировать, к нему необходимо извне подвестиопределенное количество энергии. Тогда его частицы переходят в новое, болеебогатое энергией, возбужденное состояние, в котором они пребывают определенное время, после чего вновь возвращаются в невозбужденное состояние, отдавая при этом часть энергии возбуждения в виде квантовлюминесценции.
<span Arial",«sans-serif»; color:black;letter-spacing:.05pt">Энергия возбуждения может быть подведена квеществу различ
ными способами. В зависимости от метода возбуждениявозникающее свечение получает различные названия. Так, при возбуждении свеченияоптическими частотами оно носит название фотолюминесценции; свечение, возникающее под действием катодных лучей,называется катодолюминесценцией; при возбуждении веществ рентгеновыми лучами возникает рентгенолюминесценция; при облучении ихлучами<span Arial",«sans-serif»; color:black;letter-spacing:-.05pt">
<span Arial",«sans-serif»;color:black; letter-spacing:-.05pt">радиоактив
ныхэлементов наблюдается радиолюминесценция;свечение, появляющеесяпри химических реакциях, получило название хемилюминесценции;свечение, возникающее под действием электрического поля,называется электролюминесценцией. Люминесценция может быть получена и с помощью других источников возбуждения.<span Arial",«sans-serif»; color:black;letter-spacing:-.15pt">Возникновение люминесценции и ряд еесвойств легко понять
из схемы, изображенной на рис.1. Энергия молекулы складывается из электронной энергии, колебательной энергии ядер и энергии вращения. Все виды энергии квантованы, причем кванты энергии вращения гораздо меньше квантов электронной и колебательной энергии. На рис. 1 уровни 0" и0' являются нижними колебательными энергетическими уровнями нормального I ивоз-<span Arial",«sans-serif»;color:black; letter-spacing:-.05pt">бужденного
II состояния молекулы. Состояние0' отличается от 0" на квант электронной энергии, величина которого определяет расстояние по вертикали междууровнями 0" и 0'. Каждомузначению электронной энергии соответствует ряд возможных значений колебательнойэнергии молекулы. Если не учитывать энергию вращения, то возможные значенияэнергии молекулы для электронных состояний I и IIхарактеризуются системой энергетических уровней 0" — 4" и 0'— 4', положение последних определяется суммой электронной и колебательной энергии.<span Arial",«sans-serif»; color:black">Распределение молекул по колебательным уровням как невозбужденного, так и возбужденного электронногосостояния описывается
<span Arial",«sans-serif»; color:black;letter-spacing:-.1pt">
<span Arial",«sans-serif»;color:black; letter-spacing:-.05pt">формулой Больцмана:
<span Arial",«sans-serif»;color:black; letter-spacing:-.05pt">
(1)<span Arial",«sans-serif»;mso-ansi-language: EN-US">
<span Arial",«sans-serif»;color:black; letter-spacing:-.05pt">где
N0 — полноечисло всех молекул; Ni — число молекул на уровне i; Еi — значениеколебательной энергии, соответствующее уровню i. Если при некоторой температуреEi >> kT, то в соответствии с формулой (1) подавляющая часть молекул должна находиться на нулевомколебательном уровне. Для комнатной температуры это условие обычновыполняется, что позволяет считать, что в этом случае практически все молекулынаходятся на нулевом уровне. Таким образом, по мере роста номера уровня числонаходящихся на нем молекул быстро убывает.<span Arial",«sans-serif»">На рис.1 поглощение световых квантов различной величины обозначено стрелками, идущимивверх, а излучение квантов люминесценции — стрелками, направленными вниз.Длины стрелок пропорциональны величинам энергии поглощенных или излученныхквантов
hnт. е. пропорциональны частотам соответствующих линий в спектрах поглощения илиизлучения. Из рис. 1 видно, что разности частот линий поглощения даютрасстояния между колебательными уровнями верхнего электронного состояния; остроении нижнего электронного состояния можно судить по разностям частот линий излучения. Это открывает возможностьанализа колебательных состояний молекул с помощью спектров люминесценции.<span Arial",«sans-serif»">Оптическиесвойства люминесцирующих веществ описываются с помощью целого рядахарактеристик. Сюда относятся спектры поглощения и люминесценции, поляризациясвечения (и поляризационные спектры), выход люминесценции, длительностьвозбужденного состояния молекул, закон затухания свечения и кривые термическоговысвечивания.
<span Arial",«sans-serif»">Спектры поглощения.
<span Arial",«sans-serif»">Спектромпоглощения вещества называется совокупность коэффициентов поглощения,характеризующих его поглощательную способность к лучам оптического диапазоначастот. Коэффициенты поглощения определяются из закона Ламберта—Бера.
<span Arial",«sans-serif»">Спектрыпоглощения люминесцирующих веществ крайне разнообразны. Одни из них имеют видочень узких полос (растворы солей редкоземельных элементов), другие — более широкихполос с четко выраженной колебательной структурой(растворы ураниловых солей), наконец, спектры поглощения многих веществ представляютсобой широкие размытые полосы, структуру которых не удается выяснить даже принизких температурах (растворы красителей).
<span Arial",«sans-serif»; color:black">Спектры поглощения могутсущественно меняться при изменении концентрации раствора, его кислотности или щелочности (величины его рН), природы растворителя, температуры и ряда других факторов.
<span Arial",«sans-serif»;color:black">Спектрылюминесценции.
<span Arial",«sans-serif»; color:black">Спектром люминесценции называется распределение излучаемойвеществом энергии по частотам или длинам волн. Подобно спектрам поглощения,интенсивность и форма спектров люминесценции у разных веществ могут бытьвесьма различными, и они могут существенно изменяться при вариации тех жепараметров (концентрации, величины
pH раствораи т. д.)<span Arial",«sans-serif»">Выход люминесценции.
<span Arial",«sans-serif»"> Выход люминесценции характеризуетэффективность трансформации возбуждающего света в свет люминесценции висследуемом веществе. Различают энергетический и квантовый выходы люминесценции.Энергетическим выходом люминесценцииназывают отношение излучаемой веществом энергии
Eл к поглощеннойэнергии возбуждения Еп:<span Arial",«sans-serif»"> <img src="/cache/referats/22395/image004.gif" v:shapes="_x0000_i1026"> (2)
<span Arial",«sans-serif»">Квантовымвыходом люминесценции называют отношение числа квантов люминесценции,излученных веществом
Nл к числу поглощенныхквантов возбуждающего света Nп:<span Arial",«sans-serif»"> <img src="/cache/referats/22395/image006.gif" v:shapes="_x0000_i1027"> (3)
<span Arial",«sans-serif»">Выходлюминесценции очень чувствителен к внешним воздействиям, которые во многихслучаях приводят к тушению свечения. Так, известно тушение люминесценциипосторонними примесями, возникающее при добавлении к раствору постороннихвеществ — тушителей. Тушителями могут служить
KI,анилин и другие вещества. В результате взаимодействия возбужденных молекуллюминесцентного вещества с молекулами тушителя возникает безизлучательный разменэнергии возбуждения. Безизлучательные переходы развиваются и при увеличениитемпературы раствора, обуславливая появление температурного тушения.<span Arial",«sans-serif»">Вбольшинстве случаев увеличение концентрации также приводит к тушению свечения.При этом концентрационное тушение обычно начинает проявляться лишь придостижении некоторой пороговой концентрации, величина которой характерна дляисследуемого вещества. В более разведенных растворах выход люминесценции независит от концентрации. Это обстоятельство может быть использовано в люминесцентноманализе при подборе оптимальных условий его проведения.
<span Arial",«sans-serif»">Концентрационноетушение имеет двоякую природу. С одной стороны, при увеличении концентрациимогут образовываться ассоциированные молекулы, не обладающие люминесцентнойспособностью, но поглощающие энергию возбуждения. С другой стороны, междувозбужденными и невозбужденными молекулами может осуществляться индукционныйперенос, или, как говорят, миграция энергии возбуждения. Такой перенос энергиивозбуждения прежде всего на нелюминесцентные ассоциаты приводит к развитиюконцентрационного тушения.
<span Arial",«sans-serif»">Известныи другие виды тушения (тушение растворителем, тушение электролитами, тушениепри диссоциации и ионизации молекул и т. д.). При проведении люминесцентногоанализа интенсивность свечения играет очень большую роль. Поэтому учет тушения,изменяющего интенсивность люминесценции и затрудняющего анализ, является крайневажным.
<span Arial",«sans-serif»">Закон затухания люминесценции.
<span Arial",«sans-serif»">Законзатухания свечения после прекращения возбуждения может быть различным у разныхвеществ, что часто позволяет по нему определять природу и кинетику свечения; вместе с тем он может служить ианалитической характеристикой. Закон затухания свечения растворов имолекулярных кристаллов обычно достаточно хорошо выражается экспоненциальной зависимостью
<span Arial",«sans-serif»">
<span Arial",«sans-serif»"> <img src="/cache/referats/22395/image008.gif" v:shapes="_x0000_i1028"> (4).
<span Arial",«sans-serif»"> где
I — интенсивностьсвечения в момент времени t; I0— интенсивность свечения вмомент прекращения возбуждения; t — средняядлительность возбужденного состояния (время, в течение которого интенсивностьсвечения уменьшается в е раз, т. е. в 2,7 раза). В других случаях затуханиесвечения может происходить по более сложному закону. Так, например, затуханиесвечения кристаллофосфоров хорошо описывается эмпирической формулой<span Arial",«sans-serif»"> <img src="/cache/referats/22395/image010.gif" v:shapes="_x0000_i1029"> (5)
<span Arial",«sans-serif»">где
A,b, a — постоянные, причемобычно a<span Arial",«sans-serif»">Длительность возбужденного состояния молекул.
<span Arial",«sans-serif»">Послепрекращения возбуждения свечение не исчезает мгновенно, а продолжается определенный промежуток времени.Длительность возбужденного состояния у разных соединений может существенноразличаться. Она характерна для каждого вещества и является его важнойоптической характеристикой. Так, для растворов обычно
t~10-8—10-9сек. Затухание свечения кристаллофосфоров протекает по сложным законам и можетпродолжаться секунды, минуты и даже часы.<span Arial",«sans-serif»">Такимобразом, у жидких растворов
t очень невелико и ихлюминесценция затухает практически мгновенно. Такие свечения часто называют флуоресценцией. При введении тех жевеществ в очень вязкие среды (в желатину, сахарные леденцы и т. д.), а такжепри замораживании растворов возникает длительное свечение, продолжающееся долисекунды и даже целые секунды. Свечение такого вида называют замедленной флуоресценцией, или фосфоресценцией. Известны два видазамедленной флуоресценции: при одном спектр свечения совпадает со спектромфлуоресценции (a-процесс), при второмнаблюдается резко отличный спектр свечения, сдвинутый в сторону длинных волн (b-процесс).<span Arial",«sans-serif»">Замедленнаяфлуоресценция обусловлена попаданием возбужденных молекул на энергетическиеуровни, непосредственный переход с которых в невозбужденное состояние неразрешен. Эти уровни называются метастабильными; молекула может их покинутьлишь под влиянием внешних воздействий (например, при нагревании). Возбужденныемолекулы пребывают на метастабильных уровнях значительное время, вызываяувеличение длительности послесвечения.
<span Arial",«sans-serif»">Присложном законе затухания (например, (5)) понятие средней длительности возбужденногосостояния
t уже неприменимо. В этом случае дляхарактеристики длительности послесвечения обычно принимают время, в течениекоторого интенсивность свечения исследуемого образца уменьшается в определенноечисло раз (в 100—1000 раз).<span Arial",«sans-serif»">Кривые термического высвечивания.
<span Arial",«sans-serif»">У многихвеществ (кристаллофосфоров, минералов, кварца и др.), предварительновозбужденных ультрафиолетовой, рентгеновской или радиоактивной радиацией, принагревании возникает свечение, получившее название термолюминесценции. Оно наблюдаетсяпри температурах, значительно меньших тех, при которых появляется видимоетемпературное излучение.
<span Arial",«sans-serif»">Термолюминесценцияимеет следующее происхождение. Под действием возбуждающей радиации электроныотрываются от ионов облучаемого вещества; часть их непосредственнорекомбинирует с ионизованными центрами, что приводит к возникновению кратковременногосвечения кристаллофосфоров; другая часть электронов задерживается вблизи местнарушения периодичности кристаллической решетки — на уровнях локализации. Освобождениеэлектронов с мест локализации происходит за счет тепловой энергии. Их последующаярекомбинация с ионизованными центрами вызывает длительное свечениекристаллофосфоров.
<span Arial",«sans-serif»">Уровнилокализации могут иметь различную энергетическую глубину, т. е. могут удерживатьэлектроны с различной силой. Мелкие уровни освобождаются уже при температурежидкого азота, глубокие — при +300, +400°С. При постепенном нагреваниипредварительно возбужденного фосфора последовательно освобождаются уровниразной глубины, и интенсивность термолюминесценции то увеличивается, тоуменьшается. Кривые, характеризующие зависимость яркости свечения фосфора оттемпературы, получили название кривых термического высвечивания. Они являютсяважной характеристикой кристаллофосфоров и могут быть использованы для аналитическихцелей.
<span Arial",«sans-serif»">
<span Arial",«sans-serif»">Основные закономерности свечения, используемые в люминесцентноманализе.
<span Arial",«sans-serif»">
<span Arial",«sans-serif»">Закон независимости спектра люминесценции от длины
<span Arial",«sans-serif»">волны возбуждающего света.
<span Arial",«sans-serif»">
При возбуждении свечения различнымидлинами волн молекулы вещества, поглощая кванты разной величины, попадают наразличные колебательные уровни возбужденного электронного состояния. Поэтомуможно ожидать, что спектр люминесценции будет зависеть от длины волнывозбуждающего света. Однако оказалось, что каждое вещество в конденсированномсостоянии имеет совершенно определенный спектр люминесценции, который нечувствителен к изменению длины волны возбуждающего света.<span Arial",«sans-serif»">Этообъясняется тем, что молекулы, перешедшие в результате возбуждения на различныеколебательные уровни возбужденного состояния (рис. 1), успевают за время, многоменьшее, чем средняя длительность возбужденного состояния
t,растратить часть колебательной энергии и образовать систему возбужденных молекул,обладающих равновесным распределением колебательной энергии, определяемым температурой.Из этих вполне определенных для данной температуры состояний и происходятпереходы молекул в невозбужденное состояние, сопровождающиеся излучением. Поэтомуна опыте всегда наблюдается один и гот же спектр люминесценции, не зависящий отдлины волны возбуждающего света.<span Arial",«sans-serif»">Независимостьспектра люминесценции от длины волны возбуждающего света позволяет на практикепользоваться для возбуждения широкими спектральными участками. При отсутствиивторичного поглощения оказывается возможным не обращать внимания на составвозбуждающего света, что очень сильно облегчает проведение анализа.
<span Arial",«sans-serif»">Закон Стокса—Ломмеля.
<span Arial",«sans-serif»">Стоксомбыло сформулировано правило, согласно которому свет люминесценции всегда имеетбольшую длину волны по сравнению со светом, применявшимся для возбуждения.Однако во многих случаях правило Стокса не выполняется. Спектры поглощения илюминесценции многих веществ частично накладываются друг на друга. Если длявозбуждения взять частоту (например,
n = 530·10-12сек-1), находящуюся в области наложения спектров, то согласноправилу Стокса должна появляться лишь та часть спектра люминесценции, котораярасположена по левую сторону от выбранной частоты. Однако в соответствии сзаконом независимости спектра люминесценции от возбуждающей длины волны вбольшинстве случаев наблюдается полный спектр люминесценции, имеющий целый рядчастот, превышающих частоту возбуждающего света (заштрихованная область). Такимобразом, правило Стокса нарушается. Часть спектра люминесценции, состоящая излучей с частотами, большими частоты возбуждающего света, называется антистоксовской. Ее возникновение можнообъяснить наличием у излучающих молекул помимо энергии возбуждения ещеопределенного запаса колебательной энергии. Сумма энергий возбуждающего и колебательногоквантов позволяет получать большие кванты люминесценции, обусловливающиепоявление антистоксовской части спектра. Ломмель уточнил правило Стокса,предложив для него следующую формулировку: спектр излучения в целом и егомаксимум всегда сдвинуты по сравнению со спектром поглощения и его максимумом всторону длинных волн. Закон Стокса—Ломмеля строго выполняется для очень широкогокруга веществ.<span Arial",«sans-serif»">Сдвигспектров люминесценции относительно спектров поглощения дает возможность болееили менее просто отфильтровывать рассеянную часть возбуждающего света,примешивающегося к люминесценции. Это обстоятельство широко используется впрактике люминесцентного анализа.
<span Arial",«sans-serif»">Закон Вавилова.
<span Arial",«sans-serif»">С. И.Вавиловым установлено, что энергетический выход люминесценции растет пропорциональнодлине волны возбуждающего света, затем в некотором спектральном интервале оностается постоянным, после чего в области наложения спектров поглощения илюминесценции начинает быстро падать. Падение энергетического выхода свеченияпроисходит в антистоксовской части спектра.
<span Arial",«sans-serif»">Легкопоказать, что пропорциональность энергетического выхода длине волнывозбуждающего света соответствует постоянству квантового выхода в той же спектральнойобласти, где в излучение всегда переходит одна и та же доля возбуждающих световых квантов. С. И. Вавилов дал своему закону формулировку, согласно которойлюминесценция может сохранять постоянный квантовый выход, если возбуждающаяволна преобразуется в среднем в более длинную, чем она сама. Наоборот, выход люминесценциирезко уменьшается при обратном преобразовании длинных волн в короткие. Закон Вавилова широкоиспользуется в люминесцентном анализе при подборе оптимальных условий проведенияопыта.
<span Arial",«sans-serif»">Правило зеркальной симметрии спектров поглощения и
<span Arial",«sans-serif»"> люминесценции.
<span Arial",«sans-serif»">Дляширокого круга веществ (растворов красителей, ряда ароматических и многихдругих соединений) выполняется установленное В. Л. Левшиным правило зеркальнойсимметрии спектров поглощения и излучения, согласно которому спектры поглощенияи люминесценции, изображенные в функции частот, оказываются зеркально-симметричнымиотносительно прямой, проходящей перпендикулярно оси частот через точкупересечения обоих спектров, т. е.
<span Arial",«sans-serif»"> <img src="/cache/referats/22395/image012.gif" v:shapes="_x0000_i1030"> (6)
<span Arial",«sans-serif»">или
<span Arial",«sans-serif»"> <img src="/cache/referats/22395/image014.gif" v:shapes="_x0000_i1031"> (7)
<span Arial",«sans-serif»">Здесь
nП—частота поглощаемого света; nЛ — симметричная частоталюминесценции; n0 — частота линиисимметрии. При этом по оси ординат для спектров поглощения откладываютсякоэффициенты поглощения a, а для спектровлюминесценции — квантовые интенсивности IКВ=I/n.<span Arial",«sans-serif»">Изуравнения (9) видно, что при наличии зеркальной симметрии
Dn=nП- nЛ, и nП связаны линейнойзависимостью. Если откладывать по оси абсцисс nП, а по оси ординат Dn, то при строгомвыполнении правила должна получиться прямая линия.<span Arial",«sans-serif»">Дляосуществления зеркальной симметрии необходимо выполнение двух условий —зеркальной симметрии частот и зеркальной симметрии интенсивностей поглощения илюминесценции в соответствующих частях спектра.
<span Arial",«sans-serif»">Дляосуществления симметрии частот необходимо, чтобы энергетические уровнивозбужденного и невозбужденного состояний были построены одинаково. Для наличиязеркальной симметрии интенсивностей необходимо, чтобы распределение молекул поэнергетическим уровням верхней и нижней систем было одинаковым и чтобывероятности соответствующих излучательных и поглощательных переходов были равны,или пропорциональны друг другу. Эти условия выполняются лишь у части молекул. Увеществ, следующих правилу зеркальной симметрии, можно по одному из спектров(люминесценции или поглощения) без измерений установить форму другого. Отступленияот правила зеркальной симметрии могут быть использованы для установления величиныотклонений от условий его выполнения.
<span Arial",«sans-serif»">Правилозеркальной симметрии оказывается весьма полезным при проведении люминесцентногоанализа, а также при расшифровке спектров и установлении энергетических уровнейисследуемых молекул.
<span Arial",«sans-serif»">
<span Arial",«sans-serif»">Виды люминесцентного анализа и характеристика его особенностей.
<span Arial",«sans-serif»">
<span Arial",«sans-serif»">Люминесцентным анализом
называетсяобнаружение и исследование различных объектов с помощью явлений люминесценции.Наиболее важной задачей люминесцентного анализа является определениехимического состава исследуемых веществ и установление процентного содержания вних отдельных компонентов. Анализ такого вида носит соответственно название качественного и количественного химическоголюминесцентного анализа.<span Arial",«sans-serif»">Качественныйхимический люминесцентный анализ основан на том, что люминесцентные свойстваявляются характерным признаком излучающего вещества, тесно связанным с его составом,общим состоянием и структурой его молекул.
<span Arial",«sans-serif»">Количественныйхимический люминесцентный анализ основан на использовании определеннойзависимости между интенсивностью люминесценции и концентрацией люминесцентноговещества. В большинстве случаев условия анализа подбираются так, чтобы осуществляласьпропорциональность между интенсивностью свечения и концентрацией вещества.Однако такая зависимость имеет место лишь в случаях, когда концентрацииневелики. При высоких концентрациях определяемого вещества для осуществленияанализа приходится тем или иным способом учитывать сложную зависимость интенсивностисвечения от концентрации.
<span Arial",«sans-serif»">Клюминесцентному анализу относится также изучение структуры и колебательныхчастот молекул по спектрам излучения, создающее фундамент для качественноголюминесцентного анализа.
<span Arial",«sans-serif»">Чистохимические задачи не исчерпывают возможностей люминесцентного анализа. С егопомощью можно обнаруживать и выявлять различные объекты и их детали, изучение которыхоказывается невозможным при обычных условиях наблюдения и освещения. Люминесцентныйанализ такого рода получил название люминесцентногоанализа обнаружения или сортовоголюминесцентного анализа.
<span Arial",«sans-serif»">Люминесцентныйанализ обладает рядом особенностей, которые отличают его от всех других видованализа. Люминесцентный анализ необычайно чувствителен. С его помощью можнообнаружить в пробе присутствие вещества с концентрацией ~10-10 – 10-11г/г. Это более чем на три порядка превосходит чувствительность эмиссионногоспектрального анализа, что позволяет работать с исчезающе малыми количествамиисследуемого вещества ~10-12 – 10-15 г. С помощью люминесцентного анализа можноисследовать очень небольшие объемы раствора, а также анализировать мельчайшиекрупинки порошков, в которых содержатся следы других люминесцирующих веществ.
<span Arial",«sans-serif»">Важным преимуществом люминесцентного анализа являются его простота и скорость, во много раз превосходящие скорость химическогоанализа.
<span Arial",«sans-serif»">В товремя как при химическом и эмиссионном спектральном анализе анализируемыевещества разлагаются, при люминесцентном анализе они, как правило, неподвергаются изменениям и их можно использовать в дальнейшей работе. Этопреимущество люминесцентного анализа особенно существенно при исследованиитрудно синтезируемых уникальных веществ, получаемых в ничтожных количествах. Вотдельных случаях возбуждения люминесценции коротковолновыми ультрафиолетовымилучами в веществе могут происходить фотохимические превращения. Однакосоответствующим подбором условий опыта эти трудности обычно могут быть обойдены.
<span Arial",«sans-serif»">Перечисленныесвойства люминесцентного анализа дают представление о его исключительныхвозможностях, в определенных отношениях значительно превосходящих возможностидругих видов анализа. Однако следует отметить, что необычайно высокая чувствительностьлюминесцентного анализа одновременно создает и серьезные трудности егопроведения, существенно ограничивая области его применения. Присутствие вобразце даже ничтожных количеств люминесцирующих примесей обусловливаетпоявление нового свечения, которое накладывается на люминесценцию основного вещества,искажая как спектральный состав, так и интенсивность его излучения. Поэтомузначительные успехи в применении люминесцентного анализа могли быть достигнутылишь на основе всестороннего развития учения о люминесценции в целом, послетого как были установлены общие законы свечения и накоплен большой материал олюминесцентных свойствах различных классов соединений.
<span Arial",«sans-serif»">Наиболеераспространенным и хорошо разработанным является люминесцентный анализ,основанный на возбуждении фотолюминесценции. При анализе кристаллических неорганическихвеществ (минералов, алмазов и др.) применяют катодное и рентгеновскоевозбуждения. В отдельных случаях в аналитических целях используют явленияхемилюминесценции и радиолюминесценции.
<span Arial",«sans-serif»">
<span Arial",«sans-serif»">
www.ronl.ru