|
|
|
|
 Far Far |
 WinNavigator WinNavigator |
 Frigate Frigate |
 Norton
Commander Norton
Commander |
 WinNC WinNC |
 Dos
Navigator Dos
Navigator |
 Servant
Salamander Servant
Salamander |
 Turbo
Browser Turbo
Browser |
|
|
 Winamp,
Skins, Plugins Winamp,
Skins, Plugins |
 Необходимые
Утилиты Необходимые
Утилиты |
 Текстовые
редакторы Текстовые
редакторы |
 Юмор Юмор |
|
|
|
File managers and best utilites |
Доклад: Круговорот углерода в природе. Круговорот углерода в природе реферат
Доклад - Круговорот углерода в природе
Круговорот углерода в природе.
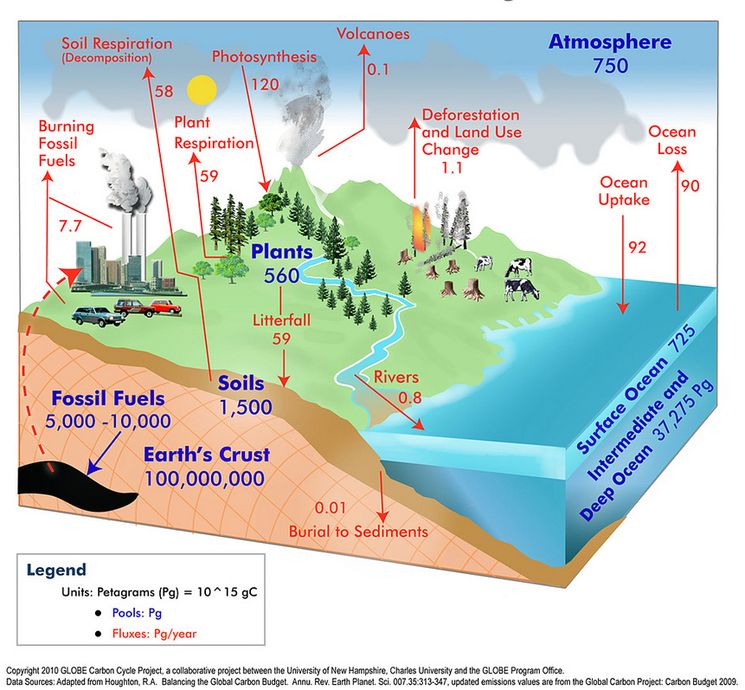
Основным резервуаром углерода являются горные породы; в них, по существующим оценкам, его содержится примерно 75 квадриллионов тонн. Еще 5 триллионов тонн содержится в горючих полезных ископаемых — угле, нефти, газе и торфе. Примерно 150 млрд. т приходится на верхний слой донных океанических осадков. Эти запасы в обычных условиях недоступны для живых организмов. Для них важнее «оборотный пул» углерода, представленный на рисунке.
Главный источник углерода для живых организмов — это диоксид углерода (углекислый газ), содержащийся в атмосфере и растворенный в поверхностных водах. В процессе фотосинтеза зеленые растения, водоросли и цианобактерии превращают это неорганическое вещество в углеводы, из которых затем образуется углеродный скелет всех прочих органических молекул. Фотосинтетическая ассимиляция диоксида углерода компенсируется его выделением в процессе дыхания, что способствует поддержанию природного равновесия. Однако не весь фиксированный диоксид углерода возвращается в атмосферу за счет дыхания. В анаэробной среде, например в болотах или на слабо освещенном дне стоячих водоемов, минерализация органики идет очень медленно, и она накапливается в виде ила или торфа. В определенных условиях через длительный период времени эти осадки могут образовать залежи ископаемого топлива.
В океанах основными механизмами поглощения диоксида углерода из атмосферы является фотосинтез, главным образом фитопланктонный, и растворение в поверхностных водах. Значительная часть этого связанного диоксида углерода быстро возвращается назад — непосредственно из раствора или в результате дыхания. Однако, как и в наземных экосистемах, некоторая доля углерода надолго задерживается, например при погружении холодных поверхностных вод в глубину или в составе образуемых морскими организмами карбонатных структур (раковин, кораллов и т. д.), которые со временем превращаются в горные породы типа известняка.
Скорость переноса углерода между его резервным и оборотным пулами может меняться из года в год в зависимости от климатических флуктуации. На этот баланс влияет также деятельность человека, особенно изменение землепользования (сведение леса или лесопосадки), использование ископаемого топлива и производство цемента. Судя по имеющимся данным, именно человек обусловливает значительный рост содержания диоксида углерода в атмосфере с эпохи промышленной революции.
Повышение скорости мобилизации углерода из его резервуаров типа ископаемого топлива и карбонатов (при производстве цемента) и потенциальное влияние этого ускорения на глобальный климат и экосистемы — весьма актуальные темы ведущихся сейчас экологических исследований и дебатов. Преобладает мнение, что сохранение нынешних темпов поступления в атмосферу диоксида углерода грозит весьма серьезными последствиями для всей планеты. Правительства предпринимают усилия к сокращению выбросов диоксида углерода промышленностью и масштабов использования ископаемого топлива в целом за счет более широкого применения альтернативных видов энергии, например солнечной и ветровой.
Аллотропные модификации
Общие сведения, аллотропия углерода Углерод (лат. carboneuia) известен с глубокой древности. В земной коре его содержится примерно 0,35% по массе. В природе углерод встречается в свободном и связанном состоянии, главным образом в виде карбонатов (мел, известняк, мрамор), в каменных и бурых углях, торфе. Углерод входит в состав нефти, природного газа, воздуха, растений, организмов человека и животных. Его соединения составляют основу живой природы — флоры и фауны. Атом углерода имеет 6 электронов, 2 на внутреннем слое (1s2), а 4 (2s22р2) — на внешнем. С наиболее активными металлами углерод проявляет степень окисления -4. Углерод способен соединяться между собой с образованием прочных длинных цепей. В отличие от кислорода и азота углерод при обычных условиях не образует молекул, у него атомная кристаллическая решетка. Существуют четыре аллотропных модификации углерода: алмаз, графит, карбин и букибол. Кристаллическая решетка алмаза состоит из атомов углерода, соединенных между собой очень прочными s-связями. В кристалле алмаза все связи эквивалентны и атомы образуют трехмерный каркас из сочлененных тетраэдров. Алмаз — самое твердое вещество, найденное в природе. Графит представляет собой темно-серое с металлическим блеском, мягкое, жирное на ощупь вещество. Хорошо проводит электрический ток. В графите атомы углерода расположены в параллельных слоях, образуя гексагональную сетку. Внутри слоя атомы связаны гораздо сильнее, чем один слой с другим, поэтому свойства графита сильно различаются по разным направлениям. Карбин — получен искусственным путем. Существует два вида карбина: поликумулен =С=С=С=С= и полиин -C=C-C=C-C=C-. Букибол — получен в 1985г., имеет сферическую форму (как футбольный мяч), состоит из 60 или 70 атомов углерода. Углерод в виде сажи, кокса, древесного угля, костных углей широко используется в металлургии, синтезе органических веществ, как топливо, в быту.
www.ronl.ru
Курсовая работа - Круговорот углерода в природе
Круговорот углерода в природе.
Основным резервуаром углерода являются горные породы; в них, по существующим оценкам, его содержится примерно 75 квадриллионов тонн. Еще 5 триллионов тонн содержится в горючих полезных ископаемых — угле, нефти, газе и торфе. Примерно 150 млрд. т приходится на верхний слой донных океанических осадков. Эти запасы в обычных условиях недоступны для живых организмов. Для них важнее «оборотный пул» углерода, представленный на рисунке.
Главный источник углерода для живых организмов — это диоксид углерода (углекислый газ), содержащийся в атмосфере и растворенный в поверхностных водах. В процессе фотосинтеза зеленые растения, водоросли и цианобактерии превращают это неорганическое вещество в углеводы, из которых затем образуется углеродный скелет всех прочих органических молекул. Фотосинтетическая ассимиляция диоксида углерода компенсируется его выделением в процессе дыхания, что способствует поддержанию природного равновесия. Однако не весь фиксированный диоксид углерода возвращается в атмосферу за счет дыхания. В анаэробной среде, например в болотах или на слабо освещенном дне стоячих водоемов, минерализация органики идет очень медленно, и она накапливается в виде ила или торфа. В определенных условиях через длительный период времени эти осадки могут образовать залежи ископаемого топлива.
В океанах основными механизмами поглощения диоксида углерода из атмосферы является фотосинтез, главным образом фитопланктонный, и растворение в поверхностных водах. Значительная часть этого связанного диоксида углерода быстро возвращается назад — непосредственно из раствора или в результате дыхания. Однако, как и в наземных экосистемах, некоторая доля углерода надолго задерживается, например при погружении холодных поверхностных вод в глубину или в составе образуемых морскими организмами карбонатных структур (раковин, кораллов и т. д.), которые со временем превращаются в горные породы типа известняка.
Скорость переноса углерода между его резервным и оборотным пулами может меняться из года в год в зависимости от климатических флуктуации. На этот баланс влияет также деятельность человека, особенно изменение землепользования (сведение леса или лесопосадки), использование ископаемого топлива и производство цемента. Судя по имеющимся данным, именно человек обусловливает значительный рост содержания диоксида углерода в атмосфере с эпохи промышленной революции.
Повышение скорости мобилизации углерода из его резервуаров типа ископаемого топлива и карбонатов (при производстве цемента) и потенциальное влияние этого ускорения на глобальный климат и экосистемы — весьма актуальные темы ведущихся сейчас экологических исследований и дебатов. Преобладает мнение, что сохранение нынешних темпов поступления в атмосферу диоксида углерода грозит весьма серьезными последствиями для всей планеты. Правительства предпринимают усилия к сокращению выбросов диоксида углерода промышленностью и масштабов использования ископаемого топлива в целом за счет более широкого применения альтернативных видов энергии, например солнечной и ветровой.
Аллотропные модификации
Общие сведения, аллотропия углерода Углерод (лат. carboneuia) известен с глубокой древности. В земной коре его содержится примерно 0,35% по массе. В природе углерод встречается в свободном и связанном состоянии, главным образом в виде карбонатов (мел, известняк, мрамор), в каменных и бурых углях, торфе. Углерод входит в состав нефти, природного газа, воздуха, растений, организмов человека и животных. Его соединения составляют основу живой природы — флоры и фауны. Атом углерода имеет 6 электронов, 2 на внутреннем слое (1s2), а 4 (2s22р2) — на внешнем. С наиболее активными металлами углерод проявляет степень окисления -4. Углерод способен соединяться между собой с образованием прочных длинных цепей. В отличие от кислорода и азота углерод при обычных условиях не образует молекул, у него атомная кристаллическая решетка. Существуют четыре аллотропных модификации углерода: алмаз, графит, карбин и букибол. Кристаллическая решетка алмаза состоит из атомов углерода, соединенных между собой очень прочными s-связями. В кристалле алмаза все связи эквивалентны и атомы образуют трехмерный каркас из сочлененных тетраэдров. Алмаз — самое твердое вещество, найденное в природе. Графит представляет собой темно-серое с металлическим блеском, мягкое, жирное на ощупь вещество. Хорошо проводит электрический ток. В графите атомы углерода расположены в параллельных слоях, образуя гексагональную сетку. Внутри слоя атомы связаны гораздо сильнее, чем один слой с другим, поэтому свойства графита сильно различаются по разным направлениям. Карбин — получен искусственным путем. Существует два вида карбина: поликумулен =С=С=С=С= и полиин -C=C-C=C-C=C-. Букибол — получен в 1985г., имеет сферическую форму (как футбольный мяч), состоит из 60 или 70 атомов углерода. Углерод в виде сажи, кокса, древесного угля, костных углей широко используется в металлургии, синтезе органических веществ, как топливо, в быту.
www.ronl.ru
Доклад - Круговорот углерода - Биология и химия
Биотический является составной частью большого круговорота в связи с жизнедеятельностью организмов. Углекислота, или СО2, находящаяся в атмосфере (23, 5·1011 т) или в растворенном состоянии в воде, служит сырьем для фотосинтеза растений и переработки углерода в органическое вещество живых существ, т.е. в процессе фотосинтеза превращается в сахара, затем преобразуется в протеины, липиды и т.д. Эти вещества служат углеводным питанием животным и наземным растениям, т.е. поступают в распоряжение консументов разных уровней, а далее — редуцентов.
При дыхании организмов СО2 возвращается в атмосферу. Определенная часть углерода накапливается в виде мертвой органики и переходит в ископаемое состояние. Когда наступает смерть, то сапрофаги и биоредуценты двух типов разлагают и минерализуют трупы, образуя цепи питания, в конце которых углерод нередко поступает в круговорот в форме углекислоты («почвенное дыхание»).
Животные-сапрофаги и сапрофатические микроорганизмы, обитающие в почве, превращают накопившиеся в ней остатки в новое образование органической материи, более или менее мощный слой коричневой или черной массы — гумус.
Иногда из-за недостатка воздуха или высокой кислотности цепь бывает неполной или короткой, т.е. органические остатки накапливаются в виде торфа, образуя торфяные болота. В некоторых болотах слой торфа достигает мощности 20 м и более. Здесь и приостанавливается природный (биологический) круговорот. Залежи каменного угля или торфа — продукт процессов фотосинтеза растений прошлых геологических эпох.
Однако солнечную энергию, аккумулированную в ископаемом топливе, человек интенсивно высвобождает при сжигании топлива, при этом СО2 поступает в атмосферу.
Основная масса углерода биосферы аккумулирована в карбонатных отложениях дна океана (известняки и кораллы): 1, 3·1016 т, кристаллических породах — 1, 0·1016 т. В каменном угле и нефти — 3, 4·1015 т. Именно этот углерод принимает участие в медленном геологическом круговороте. Жизнь на Земле и газовый баланс атмосферы поддерживается количеством углерода, содержащегося в растительных (5·1011 т) и животных (5·109 т) тканях. Однако в настоящее время человек интенсивно замыкает на себя круговорот веществ, в том числе и углерода.
Так, например, подсчитано, что суммарная биомасса всех домашних животных уже превышает биомассу всех диких наземных животных. Площади культурных растений приближаются к площади естественных биогеоценозов, и многие культурные растения экосистемы по своей продуктивности значительно превосходят природные.
С другой стороны, поступление диоксида углерода в атмосферу в результате сжигания энергоносителей ведет к глобальным нарушениям в биосфере — нарушению теплового баланса. За последнее столетие содержание СО2 увеличилось на 10%, причем основной прирост произошел в последние десятилетия.
В атмосфере задерживается около половины всего «антропогенного» СО2, остальное поглощается Мировым океаном. Считается, что экосистемы (наземные) ассимилируют около 12% СО2, общее время его переноса — 8 лет.
В пособии Н.М. Кузьменко, Е.А. Стрельцова и А.И. Кумачева «Экология на уроках химии» отмечается, что еще в 1962 году климатолог и метеоролог М.И. Будыко предостерегал, что сжигание огромного количества топлива неизбежно приведет к возрастанию в атмосфере СО2. Так, в 1956 г. содержание СО2 было 0, 028%, в 1985 г. — 0, 034%, а в 1989 г. составило 0, 035%. Следовательно, за 33 года содержание СО2 возросло на 25% от первоначальной величины.
По прогнозам, к середине XXI века содержание СО2 в атмосфере удвоится.
Накопление СО2 в атмосфере во всем мире связывается сейчас с так называемым «парниковым эффектом» (этому способствует также накопление СН4, СFCl2, N2О). Диоксид углерода не поглощает видимую и ближнюю УФ-области солнечной радиации, а с другой стороны, ИК-излучение Земли поглощается СО2 в атмосфере, не пропускается в космос.
Задерживание тепла вблизи поверхности Земли — процесс очень важный для поддержания жизни на Земле, иначе средняя температура была бы на 33оС ниже существующей. Но перспективы быстрого повышения tоС Земли очень опасны, так как приведут к повышению уровня Мирового океана. Многие климатологии рассматривают длительную жару 1988 г. в Северном полушарии последствиями «парникового эффекта».
www.ronl.ru
Реферат: Круговорот углерода в природе
Круговорот углерода в природе.
Основным резервуаром углерода являются горные породы; в них, по существующим оценкам, его содержится примерно 75 квадриллионов тонн. Еще 5 триллионов тонн содержится в горючих полезных ископаемых — угле, нефти, газе и торфе. Примерно 150 млрд. т приходится на верхний слой донных океанических осадков. Эти запасы в обычных условиях недоступны для живых организмов. Для них важнее «оборотный пул» углерода, представленный на рисунке.
Главный источник углерода для живых организмов — это диоксид углерода (углекислый газ), содержащийся в атмосфере и растворенный в поверхностных водах. В процессе фотосинтеза зеленые растения, водоросли и цианобактерии превращают это неорганическое вещество в углеводы, из которых затем образуется углеродный скелет всех прочих органических молекул. Фотосинтетическая ассимиляция диоксида углерода компенсируется его выделением в процессе дыхания, что способствует поддержанию природного равновесия. Однако не весь фиксированный диоксид углерода возвращается в атмосферу за счет дыхания. В анаэробной среде, например в болотах или на слабо освещенном дне стоячих водоемов, минерализация органики идет очень медленно, и она накапливается в виде ила или торфа. В определенных условиях через длительный период времени эти осадки могут образовать залежи ископаемого топлива.
В океанах основными механизмами поглощения диоксида углерода из атмосферы является фотосинтез, главным образом фитопланктонный, и растворение в поверхностных водах. Значительная часть этого связанного диоксида углерода быстро возвращается назад — непосредственно из раствора или в результате дыхания. Однако, как и в наземных экосистемах, некоторая доля углерода надолго задерживается, например при погружении холодных поверхностных вод в глубину или в составе образуемых морскими организмами карбонатных структур (раковин, кораллов и т. д.), которые со временем превращаются в горные породы типа известняка.
Скорость переноса углерода между его резервным и оборотным пулами может меняться из года в год в зависимости от климатических флуктуации. На этот баланс влияет также деятельность человека, особенно изменение землепользования (сведение леса или лесопосадки), использование ископаемого топлива и производство цемента. Судя по имеющимся данным, именно человек обусловливает значительный рост содержания диоксида углерода в атмосфере с эпохи промышленной революции.
Повышение скорости мобилизации углерода из его резервуаров типа ископаемого топлива и карбонатов (при производстве цемента) и потенциальное влияние этого ускорения на глобальный климат и экосистемы — весьма актуальные темы ведущихся сейчас экологических исследований и дебатов. Преобладает мнение, что сохранение нынешних темпов поступления в атмосферу диоксида углерода грозит весьма серьезными последствиями для всей планеты. Правительства предпринимают усилия к сокращению выбросов диоксида углерода промышленностью и масштабов использования ископаемого топлива в целом за счет более широкого применения альтернативных видов энергии, например солнечной и ветровой.
Аллотропные модификации
Общие сведения, аллотропия углерода Углерод (лат. carboneuia) известен с глубокой древности. В земной коре его содержится примерно 0,35% по массе. В природе углерод встречается в свободном и связанном состоянии, главным образом в виде карбонатов (мел, известняк, мрамор), в каменных и бурых углях, торфе. Углерод входит в состав нефти, природного газа, воздуха, растений, организмов человека и животных. Его соединения составляют основу живой природы - флоры и фауны. Атом углерода имеет 6 электронов, 2 на внутреннем слое (1s2), а 4 (2s22р2) - на внешнем. С наиболее активными металлами углерод проявляет степень окисления -4. Углерод способен соединяться между собой с образованием прочных длинных цепей. В отличие от кислорода и азота углерод при обычных условиях не образует молекул, у него атомная кристаллическая решетка. Существуют четыре аллотропных модификации углерода: алмаз, графит, карбин и букибол. Кристаллическая решетка алмаза состоит из атомов углерода, соединенных между собой очень прочными s-связями. В кристалле алмаза все связи эквивалентны и атомы образуют трехмерный каркас из сочлененных тетраэдров. Алмаз - самое твердое вещество, найденное в природе. Графит представляет собой темно-серое с металлическим блеском, мягкое, жирное на ощупь вещество. Хорошо проводит электрический ток. В графите атомы углерода расположены в параллельных слоях, образуя гексагональную сетку. Внутри слоя атомы связаны гораздо сильнее, чем один слой с другим, поэтому свойства графита сильно различаются по разным направлениям. Карбин - получен искусственным путем. Существует два вида карбина: поликумулен =С=С=С=С= и полиин -C=C-C=C-C=C-. Букибол - получен в 1985г., имеет сферическую форму (как футбольный мяч), состоит из 60 или 70 атомов углерода. Углерод в виде сажи, кокса, древесного угля, костных углей широко используется в металлургии, синтезе органических веществ, как топливо, в быту.
www.referatmix.ru
Книга - Круговорот углерода в природе
Круговорот углерода в природе.
Основным резервуаром углерода являются горные породы; в них, по существующим оценкам, его содержится примерно 75 квадриллионов тонн. Еще 5 триллионов тонн содержится в горючих полезных ископаемых — угле, нефти, газе и торфе. Примерно 150 млрд. т приходится на верхний слой донных океанических осадков. Эти запасы в обычных условиях недоступны для живых организмов. Для них важнее «оборотный пул» углерода, представленный на рисунке.
Главный источник углерода для живых организмов — это диоксид углерода (углекислый газ), содержащийся в атмосфере и растворенный в поверхностных водах. В процессе фотосинтеза зеленые растения, водоросли и цианобактерии превращают это неорганическое вещество в углеводы, из которых затем образуется углеродный скелет всех прочих органических молекул. Фотосинтетическая ассимиляция диоксида углерода компенсируется его выделением в процессе дыхания, что способствует поддержанию природного равновесия. Однако не весь фиксированный диоксид углерода возвращается в атмосферу за счет дыхания. В анаэробной среде, например в болотах или на слабо освещенном дне стоячих водоемов, минерализация органики идет очень медленно, и она накапливается в виде ила или торфа. В определенных условиях через длительный период времени эти осадки могут образовать залежи ископаемого топлива.
В океанах основными механизмами поглощения диоксида углерода из атмосферы является фотосинтез, главным образом фитопланктонный, и растворение в поверхностных водах. Значительная часть этого связанного диоксида углерода быстро возвращается назад — непосредственно из раствора или в результате дыхания. Однако, как и в наземных экосистемах, некоторая доля углерода надолго задерживается, например при погружении холодных поверхностных вод в глубину или в составе образуемых морскими организмами карбонатных структур (раковин, кораллов и т. д.), которые со временем превращаются в горные породы типа известняка.
Скорость переноса углерода между его резервным и оборотным пулами может меняться из года в год в зависимости от климатических флуктуации. На этот баланс влияет также деятельность человека, особенно изменение землепользования (сведение леса или лесопосадки), использование ископаемого топлива и производство цемента. Судя по имеющимся данным, именно человек обусловливает значительный рост содержания диоксида углерода в атмосфере с эпохи промышленной революции.
Повышение скорости мобилизации углерода из его резервуаров типа ископаемого топлива и карбонатов (при производстве цемента) и потенциальное влияние этого ускорения на глобальный климат и экосистемы — весьма актуальные темы ведущихся сейчас экологических исследований и дебатов. Преобладает мнение, что сохранение нынешних темпов поступления в атмосферу диоксида углерода грозит весьма серьезными последствиями для всей планеты. Правительства предпринимают усилия к сокращению выбросов диоксида углерода промышленностью и масштабов использования ископаемого топлива в целом за счет более широкого применения альтернативных видов энергии, например солнечной и ветровой.
Аллотропные модификации
Общие сведения, аллотропия углерода Углерод (лат. carboneuia) известен с глубокой древности. В земной коре его содержится примерно 0,35% по массе. В природе углерод встречается в свободном и связанном состоянии, главным образом в виде карбонатов (мел, известняк, мрамор), в каменных и бурых углях, торфе. Углерод входит в состав нефти, природного газа, воздуха, растений, организмов человека и животных. Его соединения составляют основу живой природы — флоры и фауны. Атом углерода имеет 6 электронов, 2 на внутреннем слое (1s2), а 4 (2s22р2) — на внешнем. С наиболее активными металлами углерод проявляет степень окисления -4. Углерод способен соединяться между собой с образованием прочных длинных цепей. В отличие от кислорода и азота углерод при обычных условиях не образует молекул, у него атомная кристаллическая решетка. Существуют четыре аллотропных модификации углерода: алмаз, графит, карбин и букибол. Кристаллическая решетка алмаза состоит из атомов углерода, соединенных между собой очень прочными s-связями. В кристалле алмаза все связи эквивалентны и атомы образуют трехмерный каркас из сочлененных тетраэдров. Алмаз — самое твердое вещество, найденное в природе. Графит представляет собой темно-серое с металлическим блеском, мягкое, жирное на ощупь вещество. Хорошо проводит электрический ток. В графите атомы углерода расположены в параллельных слоях, образуя гексагональную сетку. Внутри слоя атомы связаны гораздо сильнее, чем один слой с другим, поэтому свойства графита сильно различаются по разным направлениям. Карбин — получен искусственным путем. Существует два вида карбина: поликумулен =С=С=С=С= и полиин -C=C-C=C-C=C-. Букибол — получен в 1985г., имеет сферическую форму (как футбольный мяч), состоит из 60 или 70 атомов углерода. Углерод в виде сажи, кокса, древесного угля, костных углей широко используется в металлургии, синтезе органических веществ, как топливо, в быту.
www.ronl.ru
Статья - Круговорот углерода в природе
Круговорот углерода в природе.
Основным резервуаром углерода являются горные породы; в них, по существующим оценкам, его содержится примерно 75 квадриллионов тонн. Еще 5 триллионов тонн содержится в горючих полезных ископаемых — угле, нефти, газе и торфе. Примерно 150 млрд. т приходится на верхний слой донных океанических осадков. Эти запасы в обычных условиях недоступны для живых организмов. Для них важнее «оборотный пул» углерода, представленный на рисунке.
Главный источник углерода для живых организмов — это диоксид углерода (углекислый газ), содержащийся в атмосфере и растворенный в поверхностных водах. В процессе фотосинтеза зеленые растения, водоросли и цианобактерии превращают это неорганическое вещество в углеводы, из которых затем образуется углеродный скелет всех прочих органических молекул. Фотосинтетическая ассимиляция диоксида углерода компенсируется его выделением в процессе дыхания, что способствует поддержанию природного равновесия. Однако не весь фиксированный диоксид углерода возвращается в атмосферу за счет дыхания. В анаэробной среде, например в болотах или на слабо освещенном дне стоячих водоемов, минерализация органики идет очень медленно, и она накапливается в виде ила или торфа. В определенных условиях через длительный период времени эти осадки могут образовать залежи ископаемого топлива.
В океанах основными механизмами поглощения диоксида углерода из атмосферы является фотосинтез, главным образом фитопланктонный, и растворение в поверхностных водах. Значительная часть этого связанного диоксида углерода быстро возвращается назад — непосредственно из раствора или в результате дыхания. Однако, как и в наземных экосистемах, некоторая доля углерода надолго задерживается, например при погружении холодных поверхностных вод в глубину или в составе образуемых морскими организмами карбонатных структур (раковин, кораллов и т. д.), которые со временем превращаются в горные породы типа известняка.
Скорость переноса углерода между его резервным и оборотным пулами может меняться из года в год в зависимости от климатических флуктуации. На этот баланс влияет также деятельность человека, особенно изменение землепользования (сведение леса или лесопосадки), использование ископаемого топлива и производство цемента. Судя по имеющимся данным, именно человек обусловливает значительный рост содержания диоксида углерода в атмосфере с эпохи промышленной революции.
Повышение скорости мобилизации углерода из его резервуаров типа ископаемого топлива и карбонатов (при производстве цемента) и потенциальное влияние этого ускорения на глобальный климат и экосистемы — весьма актуальные темы ведущихся сейчас экологических исследований и дебатов. Преобладает мнение, что сохранение нынешних темпов поступления в атмосферу диоксида углерода грозит весьма серьезными последствиями для всей планеты. Правительства предпринимают усилия к сокращению выбросов диоксида углерода промышленностью и масштабов использования ископаемого топлива в целом за счет более широкого применения альтернативных видов энергии, например солнечной и ветровой.
Аллотропные модификации
Общие сведения, аллотропия углерода Углерод (лат. carboneuia) известен с глубокой древности. В земной коре его содержится примерно 0,35% по массе. В природе углерод встречается в свободном и связанном состоянии, главным образом в виде карбонатов (мел, известняк, мрамор), в каменных и бурых углях, торфе. Углерод входит в состав нефти, природного газа, воздуха, растений, организмов человека и животных. Его соединения составляют основу живой природы — флоры и фауны. Атом углерода имеет 6 электронов, 2 на внутреннем слое (1s2), а 4 (2s22р2) — на внешнем. С наиболее активными металлами углерод проявляет степень окисления -4. Углерод способен соединяться между собой с образованием прочных длинных цепей. В отличие от кислорода и азота углерод при обычных условиях не образует молекул, у него атомная кристаллическая решетка. Существуют четыре аллотропных модификации углерода: алмаз, графит, карбин и букибол. Кристаллическая решетка алмаза состоит из атомов углерода, соединенных между собой очень прочными s-связями. В кристалле алмаза все связи эквивалентны и атомы образуют трехмерный каркас из сочлененных тетраэдров. Алмаз — самое твердое вещество, найденное в природе. Графит представляет собой темно-серое с металлическим блеском, мягкое, жирное на ощупь вещество. Хорошо проводит электрический ток. В графите атомы углерода расположены в параллельных слоях, образуя гексагональную сетку. Внутри слоя атомы связаны гораздо сильнее, чем один слой с другим, поэтому свойства графита сильно различаются по разным направлениям. Карбин — получен искусственным путем. Существует два вида карбина: поликумулен =С=С=С=С= и полиин -C=C-C=C-C=C-. Букибол — получен в 1985г., имеет сферическую форму (как футбольный мяч), состоит из 60 или 70 атомов углерода. Углерод в виде сажи, кокса, древесного угля, костных углей широко используется в металлургии, синтезе органических веществ, как топливо, в быту.
www.ronl.ru
Круговорот углерода в природе | Science Debate
Нужно отметить тот факт, что абсолютно вся жизнь на Земле имеет в своем основании химические элементы углеродного типа. Каждая составляющая, которая принадлежит живому организму, имеет строение скелета углеродного типа. Словом, углерод с нами везде и всюду.
К тому же, атомы, относящиеся, непосредственно, к углероду, непрерывно осуществляют миграцию из одной области биосферы, которая принадлежит более узкой оболочке земли и на которой есть жизнь, в совершенно иную. Если основываться на примерах, то круговорот представленного элемента в природе можно проконтролировать, но только на этапе динамики.
Наиболее важные и значимые запасы углерода представляются в виде диоксида углерода, которые, так или иначе распространены в атмосфере. Именно поэтому, стоит изучить все те составляющие углекислого газа, которые содержатся в атмосфере.
Важным этапом является то, что растения осуществляют процесс поглощения молекул, после чего и происходит превращение атома в самые разные воссоединения органического типа. Этот процесс является неотъемлемой частью структуры всех растений на земле.
Помимо всего этого, углерод способен оставаться и производить все важные процессы до тех пор, пока растение не придет к своему концу жизни. Как правило, в таком случае, все молекулы идут напрямую в пищу в виде редуцента. Стоит напомнить, что редуцент, в свою очередь, является тем организмом, который питается омертвевшими составляющими органического типа, после чего идет полное разрушение его до самых элементарных соединений антибазисной категории.
Так, на завершающем этапе, представленный химический элемент возвращается в среду в вариации газа углекислой категории. Обозначение, которого известно всем – общепринятая формула СО2.
Стоит не забывать о том, что растения могут быть поглощены животными травоядного класса. На таком этапе, элемент возвращается либо обратно в атмосферу, либо же животные травоядного класса подвергаются съедению более хищными видами фауны. В первом случае, процесс дыхания осуществляется тогда, когда животное разлагается на самом последнем этапе.
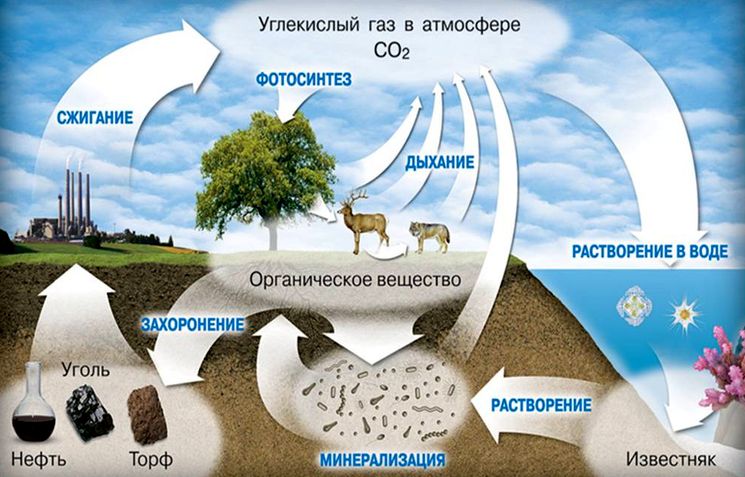
Второй процесс может быть осуществим только после того, как углерод возвратится сразу же в живую среду. Растения также могут просто погибнуть и в завершении, оказаться под земной корой. Если такой процесс все же осуществился, то растения преобразуются в топливо ископаемого типа, к примеру, в уголь.
Если же исходные элементы углекислого газа просто растворятся в воде морского типа, то может произойти следующее:
- Химический элемент возвращается обратно в живую среду. Именно эта вариация совместного обмена газами между океаном и атмосферой, происходит очень часто. Точно с таким же успехом, представленный химический элемент может войти в строение растений или же животного организма – обитателя морских просторов.
- В случае если химический элемент войдет в структуру отложений осадочного типа, то он просто вымоется из живой среды и не усвоится. В процессе всего того времени, пока существует планета Земля, углерод всегда замещался углекислым газом, который в свою очередь попадал в атмосферу при извержениях вулканического типа.
На сегодняшний день, ко всем перечисленным факторам прибавились еще и все те выбросы, которые непосредственно образуются при процессе сжигания топлива ископаемого класса. В последнее время ощутимым камнем преткновения является то, что правительства различных стран уже несколько лет пытаются прийти к международному соглашению в области выбросов углекислого газа.

Но ученые еще не могут быть уверены в том, что процесс накопления углекислого газа в живой среде можно приостановить одними лишь посадками растений и обширных лесопосадок. Надо отметить, что такой процесс как круговорот углерода в живой среде еще не является до конца открытым. Ученые постоянно работают над этим, и с каждым годом в науке происходят еще более удивительные открытия.
www.sciencedebate2008.com
|
|
..:::Счетчики:::.. |
|
|
|
|
|
|
|
|


