Контрольная работа по теме «Строение атома»
Автор: Кашутина Светлана Николаевна, учитель химии филиала МКОУ «Карачельская СОШ» Шумихинского района Курганской области- Стариковская средняя общеобразовательная школа
Контрольная работа № 1
Строение атома. Периодический закон и периодическая система химических элементов.
Цель:
Проверить знания обучающихся по теме «Строение атома. Периодический закон и периодическая система химических элементов»
Планируемые результаты Ученик научится:
1. Раскрывать смысл понятий «простое» и «сложное» вещество;
2.
Раскрывать физический смысл порядкового номера химического
элемента, номера группы и периода в периодической системе Д.
3. Определять состав веществ по их формулам;
4. Объяснять закономерности изменения строения атомов, свойства элементов в пределах малых периодов главных подгрупп;
5. Вычислять относительную молекулярную и молярную массы веществ;
6. Вычислять массовую долю химического элемента по формуле соединения;
7. Определять вид химической связи в неорганических соединениях;
8. Раскрывать смысл основных химических понятий «простое» и «сложное» вещество, «химический элемент»;
9. Характеризовать химические элементы на основе их положения в периодической системе Д.И.Менделеева и особенностей строения их атомов;
10. Составлять схемы строения атомов первых 20 элементов ПСХЭ Д.И.Менделеева.
Часть 1
А1.( 2 б.) Разделите модели
молекул, изображенные на рисунке на две равные группы. Назовите каждую группу.
Группа 1________________________________________________
Группа 2________________________________________________ Укажите признак, по которому проведено деление моделей на группы.
А.2 ( 1 б.) Пара химических элементов, имеющих на внешнем электронном слое по 7 электронов:
1. F и Cl 3. Al и Si
2. Li и Mg 4. C и P
А.3(2б) Укажите пары формул веществ, в которых молекулы имеют одинаковое число атомов, но различаются качественным составом.
1. СО и CO2 3. СН4 и CCl4
2. SO2 и CO2 4. N2O и NO2
А. 4 (1 б.)
Верны ли следующие высказывания?
А. В главной подгруппе
неметаллические свойства атомов элементов с увеличением порядкового номера
усиливаются.
Б. В периоде неметаллические свойства атомов химических элементов с увеличением порядкового номера усиливаются.
1. верно только А. 3. верны оба суждения
2. верно только Б 4. оба суждения неверны
А 5. (2 б.) Выберите формулу вещества с наименьшей относительной молекулярной массой
1. NH3 2.
Н2O 3. CO 4.O
Часть 2
В1.(2 б.) Установите соответствие между веществом и типом химической связи, при помощи которой оно образовано.
|
Тип химической связи |
Формула вещества |
|
А) металлическая |
1) Са |
|
Б) ковалентная полярная |
2) О2 |
В) ковалентная неполярная |
3) Н2S |
|
|
4) Cu |
|
|
5) Mg3N2 |
В. 2 ( 2 б.) В результате
возникновения ковалентной связи
2 ( 2 б.) В результате
возникновения ковалентной связи
1. Атомы завершают внешние энергетические уровни;
2. Атомы превращаются в заряженные частицы;
3. Происходит переход электронов от одного атома к другому; 4. Образуются общие электронные пары; 5.Образуется сложный ион.
Часть 3.
С.1 (4 б.) Составьте формулы и схемы образования одного простого и одного сложного вещества, используя два элемента третьего периода ( у одного из элементов во внешнем электронном слое атома содержится два электрона, у другого – семь).
С. 2 (3 б.) Для определения возраста археологических находок, ученые устанавливают в них содержание радиоактивного изотопа атома углерода 14С. Составьте схему электронного строения атома углерода 14С. Укажите состав атомного ядра и его электронной оболочки.
Критерии оценивания:
«2» — 0-35%
«3» — 36-61%
«4» — 62-85%
«5» — 86-100%
«2» — 0- 7 баллов
«3» — 8- 12 баллов
«4» — 13- 16 баллов
«5» — 17-19 баллов
|
№ задания |
Содержание верного ответа |
баллы |
|
А. |
Правильно разделено на группы. Указан признак по которому проведено деление на группы. |
1 балл 1 балл |
|
А.2 |
Выбрана правильно пара химических элементов |
1 балл |
|
А.3 |
Правильно выбраны две пары Правильно выбрана одна пара |
2 балла 1 балл |
|
А. 4 |
Выбран правильный ответ |
1 балл |
|
А. |
Правильно найдено вещество с наименьшей молекулярной массой |
2 балла |
|
В. 1 |
Задание выполнено верно Допущена 1 ошибка |
2 балла 1 балл |
|
В. 2 |
Задание выполнено верно Допущена 1 ошибка |
2 балла 1 балл |
|
С.1 |
Составлена одна формула Составлены две формулы Составлена одна схема образования вещества Составлены две схемы образования веществ |
1 балл 2 балла 1 балл 2 балла |
|
С. |
Составлена схема электронного строения атома Указано число протонов в ядре Указано число электронов |
1 балл 1 балл 1 балл |
|
всего |
|
19 баллов |
Контрольная работа по теме «Строение атома и типы химической связи»
Вариант 1.
ЧАСТЬ А (11 баллов)
1. Число протонов в атоме фосфора равно:
а) 3 б) 5 в) 15 г) 16
2. Число нейтронов в атоме хлора равно:
Число нейтронов в атоме хлора равно:
а) 7 б) 18 в) 19 г) 17
3. Число энергетических уровней в атоме магния равно:
а) 3 б) 2 в) 4 г) 1
4. Химический элемент ртуть находится в Периодической таблице Д. И Менделеева:
а) в шестом периоде, второй группе, главной подгруппе
б) во втором периоде, четвёртой группе, главной подгруппе
в) во втором периоде, четвёртой группе, побочной подгруппе
г) в шестом периоде, второй группе, побочной подгруппе
5. Число электронов на внешнем энергетическом уровне атома серы равно:
а) 3 б) 6 в) 32 г) 16
6. Строение внешнего энергетического уровня, выражаемое формулой …2s22p4 характерно для элемента:
а) кремния б) бора в) кислорода г) лития
7. Ряд химических элементов, в котором происходит уменьшение радиуса атома:
Ряд химических элементов, в котором происходит уменьшение радиуса атома:
а) углерод – бор – бериллий б) азот – фосфор — мышьяк
в) сера – фосфор — кремний г) алюминий – кремний – фосфор
8.Ряд химических элементов, в котором происходит уменьшение электроотрицательности:
а) бром-хлор-фтор б) бром-селен-мышьяк
в) кремний-фосфор-сера г) селен-сера-кислород
9. Вещества с ионным типом химической связи представлены в ряду:
а) NaCl, HCl, K2O б) N2, N2O3, Fe2O3 в) KCl, MgO, K2S г) CuS, CH4, CO2
10. Ковалентная полярная химическая связь образуется между элементами следующих веществ:
а) H2, H2O, NH3 б) NH3, K2S, CO2, в) CO2, NH3, H2O г) C, Cl2, N2
11. Верны ли следующие суждения:
Верны ли следующие суждения:
А) У химических элементов в главных подгруппах с увеличением порядкового номера металлические свойства ослабевают.
Б) Ковалентная неполярная химическая связь образуется между атомами разных неметаллов.
а) верно только А б) верно только Б в) верны оба суждения г) оба суждения неверны
ЧАСТЬ В (6 баллов)
1. Расположите элементы, символы которых приведены ниже в порядке уменьшения металлических свойств:
P, Cl, S, Na, Mg.
2. Установите соответствие:
- Вид химической связи
Химическое соединение
А. Ковалентная неполярная связь.
Б. Ионная связь.
В. Ковалентная полярная связь.
1. N2O5
2. CaCl2
3.
 Br2
Br24. K3P
5. HF
3. Установите соответствие:
- Электронная формула частицы (атом, ион)
Обозначение частицы (атом, ион)
А. 1s2
Б. 1s22s22p3
В. 1s22s22p6
Г. 1s22s2
1. N0
2. Na+
3. Li+
4. Na0
5.Be0
6. Ca2+
ЧАСТЬ С (5 баллов)
Составьте электронную и электронно-графическую формулы атома элемента под номером 16. Покажите распределение электронов по энергетическим уровням в атоме этого элемента. Какой тип связи будет характерен для химического соединения этого элемента с натрием? Приведите механизм образования этой связи.
Какой тип связи будет характерен для химического соединения этого элемента с натрием? Приведите механизм образования этой связи.
Вариант 2.
ЧАСТЬ А (11 баллов)
1. Число протонов в атоме азота равно:
а) 7 б) 5 в) 2 г) 14
2. Число нейтронов в атоме фосфора равно:
а) 10 б) 16 в) 31 г) 15
3. Число энергетических уровней в атоме серы равно:
а) 16 б) 2 в) 3 г) 6
4. Химический элемент медь находится в Периодической таблице Д. И Менделеева:
а) в четвертом периоде, первой группе, главной подгруппе
б) в первом периоде, четвёртой группе, главной подгруппе
в) в первом периоде, четвёртой группе, побочной подгруппе
г) в четвёртом периоде, первой группе, побочной подгруппе
5.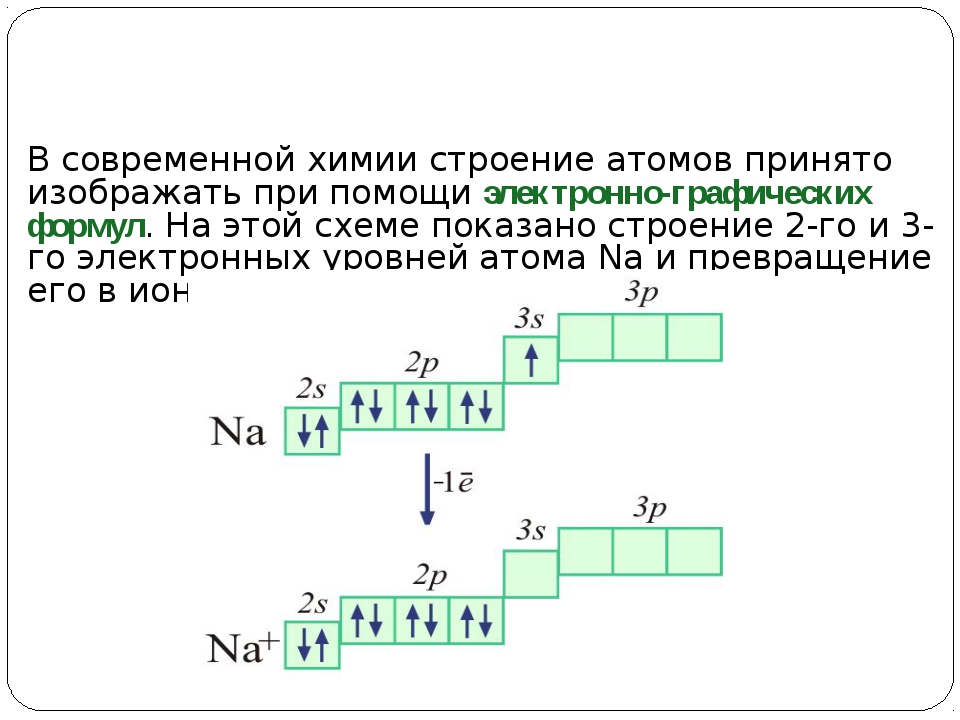 Число электронов на внешнем энергетическом уровне атома брома равно:
Число электронов на внешнем энергетическом уровне атома брома равно:
а) 3 б) 35 в) 7 г) 6
6. Строение внешнего энергетического уровня, выражаемое формулой …2s22p3 характерно для элемента:
а) фосфора б) азота в) кислорода г) натрия
7. Ряд химических элементов, в котором происходит увеличение радиуса атома:
а) калий – натрий – литий б) фосфор – сера — хлор
в) углерод – кремний — германий г) алюминий – кремний – фосфор
8.Ряд химических элементов, в котором происходит увеличение электроотрицательности:
а) фтор-хлор-бром б) бром-селен-мышьяк
в) магний-алюминий-кремний г) литий-натрий-калий
9. Вещества с ионным типом химической связи представлены в ряду:
а) AlCl3, HCl, H2O б) KCl, CO, Li2S в) N2, N2O, FeO г) CаS, MgO, CaCl2
10. Ковалентная полярная химическая связь образуется между элементами следующих веществ:
Ковалентная полярная химическая связь образуется между элементами следующих веществ:
а) N2, F2O, NH3 б) PH3, H2S, SO2, в) NO2, NH3, K2O г) P2O5, Cl2, Li2O
11. Верны ли следующие суждения:
А) У химических элементов в периодах с увеличением порядкового номера металлические свойства ослабевают.
Б) Ионная химическая связь возникает за счёт образования общих электронных пар.
а) верно только А б) верно только Б в) верны оба суждения г) оба суждения неверны
ЧАСТЬ В (6 баллов)
1. Расположите элементы, символы которых приведены ниже в порядке увеличения металлических свойств:
С, Be, Li, O, F.
2. Установите соответствие:
- Вид химической связи
Химическое соединение
А.
 Ковалентная неполярная связь.
Ковалентная неполярная связь.Б. Ионная связь.
В. Ковалентная полярная связь.
1. MgCl2
2. N2
3. H2
4. CO
5. K2O
3. Установите соответствие:
- Электронная формула частицы (атом, ион)
Обозначение частицы (атом, ион)
А. 1s22s22p1
Б. 1s22s22p63s23p6
В. 1s22s22p5
Г. 1s22s22p2
1. C0
2. Na+
3. Li+
4. F0
5.B0
6.
 Ca2+
Ca2+
ЧАСТЬ С (5 баллов)
Составьте электронную и электронно-графическую формулы атома элемента под номером 12. Покажите распределение электронов по энергетическим уровням в атоме этого элемента. Какой тип связи будет характерен для химического соединения этого элемента с фтором? Приведите механизм образования этой связи.
Вариант 3.
ЧАСТЬ А (11 баллов)
1. Число протонов в атоме натрия равно:
а) 12 б) 11 в) 23 г) 3
2. Число нейтронов в атоме аргона равно:
а) 18 б) 8 в) 22 г) 21
3. Число энергетических уровней в атоме хлора равно:
а) 7 б) 2 в) 3 г) 1
4. Химический элемент цинк находится в Периодической таблице Д. И Менделеева:
а) в четвертом периоде, второй группе, главной подгруппе
б) в первом периоде, четвёртой группе, главной подгруппе
в) в первом периоде, четвёртой группе, побочной подгруппе
г) в четвёртом периоде, второй группе, побочной подгруппе
5. Число электронов на внешнем энергетическом уровне калия равно:
Число электронов на внешнем энергетическом уровне калия равно:
а) 3 б) 4 в) 1 г) 5
6. Строение внешнего энергетического уровня, выражаемое формулой …3s23p3 характерно для элемента:
а) фосфора б) азота в) кислорода г) натрия
7. Ряд химических элементов, в котором происходит увеличение радиуса атома:
а) калий – натрий – литий б) азот – углерод — бор
в) германий – кремний -углерод г) алюминий – кремний – фосфор
8.Ряд химических элементов, в котором происходит увеличение электроотрицательности:
а) фтор-хлор-бром б) бром-селен-мышьяк
в) магний-алюминий-кремний г) литий-натрий-калий
9. Вещества с ионным типом химической связи представлены в ряду:
а) AlCl3, HCl, H2O б) KCl, MgO, Li2S в) N2, N2O, FeO г) CаS, CaCl2, CO
10. Ковалентная полярная химическая связь образуется между элементами следующих веществ:
Ковалентная полярная химическая связь образуется между элементами следующих веществ:
а) Н2, F2O, P2O5 б) PH3, H2S, K2O в) NO2, NH3,SO2, г) NH3, Cl2, Li2O
11. Верны ли следующие суждения:
А) У химических элементов в пределах периода с увеличением порядкового номера радиус атома уменьшается.
Б) Ковалентная химическая связь возникает за счёт образования общих электронных пар.
а) верно только А б) верно только Б в) верны оба суждения г) оба суждения неверны
ЧАСТЬ В (6 баллов)
1. Расположите элементы, символы которых приведены ниже в порядке увеличения металлических свойств:
Сs,Na, Li, Rb, K.
2. Установите соответствие:
- Вид химической связи
Химическое соединение
А.
 Ковалентная неполярная связь.
Ковалентная неполярная связь.Б. Ионная связь.
В. Ковалентная полярная связь.
1. HCl
2. F2
3. N2O
4. CaO
5. LiCl
3. Установите соответствие:
- Электронная формула частицы (атом, ион)
Обозначение частицы (атом, ион)
А. 1s22s22p2
Б. 1s22s22p63s23p6
В. 1s22s22p5
Г. 1s22s22p6
1. C0
2. Na+
3. Li+
4. F0
5.B0
6.
 Ca2+
Ca2+
ЧАСТЬ С (5 баллов)
Составьте электронную и электронно-графическую формулы атома элемента под номером 7. Покажите распределение электронов по энергетическим уровням в атоме этого элемента. Какой тип связи будет характерен для химического соединения этого элемента с натрием? Приведите механизм образования этой связи.
Вариант 4.
ЧАСТЬ А (11 баллов)
1. Число протонов в атоме серы равно:
а) 32 б) 6 в) 14 г) 16
2. Число нейтронов в атоме алюминия равно:
а) 27 б) 13 в) 14 г) 3
3. Число энергетических уровней в атоме кальция равно:
а) 4 б) 2 в) 3 г) 6
4. Химический элемент калий находится в Периодической таблице Д. И Менделеева:
а) в четвертом периоде, первой группе, главной подгруппе
б) в первом периоде, четвёртой группе, главной подгруппе
в) в первом периоде, четвёртой группе, побочной подгруппе
г) в четвёртом периоде, первой группе, побочной подгруппе
5. Число электронов на внешнем энергетическом уровне атома кремния равно:
Число электронов на внешнем энергетическом уровне атома кремния равно:
а) 3 б) 4 в) 14 г) 6
6. Строение внешнего энергетического уровня, выражаемое формулой …3s23p1 характерно для элемента:
а) фосфора б) алюминия в) бора г) серы
7. Ряд химических элементов, в котором происходит уменьшение радиуса атома:
а) кремний – алюминий – магний б) хлор– сера — фосфор
в) углерод – кремний — германий г) кальций – магний – бериллий
8.Ряд химических элементов, в котором происходит увеличение электроотрицательности:
а) фтор-хлор-бром б) бром-селен-мышьяк
в) магний-алюминий-кремний г) литий-натрий-калий
9. Вещества с ионным типом химической связи представлены в ряду:
а) СаBr2, MgCl2, Na2O б) KCl, CO, Li2S в) N2, N2O, FeO г) CаS, N2O, MgCl2
10. Ковалентная полярная химическая связь образуется между элементами следующих веществ:
Ковалентная полярная химическая связь образуется между элементами следующих веществ:
а) N2, F2O, NH3 б) PH3, H2S, SO2, в) NO2, NH3, K2O г) P2O5, Cl2, Li2O
11. Верны ли следующие суждения:
А) У химических элементов в группе с увеличением порядкового номера металлические свойства ослабевают.
Б) Ионная химическая связь возникает за счёт образования общих электронных пар.
а) верно только А б) верно только Б в) верны оба суждения г) оба суждения неверны
ЧАСТЬ В (6 баллов)
1. Расположите элементы, символы которых приведены ниже в порядке увеличения металлических свойств:
С, Be, Li, O, F.
2. Установите соответствие:
- Вид химической связи
Химическое соединение
А.
 Ковалентная неполярная связь.
Ковалентная неполярная связь.Б. Ионная связь.
В. Ковалентная полярная связь.
1. Cl2
2. Na2O
3. CaH2
4. CO
5. K2O
3. Установите соответствие:
- Электронная формула частицы (атом, ион)
Обозначение частицы (атом, ион)
А. 1s22s22p5
Б. 1s22s22p63s23p6
В. 1s22s22p3
Г. 1s2
1. C0
2. Cl0
3. Li+
4. F0
5.N0
6. Ca2+
ЧАСТЬ С (5 баллов)
Составьте электронную и электронно-графическую формулы атома элемента под номером 17. Покажите распределение электронов по энергетическим уровням в атоме этого элемента. Какой тип связи будет характерен для химического соединения этого элемента с магнием? Приведите механизм образования этой связи.
Покажите распределение электронов по энергетическим уровням в атоме этого элемента. Какой тип связи будет характерен для химического соединения этого элемента с магнием? Приведите механизм образования этой связи.
Ответы 8 класс Контрольная работа №1.
Контрольная работа «Атомы» (8 класс)
Контрольная работа №1.
«Атомы химических элементов, химическая связь».
по химии 8 класс
Вариант – I
А1. Каков заряд ядра атома хлора?
А) +24 Б) +17 В) +12 Г) -17
А2. Определите элемент, если в его атоме 33 электронов
А) алюминий Б) мышьяк В) германий Г) криптон
А3. Чему равняется количество протонов, нейтронов и электронов в атоме фосфора?
А) р=31, n=16, е=31 Б) р=15, n=15, е=15 В) р=15, n=31, е=15 Г) р=15, n=16, е=15
А4. Каков физический смысл порядкового номера элемента
Каков физический смысл порядкового номера элемента
А) это число энергетических уровней в атоме Б) это заряд ядра атома В) это относительная атомная масса Г) это число нейтронов в ядре
А5. Каков физический смысл номера периода таблицы Д.И.Менделеева?
А) это число энергетических уровней в атоме Б) это число электронов в атоме
В) это заряд ядра атома Г) это число электронов на внешнем энергетическом уровне
А6. Чему равно число электронов на внешнем энергетическом уровне атома
А) порядковому номеру Б) номеру группы
В) номеру периода Г) числу нейтронов в ядре
А7. Укажите количество электронов на внешнем энергетическом уровне в атоме хлора
А) 2 Б) 5 В) 7 Г) 17
А8. Укажите пару химических элементов, между которыми может возникнуть ковалентная неполярная связь
А) водород и хлор Б) калий и фтор В) азот и азот Г) кислород и натрий
А9. Укажите формулу соединения с ковалентной полярной связью
А) O3 Б) KCl2 В) HBr Г) PH3
А10.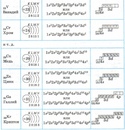 Атому, какого химического элемента соответствует электронная формула 1S22S22P4
Атому, какого химического элемента соответствует электронная формула 1S22S22P4
А) углерод Б) сера В) магний Г) кислород
А11. В ядре атома, какого химического элемента 19 протонов и 20 нейтронов
А) фтор Б) калий В) фосфор Г) кислород
А12. Какова относительная молекулярная масса вещества с химической формулой C2H2O4
А) 100 Б) 90 В) 56 Г) 124
В1. Установите соответствие между типом химической связи и формулой соединения
Вид химической связи
А) Ковалентная неполярная
Б) Ионная
В) Ковалентная полярная
Г) Металлическая
Химическое соединение
1) P2O5 2) KCl2
3) HF 4) O3
5) K3P 6) Zn
С1. Найдите массовую долю натрия в составе молекулы Na3PO4
С2. Определите тип химической связи и составьте схему образования связи у следующих веществ:
а) MgCl2 б) F2 в) h3S
Контрольная работа №1.
«Атомы химических элементов, химическая связь».
по химии 8 класс
Вариант – II
А1. Каков заряд ядра атома цезия?
А) -55 Б) +35 В) +55 Г) +30
А2. Определите элемент, если в его атоме 35 электронов
А) титан Б) хром В) марганец Г) бром
А3. Чему равняется количество протонов, нейтронов и электронов в атоме кальция?
А) р=20, n=40, е=20 Б) р=40, n=20, е=40 В) р=20, n=20, е=20 Г) р=40, n=40, е=40
А4. Каков физический смысл порядкового номера элемента
А) это число нейтронов в ядре Б) это число протонов в ядре атома В) это число энергетических уровней в атоме Г) это относительная атомная масса
А5. Каков физический смысл номера периода таблицы Д.И.Менделеева?
А) это заряд ядра атома Б) это число электронов на внешнем энергетическом уровне В) это число электронов в атоме Г) это число энергетических уровней в атоме
А6. Чему равно общее число электронов атома
Чему равно общее число электронов атома
А) номеру группы Б) номеру периода
В) порядковому номеру Г) числу нейтронов в ядре
А7. Укажите количество электронов на внешнем энергетическом уровне в атоме бериллия
А) 2 Б) 5 В) 7 Г) 17
А8. Укажите пару химических элементов, между которыми может возникнуть ионная связь
А) водород и кислород Б) фтор и углерод В) хлор и хлор Г) натрий и хлор
А9. Укажите формулу соединения с ковалентной неполярной связью
А) CF4 Б) H2 В) KBr Г) P2O5
А10. Атому, какого химического элемента соответствует электронная формула 1S22S22P3
А) литий Б) натрий В) калий Г) азот
А11. В ядре атома, какого химического элемента 7 протонов и 7 нейтронов
А) фтор Б) азот В) фосфор Г) кислород
А12. Какова относительная молекулярная масса вещества с химической формулой H2CrO4
А) 142 Б) 118 В) 150 Г) 124
В1. Установите соответствие между типом химической связи и формулой соединения
Установите соответствие между типом химической связи и формулой соединения
Вид химической связи
А) Ковалентная неполярная
Б) Ионная
В) Ковалентная полярная
Г) Металлическая
Химическое соединение
1) O2 2) Br2
3) Zn 4) MgCl2
5) CaO 6) HCl
С1. Найдите массовую долю калия в составе молекулы K2SiO3
С2. Определите тип химической связи и составьте схему образования связи у следующих веществ:
а) NaCl б) O2 в) HF
Контрольная работа по химии «Строение атомов химических элементов»
Контрольная работа по учебнику О.С. Габриеляна. Представлена в 2 вариантах.
Просмотр содержимого документа
«Контрольная работа по химии «Строение атомов химических элементов»»
Контрольная работа № 1 «Строение атомов химических элементов»
Вариант 1
1. Расположите химические элементы
Расположите химические элементы
А) в порядке возрастания неметаллических свойств P, Cl, Mg.
Б) в порядке возрастания неметаллических свойств Tl, Al, Ga.
2. Дайте характеристику химических элементов B, C, Si
по плану:
химический символ и название элемента.
порядковый номер.
номер периода, группы, главная или побочная подгруппа.
заряд ядра атома.
число протонов и нейтронов в ядре.
общее число электронов.
число энергетических уровней.
число электронов на внешнем энергетическом уровне.
схема строения атома.
свойства химического элемента (металлические или неметаллические).

3. Укажите тип химической связи в соединениях: O2, Na, HBr, NaF. Запишите схему образования одного вида связи (по выбору).
Контрольная работа № 1 «Строение атомов химических элементов»
Вариант 2
1. Расположите химические элементы
А) в порядке возрастания неметаллических свойств C, Be, N.
Б) в порядке возрастания неметаллических свойств Ba, Mg, Sr.
2. Дайте характеристику химических элементов O, S, Cl
по плану:
химический символ и название элемента.
порядковый номер.
номер периода, группы, главная или побочная подгруппа.
заряд ядра атома.
число протонов и нейтронов в ядре.
общее число электронов.

число энергетических уровней.
число электронов на внешнем энергетическом уровне.
схема строения атома.
свойства химического элемента (металлические или неметаллические).
3. Укажите тип химической связи в соединениях: H2O, F2, K, KCl. Запишите схему образования одного вида связи (по выбору).
Контрольная работа по теме Строение атома. Химическая связь
Муниципальное общеобразовательное бюджетное учреждение
«Гимназия № 5» г. Оренбург
Контрольная работа
по теме
«Строение атома.
Химическая связь»
8 класс
подготовила учитель химии
Сидоренко Светлана Викторовна
г. Оренбург
2017 г.
8 класс Контрольная работа № 1 по теме «Строение атома. Химическая связь»
Химическая связь»
вариант 1
№ 1
Определите число электронов, протонов и нейтронов в изотопах брома с массовыми числами 79 и 81.
№ 2
Запишите схемы строения атомов элементов с порядковыми номерами 10, 13, 16. Определите их принадлежность к металлам, неметаллам, благородным газам.
№ 3
Заполните таблицу
молекулярная формула(формульная единица) | вид связи | электронная формула, С.О.(для ИС) | структурная формула, С.О.(для КПС, КНС) |
F2 | |||
Na3P | |||
H2O |
№ 4
Составьте формулы бинарных веществ:
оксид кальция, хлорид натрия, оксид серы (VI), гидрид калия, сульфид железа (III), нитрид кальция, бромид бария.
№ 5
Определите степени окисления элементов, дайте названия веществам:
СaCl2—
Na2S-
MgО —
H3N-
N2О3—
№6
Вычислите количество вещества, объём, число молекул в порции азота N2 массой 56 г.
№7
Установите формулу вещества, применяемого для рентгеноскопии желудка. В его составе 58,8 % бария; 13,73 % серы; кислород.
______________________________________________________________________________________________
8 класс Контрольная работа № 1 по теме «Строение атома. Химическая связь»
вариант 2
№ 1
Определите число электронов, протонов и нейтронов в изотопах кальция с массовыми числами 40 и 42.
№ 2
Запишите схемы строения атомов элементов с порядковыми номерами 7, 18, 19. Определите их принадлежность к металлам, неметаллам, благородным газам.
№ 3
Заполните таблицу
молекулярная формула(формульная единица) | вид связи | электронная формула, С.О.(для ИС) | структурная формула, С.О.(для КПС, КНС) |
S2 | |||
CaCl2 | |||
HCl |
№ 4
Составьте формулы бинарных веществ:
оксид калия, хлорид кальция, оксид азота (V), гидрид лития, сульфид кремния (IV), нитрид кальция, бромид натрия.
№ 5
Определите степени окисления элементов, дайте названия веществам:
ВaCl2—
К2S-
Nа2О —
H2S —
NО2—
№6
Вычислите количество вещества, объём, число молекул в порции азота N2 массой 84 г.
№7
Установите формулу вещества, применяемого для лечения кожных заболеваний. В его составе 63,53 % серебра; 8,24 % азота; кислород.
Список использованной литературы
Габриелян О.С., Яшукова А.В. Химия. 8 класс. Учебник — М.: Дрофа, 2013.
Габриелян О.С., Яшукова А.В. Химия. 8 класс. Рабочая тетрадь к учебнику О.С.Габриеляна «Химия. 8» — М.: Дрофа, 2013.
Габриелян О.С., Яшукова А.В. Химия. 8 — 9 классы. Методическое пособие — М.: Дрофа, 2004.
Контрольная работа «Строение атома. Периодический закон и Периодическая система химических элементов Д.И. Менделеева. Строение вещества. Окислительно-восстановительные реакции.
 » 8 класс
» 8 классХимия. 8 класс. Тематическая контрольная работа | 0 |
Контрольная работа по ХИМИИ
по теме: «Строение атома. Периодический закон и Периодическая система химических элементов Д.И. Менделеева. Строение вещества.
Окислительно-восстановительные реакции.»
8 класс
II вариант
Инструкция по выполнению работы
На выполнение работы по химии отводится 40 минут. Работа состоит из двух частей и включает в себя 15 заданий.
Ответы к заданиям 1–12 записываются в виде одной цифры, которая соответствует номеру правильного ответа. Эту цифру запишите в поле ответа в тексте работы, а затем перенесите в бланк ответов № 1.
Ответом к заданиям 13–14 является последовательность цифр. Ответ запишите в поле ответа в тексте работы, а затем перенесите в бланк ответов № 1.
На задание 15 следует дать полный развёрнутый ответ.
При выполнении заданий можно пользоваться черновиком. Записи в черновике не учитываются при оценивании работы.
Советуем выполнять задания в том порядке, в котором они даны. Для экономии времени пропускайте задание, которое не удаётся выполнить сразу, и переходите к следующему. Если после выполнения всей работы у Вас останется время, то можно вернуться к пропущенным заданиям.
Баллы, полученные Вами за все выполненные задания, суммируются. Постарайтесь выполнить как можно больше заданий и набрать наибольшее количество баллов.
Желаем успеха!
Ответом к заданиям 1–12 является одна цифра, которая соответствует номеру правильного ответа. Запишите эту цифру в поле ответа в тексте работы, а затем перенесите в бланк ответов № 1 справа от номера соответствующего задания.
Запишите эту цифру в поле ответа в тексте работы, а затем перенесите в бланк ответов № 1 справа от номера соответствующего задания.
1
Какому химическому элементу она соответствует?
1) магния
2) кальция
3) лития
4) калия
2
1) и
2) и
3) и
4) и
3
1) общее число электронов
2) число завершенных энергетических уровней
3) число электронов на внешнем уровне
4) число протонов в ядре
4
1) алюминий → фосфор → хлор
2) фтор → азот → углерод
3) хлор → бром → иод
4) кремний → сера → фосфор
5
1) усиливаются неметаллические свойства
2) уменьшаются металлические свойства
3) изменяется валентность в водородных соединениях
4) остается постоянной высшая валентность
6
1) кальция
2) бериллия
3) калия
4) бария
7
1) хлороводороде
2) гидроксиде натрия
3) оксиде углерода(II)
4) оксиде углерода(IV)
8
1)
2)
3)
4)
9
1) оксида кальция
2) хлорида лития
3) натрия
4) серы
10
1)
2)
3)
4)
11
1)
2)
3)
4)
12
1)
2)
3)
4)
При выполнении задания 13 из предложенного перечня ответов выберите два правильных и запишите цифры, под которыми они указаны. Получившуюся последовательность цифр запишите в бланк ответов № 1 справа от номера соответствующего задания, начиная с первой клеточки, без пробелов, запятых и других дополнительных символов.
Получившуюся последовательность цифр запишите в бланк ответов № 1 справа от номера соответствующего задания, начиная с первой клеточки, без пробелов, запятых и других дополнительных символов.
В ряду химических элементов уменьшается
1) заряд ядра атома
2) радиус атома
3) электроотрицательность элемента
4) валентность в летучем водородном соединении
5) число заполненных электронами энергетических уровней
13
При выполнении задания 14 к каждому элементу первого столбца подберите соответствующий элемент из второго столбца. Выбранные цифры запишите под соответствующими буквами таблицы. Цифры в ответе могут повторяться. Получившуюся последовательность цифр запишите в бланк ответов № 1 справа от номера соответствующего задания, начиная с первой клеточки, без пробелов, запятых и других дополнительных символов.
14
СХЕМА РЕАКЦИИ | ВОССТАНОВИТЕЛЬ |
A) | 1) |
Б) | 2) |
B) | 3) |
4) | |
5) |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Для задания 15 запишите в поле ответа в тексте работы полный развёрнутый ответ, включающий необходимые уравнения реакций и расчёты. Ответы записывайте чётко и разборчиво.
Используя метод электронного баланса, составьте уравнение реакции, соответствующее схеме превращений
Определите окислитель и восстановитель.
15
Ответы к заданиям
№ задания | Ответ |
1 | 1 |
2 | 2 |
3 | 2 |
4 | 1 |
5 | 4 |
6 | 2 |
7 | 2 |
8 | 3 |
9 | 4 |
10 | 3 |
11 | 1 |
12 | 2 |
13 | 24 |
14 | 245 |
Критерии оценивания задания с развёрнутым ответом
15
Определите окислитель и восстановитель.
Содержание верного ответа и указания по оцениванию (допускаются иные формулировки ответа, не искажающие его смысла) | Баллы |
1) Составлен электронный баланс: 2) Определён окислитель и восстановитель: — окислитель, — восстановитель. 3) Составлено уравнение реакции: | |
Ответ правильный и полный, включает все названные элементы. | 3 |
В ответе допущена ошибка только в одном из элементов. | 2 |
В ответе допущены ошибки в двух элементах. | 1 |
Все элементы ответа записаны неверно | 0 |
Максимальный балл | 3 |
2017 г.
контрольная работа «Строение атома. Периодический закон Д.И.Менделеева. Строение вещества.» | Методическая разработка по химии (8 класс):
По теме: методические разработки, презентации и конспекты
ЕГЭ тест по теме «Периодический закон Д.И.Менделеева и строение атома»; Тема «Электроотрицательность», «Строение вещества»Тесты по основным темам ЕГЭ…
Контрольная работа №1 по темам «Строение атома. Периодический закон Д.И.Менделеева»Контрольная работа №1по темам «Строение атома. Периодический закон Д.И.Менделеева».11 класс, базовый уровень…
Тест по теме «Строение атома. Периодический закон Д.И.Менделеева» (8 класс)
Периодический закон Д.И.Менделеева» (8 класс)Предлагаемый тест может быть использован восьмиклассниками для самопроверки знаний и самоконтроля при завершении изучения данной темы….
Подготовка к контрольной работе 11 класс по теме: Строение атома. периодический закон Д.И.Менделеева, учебник О.С.ГабриелянВариант контрольной работы для подготовки учащихся к контролю знаний по теме: Строение атома.Периодический закон Д.И.Менделеева…
Строение атома. Периодический закон Д.И. МенделееваВ соответствии с программой О.С. Габриеляна на тему «Атомы химических элементов» отводится 11 часов.Учащиеся должны:Знать Определение понятия «химический элемент», формулировку Периодического закона.У…
Кроссворды по темам «Периодический закон Д.И.Менделеева. Строение атома.» и «Химическая связь. Строение вещества.»Предлагаемые кроссворды могут быть использованы при проведении предметной недели, при обобщении темы или в качестве индивидуального задания ученику. Кроссворды составлены в трех вариантах (на одном ма…
Кроссворды составлены в трех вариантах (на одном ма…
В соответствии с программой О.С. Габриеляна на тему «Атомы химических элементов» отводится 11 часов.Учащиеся должны:Знать Определение понятия «химический элемент», формулировку…
Тест по химии атомной структуры
1. Атом бериллия имеет 4 протона, 5 нейтронов и 4 электрона. Какое массовое число у этого атома?
Верный Неправильный
Массовое число — это количество протонов и нейтронов в ядре. Для этого вопроса вы добавляете 4 протона и 5 нейтронов, чтобы получить ответ 9.
2. Наименьшее главное квантовое число для электрона:
Верный Неправильный
Главное квантовое число указывает размер электронной орбитали.Он имеет положительное целочисленное значение, но никогда не может быть 0. Итак, наименьшее число — 1.
3. Символ электронной точки для элемента показывает символ этого элемента и расположение точек, обозначающее:
Верный Неправильный
Структура Льюиса или структура электронных точек показывает несвязанные электронные пары. Несвязанные электроны — это валентные электроны или электроны во внешней электронной оболочке.
Несвязанные электроны — это валентные электроны или электроны во внешней электронной оболочке.
4. Наиболее распространенная степень окисления кремния в соединении:
.Верный Неправильный
Существует набор правил, используемых для определения степени окисления.Степень окисления свободного элемента всегда равна нулю, но поскольку этот вопрос касается кремния в соединении, вы смотрите на количество электронов, необходимое для заполнения его валентной оболочки. Вы можете понять это по электронной конфигурации. Позиция в таблице Менделеева тоже обычно дает ответ. Кремний находится в той же группе, что и углерод. Кремний обычно показывает степень окисления +4.
5. На каком подуровне может находиться максимум 10 электронов?
Верный Неправильный
Есть удобная диаграмма, которую вы можете нарисовать, чтобы выяснить конфигурацию электронов, так что вам не нужно их запоминать.На подуровне s 2 электрона, на подуровне p — 6, на подуровне d — 10 и на подуровне f — 14.
6. Две основные части атома:
Верный Неправильный
Две части атома — это его ядро, которое состоит из протонов и нейтронов, и электроны, вращающиеся вокруг ядра.
7. Какой элемент с наибольшей вероятностью образует ковалентное соединение?
Верный Неправильный
Двумя основными типами химических связей являются ионные и ковалентные связи.Металлы имеют тенденцию к образованию ионных связей. Неметаллы с большей вероятностью образуют ковалентные связи. Вы можете предсказать, будут ли два атома образовывать ионные или ковалентные связи, сравнив разницу между их значениями электроотрицательности. Углерод — единственный неметалл, упомянутый в вопросе.
8. Электронная точечная диаграмма хлора представляет собой Cl, окруженный семью точками. Атом с идентичным расположением имеет атомный номер:
.Верный Неправильный
Электронно-точечная структура зависит от количества валентных электронов.Чтобы ответить на вопрос, вам нужно знать электронную конфигурацию атомов, чтобы увидеть, какой из них имеет 7 несвязанных электронов, например хлор. Фтор, элемент номер 9, имеет 2 электрона на s-подуровне (оболочка K). L-оболочка заполнена не полностью, 7 электронов.
Фтор, элемент номер 9, имеет 2 электрона на s-подуровне (оболочка K). L-оболочка заполнена не полностью, 7 электронов.
9. Орбитали не заняты:
Верный Неправильный
Если у вас возникли проблемы с этим вопросом, вы можете рассмотреть квантовые числа и электронные орбитали. Орбитали никогда не содержат 3 электрона.
10. Число орбиталей на втором основном энергетическом уровне атома (n = 2) равно:
Верный Неправильный
Это еще один вопрос, связанный с квантовыми числами. Если n = 2, то может быть 4 орбитали (1 с орбиталь и 3 p орбитали).
Тест по химии атомной структуры
Вы получили:% Верно. Атомная бомба
Вы провалили викторину по атомной структуре. Это как атомная бомба, только разное .. FPG / Getty ImagesВы провалили викторину, но она не для оценки, так что не волнуйтесь! Кроме того, вы многому научились, просто пройдя тест.
Если вы серьезно относитесь к изучению атомов, начните с изучения основ. Вы также можете пройти викторину по основам атома, чтобы убедиться, что вы знаете основы строительных блоков материи.
Вы также можете пройти викторину по основам атома, чтобы убедиться, что вы знаете основы строительных блоков материи.
Поделитесь своими результатами
Тест по химии атомной структуры
Вы получили:% Верно. Ноу-хау по средней атомной структуре
Вы приобретаете знания об атомной структуре .. Креатив из бумажного кораблика / Getty ImagesХотя вы знакомы с некоторыми аспектами атомной структуры, вы еще не определились с деталями.Отсюда вы можете просмотреть общие темы по химии или переключить передачи и пройти тест, чтобы узнать, насколько хорошо вы знаете общие научные мелочи.
Поделитесь своими результатами
Тест по химии атомной структуры
Вы получили:% Верно. Плюс в атомной теории
Вы много знаете об атомной структуре .. АЛЬФРЕД ПАСЬЕКА / Getty Images Отличная работа! Вы хорошо справились с викториной по атомной структуре. Готовы к еще одной викторине? Посмотрите, насколько хорошо вы справитесь с 20 вопросами химического теста. Готовы к чему-то другому? Узнайте интересные факты о науке.
Готовы к чему-то другому? Узнайте интересные факты о науке.
Поделитесь своими результатами
Структура атома
Обзор атомной структуры
Атомы состоят из частиц, называемых протонами, нейтронами и электронами, которые отвечают за массу и заряд атомов.
Задачи обучения
Обсудить электронные и структурные свойства атома
Основные выводы
Ключевые моменты
- Атом состоит из двух областей: ядра, которое находится в центре атома и содержит протоны и нейтроны, и внешней области атома, которая удерживает свои электроны на орбите вокруг ядра.
- Протоны и нейтроны имеют примерно одинаковую массу, около 1,67 × 10-24 грамма, которую ученые определяют как одну атомную единицу массы (а.е.м.) или один дальтон.
- Каждый электрон имеет отрицательный заряд (-1), равный положительному заряду протона (+1).
- Нейтроны — это незаряженные частицы, находящиеся в ядре.
Ключевые термины
- атом : Наименьшее возможное количество вещества, которое все еще сохраняет свою идентичность как химический элемент, состоящее из ядра, окруженного электронами.

- протон : положительно заряженная субатомная частица, составляющая часть ядра атома и определяющая атомный номер элемента. Он весит 1 а.е.м.
- нейтрон : субатомная частица, составляющая часть ядра атома. Это бесплатно. По массе он равен протону или весит 1 а.е.м.
Атом — это наименьшая единица вещества, которая сохраняет все химические свойства элемента. Атомы объединяются в молекулы, которые затем взаимодействуют с образованием твердых тел, газов или жидкостей.Например, вода состоит из атомов водорода и кислорода, которые объединились, чтобы сформировать молекулы воды. Многие биологические процессы посвящены расщеплению молекул на составляющие их атомы, чтобы из них можно было собрать более полезную молекулу.
Атомные частицы
Атомы состоят из трех основных частиц: протонов, электронов и нейтронов. Ядро (центр) атома содержит протоны (положительно заряженные) и нейтроны (без заряда). Внешние области атома называются электронными оболочками и содержат электроны (отрицательно заряженные). Атомы имеют разные свойства в зависимости от расположения и количества их основных частиц.
Атомы имеют разные свойства в зависимости от расположения и количества их основных частиц.
Атом водорода (H) содержит только один протон, один электрон и не содержит нейтронов. Это можно определить, используя атомный номер и массовое число элемента (см. Понятие атомных номеров и массовых чисел).
Структура атома : Изображенные здесь элементы, такие как гелий, состоят из атомов. Атомы состоят из протонов и нейтронов, расположенных внутри ядра, а электроны находятся на орбиталях, окружающих ядро.
Атомная масса
Протоны и нейтроны имеют примерно одинаковую массу, примерно 1,67 × 10 -24 грамма. Ученые определяют это количество массы как одну атомную единицу массы (а.е.м.) или один дальтон. Протоны схожи по массе, но заряжены положительно, а нейтроны не имеют заряда. Следовательно, количество нейтронов в атоме существенно влияет на его массу, но не на его заряд.
Электроны по массе намного меньше протонов, их вес составляет всего 9 единиц. 11 × 10 -28 грамма, или примерно 1/1800 атомной единицы массы. Следовательно, они не вносят большой вклад в общую атомную массу элемента. При рассмотрении атомной массы принято игнорировать массу любых электронов и вычислять массу атома, исходя только из числа протонов и нейтронов.
11 × 10 -28 грамма, или примерно 1/1800 атомной единицы массы. Следовательно, они не вносят большой вклад в общую атомную массу элемента. При рассмотрении атомной массы принято игнорировать массу любых электронов и вычислять массу атома, исходя только из числа протонов и нейтронов.
Электроны вносят большой вклад в заряд атома, поскольку каждый электрон имеет отрицательный заряд, равный положительному заряду протона. Ученые определяют эти обвинения как «+1» и «-1».В незаряженном нейтральном атоме количество электронов, вращающихся вокруг ядра, равно количеству протонов внутри ядра. В этих атомах положительный и отрицательный заряды нейтрализуют друг друга, в результате чего получается атом без чистого заряда.
Протоны, нейтроны и электроны : Протоны и нейтроны имеют массу 1 а.е.м. и находятся в ядре. Однако протоны имеют заряд +1, а нейтроны не заряжены. Электроны имеют массу примерно 0 а.е.м., вращаются вокруг ядра и имеют заряд -1.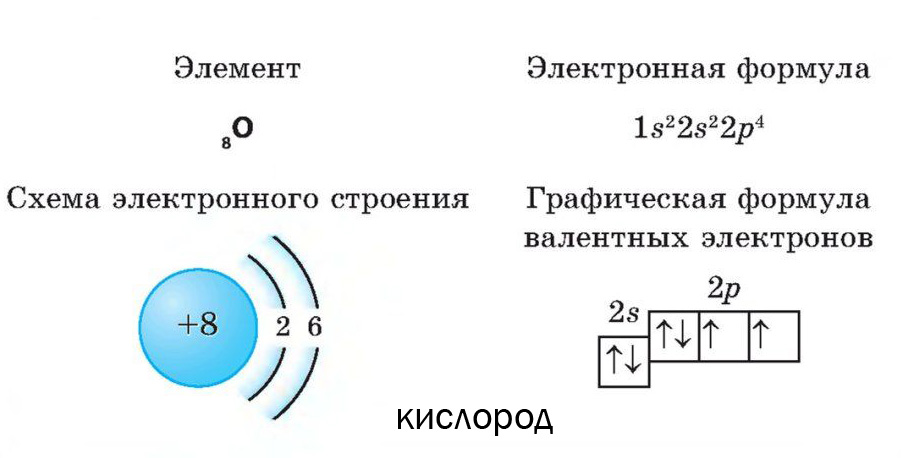
Изучение свойств электрона : Сравните поведение электронов с поведением других заряженных частиц, чтобы обнаружить такие свойства электронов, как заряд и масса.
Объем атомов
С учетом размеров протонов, нейтронов и электронов большая часть объема атома — более 99 процентов — фактически является пустым пространством. Несмотря на все это пустое пространство, твердые объекты не проходят сквозь друг друга. Электроны, окружающие все атомы, заряжены отрицательно и заставляют атомы отталкиваться друг от друга, не позволяя атомам занимать одно и то же пространство.Эти межмолекулярные силы не позволяют вам провалиться сквозь такой предмет, как стул.
Interactive: создайте атом : создайте атом из протонов, нейтронов и электронов и посмотрите, как изменяются элемент, заряд и масса. Тогда сыграйте в игру, чтобы проверить свои идеи!
Атомный номер и массовое число
Атомный номер — это количество протонов в элементе, а массовое число — это количество протонов плюс количество нейтронов.
Задачи обучения
Определите соотношение между массовым числом атома, его атомным номером, его атомной массой и количеством субатомных частиц.
Основные выводы
Ключевые моменты
- Нейтральные атомы каждого элемента содержат равное количество протонов и электронов.
- Число протонов определяет атомный номер элемента и используется, чтобы отличить один элемент от другого.
- Число нейтронов варьируется, в результате чего образуются изотопы, которые представляют собой разные формы одного и того же атома, которые различаются только количеством нейтронов, которыми они обладают.
- Вместе количество протонов и количество нейтронов определяют массовое число элемента.
- Поскольку изотопы элемента имеют несколько разные массовые числа, атомная масса рассчитывается путем получения среднего массового числа его изотопов.
Ключевые термины
- массовое число : сумма количества протонов и количества нейтронов в атоме.
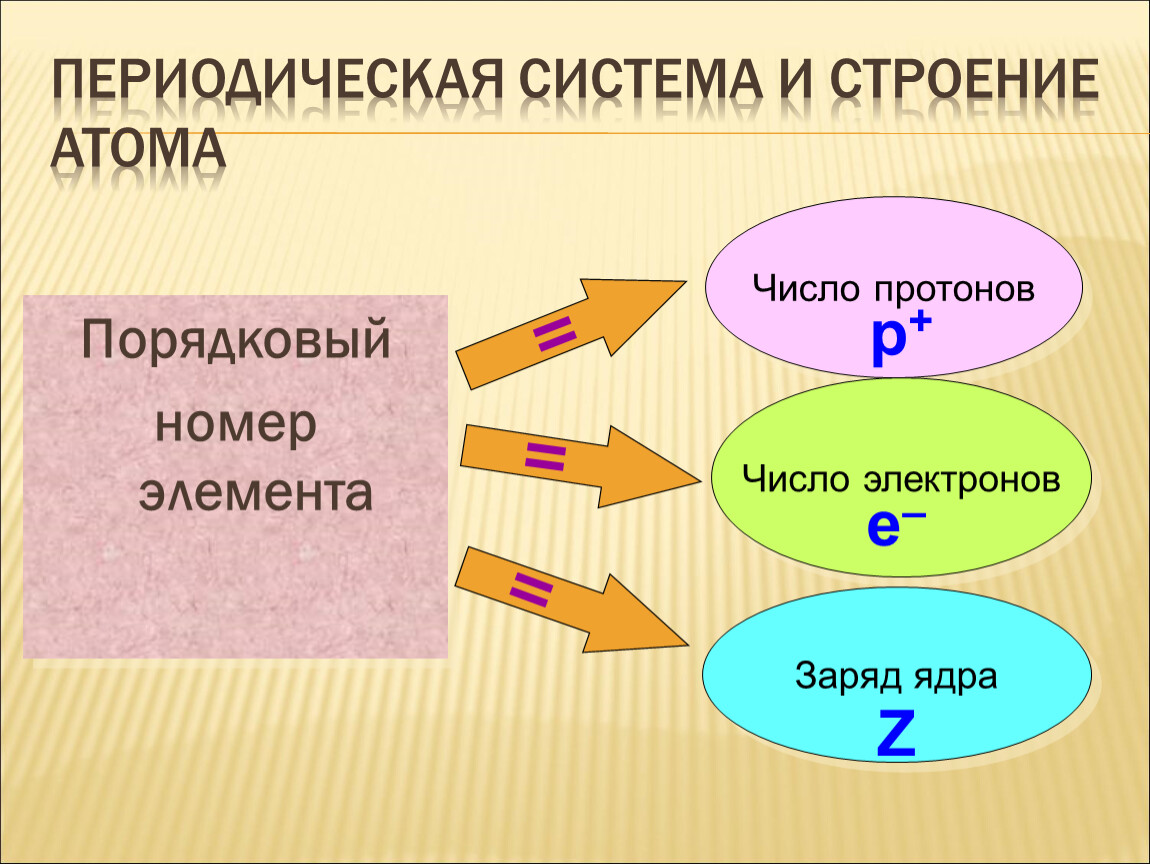
- атомный номер : число протонов в атоме.
- атомная масса : средняя масса атома с учетом всех его встречающихся в природе изотопов.
Атомный номер
Нейтральные атомы элемента содержат равное количество протонов и электронов. Число протонов определяет атомный номер элемента (Z) и отличает один элемент от другого. Например, атомный номер углерода (Z) равен 6, потому что у него 6 протонов. Количество нейтронов может изменяться для получения изотопов, которые представляют собой атомы одного и того же элемента, имеющие разное количество нейтронов.Число электронов также может быть различным в атомах одного и того же элемента, в результате чего образуются ионы (заряженные атомы). Например, железо Fe может существовать в нейтральном состоянии или в ионных состояниях +2 и +3.
Массовое число
Массовое число элемента (A) — это сумма количества протонов и количества нейтронов. Небольшой вклад массы электронов не учитывается при вычислении массового числа. Это приближение массы можно использовать, чтобы легко вычислить, сколько нейтронов имеет элемент, просто вычтя количество протонов из массового числа.Протоны и нейтроны весят около одной атомной единицы массы или а.е.м. Изотопы одного и того же элемента будут иметь одинаковый атомный номер, но разные массовые числа.
Это приближение массы можно использовать, чтобы легко вычислить, сколько нейтронов имеет элемент, просто вычтя количество протонов из массового числа.Протоны и нейтроны весят около одной атомной единицы массы или а.е.м. Изотопы одного и того же элемента будут иметь одинаковый атомный номер, но разные массовые числа.
Атомный номер, химический символ и массовое число : Углерод имеет атомный номер шесть и два стабильных изотопа с массовыми числами двенадцать и тринадцать соответственно. Его средняя атомная масса 12,11.
Ученые определяют атомную массу, вычисляя среднее значение массовых чисел естественных изотопов.Часто полученное число содержит десятичную дробь. Например, атомная масса хлора (Cl) составляет 35,45 а.е.м., потому что хлор состоит из нескольких изотопов, некоторые (большинство) с атомной массой 35 а.е.м. (17 протонов и 18 нейтронов), а некоторые с атомной массой 37 а.е.м. (17 протонов и 20 нейтронов).
Зная атомный номер (Z) и массовое число (A), вы можете найти количество протонов, нейтронов и электронов в нейтральном атоме. Например, атом лития (Z = 3, A = 7 а.е.м.) содержит три протона (находится из Z), три электрона (поскольку количество протонов равно количеству электронов в атоме) и четыре нейтрона (7 — 3 = 4).
Например, атом лития (Z = 3, A = 7 а.е.м.) содержит три протона (находится из Z), три электрона (поскольку количество протонов равно количеству электронов в атоме) и четыре нейтрона (7 — 3 = 4).
Изотопы
Изотопы — это различные формы элементов, которые имеют одинаковое количество протонов, но разное количество нейтронов.
Задачи обучения
Обсудить свойства изотопов и их использование в радиометрическом датировании
Основные выводы
Ключевые моменты
- Изотопы — это атомы одного и того же элемента, содержащие одинаковое количество протонов, но разное количество нейтронов.
- Несмотря на разное количество нейтронов, изотопы одного и того же элемента имеют очень похожие физические свойства.
- Некоторые изотопы нестабильны и подвергаются радиоактивному распаду, чтобы превратиться в другие элементы.
- Предсказуемый период полураспада различных распадающихся изотопов позволяет ученым датировать материал на основе его изотопного состава, например, с помощью датировки углерода-14.

Ключевые термины
- изотоп : Любая из двух или более форм элемента, в которых атомы имеют одинаковое количество протонов, но разное количество нейтронов в их ядрах.
- период полураспада : время, за которое половина исходной концентрации изотопа распадается обратно в более стабильную форму.
- радиоактивные изотопы : атом с нестабильным ядром, характеризующийся избыточной доступной энергией, который подвергается радиоактивному распаду и чаще всего создает гамма-лучи, альфа- или бета-частицы.
- радиоуглеродное датирование : Определение возраста объекта путем сравнения отношения обнаруженной в нем концентрации 14C к количеству 14C в атмосфере.
Что такое изотоп?
Изотопы — это различные формы элементов, которые имеют одинаковое количество протонов, но разное количество нейтронов. Некоторые элементы, такие как углерод, калий и уран, содержат несколько изотопов природного происхождения. Изотопы определяются сначала их элементом, а затем суммой присутствующих протонов и нейтронов.
Изотопы определяются сначала их элементом, а затем суммой присутствующих протонов и нейтронов.
- Углерод-12 (или 12 C) содержит шесть протонов, шесть нейтронов и шесть электронов; следовательно, он имеет массовое число 12 а.е.м. (шесть протонов и шесть нейтронов).
- Углерод-14 (или 14 C) содержит шесть протонов, восемь нейтронов и шесть электронов; его атомная масса 14 а.е.м. (шесть протонов и восемь нейтронов).
Хотя масса отдельных изотопов разная, их физические и химические свойства в основном не меняются.
Изотопы действительно различаются по стабильности. Углерод-12 ( 12 C) — самый распространенный изотоп углерода, составляющий 98,89% углерода на Земле. Углерод-14 ( 14 C) нестабилен и встречается только в следовых количествах.Нестабильные изотопы чаще всего испускают альфа-частицы (He 2+ ) и электроны. Также могут испускаться нейтроны, протоны и позитроны, а электроны могут быть захвачены для достижения более стабильной атомной конфигурации (более низкого уровня потенциальной энергии) посредством процесса, называемого радиоактивным распадом. Созданные новые атомы могут находиться в состоянии высокой энергии и испускать гамма-лучи, которые понижают энергию, но сами по себе не превращают атом в другой изотоп. Эти атомы называются радиоактивными изотопами или радиоизотопами.
Созданные новые атомы могут находиться в состоянии высокой энергии и испускать гамма-лучи, которые понижают энергию, но сами по себе не превращают атом в другой изотоп. Эти атомы называются радиоактивными изотопами или радиоизотопами.
Радиоуглеродное датирование
Углерод обычно присутствует в атмосфере в виде газообразных соединений, таких как диоксид углерода и метан. Углерод-14 ( 14 C) представляет собой радиоизотоп природного происхождения, который создается из атмосферного 14 N (азота) в результате добавления нейтрона и потери протона, вызванной космическими лучами. Это непрерывный процесс, поэтому в атмосфере всегда образуется больше 14 C. После производства 14 C часто соединяется с кислородом атмосферы с образованием диоксида углерода.Образовавшийся таким образом углекислый газ диффундирует в атмосфере, растворяется в океане и попадает в организм растений посредством фотосинтеза. Животные поедают растения, и в конечном итоге радиоуглерод распространяется по биосфере.
В живых организмах относительное количество 14 C в их теле примерно равно концентрации 14 C в атмосфере. Когда организм умирает, он больше не поглощает 14 C, поэтому соотношение между 14 C и 12 C будет снижаться, поскольку 14 C постепенно возвращается к 14 N.Этот медленный процесс, который называется бета-распадом, высвобождает энергию за счет испускания электронов из ядра или позитронов.
Примерно через 5730 лет половина исходной концентрации 14 C будет преобразована обратно в 14 Н. Это называется периодом полураспада или временем, которое требуется для получения половины исходной концентрации вещества. изотоп, чтобы вернуться в более стабильную форму. Поскольку период полураспада 14 C большой, он используется для датирования ранее живых объектов, таких как старые кости или дерево.Сравнивая отношение концентрации 14 C, обнаруженной в объекте, к количеству 14 C в атмосфере, можно определить количество еще не распавшегося изотопа. На основе этого количества можно точно рассчитать возраст материала, если предполагается, что возраст материала составляет менее 50 000 лет. Этот метод называется радиоуглеродным датированием, или сокращенно углеродным датированием.
На основе этого количества можно точно рассчитать возраст материала, если предполагается, что возраст материала составляет менее 50 000 лет. Этот метод называется радиоуглеродным датированием, или сокращенно углеродным датированием.
Применение углеродного датирования : Возраст углеродсодержащих останков менее 50 000 лет, таких как этот карликовый мамонт, можно определить с помощью углеродного датирования.
Другие элементы имеют изотопы с разным периодом полураспада. Например, 40 K (калий-40) имеет период полураспада 1,25 миллиарда лет, а 235 U (уран-235) имеет период полураспада около 700 миллионов лет. Ученые часто используют эти другие радиоактивные элементы для датирования объектов, возраст которых превышает 50 000 лет (предел углеродного датирования). Используя радиометрическое датирование, ученые могут изучать возраст окаменелостей или других останков вымерших организмов.
2.2: Структура атома и как мы ее представляем
Развитие современной атомной теории многое раскрыло о внутренней структуре атомов. Стало известно, что атом содержит очень маленькое ядро, состоящее из положительно заряженных протонов и незаряженных нейтронов, окруженное гораздо большим объемом пространства, содержащим отрицательно заряженные электроны. Ядро содержит большую часть массы атома, потому что протоны и нейтроны намного тяжелее электронов, тогда как электроны занимают почти весь объем атома.Диаметр атома составляет порядка 10 −10 м, тогда как диаметр ядра примерно 10 −15 м — примерно в 100 000 раз меньше. Чтобы получить представление об их относительных размерах, рассмотрим следующее: если бы ядро было размером с чернику, атом был бы размером с футбольный стадион (рис. \ (\ PageIndex {1} \)).
Стало известно, что атом содержит очень маленькое ядро, состоящее из положительно заряженных протонов и незаряженных нейтронов, окруженное гораздо большим объемом пространства, содержащим отрицательно заряженные электроны. Ядро содержит большую часть массы атома, потому что протоны и нейтроны намного тяжелее электронов, тогда как электроны занимают почти весь объем атома.Диаметр атома составляет порядка 10 −10 м, тогда как диаметр ядра примерно 10 −15 м — примерно в 100 000 раз меньше. Чтобы получить представление об их относительных размерах, рассмотрим следующее: если бы ядро было размером с чернику, атом был бы размером с футбольный стадион (рис. \ (\ PageIndex {1} \)).
Рисунок \ (\ PageIndex {1} \): Если бы атом можно было расширить до размеров футбольного стадиона, ядро было бы размером с одну чернику.(в середине фото: модификация работы «babyknight» / Wikimedia Commons; право на использование: изменение работы Паксона Вельбера).
Атомы и составляющие их протоны, нейтроны и электроны чрезвычайно малы. Например, атом углерода весит менее 2 \ (\ times \) 10 −23 г, а электрон имеет заряд менее 2 \ (\ times \) 10 −19 C (кулон). При описании свойств крошечных объектов, таких как атомы, мы используем соответственно небольшие единицы измерения, такие как атомная единица массы (а.е.м.) и фундаментальная единица заряда (е).Первоначально аму был определен на основе водорода, самого легкого элемента, а затем — кислорода. С 1961 года он был определен в отношении наиболее распространенного изотопа углерода, атомам которого приписываются массы ровно 12 а.е.м. (Этот изотоп известен как «углерод-12», как будет обсуждаться позже в этом модуле.) Таким образом, одна а.е.м. составляет ровно \ (1/12 \) массы одного атома углерода-12: 1 а.е.м. = 1,6605 \ ( \ раз \) 10 −24 г. (Дальтон (Да) и единая атомная единица массы (u) являются альтернативными единицами, эквивалентными аму.) Фундаментальная единица заряда (также называемая элементарным зарядом) равна величине заряда электрона (e) с e = 1,602 \ (\ times \) 10 −19 C.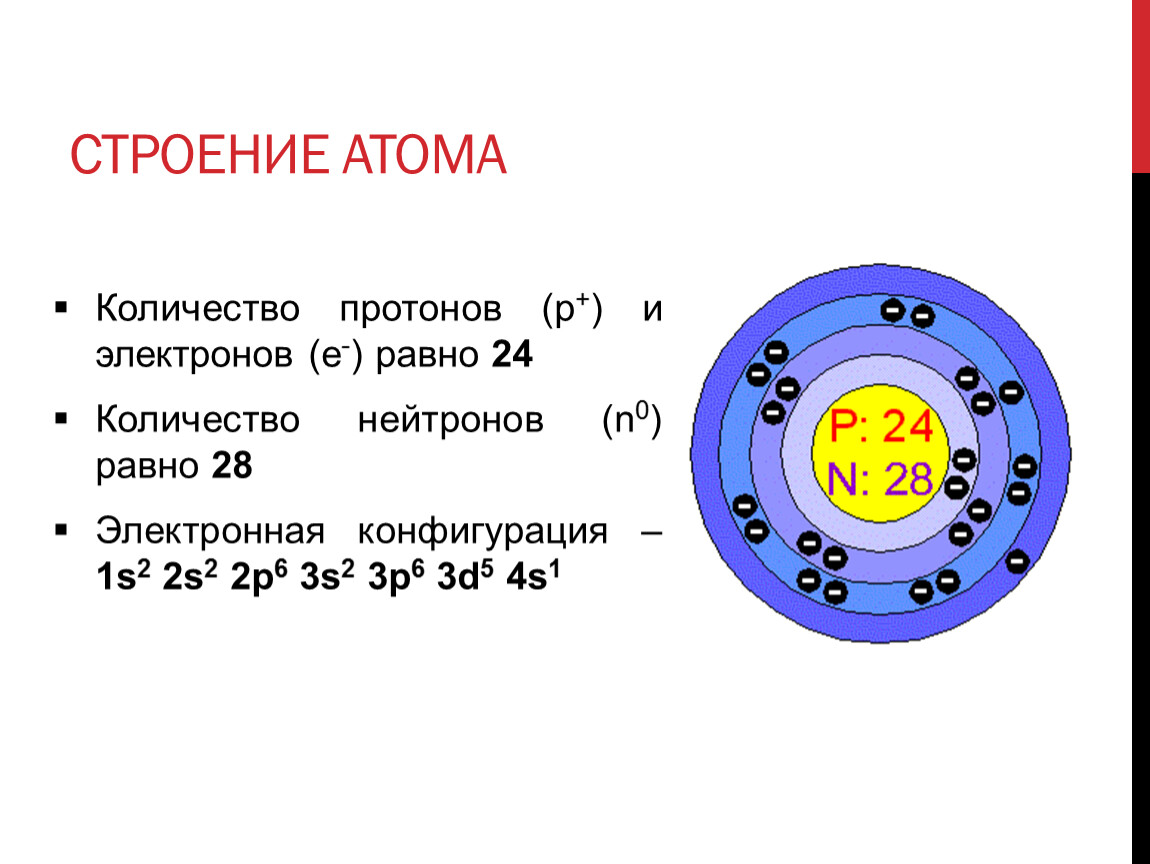
Протон имеет массу 1,0073 а.е.м. и заряд 1+. Нейтрон — это немного более тяжелая частица с массой 1,0087 а.е.м. и нулевым зарядом; как следует из названия, он нейтрален. Электрон имеет заряд 1− и является гораздо более легкой частицей с массой около 0,00055 а.е.м. (потребуется около 1800 электронов, чтобы равняться массе одного протона.Свойства этих фундаментальных частиц сведены в Таблицу \ (\ PageIndex {1} \). (Наблюдательный студент может заметить, что сумма субатомных частиц атома не равна реальной массе атома: общая масса шести протонов, шести нейтронов и шести электронов составляет 12,0993 а.е.м., что немного больше, чем 12,00 а.е.м. реального углерода. 12 атома. Эта «недостающая» масса известна как дефект массы, и вы узнаете об этом в главе, посвященной ядерной химии.)
| Имя | Расположение | Заряд (C) | Стоимость единицы | Масса (а.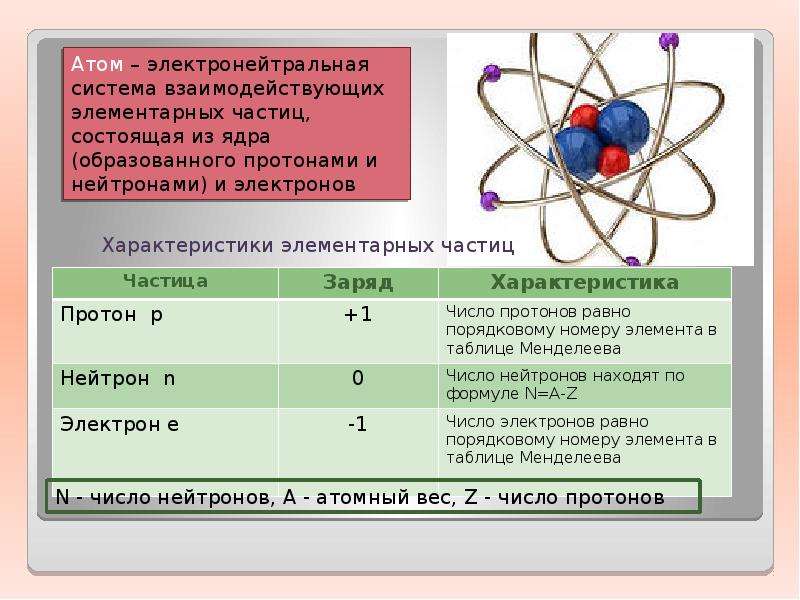 е.м.) е.м.) | Масса (г) |
|---|---|---|---|---|---|
| электрон | вне ядра | \ (- 1.{−24} \) |
Число протонов в ядре атома — это его атомный номер (Z). Это определяющая черта элемента: его значение определяет идентичность атома. Например, любой атом, содержащий шесть протонов, является элементом углерода и имеет атомный номер 6, независимо от того, сколько нейтронов или электронов он может иметь. Нейтральный атом должен содержать одинаковое количество положительных и отрицательных зарядов, поэтому количество протонов равно количеству электронов.Следовательно, атомный номер также указывает количество электронов в атоме. Общее количество протонов и нейтронов в атоме называется его массовым числом (А). Таким образом, количество нейтронов — это разница между массовым числом и атомным номером: A — Z = количество нейтронов.
\ [\ begin {align *}
\ ce {атомное \: число \ 🙁 Z) \: & = \: число \: из \: протонов \\ масса
\: число \ 🙁 A) \: & = \: число \: из \: протонов + число \: из \: нейтронов \\
AZ \: & = \: число \: из \: нейтронов}
\ end {align *} \]
Атомы электрически нейтральны, если они содержат одинаковое количество положительно заряженных протонов и отрицательно заряженных электронов.Когда количество этих субатомных частиц равно , а не , атом электрически заряжен и называется ионом. Заряд атома определяется следующим образом:
Заряд атома = количество протонов — количество электронов
Как будет обсуждаться более подробно позже в этой главе, атомы (и молекулы) обычно приобретают заряд, приобретая или теряя электроны. Атом, который получает один или несколько электронов, будет иметь отрицательный заряд и называется анионом. Положительно заряженные атомы, называемые катионами, образуются, когда атом теряет один или несколько электронов. Например, нейтральный атом натрия (Z = 11) имеет 11 электронов. Если этот атом потеряет один электрон, он станет катионом с зарядом 1+ (11-10 = 1+). Нейтральный атом кислорода (Z = 8) имеет восемь электронов, и если он получит два электрона, он станет анионом с зарядом 2− (8-10 = 2−).
Например, нейтральный атом натрия (Z = 11) имеет 11 электронов. Если этот атом потеряет один электрон, он станет катионом с зарядом 1+ (11-10 = 1+). Нейтральный атом кислорода (Z = 8) имеет восемь электронов, и если он получит два электрона, он станет анионом с зарядом 2− (8-10 = 2−).
Пример \ (\ PageIndex {1} \): состав атома
Йод — важный микроэлемент в нашем рационе; он необходим для выработки гормона щитовидной железы. Недостаток йода в рационе может привести к развитию зоба, увеличению щитовидной железы (Рисунок \ (\ PageIndex {2} \)).
Рисунок \ (\ PageIndex {2} \): (a) Недостаток йода в рационе может вызвать увеличение щитовидной железы, называемое зобом. (б) Добавление к соли небольшого количества йода, предотвращающего образование зоба, помогло устранить эту проблему в США, где потребление соли велико. (кредит а: модификация работы «Алмази» / Wikimedia Commons; кредит б: модификация работы Майка Моцарта)
Добавление небольшого количества йода к поваренной соли (йодированной соли) по существу устранило эту проблему для здоровья в Соединенных Штатах, но до 40% населения мира по-прежнему подвержены риску дефицита йода. Атомы йода добавляются в виде анионов, и каждый из них имеет заряд 1- и массовое число 127. Определите количество протонов, нейтронов и электронов в одном из этих анионов йода.
Атомы йода добавляются в виде анионов, и каждый из них имеет заряд 1- и массовое число 127. Определите количество протонов, нейтронов и электронов в одном из этих анионов йода.
Решение
Атомный номер йода (53) говорит нам, что нейтральный атом йода содержит 53 протона в своем ядре и 53 электрона вне ядра. Поскольку сумма числа протонов и нейтронов равна массовому числу 127, число нейтронов равно 74 (127 — 53 = 74).Поскольку йод добавляется в виде аниона 1−, количество электронов равно 54 [53 — (1–) = 54].
Упражнение \ (\ PageIndex {1} \)
Ион платины имеет массовое число 195 и содержит 74 электрона. Сколько протонов и нейтронов он содержит и каков его заряд?
- Ответ
78 протонов; 117 нейтронов; заряд 4+
Химические символы
Химический символ — это сокращение, которое мы используем для обозначения элемента или атома элемента.Например, ртуть обозначается символом Hg (Рисунок \ (\ PageIndex {3} \)). Мы используем один и тот же символ для обозначения одного атома ртути (микроскопический домен) или для обозначения контейнера из многих атомов элемента ртути (макроскопический домен).
Мы используем один и тот же символ для обозначения одного атома ртути (микроскопический домен) или для обозначения контейнера из многих атомов элемента ртути (макроскопический домен).
Рисунок \ (\ PageIndex {3} \) : символ Hg представляет элемент ртуть независимо от количества; он может представлять один атом ртути или большое количество ртути.
Символы для нескольких общих элементов и их атомов перечислены в Таблице \ (\ PageIndex {2} \).Некоторые символы являются производными от общего имени элемента; другие — это аббревиатуры имени на другом языке. Символы состоят из одной или двух букв, например H для водорода и Cl для хлора. Чтобы избежать путаницы с другими обозначениями, заглавными являются только первая буква символа. Например, Co — это символ элемента кобальта, но CO — это обозначение соединения монооксида углерода, которое содержит атомы элементов углерода (C) и кислорода (O). Все известные элементы и их символы находятся в периодической таблице.
| Элемент | Символ | Элемент | Символ |
|---|---|---|---|
| алюминий | Al | утюг | Fe (из железа ) |
| бром | Br | свинец | Pb (из свинца ) |
| кальций | Ca | магний | мг |
| углерод | С | ртуть | Hg (из гидраргирум ) |
| хлор | Класс | азот | N |
| хром | Cr | кислород | O |
| кобальт | Co | калий | К (из калия ) |
| медь | Cu (из меди ) | кремний | Si |
| фтор | F | серебро | Ag (из серебристый ) |
| золото | Au (из aurum ) | натрий | Na (из натрия ) |
| гелий | He | сера | S |
| водород | H | банка | Sn (из олова ) |
| йод | I | цинк | Zn |
Традиционно первооткрыватель (или первооткрыватели) нового элемента дает ему имя.Однако до тех пор, пока название не будет признано Международным союзом теоретической и прикладной химии (IUPAC), рекомендуемое название нового элемента основано на латинских словах, обозначающих его атомный номер. Например, элемент 106 назывался уннилгексий (Unh), элемент 107 назывался unnilseptium (Uns), а элемент 108 назывался уннилоктиум (Uno) в течение нескольких лет. Эти элементы теперь названы в честь ученых или мест; например, элемент 106 теперь известен как сиборгий (Sg) в честь Гленна Сиборга, лауреата Нобелевской премии, который принимал активное участие в открытии нескольких тяжелых элементов.
ИЮПАК
Посетите этот сайт, чтобы узнать больше об ИЮПАК, Международном союзе теоретической и прикладной химии, и изучить его периодическую таблицу.
Атомная структура и свойства — AP Chemistry
Если вы считаете, что контент, доступный через Веб-сайт (как определено в наших Условиях обслуживания), нарушает или несколько ваших авторских прав, сообщите нам, отправив письменное уведомление («Уведомление о нарушении»), содержащее в информацию, описанную ниже, назначенному ниже агенту.Если репетиторы университета предпримут действия в ответ на ан Уведомление о нарушении, оно предпримет добросовестную попытку связаться со стороной, которая предоставила такой контент средствами самого последнего адреса электронной почты, если таковой имеется, предоставленного такой стороной Varsity Tutors.
Ваше Уведомление о нарушении прав может быть отправлено стороне, предоставившей доступ к контенту, или третьим лицам, таким как в виде ChillingEffects.org.
Обратите внимание, что вы будете нести ответственность за ущерб (включая расходы и гонорары адвокатам), если вы существенно искажать информацию о том, что продукт или действие нарушает ваши авторские права.Таким образом, если вы не уверены, что контент находится на Веб-сайте или по ссылке с него нарушает ваши авторские права, вам следует сначала обратиться к юристу.
Чтобы отправить уведомление, выполните следующие действия:
Вы должны включить следующее:
Физическая или электронная подпись правообладателя или лица, уполномоченного действовать от их имени; Идентификация авторских прав, которые, как утверждается, были нарушены; Описание характера и точного местонахождения контента, который, по вашему мнению, нарушает ваши авторские права, в \ достаточно подробностей, чтобы позволить репетиторам университетских школ найти и точно идентифицировать этот контент; например нам требуется а ссылка на конкретный вопрос (а не только на название вопроса), который содержит содержание и описание к какой конкретной части вопроса — изображению, ссылке, тексту и т. д. — относится ваша жалоба; Ваше имя, адрес, номер телефона и адрес электронной почты; а также Ваше заявление: (а) вы добросовестно полагаете, что использование контента, который, по вашему мнению, нарушает ваши авторские права не разрешены законом, владельцем авторских прав или его агентом; (б) что все информация, содержащаяся в вашем Уведомлении о нарушении, является точной, и (c) под страхом наказания за лжесвидетельство, что вы либо владелец авторских прав, либо лицо, уполномоченное действовать от их имени.
Отправьте жалобу нашему уполномоченному агенту по адресу:
Чарльз Кон
Varsity Tutors LLC
101 S. Hanley Rd, Suite 300
St. Louis, MO 63105
Или заполните форму ниже:
Строение атома | Атом
В результате работы, проделанной предыдущими учеными над атомными моделями, ученые теперь имеют хорошее представление о том, как выглядит атом.Эти знания важны, потому что они помогают нам понять, почему материалы имеют разные свойства и почему одни материалы связываются с другими. Давайте теперь ближе познакомимся с микроскопической структурой атома (как атом выглядит внутри).
До сих пор мы обсуждали, что атомы состоят из положительно заряженного ядра , окруженного одним или несколькими отрицательно заряженными электронами . Эти электроны вращаются вокруг ядра.
Прежде чем мы рассмотрим некоторые полезные концепции, нам сначала нужно понять, что такое электроны, протоны и нейтроны.{- \ text {19}} \) \ (\ text {C} \)).
Ядро (ESABB)
В отличие от электрона, ядро можно разбить на более мелкие строительные блоки, называемые протонами и нейтронами . Вместе протоны и нейтроны называются нуклонами .
Ученые считают, что электрон можно рассматривать как точечную частицу или элементарную частицу , что означает, что он не может быть разбит на что-либо меньшее.
Протон
Электрон несет одну единицу отрицательного электрического заряда (т.е.{- \ text {19}} \)
Таблица 4.2: Сводка частиц внутри атома.
Атомный номер и атомное массовое число (ESABC)
Химические свойства элемента определяются зарядом его ядра, то есть числом протонов . Это число называется атомным номером и обозначается буквой Z .
- Атомный номер (Z)
Число протонов в атоме.
Вы можете найти атомный номер в таблице Менделеева (см. Таблицу Менделеева в начале книги). Атомный номер является целым числом от 1 до 118.
Масса атома зависит от того, сколько нуклонов содержит его ядро. Число нуклонов, то есть общее число протонов плюс нейтронов, называется атомным массовым числом и обозначается буквой A .
В настоящее время элемент 118 — это наивысший атомный номер элемента.Элементы с высокими атомными номерами (примерно от 93 до 118) не существуют долго, поскольку они распадаются в течение нескольких секунд после образования. Ученые считают, что после элемента 118 может быть «остров стабильности», на котором встречаются элементы с более высоким атомным номером, которые не распадаются за секунды.
Нуклид — это особый вид атома или ядра, характеризующийся количеством протонов и нейтронов в атоме. Чтобы быть абсолютно правильным, когда мы представляем атомы, как здесь, мы должны называть их нуклидами.{56} \ text {Fe} \), где атомный номер \ (Z = 26 \), а массовое число \ (A = 56 \). Количество нейтронов — это просто разница \ (N = A — Z = 30 \).
Не путайте обозначения, которые мы использовали здесь, с тем, как эта информация отображается в периодической таблице. В периодической таблице атомный номер обычно появляется в верхнем левом углу блока или непосредственно над символом элемента. Число под символом элемента — это его относительная атомная масса . Это не совсем то же самое, что атомное массовое число.Это будет объяснено в разделе «Изотопы». Пример железа показан ниже.
Для нейтрального атома количество электронов равно количеству протонов, так как заряд на атоме должен уравновешиваться. Но что произойдет, если атом получит или потеряет электроны? Означает ли это, что атом по-прежнему будет частью того же элемента? Изменение количества электронов в атоме не меняет его тип. Однако заряд атома изменится. нейтралитет атома изменился.{23} \ text {Na} \)
Найдите количество электронов
Натрий нейтрален, поэтому у него такое же количество электронов, как и у протонов. Число электронов \ (\ text {11} \).
Найти \ (A \)
Из периодической таблицы мы видим, что \ (A = 23 \).
Вычислить количество нейтронов
Мы знаем \ (A \) и \ (Z \), поэтому можем найти \ (N \): \ (N = A — Z = 23-11 = 12 \). {23} \ text {Na} \).Число протонов — 11, число нейтронов — 12, число электронов — 11.
Теория и структура атома
Далее следует вспомогательное содержание лекции 4 по общей химии I. Эта лекция будет охватывать историю развития теории атома, строение атома, химический символизм и вычисления атомной массы.
Начнем с обзора шагов, предпринятых для создания теории атома:
Теперь, когда мы рассмотрели, как мы пришли к теории атома, давайте посмотрим на атомную структуру, которую мы теперь считаем истинной.
Атомная структура довольно проста. Его часто описывают как похожий на солнечную систему с ядром, представляющим солнце, и электронами, действующими как планеты:
Атом состоит из трех типов частиц, расположенных в двух областях. протонов и нейтронов расположены в ядре , а электронов расположены на энергетических уровнях, окружающих ядро.
Теперь, когда вы знакомы с частицами, составляющими каждый атом элемента, давайте рассмотрим, как эти частицы представлены в периодической таблице.Другими словами, информация, которая дана в символике, используемой в периодической таблице, позволяет определить протоны, нейтроны и электроны, содержащиеся в каждом атоме или элементе.
Мы можем представить элемент или атом элемента его символом.
- C = углерод
- O = кислород
- B = бор
- Pb = свинец
Мы также используем эти символы, чтобы показать, как атомы (в молекулах) меняют партнеров в химической реакции.
- CO + PbO → CO2 + Pb
- Nh4 + HCl → Nh5Cl
Как существуют сами элементы?
Одноатомные элементы
He, Ne, Ar, Kr, Xe, Rn
(называемые благородными газами, раньше их называли инертными газами)
Двухатомные элементы
h3, O2, N2, F2, Cl2, Br2, I2
(Кислород также существует как O3 = озон. Это называется аллотропной формой; многие элементы существуют в нескольких аллотропных формах.)
Элементы других форм
P4, S8, C60 и т. Д.
Алмаз, графит и бакминстерфуллерен («бакибол», C60) — все формы одного и того же элемента — углерода.
В периодической таблице каждому элементу дана коробка, содержащая его химический символ, а также несколько других частей информации:
Посмотрев на символ магния, вы заметите несколько чисел: 24, 12 и 2+. Каждое из этих чисел дает представление об атомной структуре этого конкретного атома магния.
Начнем с самого важного из трех: числа 12. Оно называется атомным числом и соответствует количеству протонов в атоме. Количество протонов уникально для каждого элемента, поэтому, если вы измените количество протонов, вы измените элемент. Другими словами, КАЖДЫЙ атом магния будет иметь в своем ядре ровно 12 протонов.
Следующее число, на которое стоит обратить внимание, — 24. Это число называется атомной массой и представляет собой округленное значение атомной массы атома.Эта масса определяется сложением всех масс протонов и нейтронов в ядре. Итак, если вы знаете массовое число атома и атомный номер, вы можете легко вычислить количество нейтронов в атоме:
Атомное массовое число — атомный номер = количество нейтронов
24 (протоны и нейтроны) — 12 протонов = 12 нейтронов
Последняя цифра в символе может использоваться для расчета количества электронов в элементе или ионе, если есть заряд + или -.Мы знаем, что протоны несут заряд +1, а электроны несут заряд -1 из атомной теории. Таким образом, если в атоме присутствует равное количество протонов и электронов, общий заряд равен 0 или нейтрален.
Протоны + электроны = состояние заряда или ионизации
Итак, если показан заряд, как в примере выше, 2+, это означает, что протонов на два больше, чем электронов, и
(12+) — (? E-) = 2+, таким образом, количество электронов равно 10.
Давайте попрактикуемся:
Наконец, нам нужно более подробно обсудить атомное массовое число , а затем атомную массу .
Изотопы
Поскольку нам нужно рассчитать количество нейтронов, присутствующих в атоме, исходя из атомного массового числа, это означает, что существует более одного атомного массового числа. Если бы в случае с массой атома было только одно, нам не понадобились бы вычисления для определения количества нейтронов, это было бы просто известно, верно? Итак, поскольку мы можем вычислить количество нейтронов, присутствующих в каждом атоме, это означает, что даже атомы одного и того же элемента могут иметь разное количество нейтронов, и это действительно так. Мы называем атомы элементов с разным числом нейтронов Изотопами.
Для каждого элемента существует множество известных изотопов, за очень немногими исключениями, имеющими только один. Вы можете найти эти элементы только с одним изотопом, посмотрев на их атомную массу, указанную в периодической таблице. Вы можете догадаться, как? Что ж, позвольте мне дать вам подсказку. Атомная масса, указанная в периодической таблице для каждого элемента, рассчитывается путем умножения «процентного содержания» каждого изотопа на его массу.По сути, это средневзвешенная масса. НО, если бы был только один изотоп, масса была бы только одна, верно? Таким образом, вы могли бы выяснить, какие элементы имеют только один изотоп.
Атомная масса
Итак, я использовал пару терминов выше, которые я обнаружил ранее причины такой математической паники у студентов, поэтому позвольте мне привести пример, который может сделать «средневзвешенную атомную массу» и ее использование «процентного содержания» более понятным.
Предположим, вы хотите вычислить среднюю массу группы из 25 человек.13 человек — женщины, а остальные 12 — мужчины (да). Поскольку большинство мужчин весят больше, чем большинство женщин, присвоение одного веса всем не дает очень точного среднего веса. Но если каждый мужчина весит ~ 180 фунтов, а каждая женщина — ~ 130 фунтов, вы можете взять процент каждого (женщины 13/25 = 0,52 или 52%, а мужчины 12/25 = 0,48 или 48%) и умножить эти проценты на массу и получить довольно близко к средней массе группы.
Итак (0,52 x 130 фунтов) + (0,48 x 180 фунтов) = 154 фунта
Это именно то, что мы делаем, чтобы получить средневзвешенную атомную массу.Мы берем процентное содержание каждого изотопа и умножаем его на массу изотопа, чтобы получить его индивидуальный вклад в общую массу элемента:
Пример:
Вот несколько практических задач:
Атомная структура
Атомная структураАтомная структура
Вся материя состоит из основных строительных блоков, называемых атомами . Атомы состоят из еще более мелких частиц, называемых протонами , электронов и нейтронов . Протоны и нейтроны живут в ядре атома и практически идентичны по массе. Тем не мение, протоны имеют положительный заряд, тогда как нейтроны не имеют заряда. Электроны имеют отрицательный заряд и вращаются вокруг ядра в оболочках или электронов орбитали и намного менее массивны, чем другие частицы.С электроны в 1836 раз менее массивны, чем протоны или нейтроны, большинство из них масса атома находится в ядре, которое составляет лишь 1/100 000 размера атома. весь атом (!).
Организация атома водорода показана ниже:
Атом водорода
Красная точка — это протон в ядре. Имеет положительный заряд +1 ед. Синяя точка — электрон. Имеет отрицательный заряд -1 ед. Для любого нормального атома количество электронов и протоны равны, что означает, что электрический заряд уравновешен.Там это только одна орбиталь для водорода. Давайте посмотрим на атом углерода большего размера.
Атом углерода
В ядре появилась новая частица — нейтрон. (представлен белыми точками). В ядре также 6 протонов, всего 12 частиц. Кроме того, теперь есть 6 электронов. вращается вокруг ядра по двум орбиталям. Причина, по которой атом углерода нуждается в Вторая орбиталь сложна и выходит за рамки этого геологического класса. Но правила, управляющие атомами, гласят, что первая орбиталь может иметь только две электронов, на второй орбитали разрешено восемь электронов, на третьей — только восемь электронов и т. д. (См. стр. 27 вашего текста с номерами электронов на каждой орбитали для первых 20 элементов.)
В природе 91 элемент. Атомы — это самые маленькие из возможных элементов, и на самом деле слово «атом» происходит от греческого слова «томос», что означает «не резать» — то есть вы не можете вырезать меньше, чем это.Мы обычно представляют элементы их атомным символом. Водород представлен буквой «H»; углерод буквой «C».
Для атомов изменение числа протонов меняет вид элемент . Итак, если бы я бросил дополнительный протон в ядра атома углерода, проиллюстрированного выше, у меня больше не будет углерода — я будет азот. Точно так же, если бы я убрал протон из углерода атом, у меня был бы другой элемент, бор. Число протонов в ядро атома совпадает с атомным номером этого атом.Если сложить количество протонов и нейтронов, получится атомных массовое число этого конкретного атома.
Быстрая викторина : Какой атомный номер показан атом водорода выше? Что это за атомное массовое число? Что такое атомный номер и массовое атомное число указанного выше атома углерода?
Ответы : атомный номер водорода 1 (посчитайте протоны). Атомно-массовое число водорода также равно 9 · 1092 · 1 · 9 · 1095 (есть нет нейтронов!).Для углерода атомный номер 6 , а атомный номер массовое число 12 (6 протонов плюс 6 нейтронов).
Посмотрите еще раз на изображение атома углерода. Что, если бы мы добавили нейтрон вместо протона? Будет ли у нас такой же элемент? Да. Но атом был бы другим. A dding или вычитание нейтронов из ядра атома создает изотопы этого атома . Например, давайте добавим два нейтрона к атому углерода, обозначенному зеленым точки ниже:
Изотоп углерода
Сложение двух нейтронов меняет наш атом.Однако, поскольку количество протонов то же самое, это все еще углерод, но теперь это изотоп углерода. Мы представляем изотопы с помощью химического символа («C» для углерода) и число. Первый атом углерода только с 6 нейтроны будут называться 12 C или углерод-12. Новый с 8 нейтроны будут 14 C или углерод-14. Обратите внимание, что число «14» также является атомным массовым числом для этого изотопа.
Химики работали над организацией элементов особым образом, называемым Периодическая таблица.Он упорядочен так, что элементы в каждом столбце имеют общие химические и физические свойства. Ниже приведено изображение Периодическая таблица:
* Изображение с http://www.chemtutor.com/perich.htm
Каждый элемент имеет атомарный символ и атомный символ. номер.
Quick Quiz: Напомним, что атомный номер — это количество протонов в ядре. Сколько протонов в Атом натрия (Na)? Атом кислорода (O)? Атом урана (U)?
Ответы: Натрий имеет 11 протонов, Кислород 8 протонов и урана 92 протонов.
Продолжайте и узнайте об ионах.
Вернуться в главное меню.
Вернуться на страницу вводного курса наук о Земле.
(Для получения дополнительной информации по основам химии и атомной структуре, посетите http://www.chemtutor.com/.)
.

 5
5 2
2