|
|
|
|
 Far Far |
 WinNavigator WinNavigator |
 Frigate Frigate |
 Norton
Commander Norton
Commander |
 WinNC WinNC |
 Dos
Navigator Dos
Navigator |
 Servant
Salamander Servant
Salamander |
 Turbo
Browser Turbo
Browser |
|
|
 Winamp,
Skins, Plugins Winamp,
Skins, Plugins |
 Необходимые
Утилиты Необходимые
Утилиты |
 Текстовые
редакторы Текстовые
редакторы |
 Юмор Юмор |
|
|
|
File managers and best utilites |
Реферат: Спектрофотометрия и фотоколориметрия:. Реферат на тему спектрофотометрия
Реферат - Спектрофотометрия и фотоколориметрия
РЕФЕРАТ
СПЕКТРОФОТОМЕТРИЯ И ФОТОКОЛОРИМЕТРИЯ
Тамбов, 2009
Введение
Фотометрические методы – это методы качественного и ко; личественного анализа, основанные на измерении интенсивности пропускания, поглощения или рассеяния инфракрасного, видимого и ультрафиолетового излучения исследуемым веществом. К фотометрическим методам анализа относят атомно-абсорбционный анализ, фотометрию пламени, турбидлметрию, нефелометрию, люминесцентный анализ, спектроскопию отражения и молекулярно-абсорбционный фотометрический анализ.
1. Методы молекулярно-абсорбционного фотометрического анализа
В анализе древесины и технических целлюлоз для количественного определения компонентов или примесей, особенно малых количеств веществ, а также качественной характеристики и структурных исследований широко используют различные методы молекулярно-абсорбционного фотометрического анализа. Эти методы основаны на избирательном поглощении электромагнитного излучения в ультрафиолетовой, видимой и инфракрасной областях молекулами определяемого компонента или его соединения с соответствующим реагентом. Вещества, поглощающие видимый свет, окрашены. Наблюдаемый цвет раствора окрашенного вещества является дополнительным к поглощенному. Бесцветные или слабоокрашенные вещества часто можно определить, добавив реагент, который образует с ними'интенсивно окрашенное соединение или соединение, поглощающее ультрафиолетовое излучение. Обычно используют реакции синтеза окрашенных соединений, а иногда реакции окисления-восстановления.
Молекулярно-абсорбционный фотометрический анализ включает спектрофотометрию, фотоколориметрию и визуальную фотометрию. В отличие от последней фотоколориметрия и спектрофотометрия являются инструментальными методами, в которых поглощение света измеряют с помощью приборов, снабженных фотоэлементами. Из этих методов рассматриваются фотоколориметрия и спектрофотометрия, применяемые для определения окрашенных веществ и веществ, поглощающих излучение в ультрафиолетовой области. В фотоколориметрических и спектрофотометрических методах измеряют поглощение излучения при определенной длине волны как функцию концентрации анализируемого вещества в растворе с последующим расчетом массовой доли компонента древесины, остаточного компонента в технической целлюлозе и др.
При использовании монохроматического излучения в случае разбавленных растворов оптическая плотность подчиняется основному закону светопоглощения – объединенному закону Бугера–Ламберта–Бера
/>
где/>–оптическая плотность раствора; е – молярный коэффициент поглощения вещества, дм; с – концентрация поглощающего вещества, моль/дм1; / – толщина поглощающего слоя, см.
Молярный коэффициент поглощения является характеристикой определяемого вещества, тогда как оптическая плотность – характеристикой отдельной пробы раствора.
В случаях, когда концентрацию поглощающего вещества в растворе невозможно выразить в моль/дм3, вместо молярного коэффициента поглощения используют так называемый удельный коэффициент и видоизмененную форму закона Бугера–Ламберта–Бера
/>
где k– удельный коэффициент поглощения вещества, дм г-1-см-1.
Закон Бугера–Ламберта – Бера лежит в основе расчетов в фотометрических анализах. При / = constоптическая плотность раствора данного вещества прямо пропорциональна его концентрации. Это позволяет определять концентрацию растворов по градуировочным графикам, которые строят по значениям оптической плотности серии эталонных растворов различной концентрации. Также можно рассчитывать искомую концентрацию по молярным или удельным коэффициентам поглощения, установленным с помощью градуировочных графиков. В последнем случае оптическая плотность должна строго подчиняться закону Бугера–Ламберта–Бера. В первом случае допустимо отклонение градуировочного графика от линейной формы. Измерения оптической плотности можно производить при длинах волн, как соответствующих, так и не соответствующих максимумам спектров поглощения.
Спектрофотометрический метод применяют и для определения в растворах концентраций нескольких веществ при совместном присутствии. Оптическая плотность является аддитивным свойством и поэтому для смеси не взаимодействующих между собой компонентов она равна сумме оптических плотностей этих компонентов при одной и той же длине волны
/>
Для раствора, содержащегозокрашенных или поглощающих УФ-излучение веществ, проводятзнезависимых измерений оптической плотности призразличных длинах волнл.Получают систему линейных уравнений, решая которую, находят концентрации содержащихся веществ.
В частном случае двухкомпонентных систем обычно замеряют оптические плотности при двух длинах волн, соответствующих максимумам спектров поглощения каждого из двух компонентов. Тогда получают систему двух уравнений
/>
гдее'и г» – молярные коэффициенты поглощения соответствующих компонентов; с' и с» – концентрации этих компонентов.
Если еьеье2, е2известны, D1и D2измерены в опыте, то из этих двух уравнений можно рассчитать концентрации с' и с».
На принципе аддитивности оптической плотности основано введение поправок на растворитель и контрольное определение, когда при измерении оптической плотности раствора определяемого вещества вычитается оптическая плотность раствора сравнения.
Для измерения оптической плотности растворов в видимой области используют фотоэлектроколориметры, а для УФ и видимой области – спектрофотометры.
При работе с фотоэлектроколориметрами и спектрофотометрами, как и с любым другим физико-химическим прибором, сначала необходимо ознакомиться с прилагаемой к нему инструкцией и строго соблюдать ее во время работы.
В качестве растворителей следует использовать только такие, которые не поглощают света в данной области. Концентрацию рабочих растворов подбирают таким образом, чтобы измеряемое значение оптической плотности находилось в пределах 0,2…0,8. При высоких концентрациях интенсивность прошедшего излучения становится слишком малой и на измеряемую оптическую плотность оказывает влияние рассеянное излучение, что приводит к отклонениям от закона Бугера–Ламберта–Бера. Для получения растворов требуемых малых концентраций используют метод последовательных разведений, причем взвешивание растворов и растворителей дает меньшую ошибку, чем разведение по объему.
--PAGE_BREAK--При очень низких концентрациях ошибка в показаниях прибора становится слишком большой по сравнению с определяемой величиной.
2.Построение градуировочных графиков
Градуировочные графики строят, пользуясь эталонными растворами чистых веществ. Для построения графика необходимо приготовить 5… 10 растворов с различной концентрацией эталонного вещества с таким расчетом, чтобы это число растворов охватило весь интервал, в пределах которого может изменяться концентрация определяемого вещества.
В мерные колбы вместимостью 25 см с притертыми пробками наливают с помощью пипеток различные объемы эталонного раствора определяемого вещества и соответствующие реагенты согласно методике анализа, затем разбавляют до метки водой, буферным раствором или другим соответствующим растворителем и хорошо перемешивают.
При построении градуировочных графиков необходимо подбирать концентрацию раствора и толщину кюветы таким образом, чтобы крайние значения оптической плотности составляли от 0,05 до 1,5. Измерение оптической плотности ниже 0,05 и выше 1,5 приводит к значительному увеличению ошибки измерения.
Значения оптической плотности полученных разбавленных эталонных растворов измеряют в порядке увеличения их концентрации в фотоэлектроколориметре с соответствующим светофильтром или в спектрофотометре при соответствующей длине волны. В качестве раствора сравнения используют раствор, составляемый в соответствии с методикой анализа, но без определяемого вещества. Реагенты, не поглощающие излучения в данной области спектра, в раствор сравнения можно не добавлять. Измеряют оптические плотности трех параллельных проб всех приготовленных разбавленных эталонных растворов с различной концентрацией определяемого вещества. По полученным данным на миллиметровой бумаге строят график. Для, получения наиболее точного графика следует пользоваться методом наименьших квадратов. По оси абсцисс откладывают концентрацию вещества в растворе в граммах, милли- или микрограммах в 1 дм' или 1 см' раствора, а по оси ординат – значения оптической плотности.
Градуировочный график также можно построить, пользуясь эталонными растворами, приготовленными из различных навесок чистого вещества в определенном объеме растворителя. При разбавлении эталонного раствора его определенные порции можно не отмерять пипетками, а отвешивать на аналитических весах.
Градуировочные графики необходимо периодически проверять – при смене реагентов и для нового прибора.
3. Хромофоры органических соединений и применение методов фотоколориметрии и спектрофотометрии в анализах древесины и целлюлозы
Поглощение видимого и УФ-излучения органическими соединениями обусловлено переходами электронов в молекулах, переводящими их в возбужденное состояние. Практическое значение имеют переходы электроновр-связейр*и п-электронов неподеленных пар гетероатомов п->-лЛ так как им соответствуют длины волн, попадающие в рабочий интервал приборов. Полностью насыщенные соединения не проявляют избирательного поглощения ни в видимой, ни в доступной для измерений части УФ-области. Соединения, содержащие одну двойную связь, поглощают свет в дальней УФ-области при длинах волн менее 200 нм. Сопряженные двойные связи вызывают поглощение при больших длинах волн, причем чем длиннее цепь сопряжения, тем при большей длине волны наблюдается поглощение. При достаточно большой длине цепи сопряжения поглощение переходит в видимую область. 'Смещению максимума поглощения в сторону более длинных волн способствуют ароматические и гетероциклические фрагменты, а также электронодонорные группы, содержащие у гетероатома неподеленные пары электронов.
Вся сопряженная система в органическом соединении называется хромофором. От строения хромофора зависит длина волны, соответствующая максимуму поглощения в спектре. Введение заместителей вызывает смещение полосы поглощения и изменение его интенсивности. В зависимости от непосредственного окружения хромофора максимум его поглощения может сдвигаться либо в сторону более длинных волн, либо в сторону менее длинных волн .·
Основными типами хромофоров в органических соединениях служат: диеновые и полиеновые системы; карбонильные группы, сопряженные с двойными связями; бензольные кольца, особенно сопряженные с другими хромофорами; хиноны; ароматические гетероциклические системы, в том числе фуран и его производные. Следует заметить, что у бензольных колец, сопряженных с дополнительными хромофорами, положение максимумов поглощения и их интенсивность колеблются в широких пределах. Вещества, не способные к поглощению, можно определить спектрофотометрически или фотоколориметрически, добавив реагент, образующий с определяемым соединением поглощающий комплекс или хромофорную систему.
Макромолекулы целлюлозы и других полисахаридов не содержат хромофоров и поэтому не поглощают свет ни в видимой, ни в УФ-области. То же самое относится к продуктам их гидролиза, моносахаридам. Однако моносахариды дают многочисленные цветные реакции с различными реагентами с образованием окрашенных продуктов, пригодных для фотоколориметрического или спектрофотометрического определения. Обычно цветная реакция обусловливается образованием из моносахарида фуранового цикла, который и дает окрашивание.
В противоположность углеводам лигнин, имеющий ароматическое строение, поглощает УФ-излучение. В спектре лигнина имеются интенсивный максимум поглощения в области длин волн 203…208 нм, четко выраженное плечо около 230 нм и характерный, но менее интенсивный по сравнению с первым максимум в области 280 нм у лигнинов хвойных древесных пород и при 275…278 нм – у лигнинов лиственных древесных пород. Интенсивность поглощения у лиственных лигнинов ниже, чем у хвойных. Спектр лигнина представляет собой сумму накладывающихся друг на друга полос поглощения различных хромофоров, входящих в макромолекулы лигнина: бензольных колец, содержащих фенольные гидроксильные группы; сопряженных с бензольным кольцом карбонильных групп и двойных связей; дифенмльных структур; группировок хинонов и метиленхинонов и др.
Различные химические обработки лигнина, в том числе варочными агентами в процессах получения из древесины техническнх целлюлоз и других волокнистых полуфабрикатов, за исключением действия окислителей и щелочей в жестких условиях, не затрагивают основных хромофорных группировок. Это позволяет использовать УФ-поглощение лигнина для его количественного определения в технических целлюлозах, в сульфитных и сульфатных варочных растворах в ходе делигнификации, в отработанных щелоках, а также в кислых фильтратах при определении лигнина Класона.
/>
Применяемые в анализе древесины и технических целлюлоз и включенные в данное учебное пособие методы фотометрического анализа условно можно подразделить на следующие группы.
1. Прямой анализ методом поглощения в УФ-области. К этой группе относятся: методы спектрофотометрического определения кислоторастворимого лигнина в фильтратах, получаемых при определении лигнина в древесине и остаточного лигнина в технических целлюлозах гидролизом с концентрированной серной кислотой; определение остаточного лигнина в технических целлюлозах спектрофотометрическим методом в кадоксене; определение фурфурола спектрофотометрическим методом при анализе технических целлюлоз на остаточные пентозаны. Спектрофотометрию в УФ-области можно также использовать для количественного определения лигнина, содержащегося в древесине, растворением ее в ацетилбромиде.
2. Прямой анализ методом свефороглощеиия в видимой области. Этот метод в химии древесины и целлюлозы применяется сравнительно редко. К этой группе относится фотометрическое определение таннинов в водных экстрактах, извлеченных из древесины или коры.
3. Измерение поглощения в видимой области продуктами реакций с определяемым веществом. Эта группа, методов включает: фотоколориметрическое определение фурфурола с орсином при определении пентозанов в древесине и остаточных пентозанов в технических целлюлозах; фотоколориметрическое определение моносахаридов при анализе гидролизатов легко- и трудногидролизуемых полисахаридов древесины методом хроматографии на бумаге.
4. Спектрофотометрический анализ многокомпонентных систем – определение с отолуидиновым реагентом галактуронана, пентозанов и гекспзанов в пектиновых веществах, извлеченных из древесины. Спектрофотометрический анализ многокомпонентных систем можно также использовать для определения лигнина в растворах в присутствииуглеводов, измеряя поглощение при двух длинах волн рдля определения остаточных пентозанов в технических целлюлозах но фурфуролу с поправкой на гидро-ксиметплфурфурол.
5. Определениецункииональных групп в технических и окисленных целлюлозах с применением или получением в ходе анализа органических красителей. К этой группе методов относятся определение восстанавливающих карбонильных групп по реакции их с хлоридом 2. 3,5 – трифенил-тетразолпя с фотоколорнметрическнм определением образующегося красителя – формазана и определение карбоксильных групп фотоколориметрическим измерением связанного основного красителя – метилепового голубого.
www.ronl.ru
Содержание
Министерство образования и науки Российской Федерации
Федеральное государственное бюджетное образовательное учреждение
высшего профессионального образования
«Уфимский государственный нефтяной технический университет»
Кафедра автоматизации технологических процессов и производств
РЕФЕРАТ
по дисциплине «Промышленный экологический мониторинг»
на тему «Спектральные методы анализа»
ВЫПОЛНИЛ
ст. гр. МАГ01-13-01 _____ ________ Шарифисламов А.Б.
(дата, подпись)
ПРОВЕРИЛ
Доцент _____________ Прахова М.Ю.
(дата, подпись)
Уфа 2013
ВВЕДЕНИЕ 4
1 СПЕКТРОФОТОМЕТРИЧЕСКИЙ МЕТОД АНАЛИЗА 6
1.1 Общая характеристика метода 6
1.2 Важнейшие законы светопоглощения 6
(1.1) 6
1.3 Причины отклонений от закона Бера в спектрофотометрии 7
1.4 Аппаратура в спектрофотометрии 9
2 ЛЮМИНЕСЦЕНТНЫЕ МЕТОДЫ АНАЛИЗА 14
3 ИНФРАКРАСНАЯ СПЕТРОСКОПИЯ 22
4 АТОМНО-ЭМИССИОННЫЕ МЕТОДЫ АНАЛИЗА 28
4.1 Общая характеристика метода 28
4.2 Атомизаторы в атомной эмиссии 29
4.3 Аппаратура в атомно-эмиссионном анализе 30
СПИСОК ИСПОЛЬЗОВАННЫХ ИСТОЧНИКОВ 34
Введение
Спектральные методы анализа - это методы, основанные на определении химического состава и строения веществ по их спектру.
Спектром вещества называют упорядоченное по длинам волн электромагнитное излучение, испускаемое, поглощаемое, рассеиваемое или преломляемое веществом. Методы, основанные на получении и изучении спектров испускания (эмиссии) электромагнитного излучения (энергии), называют эмиссионными, поглощения (абсорбции) - абсорбционными, рассеяния - методами рассеяния, преломления - рефракционными.
Спектр вещества получают, воздействуя на него температурой, потоком электронов, световым потоком (электромагнитной энергией) с определённой длиной волны (частоты излучения) и другими способами. При определённой величине энергии воздействия вещество способно перейти в возбуждённое состояние. При этом происходят процессы, приводящие к появлению в спектре излучения с определённой длиной волны.
Излучение, поглощение, рассеяние или рефракция электромагнитного излучения может рассматриваться как аналитический сигнал, несущий информацию о качественном и количественном составе вещества или о его структуре. Частота (длина волны) излучения определяется составом исследуемого вещества, а интенсивность излучения пропорциональна числу частиц, вызвавших его появление, т.е. количеству вещества или компонента смеси.
Каждый из аналитических методов обычно использует не полный спектр вещества, охватывающий диапазон длин волн от рентгеновских излучений до радиоволн, а только определённую его часть. Спектральные методы обычно различают по диапазону длин волн спектра, являющемуся рабочим для данного метода: ультрафиолетовые (УФ), рентгеновские, инфракрасные (ИК), микроволновые и т.д.
1 Спектрофотометрический метод анализа
1.1 Общая характеристика метода
Спектрофотометрией обычно называют метод оптического молекулярного абсорбционного анализа (иногда в это понятие включают и метод атомно-абсорбционного анализа). Объектом спектрофотометрических измерений, как правило, являются растворы. Фотометрируемый раствор помещают в кювету — сосуд с плоскими параллельными прозрачными гранями.
Спектрофотометрический метод, будучи абсорбционным, основан на измерении поглощения света. Его чаще всего измеряют косвенно — путем сравнения интенсивностей света внешнего источника, падающего на образец и прошедшего сквозь образец.
1.2 Важнейшие законы светопоглощения
Закон Бугера-Ламберта-Бера. Пусть слой однородной среды толщиной dl содержит светопоглощающее вещество в концентрации с. Через него пропускают монохроматический световой поток интенсивности I. Интенсивность света на выходе из слоя равна I + dI, причем dl < 0 (поток ослабляется). Экспериментально было установлено, что доля поглощенного света - dI/I прямо пропорциональна толщине слоя и концентрации поглощающего вещества:
 (1.1)
(1.1)
Интегрируя это выражение, получаем:
 (1.2)
(1.2)
Интенсивность светового потока, падающего на образец (т.е. при l= 0) обозначим как Iо. Подставляя в (1.2) l = 0 и I = I0, находим, что const = - ln I0. Подставляя это значение в (1.2) и переходя от натуральных логарифмов к десятичным, получаем:
 (1.3)
(1.3)
(здесь k = 2.303 ).
).
Величина I/I0 называется пропусканием и обозначается Т (0 < Т < 1). Величина
 ' (1.4)
' (1.4)
называется оптической плотностью (значению Т = 1 соответствует А = 0, а Т = 0 — А = + оо). Коэффициент k называется коэффициентом поглощения.
Выражение (1.3) является основным законом светопоглощения и называется законом Бугера-Ламберта-Бера.
Если концентрация поглощающих частиц выражена в моль/л, а толщина слоя — в сантиметрах, то коэффициент поглощения обозначается буквой е и называется молярным коэффициентом поглощения. Общепринятая форма записи закона Бугера-Ламберта-Бера в спектрофотометрии выглядит как
А = elc (1.5)
studfiles.net
Реферат: Спектрофотометрия и фотоколориметрия
РЕФЕРАТ
СПЕКТРОФОТОМЕТРИЯ И ФОТОКОЛОРИМЕТРИЯ
Тамбов, 2009
Введение
Фотометрические методы – это методы качественного и ко;личественного анализа, основанные на измерении интенсивности пропускания, поглощения или рассеяния инфракрасного, видимого и ультрафиолетового излучения исследуемым веществом. К фотометрическим методам анализа относят атомно-абсорбционный анализ, фотометрию пламени, турбидлметрию, нефелометрию, люминесцентный анализ, спектроскопию отражения и молекулярно-абсорбционный фотометрический анализ.
1. Методы молекулярно-абсорбционного фотометрического анализа
В анализе древесины и технических целлюлоз для количественного определения компонентов или примесей, особенно малых количеств веществ, а также качественной характеристики и структурных исследований широко используют различные методы молекулярно-абсорбционного фотометрического анализа. Эти методы основаны на избирательном поглощении электромагнитного излучения в ультрафиолетовой, видимой и инфракрасной областях молекулами определяемого компонента или его соединения с соответствующим реагентом. Вещества, поглощающие видимый свет, окрашены. Наблюдаемый цвет раствора окрашенного вещества является дополнительным к поглощенному. Бесцветные или слабоокрашенные вещества часто можно определить, добавив реагент, который образует с ними'интенсивно окрашенное соединение или соединение, поглощающее ультрафиолетовое излучение. Обычно используют реакции синтеза окрашенных соединений, а иногда реакции окисления-восстановления.
Молекулярно-абсорбционный фотометрический анализ включает спектрофотометрию, фотоколориметрию и визуальную фотометрию. В отличие от последней фотоколориметрия и спектрофотометрия являются инструментальными методами, в которых поглощение света измеряют с помощью приборов, снабженных фотоэлементами. Из этих методов рассматриваются фотоколориметрия и спектрофотометрия, применяемые для определения окрашенных веществ и веществ, поглощающих излучение в ультрафиолетовой области. В фотоколориметрических и спектрофотометрических методах измеряют поглощение излучения при определенной длине волны как функцию концентрации анализируемого вещества в растворе с последующим расчетом массовой доли компонента древесины, остаточного компонента в технической целлюлозе и др.
При использовании монохроматического излучения в случае разбавленных растворов оптическая плотность подчиняется основному закону светопоглощения – объединенному закону Бугера–Ламберта–Бера

где –оптическая плотность раствора; е – молярный коэффициент поглощения вещества, дм; с – концентрация поглощающего вещества, моль/дм1; / – толщина поглощающего слоя, см.
–оптическая плотность раствора; е – молярный коэффициент поглощения вещества, дм; с – концентрация поглощающего вещества, моль/дм1; / – толщина поглощающего слоя, см.
Молярный коэффициент поглощения является характеристикой определяемого вещества, тогда как оптическая плотность – характеристикой отдельной пробы раствора.
В случаях, когда концентрацию поглощающего вещества в растворе невозможно выразить в моль/дм3, вместо молярного коэффициента поглощения используют так называемый удельный коэффициент и видоизмененную форму закона Бугера–Ламберта–Бера

где k – удельный коэффициент поглощения вещества, дм г-1-см-1.
Закон Бугера–Ламберта – Бера лежит в основе расчетов в фотометрических анализах. При / = const оптическая плотность раствора данного вещества прямо пропорциональна его концентрации. Это позволяет определять концентрацию растворов по градуировочным графикам, которые строят по значениям оптической плотности серии эталонных растворов различной концентрации. Также можно рассчитывать искомую концентрацию по молярным или удельным коэффициентам поглощения, установленным с помощью градуировочных графиков. В последнем случае оптическая плотность должна строго подчиняться закону Бугера–Ламберта–Бера. В первом случае допустимо отклонение градуировочного графика от линейной формы. Измерения оптической плотности можно производить при длинах волн, как соответствующих, так и не соответствующих максимумам спектров поглощения.
Спектрофотометрический метод применяют и для определения в растворах концентраций нескольких веществ при совместном присутствии. Оптическая плотность является аддитивным свойством и поэтому для смеси не взаимодействующих между собой компонентов она равна сумме оптических плотностей этих компонентов при одной и той же длине волны

Для раствора, содержащего з окрашенных или поглощающих УФ-излучение веществ, проводят з независимых измерений оптической плотности при з различных длинах волн л. Получают систему линейных уравнений, решая которую, находят концентрации содержащихся веществ.
В частном случае двухкомпонентных систем обычно замеряют оптические плотности при двух длинах волн, соответствующих максимумам спектров поглощения каждого из двух компонентов. Тогда получают систему двух уравнений
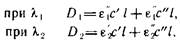
где е' и г» – молярные коэффициенты поглощения соответствующих компонентов; с' и с» – концентрации этих компонентов.
Если еьеье2, е2известны, D1и D2измерены в опыте, то из этих двух уравнений можно рассчитать концентрации с' и с».
На принципе аддитивности оптической плотности основано введение поправок на растворитель и контрольное определение, когда при измерении оптической плотности раствора определяемого вещества вычитается оптическая плотность раствора сравнения.
Для измерения оптической плотности растворов в видимой области используют фотоэлектроколориметры, а для УФ и видимой области – спектрофотометры.
При работе с фотоэлектроколориметрами и спектрофотометрами, как и с любым другим физико-химическим прибором, сначала необходимо ознакомиться с прилагаемой к нему инструкцией и строго соблюдать ее во время работы.
В качестве растворителей следует использовать только такие, которые не поглощают света в данной области. Концентрацию рабочих растворов подбирают таким образом, чтобы измеряемое значение оптической плотности находилось в пределах 0,2…0,8. При высоких концентрациях интенсивность прошедшего излучения становится слишком малой и на измеряемую оптическую плотность оказывает влияние рассеянное излучение, что приводит к отклонениям от закона Бугера–Ламберта–Бера. Для получения растворов требуемых малых концентраций используют метод последовательных разведений, причем взвешивание растворов и растворителей дает меньшую ошибку, чем разведение по объему.
При очень низких концентрациях ошибка в показаниях прибора становится слишком большой по сравнению с определяемой величиной.
2.Построение градуировочных графиков
Градуировочные графики строят, пользуясь эталонными растворами чистых веществ. Для построения графика необходимо приготовить 5… 10 растворов с различной концентрацией эталонного вещества с таким расчетом, чтобы это число растворов охватило весь интервал, в пределах которого может изменяться концентрация определяемого вещества.
В мерные колбы вместимостью 25 см с притертыми пробками наливают с помощью пипеток различные объемы эталонного раствора определяемого вещества и соответствующие реагенты согласно методике анализа, затем разбавляют до метки водой, буферным раствором или другим соответствующим растворителем и хорошо перемешивают.
При построении градуировочных графиков необходимо подбирать концентрацию раствора и толщину кюветы таким образом, чтобы крайние значения оптической плотности составляли от 0,05 до 1,5. Измерение оптической плотности ниже 0,05 и выше 1,5 приводит к значительному увеличению ошибки измерения.
Значения оптической плотности полученных разбавленных эталонных растворов измеряют в порядке увеличения их концентрации в фотоэлектроколориметре с соответствующим светофильтром или в спектрофотометре при соответствующей длине волны. В качестве раствора сравнения используют раствор, составляемый в соответствии с методикой анализа, но без определяемого вещества. Реагенты, не поглощающие излучения в данной области спектра, в раствор сравнения можно не добавлять. Измеряют оптические плотности трех параллельных проб всех приготовленных разбавленных эталонных растворов с различной концентрацией определяемого вещества. По полученным данным на миллиметровой бумаге строят график. Для, получения наиболее точного графика следует пользоваться методом наименьших квадратов. По оси абсцисс откладывают концентрацию вещества в растворе в граммах, милли- или микрограммах в 1 дм' или 1 см' раствора, а по оси ординат – значения оптической плотности.
Градуировочный график также можно построить, пользуясь эталонными растворами, приготовленными из различных навесок чистого вещества в определенном объеме растворителя. При разбавлении эталонного раствора его определенные порции можно не отмерять пипетками, а отвешивать на аналитических весах.
Градуировочные графики необходимо периодически проверять – при смене реагентов и для нового прибора.
3.Хромофоры органических соединений и применение методов фотоколориметрии и спектрофотометрии в анализах древесины и целлюлозы
Поглощение видимого и УФ-излучения органическими соединениями обусловлено переходами электронов в молекулах, переводящими их в возбужденное состояние. Практическое значение имеют переходы электронов р-связей р* и п-электронов неподеленных пар гетероатомов п->-лЛ так как им соответствуют длины волн, попадающие в рабочий интервал приборов. Полностью насыщенные соединения не проявляют избирательного поглощения ни в видимой, ни в доступной для измерений части УФ-области. Соединения, содержащие одну двойную связь, поглощают свет в дальней УФ-области при длинах волн менее 200 нм. Сопряженные двойные связи вызывают поглощение при больших длинах волн, причем чем длиннее цепь сопряжения, тем при большей длине волны наблюдается поглощение. При достаточно большой длине цепи сопряжения поглощение переходит в видимую область. 'Смещению максимума поглощения в сторону более длинных волн способствуют ароматические и гетероциклические фрагменты, а также электронодонорные группы, содержащие у гетероатома неподеленные пары электронов.
Вся сопряженная система в органическом соединении называется хромофором. От строения хромофора зависит длина волны, соответствующая максимуму поглощения в спектре. Введение заместителей вызывает смещение полосы поглощения и изменение его интенсивности. В зависимости от непосредственного окружения хромофора максимум его поглощения может сдвигаться либо в сторону более длинных волн, либо в сторону менее длинных волн .·
Основными типами хромофоров в органических соединениях служат: диеновые и полиеновые системы; карбонильные группы, сопряженные с двойными связями; бензольные кольца, особенно сопряженные с другими хромофорами; хиноны; ароматические гетероциклические системы, в том числе фуран и его производные. Следует заметить, что у бензольных колец, сопряженных с дополнительными хромофорами, положение максимумов поглощения и их интенсивность колеблются в широких пределах. Вещества, не способные к поглощению, можно определить спектрофотометрически или фотоколориметрически, добавив реагент, образующий с определяемым соединением поглощающий комплекс или хромофорную систему.
Макромолекулы целлюлозы и других полисахаридов не содержат хромофоров и поэтому не поглощают свет ни в видимой, ни в УФ-области. То же самое относится к продуктам их гидролиза, моносахаридам. Однако моносахариды дают многочисленные цветные реакции с различными реагентами с образованием окрашенных продуктов, пригодных для фотоколориметрического или спектрофотометрического определения. Обычно цветная реакция обусловливается образованием из моносахарида фуранового цикла, который и дает окрашивание.
В противоположность углеводам лигнин, имеющий ароматическое строение, поглощает УФ-излучение. В спектре лигнина имеются интенсивный максимум поглощения в области длин волн 203…208 нм, четко выраженное плечо около 230 нм и характерный, но менее интенсивный по сравнению с первым максимум в области 280 нм у лигнинов хвойных древесных пород и при 275…278 нм – у лигнинов лиственных древесных пород. Интенсивность поглощения у лиственных лигнинов ниже, чем у хвойных. Спектр лигнина представляет собой сумму накладывающихся друг на друга полос поглощения различных хромофоров, входящих в макромолекулы лигнина: бензольных колец, содержащих фенольные гидроксильные группы; сопряженных с бензольным кольцом карбонильных групп и двойных связей; дифенмльных структур; группировок хинонов и метиленхинонов и др.
Различные химические обработки лигнина, в том числе варочными агентами в процессах получения из древесины техническнх целлюлоз и других волокнистых полуфабрикатов, за исключением действия окислителей и щелочей в жестких условиях, не затрагивают основных хромофорных группировок. Это позволяет использовать УФ-поглощение лигнина для его количественного определения в технических целлюлозах, в сульфитных и сульфатных варочных растворах в ходе делигнификации, в отработанных щелоках, а также в кислых фильтратах при определении лигнина Класона.
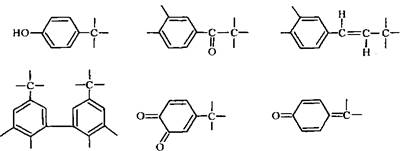
Применяемые в анализе древесины и технических целлюлоз и включенные в данное учебное пособие методы фотометрического анализа условно можно подразделить на следующие группы.
1. Прямой анализ методом поглощения в УФ-области. К этой группе относятся: методы спектрофотометрического определения кислоторастворимого лигнина в фильтратах, получаемых при определении лигнина в древесине и остаточного лигнина в технических целлюлозах гидролизом с концентрированной серной кислотой; определение остаточного лигнина в технических целлюлозах спектрофотометрическим методом в кадоксене; определение фурфурола спектрофотометрическим методом при анализе технических целлюлоз на остаточные пентозаны. Спектрофотометрию в УФ-области можно также использовать для количественного определения лигнина, содержащегося в древесине, растворением ее в ацетилбромиде.
2. Прямой анализ методом свефороглощеиия в видимой области. Этот метод в химии древесины и целлюлозы применяется сравнительно редко. К этой группе относится фотометрическое определение таннинов в водных экстрактах, извлеченных из древесины или коры.
3. Измерение поглощения в видимой области продуктами реакций с определяемым веществом. Эта группа, методов включает: фотоколориметрическое определение фурфурола с орсином при определении пентозанов в древесине и остаточных пентозанов в технических целлюлозах; фотоколориметрическое определение моносахаридов при анализе гидролизатов легко- и трудногидролизуемых полисахаридов древесины методом хроматографии на бумаге.
4. Спектрофотометрический анализ многокомпонентных систем – определение с отолуидиновым реагентом галактуронана, пентозанов и гекспзанов в пектиновых веществах, извлеченных из древесины. Спектрофотометрический анализ многокомпонентных систем можно также использовать для определения лигнина в растворах в присутствии углеводов, измеряя поглощение при двух длинах волн р для определения остаточных пентозанов в технических целлюлозах но фурфуролу с поправкой на гидро-ксиметплфурфурол.
5. Определение цункииональных групп в технических и окисленных целлюлозах с применением или получением в ходе анализа органических красителей. К этой группе методов относятся определение восстанавливающих карбонильных групп по реакции их с хлоридом 2. 3,5 – трифенил-тетразолпя с фотоколорнметрическнм определением образующегося красителя – формазана и определение карбоксильных групп фотоколориметрическим измерением связанного основного красителя – метилепового голубого.
superbotanik.net
Курсовая работа - Спектрофотометрия и фотоколориметрия
РЕФЕРАТ
СПЕКТРОФОТОМЕТРИЯ И ФОТОКОЛОРИМЕТРИЯ
Тамбов, 2009
Введение
Фотометрические методы – это методы качественного и ко; личественного анализа, основанные на измерении интенсивности пропускания, поглощения или рассеяния инфракрасного, видимого и ультрафиолетового излучения исследуемым веществом. К фотометрическим методам анализа относят атомно-абсорбционный анализ, фотометрию пламени, турбидлметрию, нефелометрию, люминесцентный анализ, спектроскопию отражения и молекулярно-абсорбционный фотометрический анализ.
1. Методы молекулярно-абсорбционного фотометрического анализа
В анализе древесины и технических целлюлоз для количественного определения компонентов или примесей, особенно малых количеств веществ, а также качественной характеристики и структурных исследований широко используют различные методы молекулярно-абсорбционного фотометрического анализа. Эти методы основаны на избирательном поглощении электромагнитного излучения в ультрафиолетовой, видимой и инфракрасной областях молекулами определяемого компонента или его соединения с соответствующим реагентом. Вещества, поглощающие видимый свет, окрашены. Наблюдаемый цвет раствора окрашенного вещества является дополнительным к поглощенному. Бесцветные или слабоокрашенные вещества часто можно определить, добавив реагент, который образует с ними'интенсивно окрашенное соединение или соединение, поглощающее ультрафиолетовое излучение. Обычно используют реакции синтеза окрашенных соединений, а иногда реакции окисления-восстановления.
Молекулярно-абсорбционный фотометрический анализ включает спектрофотометрию, фотоколориметрию и визуальную фотометрию. В отличие от последней фотоколориметрия и спектрофотометрия являются инструментальными методами, в которых поглощение света измеряют с помощью приборов, снабженных фотоэлементами. Из этих методов рассматриваются фотоколориметрия и спектрофотометрия, применяемые для определения окрашенных веществ и веществ, поглощающих излучение в ультрафиолетовой области. В фотоколориметрических и спектрофотометрических методах измеряют поглощение излучения при определенной длине волны как функцию концентрации анализируемого вещества в растворе с последующим расчетом массовой доли компонента древесины, остаточного компонента в технической целлюлозе и др.
При использовании монохроматического излучения в случае разбавленных растворов оптическая плотность подчиняется основному закону светопоглощения – объединенному закону Бугера–Ламберта–Бера
где–оптическая плотность раствора; е – молярный коэффициент поглощения вещества, дм; с – концентрация поглощающего вещества, моль/дм1; / – толщина поглощающего слоя, см.
Молярный коэффициент поглощения является характеристикой определяемого вещества, тогда как оптическая плотность – характеристикой отдельной пробы раствора.
В случаях, когда концентрацию поглощающего вещества в растворе невозможно выразить в моль/дм3, вместо молярного коэффициента поглощения используют так называемый удельный коэффициент и видоизмененную форму закона Бугера–Ламберта–Бера
где k – удельный коэффициент поглощения вещества, дм г-1 -см-1 .
Закон Бугера–Ламберта – Бера лежит в основе расчетов в фотометрических анализах. При / = const оптическая плотность раствора данного вещества прямо пропорциональна его концентрации. Это позволяет определять концентрацию растворов по градуировочным графикам, которые строят по значениям оптической плотности серии эталонных растворов различной концентрации. Также можно рассчитывать искомую концентрацию по молярным или удельным коэффициентам поглощения, установленным с помощью градуировочных графиков. В последнем случае оптическая плотность должна строго подчиняться закону Бугера–Ламберта–Бера. В первом случае допустимо отклонение градуировочного графика от линейной формы. Измерения оптической плотности можно производить при длинах волн, как соответствующих, так и не соответствующих максимумам спектров поглощения.
Спектрофотометрический метод применяют и для определения в растворах концентраций нескольких веществ при совместном присутствии. Оптическая плотность является аддитивным свойством и поэтому для смеси не взаимодействующих между собой компонентов она равна сумме оптических плотностей этих компонентов при одной и той же длине волны
Для раствора, содержащего з окрашенных или поглощающих УФ-излучение веществ, проводят з независимых измерений оптической плотности при з различных длинах волн л. Получают систему линейных уравнений, решая которую, находят концентрации содержащихся веществ.
В частном случае двухкомпонентных систем обычно замеряют оптические плотности при двух длинах волн, соответствующих максимумам спектров поглощения каждого из двух компонентов. Тогда получают систему двух уравнений
где е' и г» – молярные коэффициенты поглощения соответствующих компонентов; с' и с» – концентрации этих компонентов.
Если еь еь е2, е2 известны, D1 и D2 измерены в опыте, то из этих двух уравнений можно рассчитать концентрации с' и с».
На принципе аддитивности оптической плотности основано введение поправок на растворитель и контрольное определение, когда при измерении оптической плотности раствора определяемого вещества вычитается оптическая плотность раствора сравнения.
Для измерения оптической плотности растворов в видимой области используют фотоэлектроколориметры, а для УФ и видимой области – спектрофотометры.
При работе с фотоэлектроколориметрами и спектрофотометрами, как и с любым другим физико-химическим прибором, сначала необходимо ознакомиться с прилагаемой к нему инструкцией и строго соблюдать ее во время работы.
В качестве растворителей следует использовать только такие, которые не поглощают света в данной области. Концентрацию рабочих растворов подбирают таким образом, чтобы измеряемое значение оптической плотности находилось в пределах 0,2…0,8. При высоких концентрациях интенсивность прошедшего излучения становится слишком малой и на измеряемую оптическую плотность оказывает влияние рассеянное излучение, что приводит к отклонениям от закона Бугера–Ламберта–Бера. Для получения растворов требуемых малых концентраций используют метод последовательных разведений, причем взвешивание растворов и растворителей дает меньшую ошибку, чем разведение по объему.
При очень низких концентрациях ошибка в показаниях прибора становится слишком большой по сравнению с определяемой величиной.
2. Построение градуировочных графиков
Градуировочные графики строят, пользуясь эталонными растворами чистых веществ. Для построения графика необходимо приготовить 5… 10 растворов с различной концентрацией эталонного вещества с таким расчетом, чтобы это число растворов охватило весь интервал, в пределах которого может изменяться концентрация определяемого вещества.
В мерные колбы вместимостью 25 см с притертыми пробками наливают с помощью пипеток различные объемы эталонного раствора определяемого вещества и соответствующие реагенты согласно методике анализа, затем разбавляют до метки водой, буферным раствором или другим соответствующим растворителем и хорошо перемешивают.
При построении градуировочных графиков необходимо подбирать концентрацию раствора и толщину кюветы таким образом, чтобы крайние значения оптической плотности составляли от 0,05 до 1,5. Измерение оптической плотности ниже 0,05 и выше 1,5 приводит к значительному увеличению ошибки измерения.
Значения оптической плотности полученных разбавленных эталонных растворов измеряют в порядке увеличения их концентрации в фотоэлектроколориметре с соответствующим светофильтром или в спектрофотометре при соответствующей длине волны. В качестве раствора сравнения используют раствор, составляемый в соответствии с методикой анализа, но без определяемого вещества. Реагенты, не поглощающие излучения в данной области спектра, в раствор сравнения можно не добавлять. Измеряют оптические плотности трех параллельных проб всех приготовленных разбавленных эталонных растворов с различной концентрацией определяемого вещества. По полученным данным на миллиметровой бумаге строят график. Для, получения наиболее точного графика следует пользоваться методом наименьших квадратов. По оси абсцисс откладывают концентрацию вещества в растворе в граммах, милли- или микрограммах в 1 дм' или 1 см' раствора, а по оси ординат – значения оптической плотности.
Градуировочный график также можно построить, пользуясь эталонными растворами, приготовленными из различных навесок чистого вещества в определенном объеме растворителя. При разбавлении эталонного раствора его определенные порции можно не отмерять пипетками, а отвешивать на аналитических весах.
Градуировочные графики необходимо периодически проверять – при смене реагентов и для нового прибора.
3. Хромофоры органических соединений и применение методов фотоколориметрии и спектрофотометрии в анализах древесины и целлюлозы
Поглощение видимого и УФ-излучения органическими соединениями обусловлено переходами электронов в молекулах, переводящими их в возбужденное состояние. Практическое значение имеют переходы электронов р-связей р* и п-электронов неподеленных пар гетероатомов п->-лЛ так как им соответствуют длины волн, попадающие в рабочий интервал приборов. Полностью насыщенные соединения не проявляют избирательного поглощения ни в видимой, ни в доступной для измерений части УФ-области. Соединения, содержащие одну двойную связь, поглощают свет в дальней УФ-области при длинах волн менее 200 нм. Сопряженные двойные связи вызывают поглощение при больших длинах волн, причем чем длиннее цепь сопряжения, тем при большей длине волны наблюдается поглощение. При достаточно большой длине цепи сопряжения поглощение переходит в видимую область. 'Смещению максимума поглощения в сторону более длинных волн способствуют ароматические и гетероциклические фрагменты, а также электронодонорные группы, содержащие у гетероатома неподеленные пары электронов.
Вся сопряженная система в органическом соединении называется хромофором. От строения хромофора зависит длина волны, соответствующая максимуму поглощения в спектре. Введение заместителей вызывает смещение полосы поглощения и изменение его интенсивности. В зависимости от непосредственного окружения хромофора максимум его поглощения может сдвигаться либо в сторону более длинных волн, либо в сторону менее длинных волн .·
Основными типами хромофоров в органических соединениях служат: диеновые и полиеновые системы; карбонильные группы, сопряженные с двойными связями; бензольные кольца, особенно сопряженные с другими хромофорами; хиноны; ароматические гетероциклические системы, в том числе фуран и его производные. Следует заметить, что у бензольных колец, сопряженных с дополнительными хромофорами, положение максимумов поглощения и их интенсивность колеблются в широких пределах. Вещества, не способные к поглощению, можно определить спектрофотометрически или фотоколориметрически, добавив реагент, образующий с определяемым соединением поглощающий комплекс или хромофорную систему.
Макромолекулы целлюлозы и других полисахаридов не содержат хромофоров и поэтому не поглощают свет ни в видимой, ни в УФ-области. То же самое относится к продуктам их гидролиза, моносахаридам. Однако моносахариды дают многочисленные цветные реакции с различными реагентами с образованием окрашенных продуктов, пригодных для фотоколориметрического или спектрофотометрического определения. Обычно цветная реакция обусловливается образованием из моносахарида фуранового цикла, который и дает окрашивание.
В противоположность углеводам лигнин, имеющий ароматическое строение, поглощает УФ-излучение. В спектре лигнина имеются интенсивный максимум поглощения в области длин волн 203…208 нм, четко выраженное плечо около 230 нм и характерный, но менее интенсивный по сравнению с первым максимум в области 280 нм у лигнинов хвойных древесных пород и при 275…278 нм – у лигнинов лиственных древесных пород. Интенсивность поглощения у лиственных лигнинов ниже, чем у хвойных. Спектр лигнина представляет собой сумму накладывающихся друг на друга полос поглощения различных хромофоров, входящих в макромолекулы лигнина: бензольных колец, содержащих фенольные гидроксильные группы; сопряженных с бензольным кольцом карбонильных групп и двойных связей; дифенмльных структур; группировок хинонов и метиленхинонов и др.
Различные химические обработки лигнина, в том числе варочными агентами в процессах получения из древесины техническнх целлюлоз и других волокнистых полуфабрикатов, за исключением действия окислителей и щелочей в жестких условиях, не затрагивают основных хромофорных группировок. Это позволяет использовать УФ-поглощение лигнина для его количественного определения в технических целлюлозах, в сульфитных и сульфатных варочных растворах в ходе делигнификации, в отработанных щелоках, а также в кислых фильтратах при определении лигнина Класона.
Применяемые в анализе древесины и технических целлюлоз и включенные в данное учебное пособие методы фотометрического анализа условно можно подразделить на следующие группы.
1. Прямой анализ методом поглощения в УФ-области. К этой группе относятся: методы спектрофотометрического определения кислоторастворимого лигнина в фильтратах, получаемых при определении лигнина в древесине и остаточного лигнина в технических целлюлозах гидролизом с концентрированной серной кислотой; определение остаточного лигнина в технических целлюлозах спектрофотометрическим методом в кадоксене; определение фурфурола спектрофотометрическим методом при анализе технических целлюлоз на остаточные пентозаны. Спектрофотометрию в УФ-области можно также использовать для количественного определения лигнина, содержащегося в древесине, растворением ее в ацетилбромиде.
2. Прямой анализ методом свефороглощеиия в видимой области. Этот метод в химии древесины и целлюлозы применяется сравнительно редко. К этой группе относится фотометрическое определение таннинов в водных экстрактах, извлеченных из древесины или коры.
3. Измерение поглощения в видимой области продуктами реакций с определяемым веществом. Эта группа, методов включает: фотоколориметрическое определение фурфурола с орсином при определении пентозанов в древесине и остаточных пентозанов в технических целлюлозах; фотоколориметрическое определение моносахаридов при анализе гидролизатов легко- и трудногидролизуемых полисахаридов древесины методом хроматографии на бумаге.
4. Спектрофотометрический анализ многокомпонентных систем – определение с отолуидиновым реагентом галактуронана, пентозанов и гекспзанов в пектиновых веществах, извлеченных из древесины. Спектрофотометрический анализ многокомпонентных систем можно также использовать для определения лигнина в растворах в присутствии углеводов, измеряя поглощение при двух длинах волн р для определения остаточных пентозанов в технических целлюлозах но фурфуролу с поправкой на гидро-ксиметплфурфурол.
5. Определение цункииональных групп в технических и окисленных целлюлозах с применением или получением в ходе анализа органических красителей. К этой группе методов относятся определение восстанавливающих карбонильных групп по реакции их с хлоридом 2. 3,5 – трифенил-тетразолпя с фотоколорнметрическнм определением образующегося красителя – формазана и определение карбоксильных групп фотоколориметрическим измерением связанного основного красителя – метилепового голубого.
www.ronl.ru
Реферат - Спектрофотометрия и фотоколориметрия
РЕФЕРАТ
СПЕКТРОФОТОМЕТРИЯ И ФОТОКОЛОРИМЕТРИЯ
Тамбов, 2009
Введение
Фотометрические методы – это методы качественного и ко; личественного анализа, основанные на измерении интенсивности пропускания, поглощения или рассеяния инфракрасного, видимого и ультрафиолетового излучения исследуемым веществом. К фотометрическим методам анализа относят атомно-абсорбционный анализ, фотометрию пламени, турбидлметрию, нефелометрию, люминесцентный анализ, спектроскопию отражения и молекулярно-абсорбционный фотометрический анализ.
1. Методы молекулярно-абсорбционного фотометрического анализа
В анализе древесины и технических целлюлоз для количественного определения компонентов или примесей, особенно малых количеств веществ, а также качественной характеристики и структурных исследований широко используют различные методы молекулярно-абсорбционного фотометрического анализа. Эти методы основаны на избирательном поглощении электромагнитного излучения в ультрафиолетовой, видимой и инфракрасной областях молекулами определяемого компонента или его соединения с соответствующим реагентом. Вещества, поглощающие видимый свет, окрашены. Наблюдаемый цвет раствора окрашенного вещества является дополнительным к поглощенному. Бесцветные или слабоокрашенные вещества часто можно определить, добавив реагент, который образует с ними'интенсивно окрашенное соединение или соединение, поглощающее ультрафиолетовое излучение. Обычно используют реакции синтеза окрашенных соединений, а иногда реакции окисления-восстановления.
Молекулярно-абсорбционный фотометрический анализ включает спектрофотометрию, фотоколориметрию и визуальную фотометрию. В отличие от последней фотоколориметрия и спектрофотометрия являются инструментальными методами, в которых поглощение света измеряют с помощью приборов, снабженных фотоэлементами. Из этих методов рассматриваются фотоколориметрия и спектрофотометрия, применяемые для определения окрашенных веществ и веществ, поглощающих излучение в ультрафиолетовой области. В фотоколориметрических и спектрофотометрических методах измеряют поглощение излучения при определенной длине волны как функцию концентрации анализируемого вещества в растворе с последующим расчетом массовой доли компонента древесины, остаточного компонента в технической целлюлозе и др.
При использовании монохроматического излучения в случае разбавленных растворов оптическая плотность подчиняется основному закону светопоглощения – объединенному закону Бугера–Ламберта–Бера
где–оптическая плотность раствора; е – молярный коэффициент поглощения вещества, дм; с – концентрация поглощающего вещества, моль/дм1; / – толщина поглощающего слоя, см.
Молярный коэффициент поглощения является характеристикой определяемого вещества, тогда как оптическая плотность – характеристикой отдельной пробы раствора.
В случаях, когда концентрацию поглощающего вещества в растворе невозможно выразить в моль/дм3, вместо молярного коэффициента поглощения используют так называемый удельный коэффициент и видоизмененную форму закона Бугера–Ламберта–Бера
где k – удельный коэффициент поглощения вещества, дм г-1 -см-1 .
Закон Бугера–Ламберта – Бера лежит в основе расчетов в фотометрических анализах. При / = const оптическая плотность раствора данного вещества прямо пропорциональна его концентрации. Это позволяет определять концентрацию растворов по градуировочным графикам, которые строят по значениям оптической плотности серии эталонных растворов различной концентрации. Также можно рассчитывать искомую концентрацию по молярным или удельным коэффициентам поглощения, установленным с помощью градуировочных графиков. В последнем случае оптическая плотность должна строго подчиняться закону Бугера–Ламберта–Бера. В первом случае допустимо отклонение градуировочного графика от линейной формы. Измерения оптической плотности можно производить при длинах волн, как соответствующих, так и не соответствующих максимумам спектров поглощения.
Спектрофотометрический метод применяют и для определения в растворах концентраций нескольких веществ при совместном присутствии. Оптическая плотность является аддитивным свойством и поэтому для смеси не взаимодействующих между собой компонентов она равна сумме оптических плотностей этих компонентов при одной и той же длине волны
Для раствора, содержащего з окрашенных или поглощающих УФ-излучение веществ, проводят з независимых измерений оптической плотности при з различных длинах волн л. Получают систему линейных уравнений, решая которую, находят концентрации содержащихся веществ.
В частном случае двухкомпонентных систем обычно замеряют оптические плотности при двух длинах волн, соответствующих максимумам спектров поглощения каждого из двух компонентов. Тогда получают систему двух уравнений
где е' и г» – молярные коэффициенты поглощения соответствующих компонентов; с' и с» – концентрации этих компонентов.
Если еь еь е2, е2 известны, D1 и D2 измерены в опыте, то из этих двух уравнений можно рассчитать концентрации с' и с».
На принципе аддитивности оптической плотности основано введение поправок на растворитель и контрольное определение, когда при измерении оптической плотности раствора определяемого вещества вычитается оптическая плотность раствора сравнения.
Для измерения оптической плотности растворов в видимой области используют фотоэлектроколориметры, а для УФ и видимой области – спектрофотометры.
При работе с фотоэлектроколориметрами и спектрофотометрами, как и с любым другим физико-химическим прибором, сначала необходимо ознакомиться с прилагаемой к нему инструкцией и строго соблюдать ее во время работы.
В качестве растворителей следует использовать только такие, которые не поглощают света в данной области. Концентрацию рабочих растворов подбирают таким образом, чтобы измеряемое значение оптической плотности находилось в пределах 0,2…0,8. При высоких концентрациях интенсивность прошедшего излучения становится слишком малой и на измеряемую оптическую плотность оказывает влияние рассеянное излучение, что приводит к отклонениям от закона Бугера–Ламберта–Бера. Для получения растворов требуемых малых концентраций используют метод последовательных разведений, причем взвешивание растворов и растворителей дает меньшую ошибку, чем разведение по объему.
При очень низких концентрациях ошибка в показаниях прибора становится слишком большой по сравнению с определяемой величиной.
2. Построение градуировочных графиков
Градуировочные графики строят, пользуясь эталонными растворами чистых веществ. Для построения графика необходимо приготовить 5… 10 растворов с различной концентрацией эталонного вещества с таким расчетом, чтобы это число растворов охватило весь интервал, в пределах которого может изменяться концентрация определяемого вещества.
В мерные колбы вместимостью 25 см с притертыми пробками наливают с помощью пипеток различные объемы эталонного раствора определяемого вещества и соответствующие реагенты согласно методике анализа, затем разбавляют до метки водой, буферным раствором или другим соответствующим растворителем и хорошо перемешивают.
При построении градуировочных графиков необходимо подбирать концентрацию раствора и толщину кюветы таким образом, чтобы крайние значения оптической плотности составляли от 0,05 до 1,5. Измерение оптической плотности ниже 0,05 и выше 1,5 приводит к значительному увеличению ошибки измерения.
Значения оптической плотности полученных разбавленных эталонных растворов измеряют в порядке увеличения их концентрации в фотоэлектроколориметре с соответствующим светофильтром или в спектрофотометре при соответствующей длине волны. В качестве раствора сравнения используют раствор, составляемый в соответствии с методикой анализа, но без определяемого вещества. Реагенты, не поглощающие излучения в данной области спектра, в раствор сравнения можно не добавлять. Измеряют оптические плотности трех параллельных проб всех приготовленных разбавленных эталонных растворов с различной концентрацией определяемого вещества. По полученным данным на миллиметровой бумаге строят график. Для, получения наиболее точного графика следует пользоваться методом наименьших квадратов. По оси абсцисс откладывают концентрацию вещества в растворе в граммах, милли- или микрограммах в 1 дм' или 1 см' раствора, а по оси ординат – значения оптической плотности.
Градуировочный график также можно построить, пользуясь эталонными растворами, приготовленными из различных навесок чистого вещества в определенном объеме растворителя. При разбавлении эталонного раствора его определенные порции можно не отмерять пипетками, а отвешивать на аналитических весах.
Градуировочные графики необходимо периодически проверять – при смене реагентов и для нового прибора.
3. Хромофоры органических соединений и применение методов фотоколориметрии и спектрофотометрии в анализах древесины и целлюлозы
Поглощение видимого и УФ-излучения органическими соединениями обусловлено переходами электронов в молекулах, переводящими их в возбужденное состояние. Практическое значение имеют переходы электронов р-связей р* и п-электронов неподеленных пар гетероатомов п->-лЛ так как им соответствуют длины волн, попадающие в рабочий интервал приборов. Полностью насыщенные соединения не проявляют избирательного поглощения ни в видимой, ни в доступной для измерений части УФ-области. Соединения, содержащие одну двойную связь, поглощают свет в дальней УФ-области при длинах волн менее 200 нм. Сопряженные двойные связи вызывают поглощение при больших длинах волн, причем чем длиннее цепь сопряжения, тем при большей длине волны наблюдается поглощение. При достаточно большой длине цепи сопряжения поглощение переходит в видимую область. 'Смещению максимума поглощения в сторону более длинных волн способствуют ароматические и гетероциклические фрагменты, а также электронодонорные группы, содержащие у гетероатома неподеленные пары электронов.
Вся сопряженная система в органическом соединении называется хромофором. От строения хромофора зависит длина волны, соответствующая максимуму поглощения в спектре. Введение заместителей вызывает смещение полосы поглощения и изменение его интенсивности. В зависимости от непосредственного окружения хромофора максимум его поглощения может сдвигаться либо в сторону более длинных волн, либо в сторону менее длинных волн .·
Основными типами хромофоров в органических соединениях служат: диеновые и полиеновые системы; карбонильные группы, сопряженные с двойными связями; бензольные кольца, особенно сопряженные с другими хромофорами; хиноны; ароматические гетероциклические системы, в том числе фуран и его производные. Следует заметить, что у бензольных колец, сопряженных с дополнительными хромофорами, положение максимумов поглощения и их интенсивность колеблются в широких пределах. Вещества, не способные к поглощению, можно определить спектрофотометрически или фотоколориметрически, добавив реагент, образующий с определяемым соединением поглощающий комплекс или хромофорную систему.
Макромолекулы целлюлозы и других полисахаридов не содержат хромофоров и поэтому не поглощают свет ни в видимой, ни в УФ-области. То же самое относится к продуктам их гидролиза, моносахаридам. Однако моносахариды дают многочисленные цветные реакции с различными реагентами с образованием окрашенных продуктов, пригодных для фотоколориметрического или спектрофотометрического определения. Обычно цветная реакция обусловливается образованием из моносахарида фуранового цикла, который и дает окрашивание.
В противоположность углеводам лигнин, имеющий ароматическое строение, поглощает УФ-излучение. В спектре лигнина имеются интенсивный максимум поглощения в области длин волн 203…208 нм, четко выраженное плечо около 230 нм и характерный, но менее интенсивный по сравнению с первым максимум в области 280 нм у лигнинов хвойных древесных пород и при 275…278 нм – у лигнинов лиственных древесных пород. Интенсивность поглощения у лиственных лигнинов ниже, чем у хвойных. Спектр лигнина представляет собой сумму накладывающихся друг на друга полос поглощения различных хромофоров, входящих в макромолекулы лигнина: бензольных колец, содержащих фенольные гидроксильные группы; сопряженных с бензольным кольцом карбонильных групп и двойных связей; дифенмльных структур; группировок хинонов и метиленхинонов и др.
Различные химические обработки лигнина, в том числе варочными агентами в процессах получения из древесины техническнх целлюлоз и других волокнистых полуфабрикатов, за исключением действия окислителей и щелочей в жестких условиях, не затрагивают основных хромофорных группировок. Это позволяет использовать УФ-поглощение лигнина для его количественного определения в технических целлюлозах, в сульфитных и сульфатных варочных растворах в ходе делигнификации, в отработанных щелоках, а также в кислых фильтратах при определении лигнина Класона.
Применяемые в анализе древесины и технических целлюлоз и включенные в данное учебное пособие методы фотометрического анализа условно можно подразделить на следующие группы.
1. Прямой анализ методом поглощения в УФ-области. К этой группе относятся: методы спектрофотометрического определения кислоторастворимого лигнина в фильтратах, получаемых при определении лигнина в древесине и остаточного лигнина в технических целлюлозах гидролизом с концентрированной серной кислотой; определение остаточного лигнина в технических целлюлозах спектрофотометрическим методом в кадоксене; определение фурфурола спектрофотометрическим методом при анализе технических целлюлоз на остаточные пентозаны. Спектрофотометрию в УФ-области можно также использовать для количественного определения лигнина, содержащегося в древесине, растворением ее в ацетилбромиде.
2. Прямой анализ методом свефороглощеиия в видимой области. Этот метод в химии древесины и целлюлозы применяется сравнительно редко. К этой группе относится фотометрическое определение таннинов в водных экстрактах, извлеченных из древесины или коры.
3. Измерение поглощения в видимой области продуктами реакций с определяемым веществом. Эта группа, методов включает: фотоколориметрическое определение фурфурола с орсином при определении пентозанов в древесине и остаточных пентозанов в технических целлюлозах; фотоколориметрическое определение моносахаридов при анализе гидролизатов легко- и трудногидролизуемых полисахаридов древесины методом хроматографии на бумаге.
4. Спектрофотометрический анализ многокомпонентных систем – определение с отолуидиновым реагентом галактуронана, пентозанов и гекспзанов в пектиновых веществах, извлеченных из древесины. Спектрофотометрический анализ многокомпонентных систем можно также использовать для определения лигнина в растворах в присутствии углеводов, измеряя поглощение при двух длинах волн р для определения остаточных пентозанов в технических целлюлозах но фурфуролу с поправкой на гидро-ксиметплфурфурол.
5. Определение цункииональных групп в технических и окисленных целлюлозах с применением или получением в ходе анализа органических красителей. К этой группе методов относятся определение восстанавливающих карбонильных групп по реакции их с хлоридом 2. 3,5 – трифенил-тетразолпя с фотоколорнметрическнм определением образующегося красителя – формазана и определение карбоксильных групп фотоколориметрическим измерением связанного основного красителя – метилепового голубого.
www.ronl.ru
|
|
..:::Счетчики:::.. |
|
|
|
|
|
|
|
|


