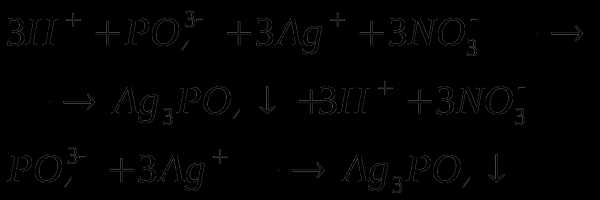|
|
|
|
 Far Far |
 WinNavigator WinNavigator |
 Frigate Frigate |
 Norton
Commander Norton
Commander |
 WinNC WinNC |
 Dos
Navigator Dos
Navigator |
 Servant
Salamander Servant
Salamander |
 Turbo
Browser Turbo
Browser |
|
|
 Winamp,
Skins, Plugins Winamp,
Skins, Plugins |
 Необходимые
Утилиты Необходимые
Утилиты |
 Текстовые
редакторы Текстовые
редакторы |
 Юмор Юмор |
|
|
|
File managers and best utilites |
Реферат по химии на тему «Фосфор». Реферат фосфор
Реферат на тему "Фосфор"
Распространенность в природе
Массовая доля фосфора в земной коре составляет 0,08%. Важнейшими минералами фосфора, встречающимися в природе, являются фторапатит Ca5(PO4)3F и фосфорит Ca3(PO4)2.
Свойства
Фосфор образует несколько аллотропных модификаций, которые заметно различаются по свойствам. Белый фосфор — мягкое кристаллическое вещество. Состоит из молекул P4. Плавится при температуре 44,1°С. Очень хорошо растворим в сероуглероде CS2. Черезвычайно ядовит и легко загорается.
При нагревании белого фосфора образуется Красный фосфор. Он представляет собой смесь нескольких модификаций, которые имеют различную длину молекул. Цвет красного фосфора в зависимости от способа и условий получения может меняться от светло-красного до фиолетового и темно-коричневого. Температура его плавления 585-600°.
Черный фосфор — наиболее устойчивая модификация. По внешнему виду он похож на графит. В отличие от белого фосфора красный и черный фосфор не растворяются в сероуглероде, они не ядовиты и не огнеопасны.
Фосфор химически более активен, чем азот. Химическая активность фосфора зависит от аллотропной модификации, в которой он находится. Так, наиболее активен белый фосфор, а наимнее активен черный фосфор.
В уравнениях химических реакций белый фосфор обычно записывают формулой P4, которая соответствует составу его молекул. Красная и черная модификации фосфора обычно записываются формулой P. Этот же символ используют, если модификация неизвестна или может быть любой.
1. Взаимодействие с простыми веществами — неметаллами. Фосфор может реагировать со многими неметаллами: кислородом, серой, галогенами, с водородом фосфор не реагирует. В зависимости от того, находится фосфор в избытке или недостатке, образуются соединения фосфора (III) и (V), например: 2P + 3Br2 = 2PBr3 или 2P + 5Br2 = 2PBr5
2. Взаимодействие с металлами. При нагревании фосфора с металлами образуются фосфиды: 3Mg + 2P = Mg3P2
Фосфиды некоторых металлов могут разлагаться водой с образованием газообразного фосфина Ph4: Mg3P2 + 6h3O = 3Mg(OH)2 + 2Ph4
Фосфин Ph4 по химическим свойствам похож на аммиак Nh4.
3. Взаимодействие со щелочами. При нагревании белого фосфора в растворе щелочи он диспропорционирует:
0 -3 +1
P4+ 3NaOH + 3h3O = Ph4+ 3Nah3PO2
Получение. Фосфор в промышленности получают из фосфата кальция Ca3(PO4)2, который выделяют из фосфоритов и фторапатитов. Метод получения основан на реакции восстановления Ca3(PO4)2 до фосфора.
В качестве восстановителя соединений фосфора используют кокс (углерод). Для связывания соединений кальция в реакционную систему добавляют кварцевый песок SiO2. Процесс проводят в электопечах (производство относят к электротермическим). Реакция протекает по уравнению: 2Ca3(PO4)2 + 6SiO2 + 10C = 6CaSiO3 + P4 + 10CO
Продукт реакции — белый фосфор. Из-за наличия примесей технический фосфор имеет желтый цвет, поэтому в промышленности его называют желтым фосфором.
Фосфорные удобрения
Фосфор, так же как и азот, является важным элементом для обеспечения роста и жизнедеятельности растений. Растения извлекают фосфор из почвы, поэтому его запасы необходимо восполнять, периодически добавляя фосфорные удобрения. Фосфорные удобрения производят из фосфата кальция, который входит в состав природных фосфоритов и фторапатитов.
Простейшее фосфорное удобрение — фосфоритная мука представляет собой перемолотый фосфорит Ca3(PO4)2. Это удобрение труднорастворимо, оно может усваиваться растениями только на кислых почвах.
Действием серной кислоты на фосфат кальция получают простой суперфосфат, основным компонентом которого является дигидрофосфат кальция Ca(h3PO4)2. Это — растворимое вещество, и оно хорошо усваивается растениями. Метод получения простого суперфосфата основан на реакции Ca3(PO4)2 + 2h3SO4 = Ca(h3PO4)2 + 2CaSO4
Кроме основного компонента суперфосфат содержит до 50% сульфата кальция, который является балластом. Для повышения содержания фосфора в удобрении проводят обработку фосфорита фосфорной кислотой: Ca3(PO4)2 + 4h4PO4 = 3Ca(h3PO4)2
Получаемое удобрение называется двойным суперфосфатом. Еще одно фосфорное удобрение с высоким содержанием фосфора — преципитат CaHPO4·2h3O.
Высококонцентрированные фосфорные удобрения приготавливают на основе суперфосфорной кислоты — смеси полифосфорных кислот h5P2O7, H5P3O10, H6P4O13 и др. Эти кислоты образуются при нагреавнии фосфорной кислоты h4PO4 в вакууме.
При взаимодействии полифосфорных кислот с аммиаком образуются полифосфаты аммония, которые используются как комплексные азотно-фосфорные удобрения.
Вместе с азотом фосфор входит в состав некоторых других комплексных удобрений, например аммофоса Nh5h3PO4 и диаммофоса (Nh5)2HPO4.
referati-besplatno.ru
Реферат - Фосфор - Химия
Фосфор
Распространенность в природе.Массоваядоля фосфора в земной коре составляет 0,08%.Важнейшими минералами фосфора, встречающимися в природе, являются фторапатит Ca5(PO4)3Fи фосфорит Ca3(PO4)2.
Свойства. Фосфор образуетнесколько аллотропных модификаций, которые заметно различаются по свойствам. Белыйфосфор — мягкое кристаллическое вещество. Состоит из молекул P4.Плавится при температуре 44,1<span Times New Roman""><span Times New Roman"">°
С. Очень хорошо растворим всероуглероде CS2.Черезвычайно ядовит и легко загорается.Принагревании белого фосфора образуется Красный фосфор. Он представляетсобой смесь нескольких модификаций, которые имеют различную длину молекул. Цветкрасного фосфора в зависимости от способа и условий получения может меняться от светло-красного до фиолетового итемно-коричневого. Температура его плавления 585-600<span Times New Roman""><span Times New Roman"">°
.Черныйфосфор — наиболее устойчивая модификация. По внешнему видуонпохож на графит. В отличие от белого фосфора красный и черный фосфор нерастворяются в сероуглероде, они не ядовиты и не огнеопасны.
Фосфорхимически более активен, чем азот. Химическая активность фосфора зависит оталлотропной модификации, в которой он находится. Так, наиболее активен белыйфосфор, а наимнее активен черный фосфор.
Вуравнениях химических реакций белый фосфор обычно записывают формулой P4,которая соответствует составу его молекул. Красная и черная модификации фосфораобычно записываются формулой P. Этот же символ используют, если модификация неизвестнаили может быть любой.
1.Взаимодействие с простыми веществами — неметаллами.Фосформожетреагировать со многими неметаллами: кислородом, серой, галогенами, с водородом фосфор не реагирует. Взависимости от того, находится фосфор в избытке или недостатке, образуютсясоединения фосфора (III)и (V), например:
2P + 3Br2= 2PBr3 или 2P + 5Br2= 2PBr5
2. Взаимодействиес металлами.При нагревании фосфора с металлами образуются фосфиды:
3Mg + 2P = Mg3P2
Фосфиды некоторых металлов могут разлагаться водойс образованием газообразного фосфина Ph4:
Mg3P2+ 6h3O = 3Mg(OH)2+ 2Ph4
Фосфин Ph4похимическим свойствам похож на аммиак Nh4.
3. Взаимодействиесо щелочами. При нагревании белого фосфора в растворе щелочи ондиспропорционирует:
0 -3 +1
P4+ 3NaOH + 3h3O = Ph4+ 3Nah3PO2
Получение. Фосфор впромышленности получают из фосфата кальция Ca3(PO4)2, который выделяют из фосфоритов и фторапатитов.Метод получения основан на реакции восстановления Ca3(PO4)2до фосфора.
Вкачестве восстановителя соединений фосфора используют кокс (углерод). Длясвязывания соединений кальция в реакционную систему добавляют кварцевый песок SiO2. Процесс проводят в электопечах (производство относят кэлектротермическим). Реакция протекает по уравнению:
2Ca3(PO4)2+ 6SiO2+ 10C = 6CaSiO3+ P4+ 10CO
Продукт реакции — белый фосфор. Из-за наличияпримесей технический фосфор имеет желтый цвет, поэтому в промышленности егоназывают желтым фосфором.
Фосфорные удобрения. Фосфор,так же как и азот, является важным элементом для обеспечения роста ижизнедеятельности растений. Растения извлекают фосфор из почвы, поэтому егозапасы необходимо восполнять, периодически добавляя фосфорные удобрения.Фосфорные удобрения производят из фосфата кальция, который входит в составприродных фосфоритов и фторапатитов.
Простейшее фосфорное удобрение — фосфоритная мука представляет собойперемолотый фосфорит Ca3(PO4)2. Этоудобрение труднорастворимо, оно можетусваиваться растениями только на кислых почвах.
Действием серной кислоты на фосфат кальция получают простой суперфосфат,основным компонентом которого является дигидрофосфат кальция Ca(h3PO4)2. Это — растворимое вещество, и оно хорошоусваивается растениями. Метод получения простого суперфосфата основан на реакции
Ca3(PO4)2+ 2h3SO4 = Ca(h3PO4)2+ 2CaSO4
Кромеосновного компонента суперфосфат содержит до 50% сульфата кальция, который является балластом. Для повышениясодержания фосфора в удобрении проводят обработку фосфорита фосфорной кислотой:
Ca3(PO4)2+ 4h4PO4 = 3Ca(h3PO4)2
Получаемое удобрение называется двойным суперфосфатом. Еще однофосфорное удобрение с высоким содержанием фосфора — преципитатCaHPO4<span Times New Roman""><span Times New Roman"">·
2h3O.Высококонцентрированные фосфорные удобрения приготавливают на основе суперфосфорнойкислоты — смеси полифосфорных кислот h5P2O7, H5P3O10, H6P4O13и др.Эти кислоты образуются принагреавнии фосфорной кислотыh4PO4в вакууме.
Привзаимодействии полифосфорных кислот с аммиаком образуются полифосфаты аммония,которые используются как комплексные азотно-фосфорные удобрения.
Вместес азотом фосфор входит в состав некоторых других комплексных удобрений,например аммофоса Nh5h3PO4 и диаммофоса(Nh5)2HPO4.
Уткин Евгений Валерьевич
СПбРТ, гр. 9В-144
При написании реферата была использована
следующая литература:
1. <span Times New Roman"">
И.Г.Хомченко ‘Общая химия’, М. ‘Химия’19872. <span Times New Roman"">
Г.П.Хомченко ‘Химия для поступающих в ВУЗы’,М.’Высшаяшкола’1994
www.ronl.ru
Реферат Фосфор
скачатьРеферат на тему:
План:
- Введение
- 1 История
- 2 Происхождение названия
- 3 Получение
- 4 Физические свойства
- 4.1 Белый фосфор
- 4.2 Жёлтый фосфор
- 4.3 Красный фосфор
- 4.4 Чёрный фосфор
- 4.5 Металлический фосфор
- 5 Химические свойства
- 5.1 Взаимодействие с простыми веществами
- 5.2 Взаимодействие с водой
- 5.3 Взаимодействие со щелочами
- 5.4 Восстановительные свойства
- 6 Применение
- 6.1 Элементарный фосфор
- 6.2 Соединения фосфора в сельском хозяйстве
- 6.3 Соединения фосфора в промышленности
- 6.4 Фосфатные связующие
- 7 Биологическая роль соединений фосфора
- 7.1 Токсикология элементарного фосфора
- 7.2 Токсикология соединений фосфора
Примечания
Введение
Фосфор(от греч. phosphoros - светоносный; лат. Phosphorus) — один из самых распространённых элементов земной коры, его содержание составляет 0,08—0,09 % её массы. Концентрация в морской воде 0,07 мг/л[4]. В свободном состоянии не встречается из-за высокой химической активности. Образует около 190 минералов, важнейшими из которых являются апатит Ca5(PO4)3(F,Cl,OH) фосфорит Ca3(PO4)2 и другие. Фосфор содержится во всех частях зелёных растений, ещё больше его в плодах и семенах (см. фосфолипиды). Содержится в животных тканях, входит в состав белков и других важнейших органических соединений (АТФ, ДНК), является элементом жизни.
1. История
Фосфор открыт гамбургским алхимиком Хеннигом Брандом в 1669 году. Подобно другим алхимикам, Бранд пытался отыскать философский камень, а получил светящееся вещество. Бранд сфокусировался на опытах с человеческой мочой, так как полагал, что она, обладая золотистым цветом, может содержать золото или нечто нужное для добычи. Первоначально его способ заключался в том, что сначала моча отстаивалась в течение нескольких дней, пока не исчезнет неприятных запах, а затем кипятилась до клейкого состояния. Нагревая эту пасту до высоких температур и доводя до появления пузырьков, он надеялся, что, сконденсировавшись, они будут содержать золото. После нескольких часов интенсивных кипячений получались крупицы белого воскоподобного вещества, которое очень ярко горело и к тому же мерцало в темноте. Бранд назвал это вещество phosphorus mirabilis (лат. «чудотворный носитель света»). Открытие Брандом фосфора стало первым открытием нового элемента со времён античности.
Несколько позже фосфор был получен другим немецким химиком — Иоганном Кункелем.
Независимо от Бранда и Кункеля фосфор был получен Р. Бойлем, описавшим его в статье «Способ приготовления фосфора из человеческой мочи», датированной 14 октября 1680 года и опубликованной в 1693 году.
Усовершенствованный способ получения фосфора был опубликован в 1743 году Андреасом Маргграфом.
Существуют данные, что фосфор умели получать еще арабские алхимики в XII в.
То, что фосфор — простое вещество, доказал Лавуазье.
2. Происхождение названия
В 1669 году Хеннинг Бранд при нагревании смеси белого песка и выпаренной мочи получил светящееся в темноте вещество, названное сначала «холодным огнём». Вторичное название «фосфор» происходит от греческих слов «φῶς» — свет и «φέρω» — несу. В древнегреческой мифологии имя Фосфор (или Эосфор, др.-греч. Φωσφόρος) носил страж Утренней звезды.
3. Получение
Фосфор получают из апатитов или фосфоритов в результате взаимодействия с коксом и кремнезёмом при температуре 1600 °С:
- 2Ca3(PO4)2 + 10C + 6SiO2 → P4 + 10CO + 6CaSiO3.
Образующиеся пары белого фосфора конденсируются в приёмнике под водой. Вместо фосфоритов восстановлению можно подвергнуть и другие соединения, например, метафосфорную кислоту:
- 4HPO3 + 12C → 4P + 2h3 + 12CO.
4. Физические свойства
Элементарный фосфор в обычных условиях представляет собой несколько устойчивых аллотропических модификаций; вопрос аллотропии фосфора сложен и до конца не решён. Обычно выделяют четыре модификации простого вещества — белую, красную, черную и металлический фосфор. Иногда их ещё называют главными аллотропными модификациями, подразумевая при этом, что все остальные являются разновидностью указанных четырёх. В обычных условиях существует только три аллотропических модификации фосфора, а в условиях сверхвысоких давлений — также металлическая форма. Все модификации различаются по цвету, плотности и другим физическим характеристикам; заметна тенденция к резкому убыванию химической активности при переходе от белого к металлическому фосфору и нарастанию металлических свойств.

Аллотропические модификации фосфора
4.1. Белый фосфор
Белый фосфор представляет собой белое вещество (из-за примесей может иметь желтоватый оттенок) с температурой плавления 44,1 °С. По внешнему виду он очень похож на очищенный воск или парафин, легко режется ножом и деформируется от небольших усилий.

Открытие Хеннигом Брандом фосфораДжозеф Райт, 1771 год
Белый фосфор имеет молекулярное строение; формула P4. Отливаемый в инертной атмосфере в виде палочек (слитков), он сохраняется в отсутствии воздуха под слоем очищенной воды или в специальных инертных средах.
Легкорастворим в органических растворителях. Растворимостью белого фосфора в сероуглероде пользуются для промышленной очистки его от примесей. Плотность белого фосфора из всех его модификаций наименьшая и составляет около 1823 кг/м³. Плавится белый фосфор при 44,1 °C. В парообразном состоянии происходит диссоциация молекул фосфора.
Химически белый фосфор чрезвычайно активен. Например, он медленно окисляется кислородом воздуха уже при комнатной температуре и светится (бледно-зелёное свечение). Явление такого рода свечения вследствие химических реакций окисления называется хемилюминесценцией (иногда ошибочно фосфоресценцией).
Белый фосфор не только активен химически, но и весьма ядовит (вызывает поражение костей, костного мозга, некроз челюстей). Летальная доза белого фосфора для взрослого мужчины составляет 0,05—0,1 г.
4.2. Жёлтый фосфор
Неочищенный белый фосфор обычно называют «жёлтый фосфор». Сильно ядовитое (ПДК в атмосферном воздухе 0,0005 мг/м³), огнеопасное кристаллическое вещество от светло-жёлтого до тёмно-бурого цвета. Удельный вес 1,83 г/см³, плавится при +34 °C, кипит при +280 °C. В воде не растворяется, на воздухе легко окисляется и самовоспламеняется. Горит ослепительным ярко-зеленым пламенем с выделением густого белого дыма — мелких частичек декаоксида тетрафосфора P4O10[5]. Несмотря на то, что в результате реакции между фосфором и водой (4Р + 6Н2О → РН3 + 3Н3РО2) выделяется ядовитый газ фосфин (РН3), для тушения фосфора используют воду в больших количествах (для снижения температуры очага возгорания и перевода фосфора в твердое состояние) или раствор сульфата меди (медного купороса), после гашения фосфор засыпают влажным песком. Для предохранения от самовозгорания желтый фосфор хранится и перевозится под слоем воды (раствора хлорида кальция).
4.3. Красный фосфор
Красный фосфор
Красный фосфор, также называемый фиолетовым фосфором, — это более термодинамически стабильная модификация элементарного фосфора. Впервые он был получен в 1847 году в Швеции австрийским химиком А. Шрёттером при нагревании белого фосфора при 500 °С в атмосфере угарного газа (СО) в запаянной стеклянной ампуле.
Красный фосфор имеет формулу Рn и представляет собой полимер со сложной структурой. В зависимости от способа получения и степени дробления красного фосфора, имеет оттенки от пурпурно-красного до фиолетового, а в литом состоянии — тёмно-фиолетовый с медным оттенком металлический блеск. Химическая активность красного фосфора значительно ниже, чем у белого; ему присуща исключительно малая растворимость. Растворить красный фосфор возможно лишь в некоторых расплавленных металлах (свинец и висмут), чем иногда пользуются для получения крупных его кристаллов. Так, например, немецкий физико-химик И. В. Гитторф в 1865 году впервые получил прекрасно построенные, но небольшие по размеру кристаллы (фосфор Гитторфа). Красный Фосфор на воздухе не самовоспламеняется, вплоть до температуры 240—250 °С (при переходе в белую форму во время возгонки), но самовоспламеняется при трении или ударе, у него полностью отсутствует явление хемолюминесценции. Нерастворим в воде, а также в бензоле, сероуглероде и других, растворим в трибромиде фосфора. При температуре возгонки красный фосфор превращается в пар, при охлаждении которого образуется в основном белый фосфор.
Ядовитость его в тысячи раз меньше, чем у белого, поэтому он применяется гораздо шире, например, в производстве спичек (составом на основе красного фосфора покрыта тёрочная поверхность коробков). Плотность красного фосфора также выше, и достигает 2400 кг/м³ в литом виде. При хранении на воздухе красный фосфор в присутствии влаги постепенно окисляется, образуя гигроскопичный оксид, поглощает воду и отсыревает («отмокает»), образуя вязкую фосфорную кислоту; поэтому его хранят в герметичной таре. При «отмокании» — промывают водой от остатков фосфорных кислот, высушивают и используют по назначению.
4.4. Чёрный фосфор
Чёрный фосфор — это наиболее стабильная термодинамически и химически наименее активная форма элементарного фосфора. Впервые чёрный фосфор был получен в 1914 году американским физиком П. У. Бриджменом из белого фосфора в виде чёрных блестящих кристаллов, имеющих высокую (2690 кг/м³) плотность. Для проведения синтеза чёрного фосфора Бриджмен применил давление в 2×109 Па (20 тысяч атмосфер) и температуру около 200 °С. Начало быстрого перехода лежит в области 13 000 атмосфер и температуре около 230 °С.
Чёрный фосфор представляет собой чёрное вещество с металлическим блеском, жирное на ощупь и весьма похожее на графит, и с полностью отсутствующей растворимостью в воде или органических растворителях. Поджечь чёрный фосфор можно, только предварительно сильно раскалив в атмосфере чистого кислорода до 400 °С. Чёрный фосфор проводит электрический ток и имеет свойства полупроводника. Температура плавления чёрного фосфора 1000 °С под давлением 18×105 Па.
4.5. Металлический фосфор
При 8,3×1010 Па чёрный фосфор переходит в новую, ещё более плотную и инертную металлическую фазу с плотностью 3,56 г/см³, а при дальнейшем повышении давления до 1,25×1011 Па — ещё более уплотняется и приобретает кубическую кристаллическую решётку, при этом его плотность возрастает до 3,83 г/см³. Металлический фосфор очень хорошо проводит электрический ток.
5. Химические свойства
Химическая активность фосфора значительно выше, чем у азота. Химические свойства фосфора во многом определяются его аллотропной модификацией. Белый фосфор очень активен, в процессе перехода к красному и чёрному фосфору химическая активность резко снижается. Белый фосфор на воздухе светится в темноте, свечение обусловлено окислением паров фосфора до низших оксидов.
В жидком и растворенном состоянии, а также в парах до 800 °С фосфор состоит из молекул Р4. При нагревании выше 800 °С молекулы диссоциируют: Р4 = 2Р2. При температуре выше 2000 °С молекулы распадаются на атомы.
5.1. Взаимодействие с простыми веществами
Фосфор легко окисляется кислородом:
- 4P + 5O2 → 2P2O5 (с избытком кислорода),
- 4P + 3O2 → 2P2O3 (при медленном окислении или при недостатке кислорода).
Взаимодействует со многими простыми веществами — галогенами, серой, некоторыми металлами, проявляя окислительные и восстановительные свойства:
с металлами — окислитель, образует фосфиды:
- 2P + 3Ca → Ca3P2,
- 2P + 3Mg → Mg3P2.
фосфиды разлагаются водой и кислотами с образованием фосфина
с неметаллами — восстановитель:
- 2P + 3S → P2S3,
- 2P + 3Cl2 → 2PCl3.
Не взаимодействует с водородом.
5.2. Взаимодействие с водой
Взаимодействует с водой, при этом диспропорционирует:
- 8Р + 12Н2О = 5РН3 + 3Н3РО4 (фосфорная кислота).
5.3. Взаимодействие со щелочами
В растворах щелочей диспропорционирование происходит в большей степени:
- 4Р + 3KOH + 3Н2О → РН3 + 3KН2РО2.
5.4. Восстановительные свойства
Сильные окислители превращают фосфор в фосфорную кислоту:
- 3P + 5HNO3 + 2h3O → 3h4PO4 + 5NO;
- 2P + 5h3SO4 → 2h4PO4 + 5SO2 + 2h3O.
Реакция окисления также происходит при поджигании спичек, в качестве окислителя выступает бертолетова соль:
- 6P + 5KClO3 → 5KCl + 3P2O5
6. Применение
Фосфор является важнейшим биогенным элементом и в то же время находит очень широкое применение в промышленности. Красный фосфор применяют в производстве спичек. Его вместе с тонко измельчённым стеклом и клеем наносят на боковую поверхность коробка. При трении спичечной головки, в состав которой входят хлорат калия и сера, происходит воспламенение.
6.1. Элементарный фосфор
Пожалуй, первое свойство фосфора, которое человек поставил себе на службу, — это горючесть. Горючесть фосфора очень велика и зависит от аллотропической модификации.
Наиболее активен химически, токсичен и горюч белый («жёлтый») фосфор, потому он очень часто применяется (в зажигательных бомбах и пр.).
Красный фосфор — основная модификация, производимая и потребляемая промышленностью. Он применяется в производстве спичек, взрывчатых веществ, зажигательных составов, различных типов топлива, а также противозадирных смазочных материалов, в качестве газопоглотителя в производстве ламп накаливания.
6.2. Соединения фосфора в сельском хозяйстве
Фосфор (в виде фосфатов) — один из трёх важнейших биогенных элементов (NPK), участвует в синтезе АТФ. Большая часть производимой фосфорной кислоты идёт на получение фосфорных удобрений — суперфосфата, преципитата, аммофоски и др.
6.3. Соединения фосфора в промышленности
Фосфаты широко используются:
- в качестве комплексообразователей (средства для умягчения воды),
- в составе пассиваторов поверхности металлов (защита от коррозии, например, т. н. состав «мажеф»).
6.4. Фосфатные связующие
Способность фосфатов формировать прочную трёхмерную полимерную сетку используется для изготовления фосфатных и алюмофосфатных связок
7. Биологическая роль соединений фосфора
Фосфор присутствует в живых клетках в виде орто- и пирофосфорной кислот, входит в состав нуклеотидов, нуклеиновых кислот, фосфопротеидов, фосфолипидов, коферментов, ферментов. Кости человека состоят из гидроксилапатита 3Са3(РО4)3·Ca(OH)2. В состав зубной эмали входит фторапатит. Основную роль в превращениях соединений фосфора в организме человека и животных играет печень. Обмен фосфорных соединений регулируется гормонами и витамином D. Суточная потребность человека в фосфоре 800—1500 мг. При недостатке фосфора в организме развиваются различные заболевания костей.
7.1. Токсикология элементарного фосфора
- Красный фосфор практически нетоксичен. Пыль красного фосфора, попадая в легкие, вызывает пневмонию при хроническом действии.
- Белый фосфор очень ядовит, растворим в липидах. Смертельная доза белого фосфора — 50—150 мг. Попадая на кожу, белый фосфор дает тяжелые ожоги.
Острые отравления фосфором проявляются жжением во рту и желудке, головной болью, слабостью, рвотой. Через 2—3 суток развивается желтуха. Для хронических форм характерны нарушение кальциевого обмена, поражение сердечно-сосудистой и нервной систем. Первая помощь при остром отравлении — промывание желудка, слабительное, очистительные клизмы, внутривенно растворы глюкозы. При ожогах кожи обработать пораженные участки растворами медного купороса или соды. ПДК паров фосфора в воздухе производственных помещений — 0,03 мг/м³, временно допустимая концентрация в атмосферном воздухе — 0,0005 мг/м³, ПДК в питьевой воде — 0,0001 мг/дм³.[6]
7.2. Токсикология соединений фосфора
Некоторые соединения фосфора (фосфин) очень токсичны. Боевые отравляющие вещества зарин, зоман, табун, V-газы являются соединениями фосфора.
Примечания
- Phosphorus: electronegativities - www.webelements.com/phosphorus/electronegativity.html (англ.). WebElements.
- Sulfur and Phosphorus Compounds - www.cem.msu.edu/~reusch/VirtualText/special2.htm (англ.).
- Редкол.:Зефиров Н. С. (гл. ред.) Химическая энциклопедия: в 5 т. — Москва: Большая Российская энциклопедия, 1999. — Т. 5. — С. 145.
- J.P. Riley and Skirrow G. Chemical Oceanography V. 1, 1965
- В. Шретер, К.-Х. Лаутеншлегер, Х. Бибрак и др. Химия = Chemie. — М.: Химия, 1989. — С. 351. — ISBN 5-7245-0360-3
- УНИАН — здоровье — Что происходит с фосфором? - health.unian.net/rus/detail/185459
wreferat.baza-referat.ru
Реферат по химии на тему «Фосфор»
План
- Открытие фосфора
- Получение фосфора
- Распространение фосфора в природе
- Физические свойства
- Химические свойства
- Строение атома фосфора
Открытие фосфора
Гамбургский купец Генниг Бранд, надеялся поправить свои финансовые дела и избежать полного разорения, решил попытать счастья в алхимии. Он пытался найти «философский камень», который дал бы возможность превращать неблагородные металлы в золото. Г. Бранду пришла действительно счастливая мыль провести опыт с мочой. Выпарив ее почти досуха, Г. Бранд оставшееся вещество смешал с углем и песком и нагревал в реторте без доступа воздуха. В результате он получил новое вещество, которое обладает удивительным свойством – светиться в темноте.
Так в 1669 г. был открыт фосфор, играющий исключительно важную роль в живой природе.
Г. Бранд не замедлил воспользоваться необычным свойством нового вещества и стал демонстрировать светящийся фосфор знатным особам за довольно высокое вознаграждение. Все, что соприкасалось с фосфором, приобретало способность светиться. Г. Бранд ловко использовал огромный интерес ученых и широкой публики к фосфору и стал продавать его по цене, превосходивший даже стоимость золота. Бранд держал в строжайшей тайне способ получения фосфора. Никто из других алхимиков не мог проникнуть в его лабораторию, и посему многие из них стали лихорадочно ставить различные опыты, стремясь разгадать способ получения светящегося вещества.
Вскоре рецепт изготовления «холодного огня» стал известен И. Кункелю и К. Кирхмейру, а в 1680 г. секрет получения фосфора был открыт в Англии знаменитым химиком Р. Бойлем. После смерти Р. Бойля его ученик – немец А. Ганквиц, сделав некоторые улучшения в методике получения фосфора, наладил его производство. Интересно, что А. Ганквиц, несмотря на свою длительную работу с фосфором и весьма опасные опыты с ним, дожил до восьмидесятилетнего возраста. Он пережил трех сыновей своих и всех тех, кто принимал участие в работах, относящихся к ранней истории фосфора.
Цена на фосфор со времени открытия его И. Кункелем и Р. Бойлем стала быстро падать, и в конце концов наследники первооткрывателей стали знакомить с секретом получения фосфора за 10 талеров.
Получение фосфора
Фосфор в промышленности получают из фосфата кальция Ca3(PO4)2, который выделяют из фосфоритов и фторапатитов. Метод получения основан на реакции восстановления Ca3(PO4)2 до фосфора.
В качестве восстановителя соединений фосфора используют кокс (углерод). Для связывания соединений кальция в реакционную систему добавляют кварцевый песок SiO2. Процесс проводят в электропечах (производство относят к электротермическим). Реакция протекает по уравнению:
2Ca3(PO4)2 + 6SiO2 + 10C = 6CaSiO3 + P4 + 10CO
Продукт реакции - белый фосфор. Из-за наличия примесей технический фосфор имеет желтый цвет, поэтому в промышленности его называют желтым фосфором.
Распространение фосфора в природе
В истории химии с фосфором связано много больших открытий. Однако лишь столетие спустя после открытия фосфор перешел из мира торговли и наживы в мир науки. Лишь одно событие за этот длительный период может быть отнесено к настоящей науке и связано оно с 1715 г., когда Генсинг открыл фосфор в мозговой ткани. Это послужило позднее для высказывания «Без фосфора нет мысли».
Ю. Ган в 1769 г. нашел фосфор в костях, а через два года знаменитый шведский химик К. Шееле показал, что кости состоят главным образом из фосфата кальция, и предложил способ получения фосфора из золы, образующейся при сжигание костей.
Фосфор по своей важности ни чуть не уступает азоту. Он участвует в великом природном круговороте веществ, и, не будь фосфора, растительный и животный мир был бы совсем иным. Однако фосфор встречается в природных условиях не так уж часто, и на его долю приходится всего лишь 0,08% массы земной коры. По распределенности он занимает тринадцатое место среди других элементов. Интересно отметить, что в теле человека на долю фосфора приходится примерно 1,16%. Из них 2/3 приходится на костную ткань, около 0,25% - на мышечную и примерно 0,4% на нервную ткань.
Фосфор встречается в природе исключительно в виде солей фосфорной кислоты, главным образом фосфорита 3Ca3(PO4)2 * Ca(OH)2 и апатита 3Ca3(PO4)2 * Ca(F, Cl)2. Лишь в отдельных местах встречаются фосфаты железа, вивианит (синяя железная руда) Fe3(PO4)2 * 8h3O, алюминия, например вавеллит 3Al2O3 * 2P2O5 * 12h3O, а также редких земель. Соединения фосфорной кислоты составляют существенную часть растительных и животных организмов. Часть фосфорной кислоты связана в них в виде органических соединений, например в желтке яйца и в веществе мозга – в форме лецитинов.
Фосфор редко встречается в больших количествах, и в целом его следует отнести к рассеянным элементам. В свободном виде в природе он не встречается, так как легко окисляется, но содержится во многих минералах. Главнейшие из них – фторапатит, гидроксилапатит, фосфорит. Несколько реже встречаются вавианит, монацит, амблигонит, трифилит и совсем ограниченных количествах – ксенотит и торбернит.
Что касается минералов фосфора, то они делятся на первичные и вторичные. Среди первичных наиболее распространены апатиты, представляющие в основном породы магматического происхождения. Химический состав апатита – фосфат кальция, содержащий некоторое количество фторида и хлорида кальция. Именно этим определяется существование минералов фторапатита и хлорапатита. Они содержат от 5 до 36% P2O5. Обычно эти минералы в большинстве случаев встречаются в зоне магмы, но не редко они обнаруживаются в местах, где изверженные породы соприкасаются с осадочными. Из всех известных месторождений фосфатов наиболее значительные имеются в Норвегии и Бразилии.
Фосфин и дифосфин в природе встречаются довольно редко и чаще приходиться иметь дело с такими соединениями фосфора, как фосфориты. Фосфориты – фосфаты органического происхождения играют особо важную роль в сельском хозяйстве. На островах Тихого океана, в Чили и Перу они образованы на основе птичьего помета – гуано, который в условиях сухого климата накапливается мощными слоями, нередко превышающие сотню метров. Образование фосфоритов может быть связано и с геологическими катастрофами,
например, с ледниковым периодом, когда гибель животных носила массовый характер. Подобные процессы возможны и в океане при массовой гибели морской фауны. Фосфор из органических остатков частично усваивается растениями, но в основном, растворяясь в морской воде, переходит в минеральные формы. Морская вода содержит фосфаты в довольно больших количествах – 100 – 200 мг/м3. При определенных химических изменениях фосфаты могут выпадать в осадок и скапливаться на дне. А при поднятии морского дна в определенные геологические периоды залежи фосфоритов оказываются на суше. Подобным образом могли образоваться фосфориты крупного отечественного месторождения фосфоритов вблизи Кара-Тау в Казахстане. Встречаются фосфориты и в Подмосковье.
Физические свойства
Фосфор существует во многих модификациях. Однако «многоликость» фосфора можно свести к трем главным видам: белому, красному и черному.
Белый фосфор получается в твердом состоянии при быстром охлаждении паров фосфора; его плотность 1,83 г/см3. Теплота плавления белого фосфора составляет 0,6 ккал, а теплота испарения 12ккал (на моль P4). В чистом виде белый фосфор совершенно бесцветен и прозрачен; Продается он обычно отлитым в палочки, которые легко режутся ножом. Эту операцию необходимо производить под водой (лучше при 20-25 оС), так как при разрезание на воздухе фосфор может воспламениться от трения. На холоду белый фосфор хрупок, но при температуре выше 15 оС становится мягким.
На воздухе белый фосфор очень быстро окисляется и при этом светится в темноте. Отсюда произошло название «фосфор», который в переводе с греческого означает «светоносный». Уже при слабом нагревании, для чего достаточно простого трения, фосфор воспламеняется и сгорает, выделяя большое количество теплоты. Он сгорает желтовато-белым пламенем, образуя пятиокись: 2P + 5/2O2 = P2O5 + 370 ккал. Фосфор может и воспламениться на воздухе вследствие выделения теплоты при окислении. Чтобы защитить белый фосфор от окисления, его сохраняют под водой. В воде белый фосфор не растворим; хорошо растворяется в сероуглероде. Растворимость его в сероуглероде исключительно велика (порядка 10:1 при обычных условиях).
Белый фосфор – сильный яд. Доза в 0,1 г смертельна для человека.
Если белый фосфор долго нагревать без доступа воздуха при температуре 250 – 300 оС, то он превращается в другое взаимодействие фосфора, имеющее красно – фиолетовый цвет и называемое красным фосфором. Такое же превращение происходит, но только очень медленно, под действием света.
Красный фосфор по своим свойствам резко отличается от белого: он очень медленно окисляется на воздухе, не светится в темноте, загорается только при температуре 260 оС, не растворяется в сероуглероде и неядовит. Плотность красного фосфора составляет 2,0-2,4 г/см3. Переменное значение плотности обусловленно тем, что красный фосфор состоит из нескольких форм.
При сильном нагревании красный фоссфор, не плавясь, испаряется (сублимируется). При охлаждении паров получается белый фосфор.
Черный фосфор образуется из белого при нагревании его до 200-220 оС под очень высоким давлении. По виду он похож на графит, жирен на ощуп и тяжелее других видоизменений; его плотность равна 2,7 г/м3. Черный фосфор обладает полупроводниковой проводимостью (с шириной запрещенной зоны 0,33 в). Под давлением 18 тыс. атм. Черный фосфор плавится около 1000 оС, а под давлением только своего пара выше 550 оС переходит в фиолетовый.
Химические свойства
1. Соединение фосфора с водородом и галогенами. С водородом фосфор образует газообразный фосфористый водород, или фосфин, Ph4. Его можно получить кипячением белого фосфора с раствором щелочи или действием соляной кислоты на фосфид кальция Ca3P2:
Строение атома фосфора
Строение внешнего электронного слоя атома фосфора 3s2p3
Энергия ионизации атома, эВ 10.49.
Относительная электроотрицательность 2,2.
Заряд ядра атома фосфора +15 (+15P)
Радиус атома, нм 0,13
mendelei.ru
Реферат по химии на тему: «Фосфор и его соединения»
Экзаменационный
реферат по химии
на тему:
«Фосфор и его соединения»
План:
| Введение……………………………………………………………………………. | 3 |
| История развития фосфора………………………………………………………... | 3 |
| Природные соединения и получение фосфора…………………………………... | 4 |
| Химические свойства……………………………………………………………… | 4 |
| Аллотропные изменения…………………………………………………………... | 5 |
| а) белый…………………………………………………………………………….. | 6 |
| б) красный………………………………………………………………………….. | 7 |
| в) черный……………………………………………………………………………. | 7 |
| Оксиды фосфора…………………………………………………………………… | 7 |
| Ортофосфорная кислота…………………………………………………………... | 9 |
| Ортофосфаты………………………………………………………………………. | 11 |
| Фосфор в организме человека…………………………………………………….. | 11 |
| Спички………………………………………………………………………………. | 12 |
| Фосфорные удобрения…………………………………………………………….. | 12 |
| Заключение…………………………………………………………………………. | 14 |
| 1. Значение фосфора……………………………………………………………….. | 14 |
| 2. Применение фосфора…………………………………………………………… | 15 |
| Список используемой литературы………………………………………………... | 17 |
Введение
Пятая группа Периодической системы включает два типических элемента азот и фосфор – и подгруппы мышьяка и ванадия. Между первым и вторым типическими элементами наблюдается значительное различие в свойствах.
В состоянии простых веществ азот – газ, а фосфор – твердое вещество. Эти два вещества получили большую область применения, хотя когда азот впервые был выделен из воздуха его посчитали вредным газом, а на продаже фосфора удавалось заработать большое количество денег (в фосфоре ценили его способность светится в темноте).
История открытия фосфора
По иронии судьбы фосфор открывался несколько раз. Причем всякий раз получали его из … мочи. Есть упоминания о том, что арабский алхимик Альхильд Бехиль (XII век) открыл фосфор при перегонке мочи в смеси с глиной, известью и углем. Однако датой открытия фосфора считается 1669 год. Гамбургский алхимик-любитель Хеннинг Бранд, разорившийся купец, мечтавший с помощью алхимии поправить свои дела, подвергал обработке самые разнообразные продукты. Предполагая, что физиологические продукты могут содержать «первичную материю», считавшейся основой философского камня, Бранд заинтересовался человеческой мочей.
Он собрал около тонны мочи из солдатских казарм и выпаривал ее до образования сиропообразной жидкости. Эту жидкость он вновь дистиллировал и получил тяжелое красное «уринное масло», которое перегонялось с образованием твердого остатка. Нагревая последний, без доступа воздуха, он заметил образование белого дыма, оседавшего на стенках сосуда и ярко светившего в темноте. Бранд назвал полученное им вещество фосфором, что в переводе с греческого означает «светоносец».
Несколько лет «рецепт приготовления» фосфора хранился в строжайшем секрете и был известен лишь нескольким алхимикам. В третий раз фосфор открыл Р.Бойль в 1680 году.
В несколько модифицированном виде старинный метод получения фосфора использовали и в XVIII столетии: нагреванию подвергали смесь мочи с оксидом свинца (PbO), поваренной солью (NaCl), поташом (K2CO3) и углем (C). Лишь 1777 году К.В.Шееле заработал способ получения фосфора из рога и костей животных.
Природные соединения и получение фосфора
По распространенности в земной коре фосфор опережает азот, серу и хлор. В отличие от азота фосфор, из-за большой химической активности встречается в природе только в виде соединений. Наиболее важные минералы фосфора - апатит Са5Х(РО4)3 (Х - фтор, реже хлор и гидрооксильная группа) и фосфорит основой которого является Са3(РО4)2. Крупнейшее месторождение апатитов находится на Кольском полуострове, в районе Хибинских гор. Залежи фосфоритов находятся в районе гор Каратау, в Московской, Калужской, Брянской областях и в других местах. Фосфор входит в состав некоторых белковых веществ, содержащихся в генеративных органах растений, в нервных и костных тканях организмов животных и человека. Особенно богаты фосфором мозговые клетки.
В наши дни фосфор производят в электрических печах, восстанавливая апатит углем в присутствии кремнезема:
Ca3(PO4)2+3SiO2+5C3CaSiO3+5CO+P2.
Пары фосфора при этой температуре почти полностью состоят из молекул Р2, которые при охлаждении конденсируются в молекулы Р4.
Химические свойства
Электронная конфигурация атома фосфора
1S22S22P63S23P33d0
Наружный электронный слой содержит 5 электронов. Наличием трех неспаренных электронов на внешнем энергетическом уровне объясняет то, что в нормальном, невозбужденном состоянии валентность фосфора равна 3.
Но на третьем энергетическом уровне имеются вакантные ячейки d-орбиталей, поэтому при переходе в возбужденное состояние 3S-электроны будут разъединяться, переходить на d подуровень, что приводит к образованию 5-ти неспаренных элементов.
Таким образом, валентность фосфора в возбужденном состоянии равна 5.
В соединениях фосфор обычно проявляет степень окисления +5, реже +3, -3.
1. Реакции с кислородом:
4P0 + 5O2 2P2+5O5
(при недостатке кислорода: 4P0 + 3O2 2P2+3O3)
2. С галогенами и серой:
2P0 + 3Cl2 2P+3Cl3
P0 + 5S P2+5S5
(галогениды фосфора легко разлагаются водой, например:
PCl3 + 3h3O h4PO3 + 3HClPCl5 + 4h3O h4PO4 + 5HCl)
3. С азотной кислотой:
3P0 + 5HN+5O3 + 2h3O 3h4P+5O4 + 5N+2O
4. С металлами образует фосфиды, в которых фосфор проявляет степень окисления - 3:
2P0 + 3Mg Mg3P2-3
(фосфид магния легко разлагается водой Mg3P2 + 6h3O 3Mg(OH)2 + 2Ph4(фосфин))
3Li + P Li3P-3
5. Со щелочью:
4P + 3NaOH + 3h3O Ph4 + 3Nah3PO2
В реакциях (1,2,3) - фосфор выступает как восстановитель, в реакции (4) - как окислитель; реакция (5) - пример реакции диспропорционирования.
Фосфор может быть как восстановителем, так и окислителем.
Аллотропные изменения
В свободном состоянии фосфор образует несколько аллотропных видоизменений. Это объясняется тем, что атомы фосфора способны, взаимно соединяясь, образовывать кристаллические решетки различного типа.
Таблица 1
Физические свойства фосфора
| Аллотропная модификация | Плотность, г/см3 | tпл, 0C | Tкип, 0C | Внешний вид и характерные признаки |
| Белый | 1,73 | 44,1 | 280,5 | Белый кристаллический порошок, ядовит, самовозгорается на воздухе. При 280—300°С переходит в красный |
| Красный | 2,3 | 590 | Возгоняется около 400°С | Красный кристаллический или аморфный порошок, неядовит. При 220°С и 12 108 Па переходит в черный фосфор. Загорается на воздухе только при поджигании |
| Черный | 2,7 | При нагревании переходит в красный фосфор | Графитоподобная структура. При нормальных условиях — полупроводник, под давлением проводит электрический ток как металл | |
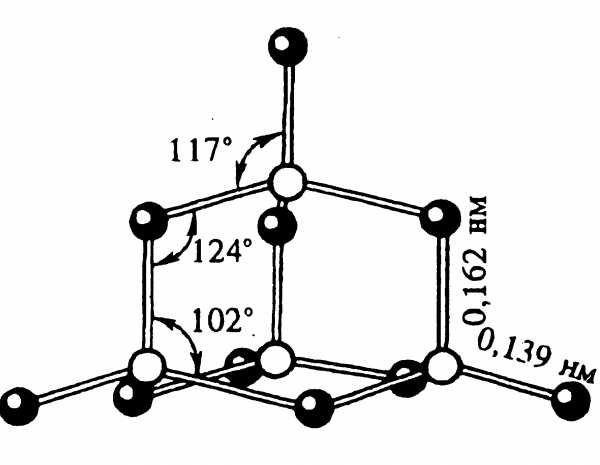
Белая модификация фосфора, получающаяся при конденсации паров, имеет молекулярную кристаллическую решетку, в узлах которой дислоцированы молекулы Р4 (рис.1). Из-за слабости межмолекулярных сил белый фосфор летуч, легкоплавок, режется ножом и растворяется в неполярных растворителях, например в сероуглероде. Белый фосфор весьма реакционноспособное вещество. Он энергично взаимодействует с кислородом, галогенами, серой и металлами. Окисление фосфора на воздухе сопровождается разогреванием и свечением. Поэтому белый фосфор хранят под водой, с которой он не реагирует. Белый фосфор очень токсичен.
Около 80% от всего производства белого фосфора идет на синтез чистой ортофосфорной кислоты. Она в свою очередь используется для получения полифосфатов натрия (их применяют для снижения жесткости питьевой воды) и пищевых фосфатов. Оставшаяся часть белого фосфора расходуется для создания дымообразующих веществ и зажигательных смесей.
Техника безопасности. В производстве фосфора и его соединений требуется соблюдение особых мер предосторожности, т.к. белый фосфор – сильный яд. Продолжительная работа в атмосфере белого фосфора может привести к заболеванию костных тканей, выпадению зубов, омертвению участков челюстей. Воспламеняясь, белый фосфор вызывает болезненные, долго не заживающие ожоги. Хранить белый фосфор следует под водой, в герметичных сосудах. Горящий фосфор тушат двуокисью углерода, раствором CuSO4 или песком. Обоженную кожу следует промыть раствором KmnO4 или CuSO4. Противоядием при отравлении фосфором является 2%-ый раствор CuSO4.
При длительном хранении, а также при нагревании белый фосфор переходит в красную модификацию (впервые его получили лишь 1847 году). Название красный фосфор относится сразу к нескольким модификациям, различающихся по плотности и окраске: она колеблется от оранжевой до темно-красной и даже фиолетовой. Все разновидности красного фосфора нерастворимы в органических растворителях, и по сравнению с белым фосфором они менее реакционноспособны и имеют полимерное строение: это тетраэдры Р4, связанные друг с другом в бесконечные цепи (рис.2).
Красный фосфор находит применение в металлургии, производстве полупроводниковых материалов и ламп накаливания, используется в спичечном производстве.
Наиболее стабильной модификацией фосфора является черный фосфор. Его получают аллотропным превращением белого фосфора при t=2200C и повышенным давлением. По внешнему виду он напоминает графит. Кристаллическая структура черного фосфора слоистая, состоящая из гофрированных слоев (рис.3). Черный фосфор – это наименее активная модификация фосфора. При нагревании без доступа воздуха он, как и красный, переходит в пар, из которого конденсируется в белый фосфор.
Оксид фосфора (V)
| Фосфор образует несколько оксидов. Важнейшим из них является оксид фосфора (V) P4O10 (Рис.4). Часто его формулу пишут в упрощенном виде – P2O5. В структуре этого оксида сохраняется тетраэдрическое расположение атомов фосфора. | |
Белые кристаллы, t0пл.= 5700С, t0кип.= 6000C, = 2,7 г/см3. Имеет несколько модификаций. В парах состоит из молекул P4h20, очень гигроскопичен (используется как осушитель газов и жидкостей).
Получение4P + 5O2 2P2O5
Химические свойства
Все химические свойства кислотных оксидов: реагирует с водой, основными оксидами и щелочами
1) P2O5 + h3O 2HPO3 (метафосфорная кислота)
P2O5 + 2h3O h5P2O7 (пирофосфорная кислота)
P2O5 + 3h3O 2h4PO4 (ортофосфорная кислота)
2) P2O5 + 3BaO Ba3(PO4)2
В зависимости от избытка щелочи образует средние и кислые соли:
гидрофосфат натрия
дигидрофосфат натрия
Благодаря исключительной гигроскопичности оксид фосфора (V) используется в лабораторной и промышленной технике в качестве осушающего и дегидратирующего средства. По своему осушающему действию он превосходит все остальные вещества. От безводной хлорной кислоты отнимает химически связанную воду с образованием ее ангидрида:
Ортофосфорная кислота. Известно несколько кислот, содержащих фосфор. Важнейшая из них — ортофосфорная кислота Н3РО4 (Рис.5).
Безводная ортофосфорная кислота представляет собой светлые прозрачные кристаллы, при комнатной температуре расплывающиеся на воздухе. Температура плавления 42,350С. С водой фосфорная кислота образует растворы любых концентраций.
Ортофосфорной кислоте соответствует следующая структурная формула:
НО ОН
Р
О ОН
В лаборатории ортофосфорную кислоту получают окислением фосфора 30%-ной азотной кислотой:
В промышленности ортофосфорную кислоту получают двумя способами: экстракционным и термическим.
1. В основе экстракционного метода лежит обработка измельченных природных фосфатов серной кислотой:
Ортофосфорная кислота затем отфильтровывается и концентрируется упариванием.
2. Термический метод состоит в восстановлении природных фосфатов до свободного фосфора с последующим его сжиганием до Р4О10 и растворением последнего в воде. Производимая по данному методу ортофосфорная кислота характеризуется более высокой чистотой и повышенной концентрацией (до 80% массовых).
Физические свойства. Ортофосфорная кислота — твердое, бесцветное, кристаллическое вещество, хорошо растворимое в воде.
Химические свойства ортофосфорной кислоты представлены в табл.2:
Таблица 2
Химические свойства ортофосфорной кислоты
| Общие с другими кислотами | Специфические |
| 1. Водный раствор кислоты изменяет окраску индикаторов. Диссоциация происходит ступенчато:
Легче всего идет диссоциация по первой ступени и труднее всего – по третьей 2. Реагирует с металлами, расположенными в вытеснительном ряду до водорода:
3. Реагирует с основными оксидами:
4. Реагирует с основаниями и аммиаком; если кислота взята в избытке, то образуются кислые соли:
гидрофосфат натрия
дигидрофосфат натрия
5. Реагирует с солями слабых кислот:
|
двуфосфорная кислота
2. При действии раствора нитрата серебра (I) появляется желтый осадок: желтый осадок 3. Ортофосфорная кислота играет большую роль в жизнедеятельности животных и растений. Ее остатки входят в состав аденозинтрифосфорной кислоты АТФ. При разложении АТФ выделяется большое количество энергии. |
Ортофосфаты. Ортофосфорная кислота образует три ряда солей. Если обозначить атомы металлов буквами Me, то можно изобразить в общем виде состав ее солей (табл.3).
Таблица 3
Химические формулы ортофосфатов, содержащих металлы
| одновалентные | двухвалентные | трехвалентные |
| Ме3РО4 | Ортофосфаты Ме3(РО4)2 | Ме3РО4 |
| Ме2НРО4 | Гидроортофосфаты МеНРО4 | Ме2(НРО4)3 |
| МеН2РО4 | Дигидроортофосфаты Ме(Н2РО4)2 | Ме(Н2РО4)3 |
Вместо одновалентного металла в состав молекул ортофосфатов может входить группа аммония: (Nh5)3PO4 - ортофосфат аммония;
(Nh5)2HPO4—гидроортофосфат аммония; Nh5h3PO4 – дигидро-ортофосфат аммония.
Ортофосфаты и гидроортофосфаты кальция и аммония широко используют в качестве удобрений, ортофосфат и гидроортофосфат натрия — для осаждения из воды солей кальция.
Фосфор в организме человека
В теле человека массой 70 кг. Содержится около 780 г. фосфора. В виде фосфатов кальция фосфор присутствует в костях человека и животных. Входит он и в состав белков, фосфолипидов, нуклеиновых кислот; соединения фосфора участвуют в энергетическом обмене (аденизинтрифосфорная кислота, АТФ). Ежедневная потребность человеческого организма в фосфоре составляет 1,2 г. Основное его количество мы потребляем с молоком и хлебом (в 100 г. хлеба содержится примерно 200 мг. фосфора). Наиболее богаты фосфором рыба, фасоль и некоторые виды сыра.
Интересно, что для правильного питания необходимо соблюдать баланс между количеством потребляемого фосфора и кальцием: оптимальное соотношение в этих элементах пищи составляет 1,51. Избыток богатой фосфором пищи приводит к вымыванию кальция из костей, а при избытке кальция развивается мочекаменная болезнь.
Спички
Зажигательная поверхность спичечного коробка покрыта смесью красного фосфора и порошка стекла. В состав спичечной головки входят окислители (PbO2, KСlO3, BaCrO4) и восстановители (S, Sb2S3). При трении от зажигательной поверхности смесь, нанесенная на спичку, воспламеняется:
Первые фосфорные спички – с головкой из белого фосфора – были созданы лишь 1827 г. Такие спички загорались при трении о любую поверхность, что нередко приводило к пожарам. Кроме того, белый фосфор очень ядовит. Описаны случаи отравления фосфорными спичками как из-за неосторожного обращения, так и с целью самоубийства: для этого достаточно было съесть несколько спичечных головок. Вот почему на смену фосфорным спичкам пришли безопасные, которые верно служат нам и по сей день. Промышленное производство безопасных спичек началось в Швеции в 60-х гг. XIX века.
Фосфорные удобрения
Минеральные удобрения – источник различных питательных элементов для растений и свойств почвы, в первую очередь азота, фосфора и калия, а затем кальция, магния, серы, железа.
Фосфор входит в состав многих органических соединений в растениях. Фосфорное питание регулирует рост и развитие растений.
Сырьем для производства фосфорных удобрений, фосфора и всех фосфорных соединений служат апатитовые и фосфоритовые руды. Состав апатитов чаще всего выражается формулой Са5(РО4)3F (фторапатит). Фосфориты отличаются от фторапатитов тем, что в них вместо ионов F- содержатся ионы ОН- или  . Фосфориты обычно содержат больше примесей, чем фторапатит.
. Фосфориты обычно содержат больше примесей, чем фторапатит.
В дореволюционной России были известны и разрабатывались лишь маломощные месторождения фосфоритов низкого качества. Поэтому событием огромного народнохозяйственного значения было открытие в 20-х годах месторождения апатита на Кольском полуострове в Хибинах. Здесь построена крупная обогатительная фабрика, которая разделяет добываемую горную породу на концентрат с высоким содержанием фосфора и примеси – «нефелиновые хвосты», используемые для производства алюминия, соды, поташа и цемента.
Мощные месторождения фосфоритов открыты в Южном Казахстане, в горах Каратау.
Самое дешевое фосфорное удобрение – это тонко измельченный фосфорит – фосфоритная мука. Фосфор содержится в ней в виде нерастворимого в воде фосфата кальция Са3(РО4)2. Поэтому фосфориты усваиваются не всеми растениями и не на всех почвах. Основную массу добываемых фосфорных руд перерабатывают химическими методами в вещества, доступные всем растениям на любой почве. Это водорастворимые фосфаты кальция:
Двойной суперфосфат (цвет и внешний вид сходен с простым суперфосфатом – серый мелкозернистый порошок).
Получается при действии на природный фосфат фосфорной кислоты:
По сравнению с простым суперфосфатом он не содержит СаSО4 и является значительно концентрированным удобрением (содержит до 50% Р2О5).
Преципитат – содержит 35-40% Р2О5.
Получается при нейтрализации фосфорной кислоты раствором гидроксида кальция:
Применяется на кислых почвах.
Аммофос – сложное удобрение, содержащее азот (до 15% N) и фосфор (до 58% Р2О5) в виде Nh5h3PO4 и (Nh5)2HPO4. Получается при нейтрализации фосфорной кислоты аммиаком.
Раньше в течение более 100 лет в качестве фосфорного удобрения широко использовали так называемый простой суперфосфат, который образуется при действии серной кислоты на природный фосфат кальция:
В этом случае в реакцию с фосфатом кальция вступает относительно меньше серной кислоты, чем при получении из него фосфорной кислоты. Получается смесь дигидрофосфата кальция и сульфата кальция. Это удобрение с массовой долей Р2О5 не выше 20%. Сейчас простой суперфосфат производится в сравнительно небольших масштабах на ранее построенных заводах.
Примеры фосфорных удобрений даны в табл.4.
Таблица 4
Удобрения, содержащие фосфор
| Название удобрения | Химический состав |
| Простые | |
| Суперфосфат двойной |
|
| Суперфосфат простой |
|
| Фосфоритная мука |
|
| Костяная мука |
|
| Преципитат |
|
| Шлак мартеновский печей | Сложный состав. Содержит P,Ca, Si, C, Fe и др. элементы |
| Комплексные | |
| Аммофос |
|
| Аммофоска |
|
| Нитроаммофос |
|
Заключение
Значение фосфора
Фосфорная кислота имеет большое значение как один из важнейших компонентов питания растений. Фосфор используется растениями для построения своих самых жизненно важных частей - семян и плодов.
Производные ортофосфорной кислоты очень нужны не только растениям, но и животным. Кости, зубы, панцири, когти, иглы, шипы у большинства живых организмов состоят, в основном, из ортофосфата кальция. Кроме того, ортофосфорная кислота, образуя различные соединения с органическими веществами, активно участвуют в процессах обмена веществ живого организма с окружающей средой. В результате этого производные фосфора содержатся в костях, мозге, крови, в мышечных и соединительных тканях организмов человека и животных. Особенно много ортофосфорной кислоты в составе нервных (мозговых) клеток, что позволило А.Е. Ферсману, известному геохимику, назвать фосфор "элементом мысли". Весьма отрицательно (заболевание животных рахитом, малокровие, и др.) сказывается на состоянии организма понижение содержания в рационе питания соединений фосфора или введение их в неусвояемой форме.
Применение фосфора
Применяют ортофосфорную кислоту в настоящее время довольно широко. Основным ее потребителем служит производство фосфорных и комбинированных удобрений. Для этих целей ежегодно добывается во всем мире фосфоросодержащей руды около 100 млн. т. Фосфорные удобрения не только способствуют повышению урожайности различных сельскохозяйственных культур, но и придают растениям зимостойкость и устойчивость к другим неблагоприятным климатическим условиям, создают условия для более быстрого созревания урожая в районах с коротким вегетативным периодом. Они также благоприятно действуют на почву, способствуя ее структурированию, развитию почвенных бактерий, изменению растворимости других содержащихся в почве веществ и подавлению некоторых образующихся вредных органических веществ.
Немало ортофосфорной кислоты потребляет пищевая промышленность. Дело в том, что на вкус разбавленная ортофосфорная кислота очень приятна и небольшие ее добавки в мармелады, лимонады и сиропы заметно улучшают их вкусовые качества. Этим же свойством обладают и некоторые соли фосфорной кислоты. Гидрофосфаты кальция, например, с давних пор входят в хлебопекарные порошки, улучшая вкус булочек и хлеба.
Интересны и другие применения ортофосфорной кислоты в промышленности. Например, было замечено, что пропитка древесины самой кислотой и ее солями делают дерево негорючим. На этой основе сейчас производят огнезащитные краски, негорючие фосфодревесные плиты, негорючий фосфатный пенопласт и другие строительные материалы.
Различные соли фосфорной кислоты широко применяют во многих отраслях промышленности, в строительстве, разных областях техники, в коммунальном хозяйстве и быту, для защиты от радиации, для умягчения воды, борьбы с котельной накипью и изготовления различных моющих средств.
Фосфорная кислота, конденсированные кислоты и дегидротированные фосфаты служат катализаторами в процессах дегидратирования, алкилирования и полимеризации углеводородов.
Особое место занимают фосфорорганические соединения как экстрагенты, пластификаторы, смазочные вещества, присадки к пороху и абсорбенты в холодильных установках. Соли кислых алкилфосфатов используют как поверхностно-активные вещества, антифризы, специальные удобрения, антикоагулянты латекса и др. Кислые алкилфосфаты применяют для экстракционной переработки урановорудных щелоков.
Список использованной литературы:
Ф.Г.Фельдман, Г.Е.Рудзитис. ХИМИЯ. Учебник для 9 класса общеобразовательных учреждений. – М., 5-е издание, ПРОСВЕЩЕНИЕ, 1997.
ХИМИЯ. Справочные материалы. Под ред.Ю.Д.Третьякова, - М., ПРОСВЕЩЕНИЕ, 1984.
ХИМИЯ. Справочник школьника, - М., 1995.
ХИМИЯ. Энциклопедия для детей. Том 17, АВАНТА, 2000.
Везер В.-Дж., Фосфор и его соединения, пер. с англ., - М., 1963.
Интернет:
Ферсман Александр Евгеньевич [27.10 (8.11).1883, Петербург, - 20.5.1945, Сочи], советский геохимик и минералог, академик АН СССР (1919). Ученик В. И. Вернадского.
refdb.ru
Реферат Химия Фосфор и его соединения
| Введение.............................. | 3 |
| История развития фосфора........................ | 3 |
| Природные соединения и получение фосфора................ | 4 |
| Химические свойства........................ | 4 |
| Аллотропные изменения......................... | 5 |
| а) белый............................... | 6 |
| б) красный.............................. | 7 |
| в) черный.............................. | 7 |
| Оксиды фосфора.......................... | 7 |
| Ортофосфорная кислота......................... | 9 |
| Ортофосфаты............................ | 11 |
| Фосфор в организме человека...................... | 11 |
| Спички............................... | 12 |
| Фосфорные удобрения......................... | 12 |
| Заключение............................. | 14 |
| 1. Значение фосфора.......................... | 14 |
| 2. Применение фосфора....................... | 15 |
| Список используемой литературы..................... | 17 |
Химические свойства
Электронная конфигурация атома фосфора 1S22S22P63S23P33d0 Наружный электронный слой содержит 5 электронов. Наличием трех неспаренных электронов на внешнем энергетическом уровне объясняет то, что в нормальном, невозбужденном состоянии валентность фосфора равна 3. Но на третьем энергетическом уровне имеются вакантные ячейки d-орбиталей, поэтому при переходе в возбужденное состояние 3S-электроны будут разъединяться, переходить на d подуровень, что приводит к образованию 5-ти неспаренных элементов. Таким образом, валентность фосфора в возбужденном состоянии равна 5. В соединениях фосфор обычно проявляет степень окисления +5, реже +3, -3. 1. Реакции с кислородом: 4P0 + 5O2 2P2+5O5 (при недостатке кислорода: 4P0 + 3O22P2+3O3) 2. С галогенами и серой: 2P0 + 3Cl2 ® 2P+3Cl3 P0 + 5S P2+5S5 (галогениды фосфора легко разлагаются водой, например: PCl3 + 3h3O ® h4PO3 + 3HCl PCl5 + 4h3O ® h4PO4 + 5HCl) 3. С азотной кислотой: 3P0 + 5HN+5O3 + 2h3O ® 3h4P+5O4 + 5N+2O 4. С металлами образует фосфиды, в которых фосфор проявляет степень окисления - 3: 2P0 + 3Mg ® Mg3P2-3 (фосфид магния легко разлагается водой Mg3P2 + 6h3O ® 3Mg(OH)2 + 2Ph4 (фосфин)) 3Li + P ® Li3P-3 5. Со щелочью: 4P + 3NaOH + 3h3O ® Ph4 + 3Nah3PO2 В реакциях (1,2,3) - фосфор выступает как восстановитель, в реакции (4) - как окислитель; реакция (5) - пример реакции диспропорционирования. Фосфор может быть как восстановителем, так и окислителем. В свободном состоянии фосфор образует несколько аллотропных видоизменений. Это объясняется тем, что атомы фосфора способны, взаимно соединяясь, образовывать кристаллические решетки различного типа. Таблица 1 Физические свойства фосфора| Аллотропная модификация | Плотность, г/см3 | tпл, 0C | Tкип, 0C | Внешний вид и характерные признаки |
| Белый | 1,73 | 44,1 | 280,5 | Белый кристаллический порошок, ядовит, самовозгорается на воздухе. При 280—300°С переходит в красный |
| Красный | 2,3 | 590 | Возгоняется около 400°С | Красный кристаллический или аморфный порошок, неядовит. При 220°С и 12 × 108 Па переходит в черный фосфор. Загорается на воздухе только при поджигании |
| Черный | 2,7 | При нагревании переходит в красный фосфор | Графитоподобная структура. При нормальных условиях — полупроводник, под давлением проводит электрический ток как металл | |
Фосфор образует несколько оксидов. Важнейшим из них является оксид фосфора (V) P4O10 (Рис.4). Часто его формулу пишут в упрощенном виде – P2O5. В структуре этого оксида сохраняется тетраэдрическое расположение атомов фосфора. |
P2+5O5 Фосфорный ангидрид (оксид фосфора (V))
Белые кристаллы, t0пл.= 5700С, t0 кип.= 6000C, r = 2,7 г/см3. Имеет несколько модификаций. В парах состоит из молекул P4h20, очень гигроскопичен (используется как осушитель газов и жидкостей).Получение
4P + 5O2 ® 2P2O5Химические свойства
Все химические свойства кислотных оксидов: реагирует с водой, основными оксидами и щелочами 1) P2O5 + h3O ®2HPO3 (метафосфорная кислота) P2O5 + 2h3O ® h5P2O7 (пирофосфорная кислота) P2O5 + 3h3O ® 2h4PO4 (ортофосфорная кислота) 2) P2O5 + 3BaO ® Ba3(PO4)2 В зависимости от избытка щелочи образует средние и кислые соли: гидрофосфат натрия дигидрофосфат натрия Благодаря исключительной гигроскопичности оксид фосфора (V) используется в лабораторной и промышленной технике в качестве осушающего и дегидратирующего средства. По своему осушающему действию он превосходит все остальные вещества. От безводной хлорной кислоты отнимает химически связанную воду с образованием ее ангидрида: Ортофосфорная кислота. Известно несколько кислот, содержащих фосфор. Важнейшая из них — ортофосфорная кислота Н3РО4 (Рис.5). Безводная ортофосфорная кислота представляет собой светлые прозрачные кристаллы, при комнатной температуре расплывающиеся на воздухе. Температура плавления 42,350С. С водой фосфорная кислота образует растворы любых концентраций. Ортофосфорной кислоте соответствует следующая структурная формула: НО ОН Р О ОН В лаборатории ортофосфорную кислоту получают окислением фосфора 30%-ной азотной кислотой: В промышленности ортофосфорную кислоту получают двумя способами: экстракционным и термическим. 1. В основе экстракционного метода лежит обработка измельченных природных фосфатов серной кислотой: Ортофосфорная кислота затем отфильтровывается и концентрируется упариванием. 2. Термический метод состоит в восстановлении природных фосфатов до свободного фосфора с последующим его сжиганием до Р4О10 и растворением последнего в воде. Производимая по данному методу ортофосфорная кислота характеризуется более высокой чистотой и повышенной концентрацией (до 80% массовых). Физические свойства. Ортофосфорная кислота — твердое, бесцветное, кристаллическое вещество, хорошо растворимое в воде. Химические свойства ортофосфорной кислоты представлены в табл.2: Таблица 2 Химические свойства ортофосфорной кислоты| Общие с другими кислотами | Специфические |
1. Водный раствор кислоты изменяет окраску индикаторов. Диссоциация происходит ступенчато: Легче всего идет диссоциация по первой ступени и труднее всего – по третьей 2. Реагирует с металлами, расположенными в вытеснительном ряду до водорода: 3. Реагирует с основными оксидами: 4. Реагирует с основаниями и аммиаком; если кислота взята в избытке, то образуются кислые соли: гидрофосфат натрия дигидрофосфат натрия 5. Реагирует с солями слабых кислот: | 1. При нагревании постепенно превращается в метафосфорную кислоту: двуфосфорная кислота 2. При действии раствора нитрата серебра (I) появляется желтый осадок: желтый осадок 3. Ортофосфорная кислота играет большую роль в жизнедеятельности животных и растений. Ее остатки входят в состав аденозинтрифосфорной кислоты АТФ. При разложении АТФ выделяется большое количество энергии. |
| одновалентные | двухвалентные | трехвалентные |
Ме3РО4 | Ортофосфаты Ме3(РО4)2 | Ме3РО4 |
Ме2НРО4 | Гидроортофосфаты МеНРО4 | Ме2(НРО4)3 |
МеН2РО4 | Дигидроортофосфаты Ме(Н2РО4)2 | Ме(Н2РО4)3 |
| Название удобрения | Химический состав |
| Простые | |
| Суперфосфат двойной | |
| Суперфосфат простой | |
| Фосфоритная мука | |
| Костяная мука | |
| Преципитат | |
| Шлак мартеновский печей | Сложный состав. Содержит P,Ca, Si, C, Fe и др. элементы |
| Комплексные | |
| Аммофос | |
| Аммофоска | |
| Нитроаммофос | |
works.tarefer.ru
Реферат - Фосфор и его соединения
Фосфор иего соединения
Реферат
Содержание
Введение
Глава I. Фосфор как элемент и как простое вещество
1.1. Фосфор в природе
1.2. Физические свойства
1.3. Химические свойства
1.4. Получение
1.5. Применение
Глава II. Соединения фосфора
2.1. Оксиды
2.2. Кислоты и их соли
2.3. Фосфин
Глава III. Фосфорные удобрения
Заключение
Библиографический список
Введение
/>Фосфор (лат. Phosphorus) P – химический элемент V группы периодической системыМенделеева атомный номер 15, атомная масса 30,973762(4). Рассмотрим строениеатома фосфора. На наружном энергетическом уровне атома фосфора находятся пятьэлектронов. Графически это выглядит так:
1s22s22p63s23p33d0
/>
В 1699 г.гамбургский алхимик X.Бранд в поисках «философского камня», якобы способногопревратить неблагородные металлы в золото, при выпаривании мочи с углём ипеском выделил белое воскообразное вещество, способное светиться.
Название«фосфор» происходит от греч. «phos» – свет и «phoros» – несущий. В Россиитермин «фосфор» введён в 1746 г. М.В. Ломоносовым.
К основным соединениямфосфора относят оксиды, кислоты и их соли (фосфаты, дигидрофосфаты,гидрофосфаты, фосфиды, фосфиты).
Очень много веществ,содержащих фосфор, содержатся в удобрениях. Такие удобрения называютфосфорными.
Глава IФосфор как элемент и какпростое вещество
1.1 Фосфор вприроде
Фосфоротносится к числу распространенных элементов. Общее содержание в земной коресоставляет около 0,08%. Вследствие лёгкой окисляемости фосфор в природевстречается только в виде соединений. Главными минералами фосфора являются фосфоритыи апатиты, из последних наиболее распространён фторапатит 3Ca3(PO4)2 • CaF2. Фосфориты широкораспространены на Урале, в Поволжье, Сибири, Казахстане, Эстонии, Беларуси.Самые большие залежи апатитов находятся на Кольском полуострове.
Фосфор –необходимый элемент живых организмов. Он присутствует в костях, мышцах, вмозговой ткани и нервах. Из фосфора построены молекулы АТФ – аденозинтрифосфорнойкислоты (АТФ – собиратель и носитель энергии). В организме взрослого человекасодержится в среднем около 4,5 кг фосфора, в основном в соединении с кальцием.
Фосфорсодержится также в растениях.
Природныйфосфор состоит лишь из одного стабильного изотопа 31Р. В наши дниизвестно шесть радиоактивных изотопов фосфора.
1.2 ФизическиесвойстваФосфор имеетнесколько аллотропных модификаций – белый, красный, чёрный, коричневый,фиолетовый фосфор и др. Первые три из названных наиболее изучены.
Белыйфосфор –бесцветное, с желтоватым оттенком кристаллическое вещество, светящееся втемноте. Его плотность 1,83 г/см3. Не растворяется в воде, хорошорастворяется в сероуглероде. Имеет характерный чесночный запах. Температураплавления 44°С, температура самовоспламенения 40°С. Чтобы защитить белый фосфорот окисления, его хранят под водой в темноте (на свету идёт превращение вкрасный фосфор). На холоде белый фосфор хрупок, при температурах выше 15°Сстановится мягким и режется ножом.
Молекулыбелого фосфора имеют кристаллическую решётку, в узлах которой находятсямолекулы Р4, имеющие форму тетраэдра.
Каждый атомфосфора связан тремя σ-связями с другими тремя атомами.
Белый фосфорядовит и даёт труднозаживающие ожоги.
Красныйфосфор –порошкообразное вещество тёмно-красного цвета без запаха, в воде исероуглероде не растворяется, не светится. Температура воспламенения 260°С,плотность 2,3 г/см3. Красный фосфор представляет собой смесьнескольких аллотропных модификаций, отличающихся цветом (от алого дофиолетового). Свойства красного фосфора зависят от условий его получения. Неядовит.
Чёрныйфосфор повнешнему виду похож на графит, жирный на ощупь, обладает полупроводниковымисвойствами. Плотность 2,7 г/см3.
Красный ичёрный фосфоры имеют атомную кристаллическую решётку.
1.3 ХимическиесвойстваФосфор – неметалл. Всоединениях он обычно проявляет степень окисления +5, реже – +3 и –3 (только вфосфидах).
Реакции сбелым фосфором идут легче, чем с красным.
I. Взаимодействие с простымивеществами.
1. Взаимодействие сгалогенами:
2P + 3Cl2 = 2PCl3 (хлорид фосфора (III)),
PCl3 + Cl2 = PCl5 (хлорид фосфора (V)).
2. Взаимодействие снематаллами:
2P + 3S = P2S3(сульфид фосфора (III).
3. Взаимодействие сметаллами:
2P + 3Ca = Ca3P2 (фосфид кальция).
4. Взаимодействие скислородом:
4P + 5O2 = 2P2O5 (оксид фосфора (V), фосфорный ангидрид).
II. Взаимодействие со сложнымивеществами.
3P + 5HNO3+ 2h3O = 3h4PO4 + 5NO↑.
1.4 ПолучениеФосфорполучают из измельченных фосфоритов и апатитов, последние смешиваются с углем ипеском и прокаливаются в печах при 1500°С:
2Ca3(PO4)2+ 10C + 6SiO2/> 6CaSiO3+ P4↑ + 10CO↑.
Фосфорвыделяется в виде паров, которые конденсируются в приёмнике под водой, при этомобразуется белый фосфор.
Принагревании до 250-300°С без доступа воздуха белый фосфор превращается вкрасный.
Чёрный фосфорполучается при длительном нагревании белого фосфора при очень большом давлении(200°С и 1200 МПа).
1.5 ПрименениеКрасныйфосфор применяется при изготовлении спичек (см. рисунок). Он входит в составсмеси, наносимой на боковую поверхность спичечного коробка. Основным компонентомсостава головки спички является бертолетова соль KClO3. От трения головкиспички о намазку коробка частицы фосфора на воздухе воспламеняются. Врезультате реакции окисления фосфора выделяется тепло, приводящее к разложениюбертолетовой соли.
KClO3/> KCl + ./>
www.ronl.ru
|
|
..:::Счетчики:::.. |
|
|
|
|
|
|
|
|