 моноаптерин
моноаптеринРеферат на тему:
Фенилкетонури́я (фенилпировиноградная олигофрения) — наследственное заболевание группы ферментопатий, связанное с нарушением метаболизма аминокислот, главным образом фенилаланина. Сопровождается накоплением фенилаланина и его токсических продуктов, что приводит к тяжёлому поражению ЦНС, проявляющемуся, в частности, в виде нарушения умственного развития.
Открытие фенилкетонурии связывают с именем норвежского врача Ивара Асбьёрна Фёлинга, описавшего в 1934 году гиперфенилаланинемию, ассоциированную с задержкой умственного развития. В Норвегии заболевание известно под названием 'болезни Фёлинга' в честь открывателя. Успешное лечение впервые было разработано и проведено в Англии (Бирмингемский детский госпиталь) группой медиков под руководством Хорста Биккеля в начале 50-х годов XX века, однако настоящий успех пришел только после широкого применения ранней диагностики фенилкетонурии по повышенному содержанию фенилаланина в крови у новорожденных (метод Гатри, разработанный и внедренный в 1958—1961 гг). Со временем и накоплением опыта в диагностике и лечении фенилкетонурии стало ясно, что это гетерогенное заболевание, вызываемое множеством мутаций в разных генах. Выделены и описаны атипичные формы ФКУ, разработаны новые методы лечения, в ближайшей перспективе — генотерапия этого тяжелого заболевания, ставшего классическим образцом успешного оказания медицинской и организационной помощи при наследственной патологии.
В большинстве случаев (классическая форма) заболевание связано с резким снижением или полным отсутствием активности печёночного фермента фенилаланин-4-гидроксилазы, который в норме катализирует превращение фенилаланина в тирозин. До 1 % случаев фенилкетонурии представлено атипичными формами, связанными с мутациями в других генах, отвечающих за кодирование ферментов, обеспечивающих синтез кофактора фенилаланингидроксилазы — тетрагидробиоптерина (Bh5). Заболевание наследуется по аутосомно-рецессивному типу.
Вследствие метаболического блока активируются побочные пути обмена фенилаланина, и в организме происходит накопление его токсичных производных — фенилпировиноградной и фенилмолочной кислот, которые в норме практически не образуются. Кроме того, образуются также почти полностью отсутствующие в норме фенилэтиламин и ортофенилацетат, избыток которых вызывает нарушение метаболизма липидов в головном мозге. Предположительно, это и ведёт к прогрессирующему снижению интеллекта у таких больных вплоть до идиотии. Окончательно механизм развития нарушений функций мозга при фенилкетонурии остается неясным. Среди причин также предполагается дефицит нейромедиаторов мозга, вызванный относительным снижением количества тирозина и других «больших» аминокислот, конкурирующих с фенилаланином при переносе через гематоэнцефалический барьер, и прямое токсическое действие фенилаланина.
Производится полуколичественным тестом или количественным определением фенилаланина в крови. При нелеченных случаях возможно выявление продуктов распада фенилаланина (фенилкетонов) в моче (не ранее 10-12 дня жизни ребенка). Также возможно определение активности фермента фенилаланингидроксилазы в биоптате печени и поиск мутаций в гене фенилаланингидроксилазы. Для диагностики 2 и 3 типа, связанных с мутацией в гене, отвечающем за синтез кофактора, необходимы дополнительные диагностические исследования. В возрасте от 2-4 месяцев у больных появляются такие симптомы, как вялость, судороги, экзема, мышиный запах.
При своевременной диагностике патологических изменений можно полностью избежать, если с рождения и до полового созревания ограничить поступление в организм фенилаланина с пищей.
Позднее начало лечения хотя и даёт определённый эффект, но не устраняет развившихся ранее необратимых изменений ткани мозга.
Некоторые из современных газированных напитков, жевательных резинок и лекарственных препаратов содержат фенилаланин в форме дипептида (аспартам), о чём производители обязаны предупреждать на этикетке.
При рождении ребёнка в роддомах на 3-4 сутки берут анализ крови и проводят неонатальный скрининг для обнаружения врожденных заболеваний обмена веществ. На этом этапе возможно обнаружение фенилкетонурии, и, как следствие, возможно раннее начало лечения для предотвращения необратимых последствий.
Лечение проводится в виде строгой диеты от обнаружения заболевания как минимум до полового созревания, многие авторы придерживаются мнения о необходимости пожизненной диеты. Диета исключает мясные, рыбные, молочные продукты и другие продукты, содержащие животный и, частично, растительный белок. Дефицит белка восполняется аминокислотными смесями без фенилаланина. Кормление грудью детей, больных фенилкетонурией, возможно и может быть успешным при соблюдении некоторых ограничений[1][2].
Расчет диеты для больного ФКУ проводит врач с учетом потребности в фенилаланине и его допустимом количестве.
Допустимое количество фенилаланина для больных ФКУ[3]
| До 2 мес. | 60 |
| 2-3 мес. | 60-55 |
| 3-6 мес. | 55-45 |
| 6-12 мес. | 45-35 |
| 1-1,5 года | 35-30 |
| 1,5-3 года | 30-25 |
| 3-6 лет | 25-15 |
| Старше 6 лет | 15-10 |
Некоторые (мягкие) формы заболевания поддаются лечению кофактором (тетрагидробиоптерином) пораженного фермента (фенилаланингидроксилазы). Разрабатываются новые подходы к лечению фенилкетонурии — использование заместительной терапии фенилаланинлиазой (PAL) — растительным ферментом, превращающим фенилаланин в безвредные метаболиты, и генотерапия на основе введения в организм вирусного вектора, содержащего ген фенилаланингидроксилазы. Эти методы пока не вышли из стен лабораторий. Атипичные формы не поддаются диетотерапии и лечатся только введением препаратов тетрагидробиоптерина или его синтетических аналогов (сапроптерин[4]).
wreferat.baza-referat.ru
Актуальность
1. Фенилкетонурия (ФКУ) является наиболее распространенной аминоацидопатией. Частота ФКУ среди новорожденных по данным массового скрининга в различных странах составляет в среднем 1:10000, однако значительно варьирует в зависимости от популяции: от 1:4560 в Ирландии, до 1:100.000 в Японии. (см. таблицу)
Табл. Заболеваемость ФКУ по данным массового скрининга
2. Ребенок с фенилкетонурией выглядит при рождении здоровым. Отставание психического развития может происходить постепенно и стать очевидным лишь через несколько месяцев. Установлено, что нелеченный ребенок теряет около 50 баллов IQ к концу первого года жизни. Отставание психического развития обычно довольно выражено, и большинство детей нуждаются в социальной помощи.
3. В связи с тяжестью клинических проявлений и возможностью профилактического лечения ФКУ рекомендована для выявления среди новорожденных. Ранняя диагностика позволяет своевременно начать лечение и предотвратить инвалидизацию больного.
4. Лечение и реабилитация больных ФКУ требует значительных финансово-экономических затрат. Это обусловлено высокой себестоимостью продуктов лечебного питания, а также усилиями по социальной реабилитации больного.
5. Помимо этого, об актуальности заболевания, свидетельствует проблема материнской ФКУ, лишь недавно появившаяся в России. Наблюдается высокая частота умственной отсталости среди потомства женщин, страдающих ФКУ и не получающих диету в зрелом возрасте.
6. Скудная клиническая картина в раннем возрасте, постепенное развитие патологических изменений, приводит к серьезным затруднениям в ранней диагностике этого заболевания. В тоже время, диетотерапия больных с ФКУ должна находиться под тщательным динамическим контролем. А психоневрологическая реабилитация больных (медикаментозная, физиолечение, медико-педагогическая) требует индивидуального подхода. Педиатры, в чьи обязанности входит реабилитация больных ФКУ, встречаются с ней в повседневной практике нечасто. Поэтому необходимо ознакомить врачей с особенностями течения и лечением ФКУ.
Этиология, патогенез
По Mc Kusick выделяется несколько типов фенилкетонурии.
Фенилкетонурия I
Классическая фенилкетонурия. Была описана А. Folling в 1934 г. Заболевание наследуется аутосомно-рецессивно и вызвано мутацией гена ФАГ, локализующегося в длинном плече 12 хромосомы. В гене ФКУ выявлено 12 различных гаплотипов. При этом 90% всех генов ФКУ ассоциировано с четырьмя гаплотипами, из них гаплотип 3 характеризует около 38% всех генов ФАГ, а гаплотип 2 - около 20%.
В основе болезни лежит дефицит фермента фенилаланин - 4 - гидроксилазы (ФАГ), обеспечивающей превращение фенилаланина в тирозин. В результате метаболического блока происходит значительное накопление в тканях и жидкостях больного организма фенилаланина и таких его производных, как фенилпировиноградная, фенилмолочная, фенилуксусная кислоты, фенилэтиламин, фенилацетилглютамин и др.
По мнению различных авторов в патогенезе ФКУ имеют значение следующие обстоятельства: прямое токсическое действие на центральную нервную систему фенилаланина и его производных, нарушения в обмене белков, липо- и гликопротеидов, расстройства транспорта аминокислот, нарушение метаболизма гормонов и др., а также перинатальные факторы. В последнее время все большее значение в патогенезе ФКУ придается нарушениям обмена моноаминовых нейромедиаторов (катехаламинов и серотонина). Известна исключительно важная роль этих медиаторов в функционировании центральной нервной системы. Исследования показали, что у больных резко снижено содержание конечных продуктов их метаболизма (гомованилиновой кислоты и 5-оксииндолуксусной кислоты) в крови, моче и цереброспинальной жидкости.
Определенное значение в генезе церебральных расстройств могут играть нарушения функции печени. У большинства больных ФКУ при обследовании обнаруживаются различные биохимические и морфологические изменения, свидетельствующие о заинтерсованности этого органа в патологическом процессе: диспротеинемия, генерализованная гипераминацидемия, повышение показателя дифениламиновой реакции, компенсированный метаболический ацидоз, признаки белковой и жировой дистрофии печени с нарушением окислительной и белоксинтезирующей функции клеточных органелл.
Фенилкетонурия II
Впервые атипичная ФКУ была описана I. Smith в 1974 г. S. Kaufman et al. В 1975 г. обнаружили дефицит дигидроптеридинредуктазы при этом состоянии.
Заболевание наследуется аутосомно-рецессивно. Генный дефект локализуется в коротком плече 4 хромосомы, участке 4р15.3. В результате недостаточности дигидроптеридинредуктазы нарушается восстановление активной формы тетрагидробиоптерина, участвующего в качестве кофактора в гидроксилировании фенилаланина, тирозина и триптофана. Вследствие этого развиваются метаболические блоки на путях превращения фенилаланина в тирозин, а также образования предшественников нейромедиаторов катехоламинового и серотонинового ряда L-дофы и 5-окситриптофана, что подтверждается резким снижением содержания в тканях и жидкостях больного организма (в том числе в мозге и цереброспинальной жидкости) их конечных продуктов - гомованилиновой и 5-оксиндолуксусной кислот.
Существенным для патогенеза заболевания является снижение уровня фолатов в сыворотке крови, эритроцитах и цереброспинальной жидкости. Это объясняется тесной взаимосвязью обмена фолатов и биоптерина, в частности участием дигидроптеринредуктазы в метаболизме тетрагидрофолиевой кислоты.
Фенилкетонурия III
Этот вариант болезни впервые описан S. Kaufman et al. в 1978 г. Заболевание наследуется аутосомно-рецессивно и связано с недостаточностью 6-пирувоилтетрагидроптерин синтазы, участвующей в процессе синтеза тетрагидробиоптерина из дигидронеоптерин трифосфата. Ключевую роль в патогенезе играет дефицит тетрагидробиоптерина. Развивающиеся при этом расстройства сходны с нарушениями, наблюдаемыми при ФКУ II.
Другие варианты ФКУ
В последние годы стали известны другие формы атипичной ФКУ, связанные с дефицитом тетрагидробиоптерина.
Недостаточность гуанозин 5-трифосфат циклогидролазы (S. Kaufman et al., 1987) описана по крайней мере у пяти больных. Этот фермент катализирует первую ступень синтеза тетрагидробиоптерина и при его дефиците в моче обнаруживается крайне низкая концентрация всех птеринов.
N. Blau и соавторы (1989) сообщили о новом варианте атипичной ФКУ - примаптеринурии - у двух детей с легкой гиперфенилаланинемией. Энзиматический дефект пока не известен. В моче обнаруживается в больших количествах продукт изомеризации биоптерина-7 - изобиоптерин (примаптерин) и некоторые другие его производные. Соотношение неоптерин/биоптерин у больных значительно повышено. Нагрузка тетрагидробиоптерином нормализует концентрацию фенилаланина в сыворотке и уровень неоптерина в моче, резко повышает экскрецию биоптерина и примаптерина. Отличием от других атипичных форм ФКУ является нормальная концентрация в цереброспинальной жидкости нейромедиаторных метаболитов - гомованилиновой и 5-оксииндолуксусной кислот.
Материнская ФКУ
В процессе изучения ФКУ было обращено внимание на высокую частоту умственной отсталости среди потомства женщин, страдающих ФКУ и не получающих диету в зрелом возрасте. Это состояние получило наименование материнской ФКУ. Патогенез патологии мало изучен, однако предполагается, что он сходен с патогенезом остальных форм ФКУ. Тяжесть поражения плода коррелирует с уровнем фенилаланина в плазме матери. Причем в связи с накоплением этой аминокислоты в плаценте, ее содержание в организме плода оказывается выше, чем у матери. Тем не менее прямое токсическое действие фенилаланина точно не подтверждено. Появление признаков патологии у потомства не зависит от наличия или отсутствия умственной отсталости у женщин и не связано с развитием у детей ФКУ. Есть данные, что тяжесть заболевания у больных ФКУ, родившихся от матерей, также страдающих этой болезнью, не отличается от степени поражения их сибсов, не унаследовавших ФКУ.
Схема 1. Пути обмена фенилаланина и его предшественников, и “точки приложения” метаболических дефектов. гуанозин 5’ трифосфат моноаптерин
моноаптерин
дигидронеоптерин

 1 дигидронеоптерин трифосфат
1 дигидронеоптерин трифосфат  |
неоптерин
2 6-пировоилтетрагидроптерин |
фенилаланин
тирозин тетрагидробиоптерин

 триптофан
триптофан
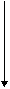
| 4 4 |
5 птерин

тирозин
 5-окситриптофан дигидробиоптерин 7,8-дигидробиоптерин
5-окситриптофан дигидробиоптерин 7,8-дигидробиоптерин
 дофа
дофа
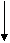 |
дофамин биоптерин
Пояснение к схеме 1.1. гуанозин 5’ трифосфат циклогидролаза
2. 6-пирувоилтетрагидроптерин синтаза
3. сепиаптерин редуктаза
4. фенилаланин-4-гидроксилаза, тирозингидроксилаза, триптофангидроксилаза
5. дигидроптеридин редуктаза
Клиническая картина
Фенилкетонурия I
Манифестация ФКУ происходит на первом году жизни, обычно в возрасте 2-6 мес. Первыми проявлениями болезни служат вялость ребенка, отсутствие интереса к окружающему, иногда повышенная раздражительность, беспокойство, срыгивания, нарушение мышечного тонуса (чаще мышечная гипотония), судороги, признаки аллергического дерматита. Появляется характерный “мышиный” запах. Отчетливо формируется задержка статикомоторного и психоречевого развития. При отсутствии лечения умственная отсталость достигает, как правило, глубокой степени.
Ранним симптомом заболевания может стать рвота, иногда настолько сильная, что ее ошибочно расценивают как проявление пилоростеноза. В более старшем возрасте нелеченные дети становятся гиперактивными, осуществляют бесцельные движения, ритмические покачивания, у них определяется атетоз.
При физикальном исследовании обращает на себя внимание то, что ребенок выглядит более белокурым, чем его здоровые сиблинги: у него светлая кожа и голубые глаза. У некоторых больных появляется себорейная или экзематоидная кожная сыпь, обычно умеренно выраженная и исчезающая по мере роста ребенка. От них исходит необычный запах фенилуксусной кислоты, который характеризуют как заплесневелый, мышиный или волчий. Не встречается характерных неврологических изменений, однако у большинства детей определяются гипертонус и повышение глубоких сухожильных рефлексов. Около 1/4 детей страдают судорогами и более чем у 50% появляются изменения на ЭЭГ. Часто у нелеченных детей определяют микроцефалию, выступающую верхнюю челюсть с широко расставленными зубами, гипоплазией эмали, отставание роста. Клинические проявления классической фенилкетонурии редко встречаются в странах, в которых эффективно действует программа неонатального скрининга на это заболевание.
Фенилкетонурия II
В клинической картине ФКУ II преобладает тяжелая умственная отсталость, судороги, признаки повышенной возбудимости, сухожильная гиперрефлексия, мышечная дистония, спастический тетрапарез. Течение болезни прогрессирующее и нередко приводит к смерти в 2-З-летнем возрасте. Больные, как правило, выявляются в результате массового скрининга новорожденных на ФКУ. Уровень фенилаланина в крови у этих детей увеличен, иногда может превышать 1200 мкмоль/л. Появление клинической симптоматики, как правило развивается в начале второго полугодия жизни, несмотря на диетотерапию.
Фенилкетонурия III
Клиническая картина болезни напоминает ФКУ II и включает тяжелую умственную отсталость, микроцефалию, спастический тетрапарез. Для подтверждения диагноза требуется:
Возможности диагностики
Диагностика основывается на совокупности генеалогических данных (возможны эндогамный брак, аналогичная патология у сибсов), результатов клинического и биохимического обследования. Уровень фенилаланина в крови у больных превышает 900-1200 мкмоль/л. В моче присутствуют продукты трансаминирования и декарбоксилирования фенилаланина, в первую очередь, фенилпировиноградная кислота.
Проба Феллинга
Выявление фенилпирувата в моче при помощи хлорида 3-х валентного железа. Метод недостаточно точный и позволяет диагностировать заболевание только со 2-го месяца жизни.
Тест Гатри
Методику теста описал Роберт Гатри в 1961 году. В ее основе лежит бактериальное ингибирование определенных штаммов Bacillus cereus.
Хроматография
Проводится тонкослойная хроматография аминокислот плазмы крови и мочи.
Флуориметрия
С помощью современных автоматических флуориметров, возможно проведение массового автоматизированного скрининга.
Определение активности ФАГ или тетрагидробиоптеринредуктазы
Значительное снижение активности ферментов, обнаруживается у гомозигот, а умеренное (до 70%) у гетерозигот по мутантному аллелю ФКУ.
Поиск мутантного гена
Проводится прямой поиск мутантного гена с помощью синтетических олигонуклеотидных зондов. Помимо этого возможно прямое определение мутаций в гене фенилаланингидроксилазы или косвенное подтверждение наследования мутантного локуса ФАГ в одной или двух копиях, идентифицируемое по ПДРФ (полиморфизм длины рестрикционных фрагментов) или ВНТР (вариабельные по количеству тандемные повторы) в ДНК пробанда и его родителей.
Скрининг
Клинический полиморфизм отклонения от классической картины, возможность проведения эффективного лечения при своевременной диагностике, диктует необходимость проведения скрининга. Целью скрининга является раннее выявление заболевания и назначение диетического лечения больным до достижения ими 8-недельного возраста. Эти сроки начала лечения по общепризнанному мнению позволяют обеспечить полноценное развитие детей.
Скрининговые исследования проводятся в два этапа:
Первый этап предусматривает обнаружение отклонений от нормы в содержании фенилаланина в сыворотке крови новорожденного.
Обследования проводятся на 4-5-й день жизни ребенка. Кровь наносится на бланк из специальной впитывающей бумаги.
Обязательное условие для выполнения скрининга: диаметр кровяного пятна должен быть равен диаметру круга на фильтрованной бумаге с пропитыванием кровью обратной стороны. Заполненные бланки направляются в ближайшую специализированную лабораторию.
Второй этап - повторное тестирование из того же пятна крови в случаях получения результата анализа на первом этапе с уровнем фенилаланина выше допустимого.
При повторно положительных тестах информация направляется в районные медико-генетические центры с целью немедленного приглашения ребенка к врачу для окончательного уточнения диагноза ФКУ.
В Российской Федерации скрининг-тесты осуществляются в 45 медико-генетических лабораториях различных регионов, куда поступают анализы крови всех новорожденных из всех родильных домов.
Если диагноз ФКУ подтверждается, необходимо сразу начинать лечение, это позволяет предотвратить тяжелые последствия в развитии ребенка.
Лечение
Элиминационная диета
Главным способом лечения ФКУ является диетотерапия, ограничивающая поступление в организм пищевого белка и фенилаланина до минимальной возрастной потребности. В пищевой рацион больных входят овощи, фрукты, соки, а также специальные малобелковые продукты (саго, хлеб, вермишель, крупка, приготовленные на крахмальной основе). Однако, в период интенсивного роста и развития ребенка поступление белка в организм должно быть достаточным. Дефицит его незамедлительно отразится на процессе формирования всех органов и систем. Поэтому нельзя полностью исключить из рациона новорожденного материнское молоко. Для коррекции питания детям даются белковые гидролизаты, лишенные фенилаланина, но содержащие все другие необходимые аминокислоты. Больные нуждаются в дополнительном введении витаминов, особенно, группы В, минеральных веществ и микроэлементов.
Сразу после подтверждения диагноза ФКУ необходимо начать незамедлительное, но постепенное (в течение З-х дней) исключение из питания больного высокобелковых продуктов питания, заменяя их малобелковыми.
Если ребенок находится в возрасте до 1 - 1,5 мес и получает только грудное молоко или его заменитель - его постепенно приучают к лечебной молочной смеси, не меняя режима кормления.
Специальные лечебные продукты питания для больных ФКУЭти продукты производятся на основе гидролизата казеина или смеси аминокислот: Лофеналак, Фенил-Фри, Нофелан, отечественный Тетрафен и другие. Для грудных детей используется Лофеналак.
Табл. 1. Состав продукта “Лофеналак” на 100 грамм сухой смеси.
| Энергия | 462 ккал |
| Белки | 15 г |
| Жиры | 18 г |
| Углеводы | 60 г |
| Фенилаланин | 16мг/100ккал |
Витамины, минеральные вещества и необходимые для роста аминокислоты добавлены в таком количестве, чтобы смесь по составу максимально приближалась к обычным молочным смесям для детского питания.
Однако содержание фенилаланина в Лофеналаке не обеспечивает суточную потребность в этой аминокислоте. Поэтому рекомендуется готовить молочную лечебную смесь, используя 2 компонента: Лофеналак и грудное молоко или его заменитель, растворяя их в кипяченой воде.
Для детей с ФКУ старте 1 года принципы лечебной диеты не отличаются от диеты детей грудного возраста. Рацион состоит из:
1. лечебного продукта питания для больных ФКУ
2. блюд из натуральных продуктов.
Отечественный продукт “Тетрафен” создан компанией АО “Нутритек” в соответствии с медико-биологическими требованиями Института питания РАМН. Продукт предназначен для диетического питания больных фенилкетонурией детей в возрасте старше 1 года.
Продукт представляет из себя смесь аминокислот с витаминами, минеральными веществами, углеводами. Последние состоят из смеси декстринмальтозной патоки, глюкозы, крахмала, что значительно улучшает вкус продукта. Тетрафен содержит минимальное количество фенилаланина, хорошо растворим в воде, обладает удовлетворительными органолептическими свойствами. Тетрафен используется в диете в качестве основного источника белка, минеральных веществ и витаминов.
В табл. 3 представлен химический состав и энергетическая ценность Тетрафена, в табл. 4 - аминокислотный состав смеси.
Табл. 2. Химический состав и энергетическая ценность специализированного продукта “Тетрафен”
| Пищевые ингредиенты | Количество в 100г. сухой смеси | Пищевые ингредиенты | Количество в 100г. сухой смеси |
| Белковый эквивалент, г | 40 | Витамины А, мг | 1,7 |
| Углеводы, г | 38 | D2, мг | 0,011 |
| Минеральные вещества кальций, г | 1,1 | Е, мг | 23 |
| фосфор, г | 0,8 | С, мг | 125 |
| калий, г | 3,2 | РР, мг | 1,5 |
| натрий, г | 1,1 | В2, мг | 2,1 |
| магний, г | 0,2 | В3, мг | 11 |
| медь, мг | 2,6 | В6, мг | 2,1 |
| цинк, мг | 16 | В12, мг | 0,005 |
| йод, мг | 0,13 | Фолаты, мг | 0,6 |
| железо, мг | 23 | холин, г | 0,5 |
| марганец, мг | 23 | биотин, мг | 0,2 |
| хлор, г | 1,9 | инозитол, г | 0,5 |
| молибден, мг | 0,013 | Энергия, ккал | 312 |
Табл. 3. Аминокислотный состав продукта “Тетрафен”
| Аминокислоты | г на 16 г азота | Аминокислоты | г на 16 г азота |
| Гистидин | 2,6 | Тирозин | 7,2 |
| Изолейцин | 4,6 | Треонин | 4,3 |
| Лейцин | 9,9 | Триптофан | 2,0 |
| Лизин | 6,6 | Валин | 5,5 |
| Метионин+цистин | 4,2 | Сумма незаменимых аминокислот | 45,3 |
| Фенилаланин | 0,0-0,5 | Таурин | - |
Расчет питания с использованием “Тетрафена”
Питание больным ФКУ назначают в зависимости от возраста и массы тела ребенка. При определении необходимого химического состава суточного рациона ребенка ориентируются на физиологические возрастные потребности детей в пищевых ингредиентах, приведенные в Рекомендуемых нормах потребления энергии, белков, жиров, углеводов, минеральных веществ и витаминов, утвержденных Главным санитарным врачом СССР 28.05.91 г. № 578691 (табл. 5)
Табл. 4. Рекомендуемые нормы потребления, для детей разных возрастных групп (в сутки)
| Ингредиенты | Возрастные группы детей | |||
| 1-3 года | 4-6 лет | 6 лет (школьники) | 7-10 лет | |
| Белки, г | 53 | 68 | 69 | 77 |
| в т.ч. животные | 37 | 45 | 45 | 46 |
| Жиры, г | 53 | 68 | 67 | 79 |
| в т.ч. растительные | 7 | 9 | 13 | 16 |
| Углеводы, г | 212 | 272 | 285 | 335 |
| Энергия, ккал | 1540 | 1970 | 2000 | 2350 |
Проводя такие расчеты, следует учитывать, что общее количество белка в рационах больных ФКУ детей снижается по сравнению с указанными физиологическими показателями. Расчет идет с ориентацией на нижнюю границу возрастном нормы (2,5 г на 1 кг массы тела) с учетом индивидуальном толерантности к фенилаланину. Белок за счет естественных продуктов в диете больного ребенка рассчитывают, исходя из допустимых суточных количеств фенилаланина (табл. 6) с учетом, что 1 г белка приблизительно равен 50 мг фенилаланина.
Табл. 5. Допустимое суточное количество фенилаланина для больных ФКУ детей различных возрастных групп.
| Возраст | Количество фенилаланина (мг на 1 кг массы тела) |
| 1-1,5 лет | 35-30 |
| 1,5-3 года | 30-25 |
| 3-5 лет | 25-20 |
| старше 5 лет | 20-15 |
Количество белка в рационе за счет “Тетрафена” составляет разницу между общим белком и белком естественных продуктов. Суточную дозу аминокислотной смеси рассчитывают по формуле:
(общее количество белка - белок естественных продуктов) х 100 количество белка в 100 г “Тетрафена”“Тетрафен” вводят в рацион больного ребенка постепенно. Начальные дозы составляют 1/5 - 1/3 от суточного количества аминокислотной смеси. В течение первой недели количество смеси постепенно увеличивают и доводят до полной дозы. Одновременно в рационе ребенка уменьшают долю белка за счет естественных продуктов.
“Тетрафен” дают детям, как правило, 2 раза в день - утром и в полдник. Разводить смесь можно теплой кипяченой водой, сладким чаем или различными соками (по желанию ребенка) до сметанообразной кашицы.
Пример расчета питания ребенку с ФКУ
Ребенок 3 лет, масса тела 14,5 кг
1. Общее суточное количество белка в рационе больного:
2,5 х 14,5 = 36,3 г
2. Допустимое суточное количество фенилаланина:
25 х 14,5 = 363 мг
3. Допустимое количество белка естественных продуктов (1 г белка содержит 50 мг фенилаланина):
З6З:50 = 7,3 г
4. Количество белка за счет смеси “Тетрафен”:
36,3 - 7,3 = 29 г
5. Суточное количество смеси “Тетрафен” (100 г смеси содержит 40г белка):
29 x 100:400 = 72,5 г
6. Необходимое суточное количество жира в рационе - 53 г.
7. Необходимое суточное количество углеводов - 212 г.
Диетическое лечение больных ФКУ детей проводят под строгим контролем содержания фенилаланина в сыворотке крови. Этот показатель является главным критерием оценки эффективности лечения и должен находится в средних пределах, равных 3-6 мг%. В тех случаях, когда уровень фенилаланина в сыворотке крови падает ниже 2 мг% или превышает 8 мг%, необходимо проводить, соответствующую коррекцию белка в рационе больного. Контрольные исследования у детей старше 1 года при достижении стабильных показателей фенилаланина можно проводить один раз в 2-3 месяца. Не рекомендуется исследовать содержание фенилаланина в сыворотке крови, если ребенок болен или не съел накануне полностью назначенную диету, т.к. в данных случаях результаты могут быть искажены.
В настоящее время не решен вопрос о продолжительности проводимого лечения и возможных сроках его окончания. Показано, что расширение диеты в младшем школьном возрасте ограничивает интеллектуальные возможности детей, отрицательно влияет на их поведение, внимание, память и др., ухудшает электроэнцефалографические данные. Рассматривается вопрос о постепенной отмене диеты у старших детей под контролем психологических тестов, ЭЭГ и содержания фенилаланина в крови. Как альтернатива диетотерапии предложен метод лечения больных дополнительным введением аминокислот с разветвленной цепью (лейцина, изолейцина и валина), а также тирозина и триптофана. Такой способ эффективно снижает содержание фенилаланина в тканях организма за счет конкурентного ингибирования транспортных систем.
Медикаментозная терапия
Параллельно осуществляется медикаментозное патогенетическое и симптоматическое лечение ноотропными средствами, антиконвульсантами, препаратами группы АТФ и др. Необходима дополнительная коррекция вторичных нейромедиаторных расстройств. В связи с этим целесообразно в комплексе лечения детей включать лекарства с промедиаторным действием (ДОФА, наком, мадопар).
Дополнительная терапия
Необходимы курсы массажа и лечебной физкультуры. В последнее время появились данные об эффективности лазеростимуляции биологически активных точек низкоэнергетическим гелий-неоновым лазером.
Хорошие перспективы в интеллектуальной реабилитации отмечены при использовании современных компьютерных технологий: средств трехмерного моделирования и распознавания речи, программно-аппаратных комплексов создания виртуальной реальности. Компьютерные системы создают для больного ребенка новый собственный мир и постепенно адаптируют его к миру реальному. Бурное развитие микропроцессорных технологий привело к резкому увеличению производительности компьютеров и одновременно значительному снижению их стоимости. Это уже сегодня позволяет создавать реабилитационные комплексы на базе стандартных вычислительных платформ (хотя еще недавно для этого требовались специализированные дорогостоящие компьютеры).
Заключение
Своевременная диагностика фенилкетонурии позволяет вовремя начать диетотерапию и избежать серьезных последствий для здоровья ребенка и снизить экономические издержки, связанные с социальной реабилитацией при поздней диагностике ФКУ.
Для этого необходимо:
1. Стремиться к 100% охвату скринингом новорожденных детей. Учитывая высокую частоту встречаемости ФКУ, это важное мероприятие для раннего выявления больных детей и предотвращения необратимых изменений.
2. Выявление семей риска и проведение в них медико-генетического консультирования. Семьи риска выявляются по данным скрининга и по обращаемости; последняя зависит от грамотности врачей и уровня информированности населения.
3. Проведение медико-генетического консультирования с использованием ДНК-диагностики, для подтверждения носительства мутации. Использование пренатальной диагностики в семьях риска.
4. Повышение уровня подготовки врачей-педиатров. Для полноценного развития ребенка, необходимо наличие грамотных специалистов по диетотерапии ФКУ, психологической и нейрореабилитации. Для этого, возможно, необходимо создание специализированного центра или ассоциации родителей, имеющих детей с ФКУ.
Список литературы
1. Ю. Е. Вельтищева, Н.П. Бочкова “Наследственная патология человека”, 1-й том, М. 1992
2. А.Е. Берман, В. К. Воган “Болезни плода и новорожденного. Врожденные нарушения обмена веществ” . 2-й том руководства по педиатрии (в 8 - ми томах) М.Мед 1991.
3. А.С. Батуева “Физиология плода и детей” М. Мед. 1988
4. С.И. Козлова “Наследственные синдромы и медико-генетическое консультирование”, Л. Мед. 1987
5. Л.О. Бадалян “Наследственные болезни”, Ташкент, Мед. 1980
6. А.П. Бочков “Наследственность человека и мутагены внешней среды”, М. Мед 1989
7. П.Б. Гофман-Кадошников “Генетика для врачей”, М. 1983
8. Ф. Фогель, А. Мотульски “Генетика человека” Р-во в 3-х томах, М. “Мир”
9. Н.П. Шабалов “Неонатология” М. Мед. 1988
10. Л. Рацев, И. Тодоров “Обмен веществ в детском возрасте” М и Ф, София 1967
11. Г. Г. Шанько “Болезни нервной системы новорожденных и детей раннего возраста” Минск, 1990.
12. “Как жить с фенилкетонурией?”, методическое пособие, Клиника наследственных нарушений обмена веществ Университета штата Колорадо, США. Республиканский центр неонатального скрининга, Россия. 1996
13. Минздравмедпром РФ, Инструкция по применению специализированного продукта “Тетрафен” для лечебного питания больных фенилкетонурией детей в возрасте старше 1 года., М. 1996
14. KidsHealth - Children's Health & Parenting Inс., The Nemours Foundation 1997, http://kidshealth.org
15. HealthGate Home Page, http://www.healthgate.com
16. Department of Medical Informatics, Columbia University., http://www.cpmc.columbia.edu
www.km.ru
Актуальность
Ребенок с фенилкетонурией выглядит при рождении здоровым. Отставание психического развития может происходить постепенно и стать очевидным лишь через несколько месяцев . Установлено, что нелеченный ребенок теряет около 50 баллов IQ к концу первого года жизни. Отставание психического развития обычно довольно выражено, и большинство детей нуждаются в социальной помощи.
Табл. Заболеваемость ФКУ по данным массового скрининга
| Москва | 1:11765 |
| Белоруссия | 1:5578 |
| Хабаровский край | 1:9708 |
| Англия | 1:14306 |
| ФРГ | 1:6697 |
| Ирландия | 1:4560 |
| Греция | 1:18460 |
| Шотландия | 1:8350 |
| США | 1:15059 |
| Австралия | 1:11224 |
| Мексика | 1:45610 |
| Япония | 1:100000 |
| ЧСФР | 1:8122 |
| Польша | 1:9248 |
Этиология, патогенез
Схема патогенеза фенилкетонурии
По Mc Kusick выделяется несколько типов фенилкетонурии.
Фенилкетонурия I
Классическая фенилкетонурия. Была описана А. Folling в 1934 г. Заболевание наследуется аутосомно- рецессивно и вызвано мутацией гена ФАГ, локализующегося в длинном плече 12 хромосомы. В гене ФКУ выявлено 12 различных гаплотипов . При этом 90% всех генов ФКУ ассоциировано с четырьмя гаплотипами, из них гаплотип 3 характеризует около 38% всех генов ФАГ, а гаплотип 2 - около 20% .
В основе болезни лежит дефицит фермента фенилаланин - 4 - гидроксилазы (ФАГ), обеспечивающей превращение фенилаланина в тирозин. В результате метаболического блока происходит значительное накопление в тканях и жидкостях больного организма фенилаланина и таких его производных, к ак фенилпировиноградная, фенилмолочная, фенилуксусная кислоты, фенилэтиламин, фенилацетилглютамин и др.
По мнению различных авторов в патогенезе ФКУ имеют значение следующие обстоятельства: прямое токсическое действие на центральную нервную систему фенилаланина и его производных, нару шения в обмене белков, липо- и гликопротеидов, расстройства транспорта аминокислот, нарушен ие метаболизма гормонов и др., а также перинатальные факторы. В последнее время все большее знач ение в патогенезе ФКУ придается нарушениям обмена моноаминовых нейромедиаторов (катехаламинов и серотонина). Известна исключительно важная роль этих медиаторов в функционировании центральной нервной системы. Исследования показали, что у больных резко снижено содержан ие конечных продуктов их метаболизма (гомованилиновой кислоты и 5- оксииндолуксусной кислоты) в крови, моче и цереброспинальной жидкости.
Определенное значение в генезе церебральных расстройств могут играть нарушения функции печени. У большинства больных ФКУ при обследовании обнаруживаются различные биохимические и морфологические изменения, свидетельствующие о заинтерсованности этого органа в патологическом процессе: диспротеинемия, генерализованная гипераминацидемия, повышение показателя дифениламиновой реакции, компенсированный метаболический ац идоз, признаки белковой и жировой дистрофии печени с нарушением окислительной и белоксинтезирую щей функции клеточных органелл.
Фенилкетонурия II
Впервые атипичная ФКУ была описана I. Smith в 1974 г. S. Kaufman et al. В 1975 г. обнаружили дефицит дигидроптеридинредуктазы при этом состоянии.
Заболевание наследуется аутосомно- рецессивно. Генный дефект локализуется в коротком плече 4 хромосомы, участке 4р15.3 . В результате недостаточности дигидроптеридинредуктазы нарушается восстановление активной формы тетрагидробиоптерина, участвующего в качестве кофактора в гидроксилировании фенилаланина, тирозина и триптофана. Вследствие этого развиваются метаболические блоки на путях превращения фенилаланина в тирозин, а также образования предшественников нейромедиаторов катехоламинового и серотонинового ряда L-дофы и 5- окситриптофана , что подтверждается резким снижением содержания в тканях и жидкостях больного организма (в том числе в мозге и цереброспинальной жидкости) их конечных продуктов - гомованилиновой и 5- оксиндолуксусной кислот.
Существенным для патогенеза заболевания является снижение уровня фолатов в сыворотке крови, эритроцитах и цереброспинальной жидкости. Это объясняется тесной взаимосвязью обмена фолатов и биоптерина, в частности участием дигидроптеринредуктазы в метаболизме тетрагидрофолиевой кислоты.
Фенилкетонурия III
Этот вариант болезни впервые описан S. Kaufman et al. в 1978 г. Заболевание наследуется аутосомно- рецессивно и связано с недостаточностью 6-пирувоилтетрагидроптерин синтазы, участвующей в процессе синтеза тетрагидробиоптерина из дигидронеоптерин трифосфата . Ключевую роль в патогенезе играет дефицит тетрагидробиоптерина. Развивающиеся при этом расстройства сходны с нарушениями, наблюдаемыми при ФКУ II.
Другие варианты ФКУ
В последние годы стали известны другие формы атипичной ФКУ, связанные с дефицитом тетрагидробиоптерина.
Недостаточность гуанозин 5- трифосфат циклогидролазы (S. Kaufman et al., 1987) описана по крайней мере у пяти больных. Этот фермент катализирует первую ступень синтеза тетрагидробиоптерина и при его дефиците в моче обнаруживается крайне низкая концентрация всех птеринов.
N. Blau и соавторы (1989) сообщили о новом варианте атипичной ФКУ - примаптеринурии - у двух детей с легкой гиперфенилаланинемией. Энзиматический дефект пока не известен. В моче обнаруживается в больших количествах продукт изомеризации биоптерина-7 - изобиоптерин (примаптерин) и некоторые другие его производные. Соотношение неоптерин/биоптерин у больных значительно повышено. Нагрузка тетрагидробиоптерином нормализует концентрацию фенилаланина в сыворотке и уровень неоптерина в моче, резко повышает экскрецию биоптерина и примаптерина. Отличием от других атипичных форм ФКУ является нормальная концентрация в цереброспинальной жидкости нейромедиаторных метаболитов - гомованилиновой и 5-оксииндолуксусной кислот.
Материнская ФКУ
В процессе изучения ФКУ было обращено внимание на высокую частоту умственной отсталости среди потомства женщин, страдающих ФКУ и не получающих диету в зрелом возрасте. Это состояние получило наименование материнской ФКУ . Патогенез патологии мало изучен , однако предполагается, что он сходен с патогенезом остальных форм ФКУ. Тяжесть поражения плода коррелирует с уровнем фенилаланина в плазме матери. Причем в связи с накоплением этой аминокислоты в плаценте, ее содержание в организме плода оказывается выше, чем у матери. Тем не менее прямое токсическое действие фенилаланина точно не подтверждено. Появление признаков патологии у потомства не зависит от наличия или отсутствия умственной отсталости у женщин и не связано с развитием у детей ФКУ. Есть данные, что тяжесть заболевания у больных ФКУ, родившихся от матерей, также страдающих этой болезнью, не отличается от степени поражения их сибсов, не унаследовавших ФКУ .
Клиническая картина
Фенилкетонурия I
Манифестация ФКУ происходит на первом году жизни, обычно в возрасте 2-6 мес. Первыми проявлениями болезни служат вялость ребенка, отсутствие интереса к окружающему, иногда повышенная раздражительность, беспокойство, срыгивания, нарушение мышечного тонуса (чаще мышечная гипотония), судороги, признаки аллергического дерматита. Появляется характерный “мышиный” запах. Отчетливо формируется задержка статикомоторного и психоречевого развития. При отсутствии лечения умственная отсталость достигает, как правило, глубокой степени.
Ранним симптомом заболевания может стать рвота, иногда настолько сильная, что ее ошибочно расценивают как проявление пилоростеноза. В более старшем возрасте нелеченные дети становятся гиперактивными, осуществляют бесцельные движения, ритмические покачивания, у них определяется атетоз.
При физикальном исследовании обращает на себя внимание то, что ребенок выглядит более белокурым, чем его здоровые сиблинги: у него светлая кожа и голубые глаза. У некоторых больных появляется себорейная или экзематоидная кожная сыпь, обычно умеренно выраженная и исчезающая по мере роста ребенка. От них исходит необычный запах фенилуксусной кислоты, который характеризуют как заплесневелый, мышиный или волчий. Не встречается характерных неврологических изменений , однако у большинства детей определяются гипертонус и повышение глубоких сухожильных рефлексов. Около 1/4 детей страдают судорогами и более чем у 50% появляются изменения на ЭЭГ. Часто у нелеченных детей определяют микроцефалию, выступающую верхнюю челюсть с широко расставленными зубами, гипоплазией эмали, отставание роста. Клинические проявления классической фенилкетонурии редко встречаются в странах, в которых эффективно действует программа неонатального скрининга на это заболевание.
Фенилкетонурия II
В клинической картине ФКУ II преобладает тяжелая умственная отсталость, судороги, признаки повышенной возбудимости, сухожильная гиперрефлексия, мышечная дистония, спастический тетрапарез. Течение болезни прогрессирующее и нередко приводит к смерти в 2- З- летнем возрасте. Больные, как правило, выявляются в результате массового скрининга новорожденных на ФКУ. Уровень фенилаланина в крови у этих детей увеличен, иногда может превышать 1200 мкмоль/л. Появление клинической симптоматики, как правило развивается в начале второго полугодия жизни, несмотря на диетотерапию.
Фенилкетонурия III
Клиническая картина болезни напоминает ФКУ II и включает тяжелую умственную отсталость, микроцефалию, спастический тетрапарез. Для подтверждения диагноза требуется :
stud24.ru